专题5第二单元胺和酰胺——课后训练(word版 含解析)
文档属性
| 名称 | 专题5第二单元胺和酰胺——课后训练(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-09 00:00:00 | ||
图片预览




文档简介
专题5第二单元胺和酰胺
一、选择题(共16题)
1.2002年瑞典科学家发现,某些高温油炸食品中含有一定量的CH2=CH—CO—NH2(丙烯酰胺)。食品中过量的丙烯酰胺可能引起食品安全问题。关于丙烯酰胺有下列叙述:
①能使酸性KMnO4溶液褪色;②能发生加聚反应生成高分子化合物;③只有4种同分异构体;④能与氢气发生加成反应;⑤能与盐酸反应;⑥能与NaOH溶液反应。
其中正确的是
A.①②③⑤ B.②③④⑥ C.①③④⑤⑥ D.①②④⑤⑥
2.茶文化是中国人民对世界饮食文化的一大贡献,茶叶中含有少量的咖啡因(结构简式如图)。关于咖啡因的说法错误的是
A.分子式为 B.能溶于水
C.具有弱碱性,能与酸反应 D.一定条件下,能与发生加成反应
3.《新型冠状病毒肺炎诊疗方案(试行第七版)》中指出,氯喹类药物可用于治疗新冠肺炎。氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物性质描述错误的是
A.均可以与盐酸反应形成离子化合物
B.分别取两种化合物,加入NaOH溶液在一定条件下充分反应,加入AgNO3溶液,均有白色沉淀产生,则证明两化合物中均含有氯原子
C.与足量的H2发生加成反应后,分子中的手性碳原子数均发生了改变
D.羟基氯喹比氯喹的水溶性更好,在人体胃肠道吸收更快
4.2002年10月26日,俄罗斯特种部队在解救歌剧院人质时,使用的气体中可能有芬太奴,芬太奴的结构简式为,它是一种医疗上速效强力镇痛药。下列关于芬太奴的说法不正确的是
A.分子式为:C19H23N2O B.芬太奴属于芳香族化合物
C.芬太奴显碱性 D.芬太奴既能与盐酸反应,又能与热的氢氧化钠溶液反应
5.2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎。氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物的描述错误的是
A.氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl
B.与足量的H2发生加成反应后,两分子中的手性碳原子数相等
C.加入NaOH溶液并加热,再加入AgNO3溶液后生成白色沉淀,可证明氯喹或羟基氯喹中含有氯原子
D.为增大溶解度,易于被人体吸收,经常把氯喹或羟基氯喹与硫酸、盐酸或磷酸制成盐类
6.维生素的结构如图所示,下列有关维生素的说法正确的是
A.分子内不存在手性碳原子 B.一定条件下能发生缩聚反应
C.不能使酸性溶液褪色 D.分子内有4种官能团
7.尿素()和甲醛在一定条件下发生类似苯酚和甲醛的反应得到线型脲醛树脂,再通过交联形成网状结构,网状结构片段如下图所示(图中表示链延长)。下列说法不正确的是
A.形成线型结构的过程发生了缩聚反应
B.网状脲醛树脂在自然界中不可能发生降解
C.线型脲醛树脂的结构简式可能是:
D.线型脲醛树脂能通过甲醛交联形成网状结构
8.某有机物的结构如图所示,关于该有机物下列说法正确的是
A.分子中最多有12个原子共平面
B.分子完全水解后所得有机物分子中手性碳原子数目为2个
C.分子可以在NaOH醇溶液加热条件下发生消去反应
D.1 mol该有机物最多可与2 mol NaOH反应
9.实验室合成乙酰苯胺的路线如下(反应条件略去):
下列说法错误的是
A.反应①完成后,碱洗和水洗可除去混合酸
B.若反应②中加入过量酸,则苯胺产率降低
C.乙酰苯胺在强酸或强碱条件下长时间加热可发生水解反应
D.上述合成路线中的反应均为取代反应
10.有关的说法不正确的是
A.分子中至少有8个碳原子共平面
B.分子中含1个手性碳原子
C.酸性条件下加热水解有CO2生成
D.与足量NaOH溶液完全反应后生成的钠盐有2种
11.2020年6月26日是第三十三个国际禁毒日,主题是“健康人生,绿色无毒”。冰毒,新型毒品的一种,又名甲基安非他明,是一种无味或微有苦味的透明结晶体,纯品很像冰糖,形似冰,故俗称冰毒。甲基苯丙胺是制作冰毒的原料,已知甲基苯丙胺的结构(键线式)如图,下列说法不正确的是
A.甲基苯丙胺的分子式为C10H15N B.甲基苯丙胺能与酸反应
C.甲基苯丙胺的核磁共振氢谱中共有7种信号峰 D.甲基苯丙胺分子中只有一种官能团
12.尿素可以作氮肥,也可以应用于医疗,尿素[13CO(NH2)2]呼气试验诊断试剂盒临床用于诊断胃幽门螺杆菌感染,是一种准确、灵敏的方法。下列说法正确的是
A.尿素中的13C与12C互为同素异形体 B.13CO(NH2)2不可以形成分子间氢键
C.尿素[13CO(NH2)2]遇水能发生水解 D.尿素为非极性分子
13.有机物的有关说法不正确的是
A.该分子中有1个手性碳原子
B.分子中所有碳原子不可能处于同一平面
C.完全水解的产物之一有两性且能使FeCl3溶液显紫色
D.与足量的NaOH溶液完全反应最多消耗NaOH 5mol
14.异吲哚啉类作为一种结构特殊且具有多种用途的重要含氨化合物,被广泛应用于材料、染料、医药等领域。下列关于异吲哚啉类化合物M的说法错误的是
A.M属于芳香族化合物,其一氯代物有2种
B.M既能与酸反应,又能与碱反应
C.M的分子式为
D.一定条件下,1molM最多可以与5 mol 发生加成反应
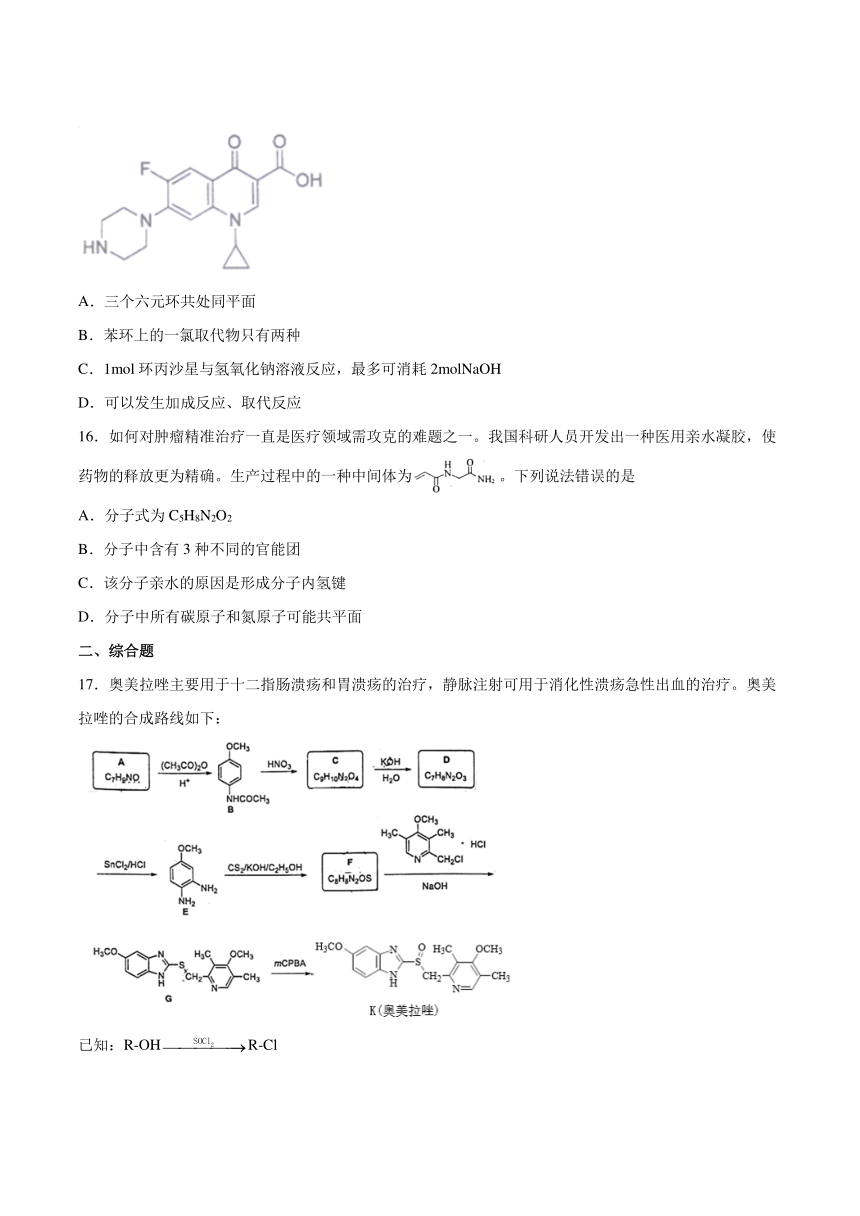
15.环丙沙星为合成的第三代喹诺酮类抗菌药物,具广谱抗菌活性,杀菌效果好。其结构式如图。以下说法正确的是
A.三个六元环共处同平面
B.苯环上的一氯取代物只有两种
C.1mol环丙沙星与氢氧化钠溶液反应,最多可消耗2molNaOH
D.可以发生加成反应、取代反应
16.如何对肿瘤精准治疗一直是医疗领域需攻克的难题之一。我国科研人员开发出一种医用亲水凝胶,使药物的释放更为精确。生产过程中的一种中间体为。下列说法错误的是
A.分子式为C5H8N2O2
B.分子中含有3种不同的官能团
C.该分子亲水的原因是形成分子内氢键
D.分子中所有碳原子和氮原子可能共平面
二、综合题
17.奥美拉唑主要用于十二指肠溃疡和胃溃疡的治疗,静脉注射可用于消化性溃疡急性出血的治疗。奥美拉唑的合成路线如下:
已知:R-OHR-Cl
R-X+
R1-SH+ R2-XR1-S-R2
结合上述合成路线、请回答:
(1)下列说法正确的是___________。
A.设计A转化为B的目的是保护其中的官能团
B.G生成H的反应类型为加成反应
C.化合物C可以发生的反应类型有取代、还原、加成
D.奥美拉唑的分子式为C18H19N3O3S
(2)化合物F的结构简式为___________。
(3)请写出C→D的反应方程式___________。
(4)写出同时满足下列条件的化合物B的同分异构体___________。
①分子中含苯环,遇FeCl3不显紫色,能发生水解反应和银镜反应
②分子中含有4种不同化学环境的氢原子。
(5)利用已有知识和题中涉及的反应,设计从1,3-丁二烯合成的路线(用流程图表示,无机试剂任选)___________。
18.已知恩杂鲁胺(G)是口服类雄激素受体抑制剂,用于化疗后进展的转移性去势耐受前列腺癌的治疗,可延长患者生存期。某种合成G的流程如下:
回答下列问题:
(1)分子中的Me的名称是___________;E中含氧官能团的名称是___________、酰胺键。
(2)的化学方程式是___________。
(3)的反应类型是___________。
(4)Q是A的同分异构体,属于芳香化合物,满足下列条件的Q有___________种(不考虑立体异构)。
Ⅰ.能与Na2CO3溶液反应 Ⅱ.能与FeCl3溶液发生显色反应
Ⅲ.不能发生银镜反应
其中Q的苯环上的氢被一个溴原子取代后的物质的核磁共振氢谱有两个峰,则该Q的结构简式是___________。
(5)根据题中流程和所学知识,写出以对溴甲苯和甲胺为原料制备的合成路线:______(无机试剂任选)。
19.A、B、C、D四种芳香族化合物,它们的结构简式如下所示:
请回答下列问题:
(1) D中含氧官能团的名称是________________________。
(2)能与新制Cu(OH)2反应产生红色沉淀的是________________(填序号)。
(3) A不能发生的反应是________________(填序号)。
①取代反应 ②加成反应 ③消去反应 ④加聚反应 ⑤与盐酸反应
(4)等物质的量的B、C与足量的NaOH溶液反应,消耗的NaOH物质的量之比为________。
(5) A在一定条件下可以生成一种高分子化合物E,E的结构简式为_________________。
(6)请写出D与CuO反应的化学方程式:_______________________________________。
20.根据下列化学反应回答问题
(1)在下列化学反应中
①试剂NH4Cl在反应中的作用是 ___________。
②画出产物D的稳定的互变异构体结构简式___________。
③产物D中碱性最强的氮原子是 ___________。
(2)下列两个反应在相同条件下发生,分别画出两个反应的产物的结构简式。
______________________
21.(1)官能团与有机物的性质密切相关。
①下列物质易溶于水的是_____________________(填字母)。
a.异丁烷 b.乙醇 c.氯乙烯
②下列物质不能发生水解反应的是_____________________(填字母)。
a.葡萄糖 b.溴乙烷 c.乙酸乙酯
③可用酸性KMnO4溶液鉴别的一组物质是_____________________(填字母)。
a.甲烷与乙烷 b.乙烯与乙炔 c.苯和甲苯
(2)对香豆酸的结构简式如右图所示。
①对香豆酸分子中位于同一平面的碳原子最多有_____________________个。
②1mol对香豆酸最多可与____________________ molH2发生加成反应。
③聚对香豆酸的结构简式为____________________。
(3)D(胡椒醛)是一种食品香料,以A为原料制备D的一种合成路线如下:
①A→B的反应类型是____________________;C中的含氧官能团名称为_____________________和____________________(填二种)。
②X的分子式为C2H2O3,B→C为加成反应,X的结构简式为____________________。
③芳香化合物Y是D的同分异构体,Y既能与NaHCO3反应生成CO2又能发生银镜反应,苯环上的一硝基取代物只有二种。符合题意的Y的结构简式为____________________。
22.三乙醇胺N(CH2CH2OH)3可以视为NH3的3个氢原子被- CH2CH2OH取代的产物,化学性质与NH3有可类比之处。三乙醇胺与H2S反应的化学方程式是___________。二乙醇胺与盐酸反应的化学方程是___________。
23.天然气是绿色、优质的能源。开采的天然气中通常会含有杂质H2S和CO2。实验室利用如下装置除去杂质并测定H2S的含量。
已知: FeS 难溶于水可溶于稀硫酸,CuS 既不溶于水又不溶于稀硫酸。
可供选择的试剂有: FeSO4溶液、CuSO4溶液、NaOH溶液、NaCl溶液。
回答下列问题:
(1)A中的试剂是___________。
(2)为测量H2S的含量,停止通气后,对洗气瓶中混合物应进行的操作是___________、______、干燥、称量。其中第一步操作用到的玻璃仪器有玻璃棒、烧杯、___________。
(3)若通入22.4L标准状况下的气体,测得生成3.84g沉淀, 则此天然气中H2S的体积分数为___________ %。
(4)室温下,氢硫酸(H2S)和碳酸的电离平衡常数如下表所示:
Kal Ka2
H2S 1.1×10-7 1.3×10-13
H2CO3 4.5×107 4.7×10-11
H2S与碳酸钠溶液反应的化学方程式是________,是否能用碳酸钠溶液替代A中的试剂?___________(填“是”或“否”)。原因是________。
(5)工业上也可使用醇胺吸收H2S, 反应原理为(HOCH2CH2)2NH+H2S=(HOCH2CH2)2NH2HS,上述反应说明(HOCH2CH2)2NH中,___________ (填基团结构简式)具有碱性。
24.苯胺()是重要的化工原料,其制备原理为:2+3Sn+12HCl2+3SnCl4+4 H2O
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐;部分物质物理性质见下表:
物质 熔点/℃ 沸点/℃ 溶解性 密度/
苯胺 184 微溶于水,易溶于乙醚 1.02
硝基苯 5.7 210.9 难溶于水,易溶于乙醚 1.23
乙醚 34.6 微溶于水 0.7134
回答下列问题:
(1)实验室用苯制取硝基苯的化学方程式为___________。
(2)往硝基苯中加入和足量盐酸充分还原,冷却后,往混合物中加入过量溶液得碱化液,加溶液的主要目的是析出苯胺,反应的离子方程式为___________。
(3)分离提纯:
步骤ⅰ.将碱化液蒸馏,收集到苯胺与水的混合物,分液得粗苯胺和水溶液;
步骤ⅱ.步骤ⅰ所得水溶液中加至饱和,用乙醚萃取得萃取液与粗苯胺合并:
步骤ⅲ。合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度时的馏分得到苯胺。
①步骤ⅰ蒸馏不需温度计控制温度,试依据收集馏分的特点,分析原因是___________。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是___________。如果没有步骤ⅱ,苯胺的产率___________(填“不变”、“增大”或“减小”)。步骤ⅲ中干燥剂可以选用___________(填序号)
a.浓硫酸 b.五氧化二磷 c.固体
③步骤ⅲ中蒸馏获得苯胺的温度的范围为___________。
(4)二次纯化:
苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:
试剂是___________,试剂是___________,“液相”是___________(填“水层”或“有机层”)
参考答案:
1.D
【详解】
①CH2=CH-CO-NH2中含有碳碳双键以及肽键,能使酸性KMnO4溶液褪色,故①正确;
②含有碳碳双键,能发生加聚反应生成高分子化合物,故②正确;
③丙烯酰胺的同分异构体,可书写其中的几种:H2N-CH=CH-CHO、CH≡C-CH2-O-NH2、CH≡C-O-CH2-NH2、CH3-C≡C-O-NH2、CH2=CH-CH2-NO、等等,不止四种,故③错误;
④含有碳碳双键,能与氢气发生加成反应,故④正确;
⑤丙烯酰胺能与盐酸发生水解反应,故⑤正确;
⑥丙烯酰胺能与NaOH溶液发生水解反应,故⑥正确;
故选:D。
2.A
【详解】
A.根据咖啡因的结构简式可知,该分子式为,故A符合题意;
B.该有机物含有羰基,具有酮的性质,能溶于水,故B不符合题意;
C.该有机物含有酰胺键,具有弱碱性,能与酸反应,故C不符合题意;
D.该有机物含有碳碳双键和碳氮双键,一定条件下,能与发生加成反应,故D不符合题意;
答案选A。
3.B
【详解】
A.两种化合物中均有多个N原子,类比氨气和氨基酸的性质可知,其均可与H+结合形成离子化合物,A正确;
B.两种化合物,加入NaOH溶液在一定条件下充分反应,直接加入AgNO3溶液会与氢氧化钠反应产生沉淀,干扰卤素的检验,B错误;
C.两种化合物均有1个手性碳原子,与足量的H2发生加成反应后,均增加4个手性碳原子,C正确;
D.羟基氯喹分子中有羟基,羟基是亲水基,故其水溶性比氯喹更好,在人体胃肠道吸收更快,D正确。
故选B。
4.A
5.C
【详解】
A.由结构简式可知,氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl,故A正确;
B.与足量的氢气发生加成反应后,所得产物都有如图*所示的5个手性碳原子:、,故B正确;
C.检验氯喹或羟基氯喹中含有氯原子时,应该先加入氢氧化钠溶液,共热后,为防止氢氧根离子干扰氯离子检验,应先加入硝酸酸化使溶液呈酸性,再加入硝酸银溶液,若生成白色沉淀,就可证明氯喹或羟基氯喹中含有氯原子,故C错误;
D.在氯喹和羟基氯喹中都含有亚氨基,能够与酸形成配位键而结合在一起,使物质在水中溶解度大大增加,从而更容易被人体吸收,故D正确;
故选C。
6.B
【详解】
A.由结构简式可知,维生素B5分子中含有如图*所示的1个连有不同原子或原子团的手性碳原子: ,故A错误;
B.由结构简式可知,维生素B5分子中含有羧基和羟基,一定条件下能发生缩聚反应生成高聚酯,故B正确;
C.由结构简式可知,维生素B5分子中与羟基相连的碳原子上连有氢原子,能与酸性高锰酸钾溶液发生氧化反应,使溶液褪色,故C错误;
D.由结构简式可知,维生素B5分子中含有羧基、酰胺基和羟基3种官能团,故D错误;
故选B。
7.B
【详解】
A.该高分子化合物可由尿素和甲醛通过缩聚反应得到,所以得到该物质的反应为缩聚反应,A正确;
B.网状脲醛树脂中含肽键,可以发生水解反应,即该物质在自然界中可以降解,B错误;
C.根据图判断其结构简式可能为:,C正确;
D.由图示结构可知,甲醛可以和线型脲醛树脂中的亚氨基继续加成反应生成网状结构的脲醛树脂,D正确;
答案选B。
8.D
【详解】
A.苯环为平面结构,且三个原子可确定1个平面,与苯环直接相连的原子一定与苯环共面,则最多共面原子大于12个,故A错误;
B.该物质完全水解后所得有机物为,其中只有与- NH2直接相连的碳原子为手性碳原子,即手性碳原子数目为1个,故B错误;
C.分子中含有醇羟基,且与羟基相连的碳原子的相邻碳原子上有氢原子,可以在浓硫酸,加热条件下发生消去反应,故C错误;
D.根据有机物的结构可知,分子中含有的-CONH-与-COO-可以和NaOH反应,则1 mol该有机物最多可与2 mol NaOH反应,故D正确;
故答案为D。
9.D
【详解】
A.苯的硝化反应中浓硫酸作催化剂,反应后硫酸和剩余的硝酸可用氢氧化钠中和后通过分液分离得到硝基苯,故A正确;
B.苯胺具有碱性,若反应②中加入过量的酸会消耗部分苯胺,从而降低了苯胺的产率,故B正确;
C.乙酰苯胺中的酰胺键在强酸催化或强碱性条件下能发生水解反应,故C正确;
D.反应②为还原反应,故D错误;
故选:D。
10.C
【详解】
A.苯环上的6个碳原子,以及与苯环直接相连的2个碳原子一定共面,单键可以旋转,所以其余碳原子不一定共面,即分子中至少有8个碳原子共平面,A正确;
B.连接四个不同原子或原子团的碳原子为手性碳原子,该分子中只有六元环中连接五元环中N原子的碳原子为手性碳,B正确;
C.该分子中含有酰胺键,可以水解,但水解产物中没有碳酸,即不会有CO2生成,C错误;
D.酰胺键可以水解产生羧基,羧基可以和NaOH反应,该物质与足量NaOH溶液完全反应后生成、两种钠盐,D正确;
综上所述答案为C。
11.C
【详解】
A.由甲基苯丙胺的结构简式可知其分子式为C10H15N,A正确;
B.甲基苯丙胺分子中存在亚氨基(-NH-),能与酸反应,B正确;
C.甲基苯丙胺分子中等效氢原子共含有8种(),所以核磁共振氢谱中共有8种信号峰,C错误;
D.甲基苯丙胺分子中只有亚氨基(-NH-)一种官能团,D正确;
故选C。
12.C
【详解】
A.同素异形体是由同种元素组成的不同单质,13C与12C为质子数相同中子数不同的不同核素、互为同位素,A错误;
B. 13CO(NH2)2中含氨基、可以形成分子间氢键,B错误;
C. 尿素[13CO(NH2)2]中含酰胺基,遇水能发生水解,C正确;
D. 尿素()中正负电荷重心不重叠、为极性分子,D错误;
答案选C。
13.CD
【详解】
A.在有机物分子中,连有4个不同原子或原子团的碳原子为手性碳原子,在该分子中只有1个手性碳原子,即标*的碳原子:,故A正确;
B.该分子中有一个六元环,全部以单键相连,环上的5个碳原子不可能处于同一平面,故B正确;
C.该有机物分子中含有两个肽键结构,完全水解生成 和, 分子中有羧基,有酸性,但没有碱性; 分子中有氨基,有碱性但没有酸性,两个分子中都没有酚羟基,不能使FeCl3溶液显紫色,故C错误;
D.该有机物分子中含有两个肽键结构,可以发生水解反应,由于肽键的存在,1mol该有机物能消耗2molNaOH;该分子中含有苯环,苯环上直接连着氯原子,可以发生卤代烃的水解,水解后生成的酚会继续和NaOH发生酸碱中和反应,由于氯原子的存在,1mol该有机物消耗2molNaOH,所以1mol该物质与足量的NaOH溶液完全反应最多消耗NaOH 4mol,故D错误;
故选CD。
14.AD
【详解】
A.M属于芳香族化合物,其苯环上的一氯代物有4种,选项A错误;
B.M中含有酰胺键和氨基,酰胺键可以在酸性或碱性条件下水解,氨基可以与酸反应,选项B正确;
C.根据结构简式可知,M的分子式为,选项C正确;
D.酰胺键不能与氢气发生加成反应,1mol M最多可以与加成,选项D错误;
答案选AD。
15.BD
16.BC
【详解】
A.根据物质分子结构可知该物质分子式是C5H8N2O2,A正确;
B.根据物质结构简式可知该物质分子中含有碳碳双键、肽键两种官能团,B错误;
C.该分子亲水的原因是分子中含有-NH2,-NH2是亲水基,能够与水分子之间形成氢键,增加了分子之间的吸引力,因此该物质易溶于水,C错误;
D.分子中含有饱和C原子与不饱和C原子,含有碳碳双键的C原子与其相连的原子在同一平面上,,两个平面共直线,可以在同一个平面上,因此分子中所有碳原子和氮原子可能共平面,D正确;
故合理选项是BC。
17. AC 、、
【详解】
根据A到B反应和B的结构简式得到A结构简式为:,B到C发生硝化反应得到C为,C到D发生水解反应得到D为:,D被还原成E,根据信息可知F为,故答案为:
(1) A.设计A转化为B的目的在硝化反应时保护一NH2,故A正确。
B.G生成H是加上氧元素了,应该属于氧化反应,故B错误;
C.C为,有苯环、硝基故可以发生还原、加成、取代,故C正确;
D.根据奥美拉唑的结构简式得出分子式为C18H18N3O3S,故D错误;
故正确答案为:AC;
(2) 根据信息和E反应生成F,推出化合物F的结构简式为:
(3) C为 ,C到D发生水解反应得到D为:,C→D的反应方程式为:;
(4) 由条件可知,分子中含苯环,遇FeCl3不显紫色,说明不存在酚羟基,能发生水解反应和银镜反应,说明含有-OOCH,分子中含有4种不同化学环境的氢原子,同分异构体有:
、、;
(5)根据题中信息可得合成路线为:,故答案为:
18. 甲基 酯基 +CH3NH2+HCl 加成反应 20 和
【详解】
(1)B是,B与CH3NH2发生取代反应产生C 和HCl,C与 发生取代反应产生D,根据C与D分子结构的不同,可知分子中Me的名称是—CH3,其名称是甲基;根据E结构简式可知:其中含氧官能团名称是酯基、酰胺键;
(2)B是,B与CH3NH2发生取代反应产生C 和HCl,该反应的化学方程式为:+CH3NH2+HCl;
(3)化合物F与发生加成反应产生G,故F变为G的反应类型为加成反应;
(4)Q是A的同分异构体,属于芳香化合物,说明分子中含有苯环,符合下列条件:Ⅰ.能与Na2CO3溶液反应;Ⅱ.能与FeCl3溶液发生显色反应,说明含有酚羟基 ;Ⅲ.不能发生银镜反应说明无醛基,苯环上有三个不同的取代基:①—OH、—F、—CBrO;或—OH、—Br、—CFO,每一种情况由于取代基在苯环上的相对位置不同而具有的同分异构体种类数目是10种;取代基有两种不同的情况,故具有的同分异构体种类数目为2×10种=20种;
其中Q的苯环上的氢被一个溴原子取代后的物质的核磁共振氢谱有两个峰,说明Q分子的苯环上具有两种不同位置的H原子,则该Q的结构简式是和;
(5)被酸性KMnO4溶液氧化产生,该物质与SOCl2发生-OH的取代反应产生,与CH3NH2发生Cl原子的取代反应产生,故由制取的合成路线为: 。
19. 羟基、醛基 B、D ③④ 3∶2
【详解】
(1) D的结构简式为,分子结构中含氧官能团的名称是羟基、醛基;
(2)含有醛基的有机物能与新制Cu(OH)2反应产生红色沉淀,则符合条件的是B、D两种有机物;
(3) A的结构简式为,分子结构中含有羧基和氨基,可发生缩聚反应生成多肽链,羧基能发生酯化反应(或取代反应)、苯环能发生加成反应、氨基有碱性能与盐酸反应,但有此有物不能发生消去反应,也不能发生加聚反应,故答案为③④;
(4)B的结构简式为,分子内有的酚羟基和酯基可与NaOH溶液反应,且每摩B可与3molNaOH完全反应;C的结构简式为,分子内羧基可与NaOH发生中和反应,烃基上连接的溴原子可在NaOH溶液中水解,且每摩C可与2molNaOH完全反应;故等物质的量的B、C与足量的NaOH溶液反应,消耗的NaOH物质的量之比为3:2;
(5) A的结构简式为,分子结构中含有羧基和氨基,可发生缩聚反应生成一种高分子化合物E,E的结构简式为;
(6) D的结构简式为,分子结构中含醇羟基,加热条件下与CuO反应的化学方程式为。
20. 作为Leiws酸与醛羰基相结合以活化反应底物 第3号N C18H19NO C21H20F2N2O
21. b a c 9 4 取代反应 醚键 羟基和羧基
【详解】
(1)①a.异丁烷难溶于水,a错误;b.乙醇与水互溶,b正确;c.氯乙烯难溶于水,c错误;答案选b;②a.葡萄糖的单糖,不能发生水解反应,a正确;b.溴乙烷是卤代烃,能发生水解反应,b错误;c.乙酸乙酯属于酯类,能发生水解反应,c错误,答案选a;③a.甲烷与乙烷都不能使酸性高锰酸钾溶液褪色,不能鉴别甲烷与乙烷,a错误;b.乙烯与乙炔都能使酸性高锰酸钾溶液褪色,不能鉴别,b错误;c.甲苯能使酸性高锰酸钾溶液褪色,能鉴别苯和甲苯,c正确,答案选c;(2)①由于碳碳双键、碳氧双键和苯环均是平面形结构,所以对香豆酸分子中位于同一平面的碳原子最多有9个。②碳碳双键和苯环均与氢气发生加成反应,1mol对香豆酸最多可与4molH2发生加成反应。③碳碳双键发生加聚反应生成聚对香豆酸,其结构简式为。(3)①A→B是酚羟基发生分子内脱水,反应类型是取代反应;C中的含氧官能团名称为醚键、羟基和羧基。②X的分子式为C2H2O3,B→C为加成反应,因此根据C的结构简式可知X的结构简式为OHC-COOH。③芳香化合物Y是D的同分异构体,Y既能与NaHCO3反应生成CO2又能发生银镜反应,含有羧基与醛基,苯环上的一硝基取代物只有二种,说明苯环上含有取代基且是对位的,则符合题意的Y的结构简式为。
点睛:有机物分子中共平面原子个数的判断是解答的难点和易错点,这类题切入点是平面型结构。有平面型结构的分子在中学主要有乙烯、1,3-丁二烯、苯三种,其中乙烯平面有6个原子共平面,1,3-丁二烯型的是10个原子共平面,苯平面有12个原子共平面。这些分子结构中的氢原子位置即使被其他原子替代,替代的原子仍共平面。只要掌握好这些结构,借助碳碳单键可以旋转而碳碳双键和碳碳三键不能旋转的特点,以及立体几何知识,各种与此有关的题目均可迎刃而解。
22. N(CH2CH2OH)3 +H2S=[H N(CH2CH2OH)3]HS (产物为[H N(CH2CH2OH)3]2S不扣分) HN(CH2CH2OH)2 +HCl=[H2N(CH2CH2OH)2]Cl
23.(1)CuSO4 溶液
(2) 过滤 洗涤 漏斗
(3)4
(4) Na2CO3+H2S= NaHS+ NaHCO3 否 碳酸钠溶液也能吸收CO2
(5)—NH—
【分析】
由实验装置图可知,第一个洗气瓶中盛有的硫酸铜溶液用于吸收测定天然气中的硫化氢气体,第二个洗气瓶中盛有的氢氧化钠溶液用于吸收二氧化碳气体,集气瓶的作用是收集除去硫化氢和二氧化碳的天然气。
(1)
由题给信息可知,氯化亚铁不溶于水溶于稀硫酸,而硫化铜既不溶于水又不溶于稀硫酸,所以试剂A为硫酸铜溶液,用于吸收测定天然气中的硫化氢气体,故答案为:CuSO4 溶液;
(2)
第一个洗气瓶中方式的反应为天然气中的硫化氢与硫酸铜溶液反应生成硫酸和硫化铜沉淀,则测量硫化氢含量时对洗气瓶中混合物应进行的操作是过滤、洗涤、干燥、称量,过滤用到的玻璃仪器有玻璃棒、烧杯、漏斗,故答案为:过滤;洗涤;漏斗;
(3)
若通入22.4L标准状况下的气体,生成3.84g硫化铜沉淀,则此天然气中硫化氢的体积分数为×100%=4%,故答案为:4;
(4)
由题给电离常数可知,弱酸或弱酸根的酸性强弱顺序为H2CO3>H2S>HCO>HS—,则由强酸制弱酸的原理可知,硫化氢与碳酸钠溶液反应生成碳酸氢钠和硫氢化钠,反应的化学方程式为Na2CO3+H2S= NaHS+ NaHCO3;二氧化碳也能与碳酸钠溶液反应生成碳酸氢钠,所以A中试剂不能用碳酸钠溶液替代硫酸铜溶液,否则会造成测定结果偏高,故答案为:Na2CO3+H2S= NaHS+ NaHCO3;否;碳酸钠溶液也能吸收CO2;
(5)
由结构简式可知,(HOCH2CH2)2NH中亚氨基中氮原子具有孤对电子,能与氢离子反应而表现碱性,故答案为:—NH—。
24. +HNO3 +H2O + OH-→+H2O(或) 蒸出物为混合物,无需控制温度 乙醚是易燃易挥发的物质 减小 c 盐酸 溶液 有机层
【详解】
(1)在催化剂的作用下,苯环上的氢原子被硝基子所取代,生成硝基苯,同时有水生成,反应的化学方程式为+HNO3+H2O,故答案为:+HNO3+H2O;
(2)往硝基苯中加入和足量盐酸充分还原,冷却后,往混合物中加入过量溶液得碱化液,加溶液的主要目的是析出苯胺,生成苯胺的离子方程式为+ OH-→+H2O(或),故答案为:+ OH-→+H2O(或);
(3)①步骤ⅰ蒸馏不需温度计控制温度,因为蒸馏出来的是水和苯胺的混合物,故无需温度计,故答案为:蒸出物为混合物,无需控制温度;
②乙醚是易燃易挥发的物质,因此步骤ⅱ萃取分液操作过程中要远离明火及热源;苯胺易溶于乙醚,如果没有步骤ⅱ,苯胺的产率将减小。苯胺类似氨气有碱性,步骤ⅲ中干燥剂可以选用碱性干燥剂,如氢氧化钠固体,不能选用酸性干燥剂,故答案为:乙醚是易燃易挥发的物质;减小;c;
③苯胺的沸点为184℃,硝基苯的沸点为210.9℃,因此步骤ⅲ中蒸馏获得苯胺的温度的范围为,故答案为:;
(4) 苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐,在混合物中加入盐酸,将苯胺转化为可溶于水的盐,然后分液,在水层中加入氢氧化钠,将转化为苯胺,分液得到苯胺,经过干燥、过滤得到较纯净的苯胺,故答案为:盐酸;溶液;有机层。
一、选择题(共16题)
1.2002年瑞典科学家发现,某些高温油炸食品中含有一定量的CH2=CH—CO—NH2(丙烯酰胺)。食品中过量的丙烯酰胺可能引起食品安全问题。关于丙烯酰胺有下列叙述:
①能使酸性KMnO4溶液褪色;②能发生加聚反应生成高分子化合物;③只有4种同分异构体;④能与氢气发生加成反应;⑤能与盐酸反应;⑥能与NaOH溶液反应。
其中正确的是
A.①②③⑤ B.②③④⑥ C.①③④⑤⑥ D.①②④⑤⑥
2.茶文化是中国人民对世界饮食文化的一大贡献,茶叶中含有少量的咖啡因(结构简式如图)。关于咖啡因的说法错误的是
A.分子式为 B.能溶于水
C.具有弱碱性,能与酸反应 D.一定条件下,能与发生加成反应
3.《新型冠状病毒肺炎诊疗方案(试行第七版)》中指出,氯喹类药物可用于治疗新冠肺炎。氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物性质描述错误的是
A.均可以与盐酸反应形成离子化合物
B.分别取两种化合物,加入NaOH溶液在一定条件下充分反应,加入AgNO3溶液,均有白色沉淀产生,则证明两化合物中均含有氯原子
C.与足量的H2发生加成反应后,分子中的手性碳原子数均发生了改变
D.羟基氯喹比氯喹的水溶性更好,在人体胃肠道吸收更快
4.2002年10月26日,俄罗斯特种部队在解救歌剧院人质时,使用的气体中可能有芬太奴,芬太奴的结构简式为,它是一种医疗上速效强力镇痛药。下列关于芬太奴的说法不正确的是
A.分子式为:C19H23N2O B.芬太奴属于芳香族化合物
C.芬太奴显碱性 D.芬太奴既能与盐酸反应,又能与热的氢氧化钠溶液反应
5.2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎。氯喹和羟基氯喹的结构分别如图1和图2所示,对这两种化合物的描述错误的是
A.氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl
B.与足量的H2发生加成反应后,两分子中的手性碳原子数相等
C.加入NaOH溶液并加热,再加入AgNO3溶液后生成白色沉淀,可证明氯喹或羟基氯喹中含有氯原子
D.为增大溶解度,易于被人体吸收,经常把氯喹或羟基氯喹与硫酸、盐酸或磷酸制成盐类
6.维生素的结构如图所示,下列有关维生素的说法正确的是
A.分子内不存在手性碳原子 B.一定条件下能发生缩聚反应
C.不能使酸性溶液褪色 D.分子内有4种官能团
7.尿素()和甲醛在一定条件下发生类似苯酚和甲醛的反应得到线型脲醛树脂,再通过交联形成网状结构,网状结构片段如下图所示(图中表示链延长)。下列说法不正确的是
A.形成线型结构的过程发生了缩聚反应
B.网状脲醛树脂在自然界中不可能发生降解
C.线型脲醛树脂的结构简式可能是:
D.线型脲醛树脂能通过甲醛交联形成网状结构
8.某有机物的结构如图所示,关于该有机物下列说法正确的是
A.分子中最多有12个原子共平面
B.分子完全水解后所得有机物分子中手性碳原子数目为2个
C.分子可以在NaOH醇溶液加热条件下发生消去反应
D.1 mol该有机物最多可与2 mol NaOH反应
9.实验室合成乙酰苯胺的路线如下(反应条件略去):
下列说法错误的是
A.反应①完成后,碱洗和水洗可除去混合酸
B.若反应②中加入过量酸,则苯胺产率降低
C.乙酰苯胺在强酸或强碱条件下长时间加热可发生水解反应
D.上述合成路线中的反应均为取代反应
10.有关的说法不正确的是
A.分子中至少有8个碳原子共平面
B.分子中含1个手性碳原子
C.酸性条件下加热水解有CO2生成
D.与足量NaOH溶液完全反应后生成的钠盐有2种
11.2020年6月26日是第三十三个国际禁毒日,主题是“健康人生,绿色无毒”。冰毒,新型毒品的一种,又名甲基安非他明,是一种无味或微有苦味的透明结晶体,纯品很像冰糖,形似冰,故俗称冰毒。甲基苯丙胺是制作冰毒的原料,已知甲基苯丙胺的结构(键线式)如图,下列说法不正确的是
A.甲基苯丙胺的分子式为C10H15N B.甲基苯丙胺能与酸反应
C.甲基苯丙胺的核磁共振氢谱中共有7种信号峰 D.甲基苯丙胺分子中只有一种官能团
12.尿素可以作氮肥,也可以应用于医疗,尿素[13CO(NH2)2]呼气试验诊断试剂盒临床用于诊断胃幽门螺杆菌感染,是一种准确、灵敏的方法。下列说法正确的是
A.尿素中的13C与12C互为同素异形体 B.13CO(NH2)2不可以形成分子间氢键
C.尿素[13CO(NH2)2]遇水能发生水解 D.尿素为非极性分子
13.有机物的有关说法不正确的是
A.该分子中有1个手性碳原子
B.分子中所有碳原子不可能处于同一平面
C.完全水解的产物之一有两性且能使FeCl3溶液显紫色
D.与足量的NaOH溶液完全反应最多消耗NaOH 5mol
14.异吲哚啉类作为一种结构特殊且具有多种用途的重要含氨化合物,被广泛应用于材料、染料、医药等领域。下列关于异吲哚啉类化合物M的说法错误的是
A.M属于芳香族化合物,其一氯代物有2种
B.M既能与酸反应,又能与碱反应
C.M的分子式为
D.一定条件下,1molM最多可以与5 mol 发生加成反应
15.环丙沙星为合成的第三代喹诺酮类抗菌药物,具广谱抗菌活性,杀菌效果好。其结构式如图。以下说法正确的是
A.三个六元环共处同平面
B.苯环上的一氯取代物只有两种
C.1mol环丙沙星与氢氧化钠溶液反应,最多可消耗2molNaOH
D.可以发生加成反应、取代反应
16.如何对肿瘤精准治疗一直是医疗领域需攻克的难题之一。我国科研人员开发出一种医用亲水凝胶,使药物的释放更为精确。生产过程中的一种中间体为。下列说法错误的是
A.分子式为C5H8N2O2
B.分子中含有3种不同的官能团
C.该分子亲水的原因是形成分子内氢键
D.分子中所有碳原子和氮原子可能共平面
二、综合题
17.奥美拉唑主要用于十二指肠溃疡和胃溃疡的治疗,静脉注射可用于消化性溃疡急性出血的治疗。奥美拉唑的合成路线如下:
已知:R-OHR-Cl
R-X+
R1-SH+ R2-XR1-S-R2
结合上述合成路线、请回答:
(1)下列说法正确的是___________。
A.设计A转化为B的目的是保护其中的官能团
B.G生成H的反应类型为加成反应
C.化合物C可以发生的反应类型有取代、还原、加成
D.奥美拉唑的分子式为C18H19N3O3S
(2)化合物F的结构简式为___________。
(3)请写出C→D的反应方程式___________。
(4)写出同时满足下列条件的化合物B的同分异构体___________。
①分子中含苯环,遇FeCl3不显紫色,能发生水解反应和银镜反应
②分子中含有4种不同化学环境的氢原子。
(5)利用已有知识和题中涉及的反应,设计从1,3-丁二烯合成的路线(用流程图表示,无机试剂任选)___________。
18.已知恩杂鲁胺(G)是口服类雄激素受体抑制剂,用于化疗后进展的转移性去势耐受前列腺癌的治疗,可延长患者生存期。某种合成G的流程如下:
回答下列问题:
(1)分子中的Me的名称是___________;E中含氧官能团的名称是___________、酰胺键。
(2)的化学方程式是___________。
(3)的反应类型是___________。
(4)Q是A的同分异构体,属于芳香化合物,满足下列条件的Q有___________种(不考虑立体异构)。
Ⅰ.能与Na2CO3溶液反应 Ⅱ.能与FeCl3溶液发生显色反应
Ⅲ.不能发生银镜反应
其中Q的苯环上的氢被一个溴原子取代后的物质的核磁共振氢谱有两个峰,则该Q的结构简式是___________。
(5)根据题中流程和所学知识,写出以对溴甲苯和甲胺为原料制备的合成路线:______(无机试剂任选)。
19.A、B、C、D四种芳香族化合物,它们的结构简式如下所示:
请回答下列问题:
(1) D中含氧官能团的名称是________________________。
(2)能与新制Cu(OH)2反应产生红色沉淀的是________________(填序号)。
(3) A不能发生的反应是________________(填序号)。
①取代反应 ②加成反应 ③消去反应 ④加聚反应 ⑤与盐酸反应
(4)等物质的量的B、C与足量的NaOH溶液反应,消耗的NaOH物质的量之比为________。
(5) A在一定条件下可以生成一种高分子化合物E,E的结构简式为_________________。
(6)请写出D与CuO反应的化学方程式:_______________________________________。
20.根据下列化学反应回答问题
(1)在下列化学反应中
①试剂NH4Cl在反应中的作用是 ___________。
②画出产物D的稳定的互变异构体结构简式___________。
③产物D中碱性最强的氮原子是 ___________。
(2)下列两个反应在相同条件下发生,分别画出两个反应的产物的结构简式。
______________________
21.(1)官能团与有机物的性质密切相关。
①下列物质易溶于水的是_____________________(填字母)。
a.异丁烷 b.乙醇 c.氯乙烯
②下列物质不能发生水解反应的是_____________________(填字母)。
a.葡萄糖 b.溴乙烷 c.乙酸乙酯
③可用酸性KMnO4溶液鉴别的一组物质是_____________________(填字母)。
a.甲烷与乙烷 b.乙烯与乙炔 c.苯和甲苯
(2)对香豆酸的结构简式如右图所示。
①对香豆酸分子中位于同一平面的碳原子最多有_____________________个。
②1mol对香豆酸最多可与____________________ molH2发生加成反应。
③聚对香豆酸的结构简式为____________________。
(3)D(胡椒醛)是一种食品香料,以A为原料制备D的一种合成路线如下:
①A→B的反应类型是____________________;C中的含氧官能团名称为_____________________和____________________(填二种)。
②X的分子式为C2H2O3,B→C为加成反应,X的结构简式为____________________。
③芳香化合物Y是D的同分异构体,Y既能与NaHCO3反应生成CO2又能发生银镜反应,苯环上的一硝基取代物只有二种。符合题意的Y的结构简式为____________________。
22.三乙醇胺N(CH2CH2OH)3可以视为NH3的3个氢原子被- CH2CH2OH取代的产物,化学性质与NH3有可类比之处。三乙醇胺与H2S反应的化学方程式是___________。二乙醇胺与盐酸反应的化学方程是___________。
23.天然气是绿色、优质的能源。开采的天然气中通常会含有杂质H2S和CO2。实验室利用如下装置除去杂质并测定H2S的含量。
已知: FeS 难溶于水可溶于稀硫酸,CuS 既不溶于水又不溶于稀硫酸。
可供选择的试剂有: FeSO4溶液、CuSO4溶液、NaOH溶液、NaCl溶液。
回答下列问题:
(1)A中的试剂是___________。
(2)为测量H2S的含量,停止通气后,对洗气瓶中混合物应进行的操作是___________、______、干燥、称量。其中第一步操作用到的玻璃仪器有玻璃棒、烧杯、___________。
(3)若通入22.4L标准状况下的气体,测得生成3.84g沉淀, 则此天然气中H2S的体积分数为___________ %。
(4)室温下,氢硫酸(H2S)和碳酸的电离平衡常数如下表所示:
Kal Ka2
H2S 1.1×10-7 1.3×10-13
H2CO3 4.5×107 4.7×10-11
H2S与碳酸钠溶液反应的化学方程式是________,是否能用碳酸钠溶液替代A中的试剂?___________(填“是”或“否”)。原因是________。
(5)工业上也可使用醇胺吸收H2S, 反应原理为(HOCH2CH2)2NH+H2S=(HOCH2CH2)2NH2HS,上述反应说明(HOCH2CH2)2NH中,___________ (填基团结构简式)具有碱性。
24.苯胺()是重要的化工原料,其制备原理为:2+3Sn+12HCl2+3SnCl4+4 H2O
已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐;部分物质物理性质见下表:
物质 熔点/℃ 沸点/℃ 溶解性 密度/
苯胺 184 微溶于水,易溶于乙醚 1.02
硝基苯 5.7 210.9 难溶于水,易溶于乙醚 1.23
乙醚 34.6 微溶于水 0.7134
回答下列问题:
(1)实验室用苯制取硝基苯的化学方程式为___________。
(2)往硝基苯中加入和足量盐酸充分还原,冷却后,往混合物中加入过量溶液得碱化液,加溶液的主要目的是析出苯胺,反应的离子方程式为___________。
(3)分离提纯:
步骤ⅰ.将碱化液蒸馏,收集到苯胺与水的混合物,分液得粗苯胺和水溶液;
步骤ⅱ.步骤ⅰ所得水溶液中加至饱和,用乙醚萃取得萃取液与粗苯胺合并:
步骤ⅲ。合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度时的馏分得到苯胺。
①步骤ⅰ蒸馏不需温度计控制温度,试依据收集馏分的特点,分析原因是___________。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是___________。如果没有步骤ⅱ,苯胺的产率___________(填“不变”、“增大”或“减小”)。步骤ⅲ中干燥剂可以选用___________(填序号)
a.浓硫酸 b.五氧化二磷 c.固体
③步骤ⅲ中蒸馏获得苯胺的温度的范围为___________。
(4)二次纯化:
苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:
试剂是___________,试剂是___________,“液相”是___________(填“水层”或“有机层”)
参考答案:
1.D
【详解】
①CH2=CH-CO-NH2中含有碳碳双键以及肽键,能使酸性KMnO4溶液褪色,故①正确;
②含有碳碳双键,能发生加聚反应生成高分子化合物,故②正确;
③丙烯酰胺的同分异构体,可书写其中的几种:H2N-CH=CH-CHO、CH≡C-CH2-O-NH2、CH≡C-O-CH2-NH2、CH3-C≡C-O-NH2、CH2=CH-CH2-NO、等等,不止四种,故③错误;
④含有碳碳双键,能与氢气发生加成反应,故④正确;
⑤丙烯酰胺能与盐酸发生水解反应,故⑤正确;
⑥丙烯酰胺能与NaOH溶液发生水解反应,故⑥正确;
故选:D。
2.A
【详解】
A.根据咖啡因的结构简式可知,该分子式为,故A符合题意;
B.该有机物含有羰基,具有酮的性质,能溶于水,故B不符合题意;
C.该有机物含有酰胺键,具有弱碱性,能与酸反应,故C不符合题意;
D.该有机物含有碳碳双键和碳氮双键,一定条件下,能与发生加成反应,故D不符合题意;
答案选A。
3.B
【详解】
A.两种化合物中均有多个N原子,类比氨气和氨基酸的性质可知,其均可与H+结合形成离子化合物,A正确;
B.两种化合物,加入NaOH溶液在一定条件下充分反应,直接加入AgNO3溶液会与氢氧化钠反应产生沉淀,干扰卤素的检验,B错误;
C.两种化合物均有1个手性碳原子,与足量的H2发生加成反应后,均增加4个手性碳原子,C正确;
D.羟基氯喹分子中有羟基,羟基是亲水基,故其水溶性比氯喹更好,在人体胃肠道吸收更快,D正确。
故选B。
4.A
5.C
【详解】
A.由结构简式可知,氯喹的化学式为C18H26N3Cl,羟基氯喹的化学式为C18H26N3OCl,故A正确;
B.与足量的氢气发生加成反应后,所得产物都有如图*所示的5个手性碳原子:、,故B正确;
C.检验氯喹或羟基氯喹中含有氯原子时,应该先加入氢氧化钠溶液,共热后,为防止氢氧根离子干扰氯离子检验,应先加入硝酸酸化使溶液呈酸性,再加入硝酸银溶液,若生成白色沉淀,就可证明氯喹或羟基氯喹中含有氯原子,故C错误;
D.在氯喹和羟基氯喹中都含有亚氨基,能够与酸形成配位键而结合在一起,使物质在水中溶解度大大增加,从而更容易被人体吸收,故D正确;
故选C。
6.B
【详解】
A.由结构简式可知,维生素B5分子中含有如图*所示的1个连有不同原子或原子团的手性碳原子: ,故A错误;
B.由结构简式可知,维生素B5分子中含有羧基和羟基,一定条件下能发生缩聚反应生成高聚酯,故B正确;
C.由结构简式可知,维生素B5分子中与羟基相连的碳原子上连有氢原子,能与酸性高锰酸钾溶液发生氧化反应,使溶液褪色,故C错误;
D.由结构简式可知,维生素B5分子中含有羧基、酰胺基和羟基3种官能团,故D错误;
故选B。
7.B
【详解】
A.该高分子化合物可由尿素和甲醛通过缩聚反应得到,所以得到该物质的反应为缩聚反应,A正确;
B.网状脲醛树脂中含肽键,可以发生水解反应,即该物质在自然界中可以降解,B错误;
C.根据图判断其结构简式可能为:,C正确;
D.由图示结构可知,甲醛可以和线型脲醛树脂中的亚氨基继续加成反应生成网状结构的脲醛树脂,D正确;
答案选B。
8.D
【详解】
A.苯环为平面结构,且三个原子可确定1个平面,与苯环直接相连的原子一定与苯环共面,则最多共面原子大于12个,故A错误;
B.该物质完全水解后所得有机物为,其中只有与- NH2直接相连的碳原子为手性碳原子,即手性碳原子数目为1个,故B错误;
C.分子中含有醇羟基,且与羟基相连的碳原子的相邻碳原子上有氢原子,可以在浓硫酸,加热条件下发生消去反应,故C错误;
D.根据有机物的结构可知,分子中含有的-CONH-与-COO-可以和NaOH反应,则1 mol该有机物最多可与2 mol NaOH反应,故D正确;
故答案为D。
9.D
【详解】
A.苯的硝化反应中浓硫酸作催化剂,反应后硫酸和剩余的硝酸可用氢氧化钠中和后通过分液分离得到硝基苯,故A正确;
B.苯胺具有碱性,若反应②中加入过量的酸会消耗部分苯胺,从而降低了苯胺的产率,故B正确;
C.乙酰苯胺中的酰胺键在强酸催化或强碱性条件下能发生水解反应,故C正确;
D.反应②为还原反应,故D错误;
故选:D。
10.C
【详解】
A.苯环上的6个碳原子,以及与苯环直接相连的2个碳原子一定共面,单键可以旋转,所以其余碳原子不一定共面,即分子中至少有8个碳原子共平面,A正确;
B.连接四个不同原子或原子团的碳原子为手性碳原子,该分子中只有六元环中连接五元环中N原子的碳原子为手性碳,B正确;
C.该分子中含有酰胺键,可以水解,但水解产物中没有碳酸,即不会有CO2生成,C错误;
D.酰胺键可以水解产生羧基,羧基可以和NaOH反应,该物质与足量NaOH溶液完全反应后生成、两种钠盐,D正确;
综上所述答案为C。
11.C
【详解】
A.由甲基苯丙胺的结构简式可知其分子式为C10H15N,A正确;
B.甲基苯丙胺分子中存在亚氨基(-NH-),能与酸反应,B正确;
C.甲基苯丙胺分子中等效氢原子共含有8种(),所以核磁共振氢谱中共有8种信号峰,C错误;
D.甲基苯丙胺分子中只有亚氨基(-NH-)一种官能团,D正确;
故选C。
12.C
【详解】
A.同素异形体是由同种元素组成的不同单质,13C与12C为质子数相同中子数不同的不同核素、互为同位素,A错误;
B. 13CO(NH2)2中含氨基、可以形成分子间氢键,B错误;
C. 尿素[13CO(NH2)2]中含酰胺基,遇水能发生水解,C正确;
D. 尿素()中正负电荷重心不重叠、为极性分子,D错误;
答案选C。
13.CD
【详解】
A.在有机物分子中,连有4个不同原子或原子团的碳原子为手性碳原子,在该分子中只有1个手性碳原子,即标*的碳原子:,故A正确;
B.该分子中有一个六元环,全部以单键相连,环上的5个碳原子不可能处于同一平面,故B正确;
C.该有机物分子中含有两个肽键结构,完全水解生成 和, 分子中有羧基,有酸性,但没有碱性; 分子中有氨基,有碱性但没有酸性,两个分子中都没有酚羟基,不能使FeCl3溶液显紫色,故C错误;
D.该有机物分子中含有两个肽键结构,可以发生水解反应,由于肽键的存在,1mol该有机物能消耗2molNaOH;该分子中含有苯环,苯环上直接连着氯原子,可以发生卤代烃的水解,水解后生成的酚会继续和NaOH发生酸碱中和反应,由于氯原子的存在,1mol该有机物消耗2molNaOH,所以1mol该物质与足量的NaOH溶液完全反应最多消耗NaOH 4mol,故D错误;
故选CD。
14.AD
【详解】
A.M属于芳香族化合物,其苯环上的一氯代物有4种,选项A错误;
B.M中含有酰胺键和氨基,酰胺键可以在酸性或碱性条件下水解,氨基可以与酸反应,选项B正确;
C.根据结构简式可知,M的分子式为,选项C正确;
D.酰胺键不能与氢气发生加成反应,1mol M最多可以与加成,选项D错误;
答案选AD。
15.BD
16.BC
【详解】
A.根据物质分子结构可知该物质分子式是C5H8N2O2,A正确;
B.根据物质结构简式可知该物质分子中含有碳碳双键、肽键两种官能团,B错误;
C.该分子亲水的原因是分子中含有-NH2,-NH2是亲水基,能够与水分子之间形成氢键,增加了分子之间的吸引力,因此该物质易溶于水,C错误;
D.分子中含有饱和C原子与不饱和C原子,含有碳碳双键的C原子与其相连的原子在同一平面上,,两个平面共直线,可以在同一个平面上,因此分子中所有碳原子和氮原子可能共平面,D正确;
故合理选项是BC。
17. AC 、、
【详解】
根据A到B反应和B的结构简式得到A结构简式为:,B到C发生硝化反应得到C为,C到D发生水解反应得到D为:,D被还原成E,根据信息可知F为,故答案为:
(1) A.设计A转化为B的目的在硝化反应时保护一NH2,故A正确。
B.G生成H是加上氧元素了,应该属于氧化反应,故B错误;
C.C为,有苯环、硝基故可以发生还原、加成、取代,故C正确;
D.根据奥美拉唑的结构简式得出分子式为C18H18N3O3S,故D错误;
故正确答案为:AC;
(2) 根据信息和E反应生成F,推出化合物F的结构简式为:
(3) C为 ,C到D发生水解反应得到D为:,C→D的反应方程式为:;
(4) 由条件可知,分子中含苯环,遇FeCl3不显紫色,说明不存在酚羟基,能发生水解反应和银镜反应,说明含有-OOCH,分子中含有4种不同化学环境的氢原子,同分异构体有:
、、;
(5)根据题中信息可得合成路线为:,故答案为:
18. 甲基 酯基 +CH3NH2+HCl 加成反应 20 和
【详解】
(1)B是,B与CH3NH2发生取代反应产生C 和HCl,C与 发生取代反应产生D,根据C与D分子结构的不同,可知分子中Me的名称是—CH3,其名称是甲基;根据E结构简式可知:其中含氧官能团名称是酯基、酰胺键;
(2)B是,B与CH3NH2发生取代反应产生C 和HCl,该反应的化学方程式为:+CH3NH2+HCl;
(3)化合物F与发生加成反应产生G,故F变为G的反应类型为加成反应;
(4)Q是A的同分异构体,属于芳香化合物,说明分子中含有苯环,符合下列条件:Ⅰ.能与Na2CO3溶液反应;Ⅱ.能与FeCl3溶液发生显色反应,说明含有酚羟基 ;Ⅲ.不能发生银镜反应说明无醛基,苯环上有三个不同的取代基:①—OH、—F、—CBrO;或—OH、—Br、—CFO,每一种情况由于取代基在苯环上的相对位置不同而具有的同分异构体种类数目是10种;取代基有两种不同的情况,故具有的同分异构体种类数目为2×10种=20种;
其中Q的苯环上的氢被一个溴原子取代后的物质的核磁共振氢谱有两个峰,说明Q分子的苯环上具有两种不同位置的H原子,则该Q的结构简式是和;
(5)被酸性KMnO4溶液氧化产生,该物质与SOCl2发生-OH的取代反应产生,与CH3NH2发生Cl原子的取代反应产生,故由制取的合成路线为: 。
19. 羟基、醛基 B、D ③④ 3∶2
【详解】
(1) D的结构简式为,分子结构中含氧官能团的名称是羟基、醛基;
(2)含有醛基的有机物能与新制Cu(OH)2反应产生红色沉淀,则符合条件的是B、D两种有机物;
(3) A的结构简式为,分子结构中含有羧基和氨基,可发生缩聚反应生成多肽链,羧基能发生酯化反应(或取代反应)、苯环能发生加成反应、氨基有碱性能与盐酸反应,但有此有物不能发生消去反应,也不能发生加聚反应,故答案为③④;
(4)B的结构简式为,分子内有的酚羟基和酯基可与NaOH溶液反应,且每摩B可与3molNaOH完全反应;C的结构简式为,分子内羧基可与NaOH发生中和反应,烃基上连接的溴原子可在NaOH溶液中水解,且每摩C可与2molNaOH完全反应;故等物质的量的B、C与足量的NaOH溶液反应,消耗的NaOH物质的量之比为3:2;
(5) A的结构简式为,分子结构中含有羧基和氨基,可发生缩聚反应生成一种高分子化合物E,E的结构简式为;
(6) D的结构简式为,分子结构中含醇羟基,加热条件下与CuO反应的化学方程式为。
20. 作为Leiws酸与醛羰基相结合以活化反应底物 第3号N C18H19NO C21H20F2N2O
21. b a c 9 4 取代反应 醚键 羟基和羧基
【详解】
(1)①a.异丁烷难溶于水,a错误;b.乙醇与水互溶,b正确;c.氯乙烯难溶于水,c错误;答案选b;②a.葡萄糖的单糖,不能发生水解反应,a正确;b.溴乙烷是卤代烃,能发生水解反应,b错误;c.乙酸乙酯属于酯类,能发生水解反应,c错误,答案选a;③a.甲烷与乙烷都不能使酸性高锰酸钾溶液褪色,不能鉴别甲烷与乙烷,a错误;b.乙烯与乙炔都能使酸性高锰酸钾溶液褪色,不能鉴别,b错误;c.甲苯能使酸性高锰酸钾溶液褪色,能鉴别苯和甲苯,c正确,答案选c;(2)①由于碳碳双键、碳氧双键和苯环均是平面形结构,所以对香豆酸分子中位于同一平面的碳原子最多有9个。②碳碳双键和苯环均与氢气发生加成反应,1mol对香豆酸最多可与4molH2发生加成反应。③碳碳双键发生加聚反应生成聚对香豆酸,其结构简式为。(3)①A→B是酚羟基发生分子内脱水,反应类型是取代反应;C中的含氧官能团名称为醚键、羟基和羧基。②X的分子式为C2H2O3,B→C为加成反应,因此根据C的结构简式可知X的结构简式为OHC-COOH。③芳香化合物Y是D的同分异构体,Y既能与NaHCO3反应生成CO2又能发生银镜反应,含有羧基与醛基,苯环上的一硝基取代物只有二种,说明苯环上含有取代基且是对位的,则符合题意的Y的结构简式为。
点睛:有机物分子中共平面原子个数的判断是解答的难点和易错点,这类题切入点是平面型结构。有平面型结构的分子在中学主要有乙烯、1,3-丁二烯、苯三种,其中乙烯平面有6个原子共平面,1,3-丁二烯型的是10个原子共平面,苯平面有12个原子共平面。这些分子结构中的氢原子位置即使被其他原子替代,替代的原子仍共平面。只要掌握好这些结构,借助碳碳单键可以旋转而碳碳双键和碳碳三键不能旋转的特点,以及立体几何知识,各种与此有关的题目均可迎刃而解。
22. N(CH2CH2OH)3 +H2S=[H N(CH2CH2OH)3]HS (产物为[H N(CH2CH2OH)3]2S不扣分) HN(CH2CH2OH)2 +HCl=[H2N(CH2CH2OH)2]Cl
23.(1)CuSO4 溶液
(2) 过滤 洗涤 漏斗
(3)4
(4) Na2CO3+H2S= NaHS+ NaHCO3 否 碳酸钠溶液也能吸收CO2
(5)—NH—
【分析】
由实验装置图可知,第一个洗气瓶中盛有的硫酸铜溶液用于吸收测定天然气中的硫化氢气体,第二个洗气瓶中盛有的氢氧化钠溶液用于吸收二氧化碳气体,集气瓶的作用是收集除去硫化氢和二氧化碳的天然气。
(1)
由题给信息可知,氯化亚铁不溶于水溶于稀硫酸,而硫化铜既不溶于水又不溶于稀硫酸,所以试剂A为硫酸铜溶液,用于吸收测定天然气中的硫化氢气体,故答案为:CuSO4 溶液;
(2)
第一个洗气瓶中方式的反应为天然气中的硫化氢与硫酸铜溶液反应生成硫酸和硫化铜沉淀,则测量硫化氢含量时对洗气瓶中混合物应进行的操作是过滤、洗涤、干燥、称量,过滤用到的玻璃仪器有玻璃棒、烧杯、漏斗,故答案为:过滤;洗涤;漏斗;
(3)
若通入22.4L标准状况下的气体,生成3.84g硫化铜沉淀,则此天然气中硫化氢的体积分数为×100%=4%,故答案为:4;
(4)
由题给电离常数可知,弱酸或弱酸根的酸性强弱顺序为H2CO3>H2S>HCO>HS—,则由强酸制弱酸的原理可知,硫化氢与碳酸钠溶液反应生成碳酸氢钠和硫氢化钠,反应的化学方程式为Na2CO3+H2S= NaHS+ NaHCO3;二氧化碳也能与碳酸钠溶液反应生成碳酸氢钠,所以A中试剂不能用碳酸钠溶液替代硫酸铜溶液,否则会造成测定结果偏高,故答案为:Na2CO3+H2S= NaHS+ NaHCO3;否;碳酸钠溶液也能吸收CO2;
(5)
由结构简式可知,(HOCH2CH2)2NH中亚氨基中氮原子具有孤对电子,能与氢离子反应而表现碱性,故答案为:—NH—。
24. +HNO3 +H2O + OH-→+H2O(或) 蒸出物为混合物,无需控制温度 乙醚是易燃易挥发的物质 减小 c 盐酸 溶液 有机层
【详解】
(1)在催化剂的作用下,苯环上的氢原子被硝基子所取代,生成硝基苯,同时有水生成,反应的化学方程式为+HNO3+H2O,故答案为:+HNO3+H2O;
(2)往硝基苯中加入和足量盐酸充分还原,冷却后,往混合物中加入过量溶液得碱化液,加溶液的主要目的是析出苯胺,生成苯胺的离子方程式为+ OH-→+H2O(或),故答案为:+ OH-→+H2O(或);
(3)①步骤ⅰ蒸馏不需温度计控制温度,因为蒸馏出来的是水和苯胺的混合物,故无需温度计,故答案为:蒸出物为混合物,无需控制温度;
②乙醚是易燃易挥发的物质,因此步骤ⅱ萃取分液操作过程中要远离明火及热源;苯胺易溶于乙醚,如果没有步骤ⅱ,苯胺的产率将减小。苯胺类似氨气有碱性,步骤ⅲ中干燥剂可以选用碱性干燥剂,如氢氧化钠固体,不能选用酸性干燥剂,故答案为:乙醚是易燃易挥发的物质;减小;c;
③苯胺的沸点为184℃,硝基苯的沸点为210.9℃,因此步骤ⅲ中蒸馏获得苯胺的温度的范围为,故答案为:;
(4) 苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐,在混合物中加入盐酸,将苯胺转化为可溶于水的盐,然后分液,在水层中加入氢氧化钠,将转化为苯胺,分液得到苯胺,经过干燥、过滤得到较纯净的苯胺,故答案为:盐酸;溶液;有机层。
