化学:4.2《铝 金属材料》课件(鲁科版必修1)
文档属性
| 名称 | 化学:4.2《铝 金属材料》课件(鲁科版必修1) |

|
|
| 格式 | zip | ||
| 文件大小 | 257.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-03-29 00:00:00 | ||
图片预览







文档简介
课件21张PPT。铝 金属材料一、铝1.铝的物理性质 铝为 金属,熔沸点较 ,硬度
较 ,密度较 ,导电性仅次
于 、 和 ,居第 位;
铝元素在地壳中含量丰富,居 位。
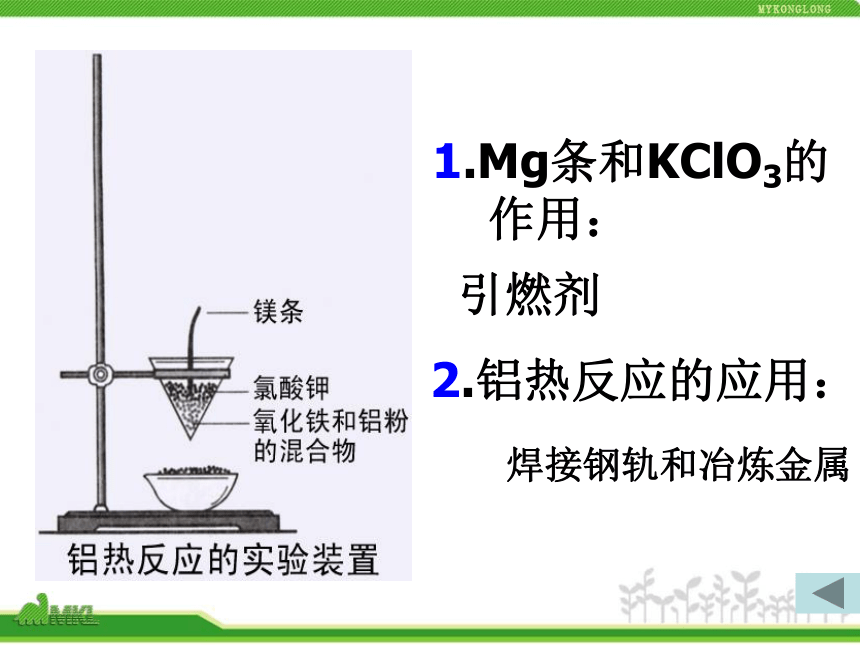
2.铝的化学性质(1)铝的金属通性①与非金属单质化合例如,氧气②与盐酸反应③与硫酸铜溶液反应2Al+6HCl====2AlCl3+3H2↑2Al+3CuSO4===3Cu+Al2(SO4)3现象:发出耀眼的白光,放出大量的热用途:燃烧弹,信号弹,火箭推进剂(2)与某些金属氧化物反应[实验]实验2现象:剧烈反应,发出耀眼的光芒,产生大量的烟,
纸漏斗被烧穿,有红热液珠落下,液珠冷却
后变为黑色。铝热反应: 铝在高温条件下和某金属氧化物发生
的反应 铝热剂:铝粉和金属氧化物的混合物1.Mg条和KClO3的
作用:引燃剂2.铝热反应的应用:焊接钢轨和冶炼金属(3)铝与碱反应2Al+2NaOH+6H2O===2Na[Al(OH) 4]+3H2↑(还原剂)(氧化剂) ①指出上面反应的氧化剂和还原剂?
②为什么铝制餐具不宜蒸煮或长期存放有酸性和碱性的食物? ?四羟基合铝酸钠1.取两份铝粉,一份投入足量浓氢氧化钠溶液中,一份投入足量盐酸中,充分反应,产生等量氢气。则两份铝粉的质量之比为:
A. 1: 2 B. 1: 3
C. 3 : 2 D. 1 : 1你会做吗?2.除去镁粉中混有的少量铝粉,可 选
用下列溶液中的:
A 盐酸 B 硝酸
C 浓氢氧化钾溶液 D 氨水3.某无色透明的溶液,放入铝粉后有氢
气产生,则一定可以在该溶液中存在的
离子是:A. Na+ B. Mg2+
C. S2- D.HCO3- 二、铝的重要化合物1.氧化铝(Al2O3) 色 溶于水,熔点很高,故可
做耐高温材料,例如,有氧化铝坩埚。①与酸反应:Al2O3+6HCl=2AlCl3+3H2OAl2O3+6H+=2Al3++3H2O②与强碱反应:Al2O3+2NaOH+3H2O===2Na[Al(OH)4]Al2O3+2OH-+3H2O===2[Al(OH)4]-___两性氧化物2.氢氧化铝(Al(OH)3)) 色 溶于水的 状物质。①与酸反应:Al(OH)3+3HCl=AlCl3+3H2OAl(OH)3+3H+=Al3++3H2O②与强碱反应:Al(OH)3+NaOH=Na[Al(OH)4]Al(OH)3+OH-===[Al(OH)4]-----两性氢氧化物③加热分解:2Al(OH)3===Al2O3+3H2O想一想 把NaOH溶液逐滴滴入到AlCl3 溶液中
现有有何现象?写出化学方程式!画出
加入NaOH 的量与沉淀量关系的图像开动脑筋,想一想! 若实验室要制取Al(OH)3,有下列两
种方法,你会选择哪种? 为什么? ①向AlCl3溶液中加NaOH溶液②向AlCl3溶液中加氨水Al2(SO4)3+6NH3?H2O=2Al(OH)3?+3(NH4)2SO4Al3++3NH3?H2O=Al(OH)3?+3NH4+3.硫酸铝钾[ KAl(SO4)2 ]KAl(SO4)2 ?12H20
俗名 明矾KAl(SO4)2=K++Al3++2SO42-练习:1.下列物质既能与NaOH溶液反应,又能
与稀盐酸反应的是:Mg B.Al(OH)3
C.NaHCO3 D.Na2CO34.铝合金及其制品①合金:两种或两种以上的金属(或金属
与非金属)熔合而成的具有金属
特性的物质。你能举出合金的例子吗? 不锈钢,生铁②合金特点:a.合金的熔点一般比它的各成分金属的低b.合金的硬度一般比它的各成分金属大本节课重要内容回顾1.氧化铝、氢氧化铝的两性及相关方程式。2.简单了解合金及其性质知识反馈 向50ml 2mol.L-1的AlCl3溶液中加
入一定量的1mol.L-1NaOH溶液,最终
得沉淀质量为3.9g,则加入的NaOH溶液
的体积可能为 。150ml或350ml ①把AlCl3溶液逐滴滴入到NaOH溶液中②把NaOH溶液逐滴滴入到AlCl3 溶液中请问上面两种操作各有什么现象?
你能画出
较 ,密度较 ,导电性仅次
于 、 和 ,居第 位;
铝元素在地壳中含量丰富,居 位。
2.铝的化学性质(1)铝的金属通性①与非金属单质化合例如,氧气②与盐酸反应③与硫酸铜溶液反应2Al+6HCl====2AlCl3+3H2↑2Al+3CuSO4===3Cu+Al2(SO4)3现象:发出耀眼的白光,放出大量的热用途:燃烧弹,信号弹,火箭推进剂(2)与某些金属氧化物反应[实验]实验2现象:剧烈反应,发出耀眼的光芒,产生大量的烟,
纸漏斗被烧穿,有红热液珠落下,液珠冷却
后变为黑色。铝热反应: 铝在高温条件下和某金属氧化物发生
的反应 铝热剂:铝粉和金属氧化物的混合物1.Mg条和KClO3的
作用:引燃剂2.铝热反应的应用:焊接钢轨和冶炼金属(3)铝与碱反应2Al+2NaOH+6H2O===2Na[Al(OH) 4]+3H2↑(还原剂)(氧化剂) ①指出上面反应的氧化剂和还原剂?
②为什么铝制餐具不宜蒸煮或长期存放有酸性和碱性的食物? ?四羟基合铝酸钠1.取两份铝粉,一份投入足量浓氢氧化钠溶液中,一份投入足量盐酸中,充分反应,产生等量氢气。则两份铝粉的质量之比为:
A. 1: 2 B. 1: 3
C. 3 : 2 D. 1 : 1你会做吗?2.除去镁粉中混有的少量铝粉,可 选
用下列溶液中的:
A 盐酸 B 硝酸
C 浓氢氧化钾溶液 D 氨水3.某无色透明的溶液,放入铝粉后有氢
气产生,则一定可以在该溶液中存在的
离子是:A. Na+ B. Mg2+
C. S2- D.HCO3- 二、铝的重要化合物1.氧化铝(Al2O3) 色 溶于水,熔点很高,故可
做耐高温材料,例如,有氧化铝坩埚。①与酸反应:Al2O3+6HCl=2AlCl3+3H2OAl2O3+6H+=2Al3++3H2O②与强碱反应:Al2O3+2NaOH+3H2O===2Na[Al(OH)4]Al2O3+2OH-+3H2O===2[Al(OH)4]-___两性氧化物2.氢氧化铝(Al(OH)3)) 色 溶于水的 状物质。①与酸反应:Al(OH)3+3HCl=AlCl3+3H2OAl(OH)3+3H+=Al3++3H2O②与强碱反应:Al(OH)3+NaOH=Na[Al(OH)4]Al(OH)3+OH-===[Al(OH)4]-----两性氢氧化物③加热分解:2Al(OH)3===Al2O3+3H2O想一想 把NaOH溶液逐滴滴入到AlCl3 溶液中
现有有何现象?写出化学方程式!画出
加入NaOH 的量与沉淀量关系的图像开动脑筋,想一想! 若实验室要制取Al(OH)3,有下列两
种方法,你会选择哪种? 为什么? ①向AlCl3溶液中加NaOH溶液②向AlCl3溶液中加氨水Al2(SO4)3+6NH3?H2O=2Al(OH)3?+3(NH4)2SO4Al3++3NH3?H2O=Al(OH)3?+3NH4+3.硫酸铝钾[ KAl(SO4)2 ]KAl(SO4)2 ?12H20
俗名 明矾KAl(SO4)2=K++Al3++2SO42-练习:1.下列物质既能与NaOH溶液反应,又能
与稀盐酸反应的是:Mg B.Al(OH)3
C.NaHCO3 D.Na2CO34.铝合金及其制品①合金:两种或两种以上的金属(或金属
与非金属)熔合而成的具有金属
特性的物质。你能举出合金的例子吗? 不锈钢,生铁②合金特点:a.合金的熔点一般比它的各成分金属的低b.合金的硬度一般比它的各成分金属大本节课重要内容回顾1.氧化铝、氢氧化铝的两性及相关方程式。2.简单了解合金及其性质知识反馈 向50ml 2mol.L-1的AlCl3溶液中加
入一定量的1mol.L-1NaOH溶液,最终
得沉淀质量为3.9g,则加入的NaOH溶液
的体积可能为 。150ml或350ml ①把AlCl3溶液逐滴滴入到NaOH溶液中②把NaOH溶液逐滴滴入到AlCl3 溶液中请问上面两种操作各有什么现象?
你能画出
