2021—2022学年人教版化学九(下)第9单元 溶液习题(word版 含答案)
文档属性
| 名称 | 2021—2022学年人教版化学九(下)第9单元 溶液习题(word版 含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-10 00:00:00 | ||
图片预览



文档简介
2021—2022学年人教版化学九(下)第9单元 溶液习题含答案
一、选择题。
1、下列判断正确的是( )
A.合金至少有两种金属熔合而成
B.不同种元素最本质的区别是质子数不同
C.饱和溶液变为不饱和溶液,其溶质质量分数一定变小
D.两种化合物相互作用生成另外两种化合物的反应一定是复分解反应
2、把下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.花生油 B.面粉 C.蔗糖 D.汽油
3、日常生活中除去油污的方法很多,下列现象不属于乳化的是( )
A.修车工用汽油洗去手上的油污
B.用洗发剂洗去头发上的油脂
C.用洗面奶洗去皮肤上的油脂
D.用洗洁精洗去餐具上的油污
4、配制溶液时,下列溶剂中最常用的是 ( )
A.酒精 B.植物油 C.汽油 D.水
5、将下列各组的物质混合,混合前后溶液总质量不改变的是( )
A.硫酸钠溶液氯化钡溶液 B.氢氧化钠溶液稀硫酸
C.碳酸钠溶液稀盐酸 D.氢氧化钠溶液硫酸铜溶液
6、保持温度不变,向接近饱和的硝酸钾溶液中加入硝酸钾晶体,如图所示。下列图像所反映的关系正确的是 ( )
7、喝了汽水以后常常打嗝儿,下列图示能正确解释这一现象的是( )
8、如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
A. t2℃时,a,b,c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水)
C. 将t2℃时 a,b,c三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数关系是b>a=c
D. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
9、实验室配制100g 10%的氯化钠溶液,有关实验操作不正确的是( )
A.用托盘天平称取10.0g氯化钠
B.用量筒量取90.0mL的水
C.将称取的氯化钠倒入量筒中溶解
D.将配制的溶液装入试剂瓶中,贴上标签
10、下列溶液中,溶剂不是水的是 ( )
A.蔗糖溶液 B.生理盐水 C.碘的酒精溶液 D.稀盐酸
11、如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是( )
A.t1℃时,甲、乙两种物质的溶解度相等
B.甲物质的溶解度随温度的升高而增大
C.将t2℃时甲、乙两种物质的饱和溶液降温到t1℃,溶液仍然饱和
D.t1℃时,将50g甲物质加入100g水中,充分搅拌,能得到甲物质的饱和溶液
12、配制溶质质量分数为5%的下列溶液,能达到目的是( )
A. 称取5.0g氯化钾,溶解在95mL.水中,充分搅拌
B. 称取5.0g生石灰,放入95mL,水中,充分搅拌
C. 量取5.0mL浓盐酸,倒入95mL.水中,充分搅拌
D. 称取5.0g碳酸钙,放入95mL水中,充分搅拌
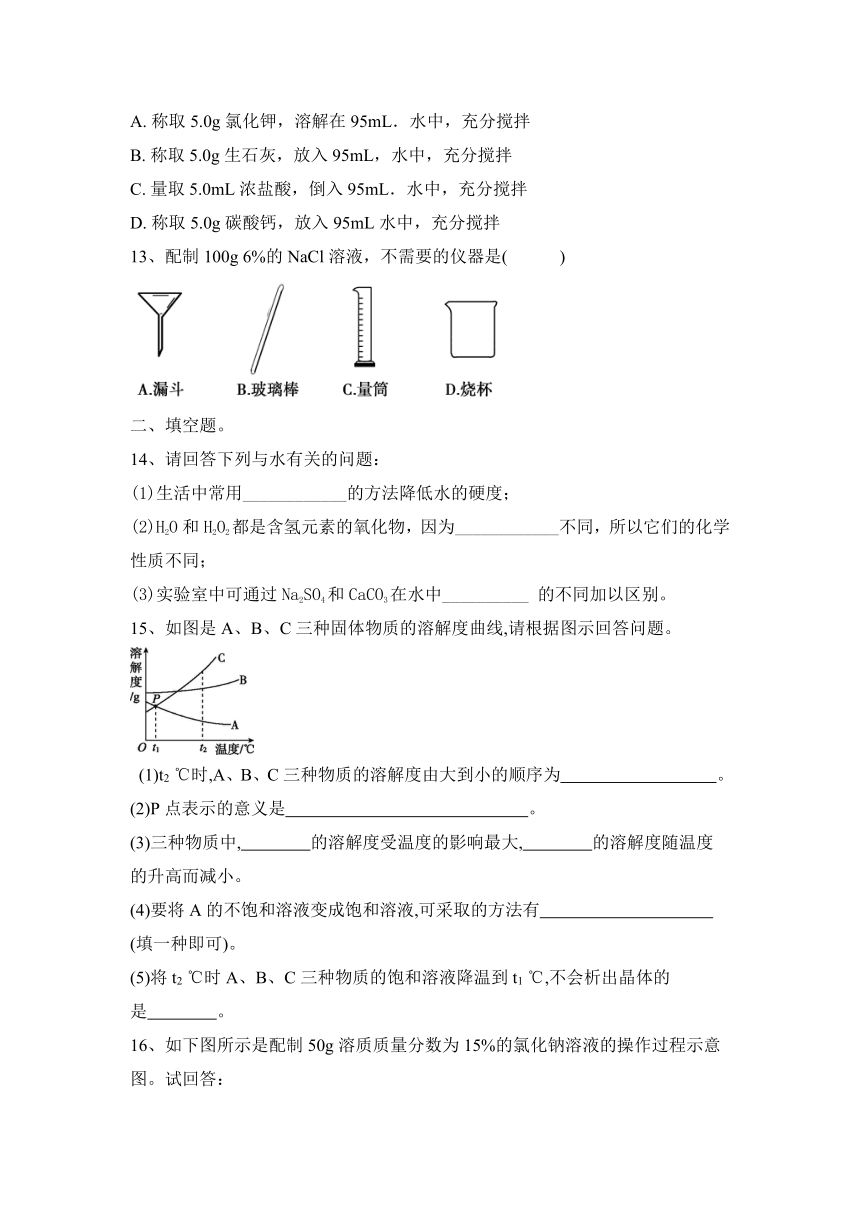
13、配制100g 6%的NaCl溶液,不需要的仪器是( )
二、填空题。
14、请回答下列与水有关的问题:
(1)生活中常用____________的方法降低水的硬度;
(2)H2O和H2O2都是含氢元素的氧化物,因为____________不同,所以它们的化学性质不同;
(3)实验室中可通过Na2SO4和CaCO3在水中__________ 的不同加以区别。
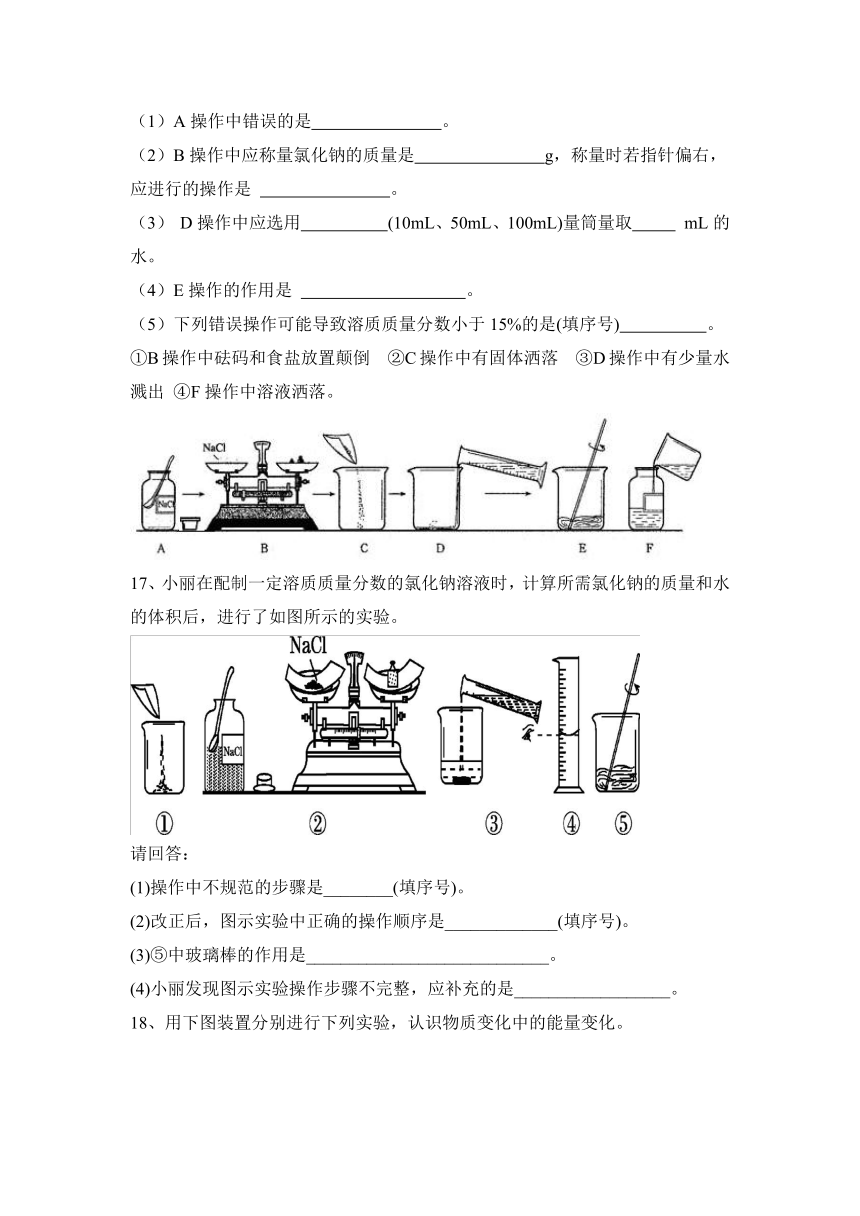
15、如图是A、B、C三种固体物质的溶解度曲线,请根据图示回答问题。
(1)t2 ℃时,A、B、C三种物质的溶解度由大到小的顺序为 。
(2)P点表示的意义是 。
(3)三种物质中, 的溶解度受温度的影响最大, 的溶解度随温度的升高而减小。
(4)要将A的不饱和溶液变成饱和溶液,可采取的方法有 (填一种即可)。
(5)将t2 ℃时A、B、C三种物质的饱和溶液降温到t1 ℃,不会析出晶体的是 。
16、如下图所示是配制50g溶质质量分数为15%的氯化钠溶液的操作过程示意图。试回答:
(1)A操作中错误的是 。
(2)B操作中应称量氯化钠的质量是 g,称量时若指针偏右,应进行的操作是 。
(3) D操作中应选用 (10mL、50mL、100mL)量筒量取 mL的水。
(4)E操作的作用是 。
(5)下列错误操作可能导致溶质质量分数小于15%的是(填序号) 。①B操作中砝码和食盐放置颠倒 ②C操作中有固体洒落 ③D操作中有少量水溅出 ④F操作中溶液洒落。
17、小丽在配制一定溶质质量分数的氯化钠溶液时,计算所需氯化钠的质量和水的体积后,进行了如图所示的实验。
请回答:
(1)操作中不规范的步骤是________(填序号)。
(2)改正后,图示实验中正确的操作顺序是_____________(填序号)。
(3)⑤中玻璃棒的作用是____________________________。
(4)小丽发现图示实验操作步骤不完整,应补充的是__________________。
18、用下图装置分别进行下列实验,认识物质变化中的能量变化。
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是_______。写出生石灰与水反应的化学方程式_________________________。
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是________ (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
19、炎热的夏天,在家中可以自制汽水来解暑消热。
[准备材料] 1.5 g小苏打、1.5 g柠檬酸、蔗糖、果汁、凉开水、500 mL的饮料瓶。(柠檬酸与小苏打发生反应生成二氧化碳气体)
[配制流程]
下列是制汽水的操作或现象的相关问题,请回答:
Ⅰ.步骤②中为什么要用凉开水制汽水
。
Ⅱ.步骤③旋紧瓶盖后,为什么汽水中的气泡会由多变少直至不再冒出
。
20、“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体________g;下列实验操作与目的分析均正确的一组是______(填序号)。
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有烧杯、玻璃棒、量筒和________。
(3)实验室若用恒温蒸发溶剂的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示,与丙烧杯中溶液溶质质量分数一定相同的是________(填序号)烧杯中的溶液。
三、实验题。
21、同学们在学习金属与盐溶液的反应时,老师强调:“金属K、Ca、Na必须除外.”化学兴趣小组的同学们对此产生了兴趣,并在老师的指导下,进行如下探究:
【提出问题】将金属钠投入到硫酸铜溶液中,结果会怎样?
【查找资料】(1)少量钠通常保存在煤油中;(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3(3)钠是一种很活泼的金属,遇水发生剧烈反应,生成氢氧化钠和氢气。
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜;
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜。
【实验探究】
实验操作 实验现象
①取10ml一定溶质质量分数的硫酸铜溶液,倒入50ml的烧杯里②取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,析出蓝色沉淀
(1)【现象分析】①钠熔成小球是因为________。
②钠球游动,发出“嘶嘶”声响说明有气体产生。
③析出蓝色沉淀是因为________ (用化学方程式表示)
(2)【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
实验操作 实验现象 结论
取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 沉淀全部溶解,溶液变蓝色 ________
(3)【实验结论】在金属活动性顺序里,位于前面的金属(K、Ca、Na必须除外)能把位于后面的金属从它们盐的溶液里置换出来.K、Ca、Na必须除外是因为________ 。
四、计算题。
22、20℃时,KNO3的溶解度为31.6g,将20g KNO3投进50g水中,充分搅拌,制成20℃时的溶液,求该溶液中溶质的质量分数。
2021—2022学年人教版化学九(下)第9单元 溶液习题含答案
一、选择题。
1、下列判断正确的是( )
A.合金至少有两种金属熔合而成
B.不同种元素最本质的区别是质子数不同
C.饱和溶液变为不饱和溶液,其溶质质量分数一定变小
D.两种化合物相互作用生成另外两种化合物的反应一定是复分解反应
【答案】B
2、把下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.花生油 B.面粉 C.蔗糖 D.汽油
【答案】C
3、日常生活中除去油污的方法很多,下列现象不属于乳化的是( )
A.修车工用汽油洗去手上的油污
B.用洗发剂洗去头发上的油脂
C.用洗面奶洗去皮肤上的油脂
D.用洗洁精洗去餐具上的油污
【答案】A
4、配制溶液时,下列溶剂中最常用的是 ( )
A.酒精 B.植物油 C.汽油 D.水
【答案】D
5、将下列各组的物质混合,混合前后溶液总质量不改变的是( )
A.硫酸钠溶液氯化钡溶液 B.氢氧化钠溶液稀硫酸
C.碳酸钠溶液稀盐酸 D.氢氧化钠溶液硫酸铜溶液
【答案】B
6、保持温度不变,向接近饱和的硝酸钾溶液中加入硝酸钾晶体,如图所示。下列图像所反映的关系正确的是 ( )
【答案】B
7、喝了汽水以后常常打嗝儿,下列图示能正确解释这一现象的是( )
【答案】B
8、如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
A. t2℃时,a,b,c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水)
C. 将t2℃时 a,b,c三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数关系是b>a=c
D. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
【答案】C
9、实验室配制100g 10%的氯化钠溶液,有关实验操作不正确的是( )
A.用托盘天平称取10.0g氯化钠
B.用量筒量取90.0mL的水
C.将称取的氯化钠倒入量筒中溶解
D.将配制的溶液装入试剂瓶中,贴上标签
【答案】C
10、下列溶液中,溶剂不是水的是 ( )
A.蔗糖溶液 B.生理盐水 C.碘的酒精溶液 D.稀盐酸
【答案】C
11、如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是( )
A.t1℃时,甲、乙两种物质的溶解度相等
B.甲物质的溶解度随温度的升高而增大
C.将t2℃时甲、乙两种物质的饱和溶液降温到t1℃,溶液仍然饱和
D.t1℃时,将50g甲物质加入100g水中,充分搅拌,能得到甲物质的饱和溶液
【答案】C
12、配制溶质质量分数为5%的下列溶液,能达到目的是( )
A. 称取5.0g氯化钾,溶解在95mL.水中,充分搅拌
B. 称取5.0g生石灰,放入95mL,水中,充分搅拌
C. 量取5.0mL浓盐酸,倒入95mL.水中,充分搅拌
D. 称取5.0g碳酸钙,放入95mL水中,充分搅拌
【答案】A
13、配制100g 6%的NaCl溶液,不需要的仪器是( )
【答案】A
二、填空题。
14、请回答下列与水有关的问题:
(1)生活中常用____________的方法降低水的硬度;
(2)H2O和H2O2都是含氢元素的氧化物,因为____________不同,所以它们的化学性质不同;
(3)实验室中可通过Na2SO4和CaCO3在水中__________ 的不同加以区别。
【答案】煮沸 分子结构 溶解性
15、如图是A、B、C三种固体物质的溶解度曲线,请根据图示回答问题。
(1)t2 ℃时,A、B、C三种物质的溶解度由大到小的顺序为 。
(2)P点表示的意义是 。
(3)三种物质中, 的溶解度受温度的影响最大, 的溶解度随温度的升高而减小。
(4)要将A的不饱和溶液变成饱和溶液,可采取的方法有 (填一种即可)。
(5)将t2 ℃时A、B、C三种物质的饱和溶液降温到t1 ℃,不会析出晶体的是 。
【答案】(1)C>B>A (2)t1 ℃时,A、C两种物质的溶解度相同
(3)C A (4)升高温度(或加入A物质或恒温蒸发溶剂) (5)A
16、如下图所示是配制50g溶质质量分数为15%的氯化钠溶液的操作过程示意图。试回答:
(1)A操作中错误的是 。
(2)B操作中应称量氯化钠的质量是 g,称量时若指针偏右,应进行的操作是 。
(3) D操作中应选用 (10mL、50mL、100mL)量筒量取 mL的水。
(4)E操作的作用是 。
(5)下列错误操作可能导致溶质质量分数小于15%的是(填序号) 。①B操作中砝码和食盐放置颠倒 ②C操作中有固体洒落 ③D操作中有少量水溅出 ④F操作中溶液洒落。
【答案】⑴试剂瓶塞正放 ⑵7.5 添加氯化钠至天平平衡 ⑶50mL,42.5
⑷加速固体溶解 ⑸①②
17、小丽在配制一定溶质质量分数的氯化钠溶液时,计算所需氯化钠的质量和水的体积后,进行了如图所示的实验。
请回答:
(1)操作中不规范的步骤是________(填序号)。
(2)改正后,图示实验中正确的操作顺序是_____________(填序号)。
(3)⑤中玻璃棒的作用是____________________________。
(4)小丽发现图示实验操作步骤不完整,应补充的是__________________。
【答案】(1)③ (2)②①④③⑤
(3)搅拌,加速溶解 (4)装瓶贴标签
18、用下图装置分别进行下列实验,认识物质变化中的能量变化。
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是_______。写出生石灰与水反应的化学方程式_________________________。
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是________ (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
【答案】 生石灰与水反应放出大量热,水温升高,使温度达到白磷的着火点 CaO + H2O = Ca(OH)2 CD
19、炎热的夏天,在家中可以自制汽水来解暑消热。
[准备材料] 1.5 g小苏打、1.5 g柠檬酸、蔗糖、果汁、凉开水、500 mL的饮料瓶。(柠檬酸与小苏打发生反应生成二氧化碳气体)
[配制流程]
下列是制汽水的操作或现象的相关问题,请回答:
Ⅰ.步骤②中为什么要用凉开水制汽水
。
Ⅱ.步骤③旋紧瓶盖后,为什么汽水中的气泡会由多变少直至不再冒出
。
【答案】Ⅰ.凉开水温度较低,二氧化碳的溶解度随温度的降低而增大
Ⅱ.旋紧瓶盖后,瓶内压强增大,二氧化碳的溶解度增大
20、“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体________g;下列实验操作与目的分析均正确的一组是______(填序号)。
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有烧杯、玻璃棒、量筒和________。
(3)实验室若用恒温蒸发溶剂的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示,与丙烧杯中溶液溶质质量分数一定相同的是________(填序号)烧杯中的溶液。
【答案】(1)4.5;D (2)胶头滴管 (3)丁
三、实验题。
21、同学们在学习金属与盐溶液的反应时,老师强调:“金属K、Ca、Na必须除外.”化学兴趣小组的同学们对此产生了兴趣,并在老师的指导下,进行如下探究:
【提出问题】将金属钠投入到硫酸铜溶液中,结果会怎样?
【查找资料】(1)少量钠通常保存在煤油中;(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3(3)钠是一种很活泼的金属,遇水发生剧烈反应,生成氢氧化钠和氢气。
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜;
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜。
【实验探究】
实验操作 实验现象
①取10ml一定溶质质量分数的硫酸铜溶液,倒入50ml的烧杯里②取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,析出蓝色沉淀
(1)【现象分析】①钠熔成小球是因为________。
②钠球游动,发出“嘶嘶”声响说明有气体产生。
③析出蓝色沉淀是因为________ (用化学方程式表示)
(2)【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
实验操作 实验现象 结论
取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 沉淀全部溶解,溶液变蓝色 ________
(3)【实验结论】在金属活动性顺序里,位于前面的金属(K、Ca、Na必须除外)能把位于后面的金属从它们盐的溶液里置换出来.K、Ca、Na必须除外是因为________ 。
【答案】(1)钠与水发生剧烈反应,反应放出的热量使钠熔化成小球;2Na+2H2O=2NaOH+H2↑,2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
(2)说明沉淀中不含红色的铜
(3)K、Ca、Na盐溶液的反应先是和里面的水的反应生成碱和氢气
四、计算题。
22、20℃时,KNO3的溶解度为31.6g,将20g KNO3投进50g水中,充分搅拌,制成20℃时的溶液,求该溶液中溶质的质量分数。
【答案】24%
一、选择题。
1、下列判断正确的是( )
A.合金至少有两种金属熔合而成
B.不同种元素最本质的区别是质子数不同
C.饱和溶液变为不饱和溶液,其溶质质量分数一定变小
D.两种化合物相互作用生成另外两种化合物的反应一定是复分解反应
2、把下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.花生油 B.面粉 C.蔗糖 D.汽油
3、日常生活中除去油污的方法很多,下列现象不属于乳化的是( )
A.修车工用汽油洗去手上的油污
B.用洗发剂洗去头发上的油脂
C.用洗面奶洗去皮肤上的油脂
D.用洗洁精洗去餐具上的油污
4、配制溶液时,下列溶剂中最常用的是 ( )
A.酒精 B.植物油 C.汽油 D.水
5、将下列各组的物质混合,混合前后溶液总质量不改变的是( )
A.硫酸钠溶液氯化钡溶液 B.氢氧化钠溶液稀硫酸
C.碳酸钠溶液稀盐酸 D.氢氧化钠溶液硫酸铜溶液
6、保持温度不变,向接近饱和的硝酸钾溶液中加入硝酸钾晶体,如图所示。下列图像所反映的关系正确的是 ( )
7、喝了汽水以后常常打嗝儿,下列图示能正确解释这一现象的是( )
8、如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
A. t2℃时,a,b,c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水)
C. 将t2℃时 a,b,c三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数关系是b>a=c
D. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
9、实验室配制100g 10%的氯化钠溶液,有关实验操作不正确的是( )
A.用托盘天平称取10.0g氯化钠
B.用量筒量取90.0mL的水
C.将称取的氯化钠倒入量筒中溶解
D.将配制的溶液装入试剂瓶中,贴上标签
10、下列溶液中,溶剂不是水的是 ( )
A.蔗糖溶液 B.生理盐水 C.碘的酒精溶液 D.稀盐酸
11、如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是( )
A.t1℃时,甲、乙两种物质的溶解度相等
B.甲物质的溶解度随温度的升高而增大
C.将t2℃时甲、乙两种物质的饱和溶液降温到t1℃,溶液仍然饱和
D.t1℃时,将50g甲物质加入100g水中,充分搅拌,能得到甲物质的饱和溶液
12、配制溶质质量分数为5%的下列溶液,能达到目的是( )
A. 称取5.0g氯化钾,溶解在95mL.水中,充分搅拌
B. 称取5.0g生石灰,放入95mL,水中,充分搅拌
C. 量取5.0mL浓盐酸,倒入95mL.水中,充分搅拌
D. 称取5.0g碳酸钙,放入95mL水中,充分搅拌
13、配制100g 6%的NaCl溶液,不需要的仪器是( )
二、填空题。
14、请回答下列与水有关的问题:
(1)生活中常用____________的方法降低水的硬度;
(2)H2O和H2O2都是含氢元素的氧化物,因为____________不同,所以它们的化学性质不同;
(3)实验室中可通过Na2SO4和CaCO3在水中__________ 的不同加以区别。
15、如图是A、B、C三种固体物质的溶解度曲线,请根据图示回答问题。
(1)t2 ℃时,A、B、C三种物质的溶解度由大到小的顺序为 。
(2)P点表示的意义是 。
(3)三种物质中, 的溶解度受温度的影响最大, 的溶解度随温度的升高而减小。
(4)要将A的不饱和溶液变成饱和溶液,可采取的方法有 (填一种即可)。
(5)将t2 ℃时A、B、C三种物质的饱和溶液降温到t1 ℃,不会析出晶体的是 。
16、如下图所示是配制50g溶质质量分数为15%的氯化钠溶液的操作过程示意图。试回答:
(1)A操作中错误的是 。
(2)B操作中应称量氯化钠的质量是 g,称量时若指针偏右,应进行的操作是 。
(3) D操作中应选用 (10mL、50mL、100mL)量筒量取 mL的水。
(4)E操作的作用是 。
(5)下列错误操作可能导致溶质质量分数小于15%的是(填序号) 。①B操作中砝码和食盐放置颠倒 ②C操作中有固体洒落 ③D操作中有少量水溅出 ④F操作中溶液洒落。
17、小丽在配制一定溶质质量分数的氯化钠溶液时,计算所需氯化钠的质量和水的体积后,进行了如图所示的实验。
请回答:
(1)操作中不规范的步骤是________(填序号)。
(2)改正后,图示实验中正确的操作顺序是_____________(填序号)。
(3)⑤中玻璃棒的作用是____________________________。
(4)小丽发现图示实验操作步骤不完整,应补充的是__________________。
18、用下图装置分别进行下列实验,认识物质变化中的能量变化。
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是_______。写出生石灰与水反应的化学方程式_________________________。
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是________ (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
19、炎热的夏天,在家中可以自制汽水来解暑消热。
[准备材料] 1.5 g小苏打、1.5 g柠檬酸、蔗糖、果汁、凉开水、500 mL的饮料瓶。(柠檬酸与小苏打发生反应生成二氧化碳气体)
[配制流程]
下列是制汽水的操作或现象的相关问题,请回答:
Ⅰ.步骤②中为什么要用凉开水制汽水
。
Ⅱ.步骤③旋紧瓶盖后,为什么汽水中的气泡会由多变少直至不再冒出
。
20、“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体________g;下列实验操作与目的分析均正确的一组是______(填序号)。
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有烧杯、玻璃棒、量筒和________。
(3)实验室若用恒温蒸发溶剂的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示,与丙烧杯中溶液溶质质量分数一定相同的是________(填序号)烧杯中的溶液。
三、实验题。
21、同学们在学习金属与盐溶液的反应时,老师强调:“金属K、Ca、Na必须除外.”化学兴趣小组的同学们对此产生了兴趣,并在老师的指导下,进行如下探究:
【提出问题】将金属钠投入到硫酸铜溶液中,结果会怎样?
【查找资料】(1)少量钠通常保存在煤油中;(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3(3)钠是一种很活泼的金属,遇水发生剧烈反应,生成氢氧化钠和氢气。
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜;
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜。
【实验探究】
实验操作 实验现象
①取10ml一定溶质质量分数的硫酸铜溶液,倒入50ml的烧杯里②取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,析出蓝色沉淀
(1)【现象分析】①钠熔成小球是因为________。
②钠球游动,发出“嘶嘶”声响说明有气体产生。
③析出蓝色沉淀是因为________ (用化学方程式表示)
(2)【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
实验操作 实验现象 结论
取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 沉淀全部溶解,溶液变蓝色 ________
(3)【实验结论】在金属活动性顺序里,位于前面的金属(K、Ca、Na必须除外)能把位于后面的金属从它们盐的溶液里置换出来.K、Ca、Na必须除外是因为________ 。
四、计算题。
22、20℃时,KNO3的溶解度为31.6g,将20g KNO3投进50g水中,充分搅拌,制成20℃时的溶液,求该溶液中溶质的质量分数。
2021—2022学年人教版化学九(下)第9单元 溶液习题含答案
一、选择题。
1、下列判断正确的是( )
A.合金至少有两种金属熔合而成
B.不同种元素最本质的区别是质子数不同
C.饱和溶液变为不饱和溶液,其溶质质量分数一定变小
D.两种化合物相互作用生成另外两种化合物的反应一定是复分解反应
【答案】B
2、把下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.花生油 B.面粉 C.蔗糖 D.汽油
【答案】C
3、日常生活中除去油污的方法很多,下列现象不属于乳化的是( )
A.修车工用汽油洗去手上的油污
B.用洗发剂洗去头发上的油脂
C.用洗面奶洗去皮肤上的油脂
D.用洗洁精洗去餐具上的油污
【答案】A
4、配制溶液时,下列溶剂中最常用的是 ( )
A.酒精 B.植物油 C.汽油 D.水
【答案】D
5、将下列各组的物质混合,混合前后溶液总质量不改变的是( )
A.硫酸钠溶液氯化钡溶液 B.氢氧化钠溶液稀硫酸
C.碳酸钠溶液稀盐酸 D.氢氧化钠溶液硫酸铜溶液
【答案】B
6、保持温度不变,向接近饱和的硝酸钾溶液中加入硝酸钾晶体,如图所示。下列图像所反映的关系正确的是 ( )
【答案】B
7、喝了汽水以后常常打嗝儿,下列图示能正确解释这一现象的是( )
【答案】B
8、如图是a,b,c三种物质的溶解度曲线,下列分析不正确的是( )
A. t2℃时,a,b,c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水)
C. 将t2℃时 a,b,c三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数关系是b>a=c
D. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
【答案】C
9、实验室配制100g 10%的氯化钠溶液,有关实验操作不正确的是( )
A.用托盘天平称取10.0g氯化钠
B.用量筒量取90.0mL的水
C.将称取的氯化钠倒入量筒中溶解
D.将配制的溶液装入试剂瓶中,贴上标签
【答案】C
10、下列溶液中,溶剂不是水的是 ( )
A.蔗糖溶液 B.生理盐水 C.碘的酒精溶液 D.稀盐酸
【答案】C
11、如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是( )
A.t1℃时,甲、乙两种物质的溶解度相等
B.甲物质的溶解度随温度的升高而增大
C.将t2℃时甲、乙两种物质的饱和溶液降温到t1℃,溶液仍然饱和
D.t1℃时,将50g甲物质加入100g水中,充分搅拌,能得到甲物质的饱和溶液
【答案】C
12、配制溶质质量分数为5%的下列溶液,能达到目的是( )
A. 称取5.0g氯化钾,溶解在95mL.水中,充分搅拌
B. 称取5.0g生石灰,放入95mL,水中,充分搅拌
C. 量取5.0mL浓盐酸,倒入95mL.水中,充分搅拌
D. 称取5.0g碳酸钙,放入95mL水中,充分搅拌
【答案】A
13、配制100g 6%的NaCl溶液,不需要的仪器是( )
【答案】A
二、填空题。
14、请回答下列与水有关的问题:
(1)生活中常用____________的方法降低水的硬度;
(2)H2O和H2O2都是含氢元素的氧化物,因为____________不同,所以它们的化学性质不同;
(3)实验室中可通过Na2SO4和CaCO3在水中__________ 的不同加以区别。
【答案】煮沸 分子结构 溶解性
15、如图是A、B、C三种固体物质的溶解度曲线,请根据图示回答问题。
(1)t2 ℃时,A、B、C三种物质的溶解度由大到小的顺序为 。
(2)P点表示的意义是 。
(3)三种物质中, 的溶解度受温度的影响最大, 的溶解度随温度的升高而减小。
(4)要将A的不饱和溶液变成饱和溶液,可采取的方法有 (填一种即可)。
(5)将t2 ℃时A、B、C三种物质的饱和溶液降温到t1 ℃,不会析出晶体的是 。
【答案】(1)C>B>A (2)t1 ℃时,A、C两种物质的溶解度相同
(3)C A (4)升高温度(或加入A物质或恒温蒸发溶剂) (5)A
16、如下图所示是配制50g溶质质量分数为15%的氯化钠溶液的操作过程示意图。试回答:
(1)A操作中错误的是 。
(2)B操作中应称量氯化钠的质量是 g,称量时若指针偏右,应进行的操作是 。
(3) D操作中应选用 (10mL、50mL、100mL)量筒量取 mL的水。
(4)E操作的作用是 。
(5)下列错误操作可能导致溶质质量分数小于15%的是(填序号) 。①B操作中砝码和食盐放置颠倒 ②C操作中有固体洒落 ③D操作中有少量水溅出 ④F操作中溶液洒落。
【答案】⑴试剂瓶塞正放 ⑵7.5 添加氯化钠至天平平衡 ⑶50mL,42.5
⑷加速固体溶解 ⑸①②
17、小丽在配制一定溶质质量分数的氯化钠溶液时,计算所需氯化钠的质量和水的体积后,进行了如图所示的实验。
请回答:
(1)操作中不规范的步骤是________(填序号)。
(2)改正后,图示实验中正确的操作顺序是_____________(填序号)。
(3)⑤中玻璃棒的作用是____________________________。
(4)小丽发现图示实验操作步骤不完整,应补充的是__________________。
【答案】(1)③ (2)②①④③⑤
(3)搅拌,加速溶解 (4)装瓶贴标签
18、用下图装置分别进行下列实验,认识物质变化中的能量变化。
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是_______。写出生石灰与水反应的化学方程式_________________________。
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是________ (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
【答案】 生石灰与水反应放出大量热,水温升高,使温度达到白磷的着火点 CaO + H2O = Ca(OH)2 CD
19、炎热的夏天,在家中可以自制汽水来解暑消热。
[准备材料] 1.5 g小苏打、1.5 g柠檬酸、蔗糖、果汁、凉开水、500 mL的饮料瓶。(柠檬酸与小苏打发生反应生成二氧化碳气体)
[配制流程]
下列是制汽水的操作或现象的相关问题,请回答:
Ⅰ.步骤②中为什么要用凉开水制汽水
。
Ⅱ.步骤③旋紧瓶盖后,为什么汽水中的气泡会由多变少直至不再冒出
。
【答案】Ⅰ.凉开水温度较低,二氧化碳的溶解度随温度的降低而增大
Ⅱ.旋紧瓶盖后,瓶内压强增大,二氧化碳的溶解度增大
20、“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一。请回答下列问题:
(1)现欲配制一瓶500 g溶质质量分数为0.9%的生理盐水,需氯化钠固体________g;下列实验操作与目的分析均正确的一组是______(填序号)。
(2)实验室若用15%的氯化钠溶液加水稀释成5%的氯化钠溶液,此时需要用到的玻璃仪器有烧杯、玻璃棒、量筒和________。
(3)实验室若用恒温蒸发溶剂的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示,与丙烧杯中溶液溶质质量分数一定相同的是________(填序号)烧杯中的溶液。
【答案】(1)4.5;D (2)胶头滴管 (3)丁
三、实验题。
21、同学们在学习金属与盐溶液的反应时,老师强调:“金属K、Ca、Na必须除外.”化学兴趣小组的同学们对此产生了兴趣,并在老师的指导下,进行如下探究:
【提出问题】将金属钠投入到硫酸铜溶液中,结果会怎样?
【查找资料】(1)少量钠通常保存在煤油中;(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3(3)钠是一种很活泼的金属,遇水发生剧烈反应,生成氢氧化钠和氢气。
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜;
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜。
【实验探究】
实验操作 实验现象
①取10ml一定溶质质量分数的硫酸铜溶液,倒入50ml的烧杯里②取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,析出蓝色沉淀
(1)【现象分析】①钠熔成小球是因为________。
②钠球游动,发出“嘶嘶”声响说明有气体产生。
③析出蓝色沉淀是因为________ (用化学方程式表示)
(2)【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
实验操作 实验现象 结论
取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 沉淀全部溶解,溶液变蓝色 ________
(3)【实验结论】在金属活动性顺序里,位于前面的金属(K、Ca、Na必须除外)能把位于后面的金属从它们盐的溶液里置换出来.K、Ca、Na必须除外是因为________ 。
【答案】(1)钠与水发生剧烈反应,反应放出的热量使钠熔化成小球;2Na+2H2O=2NaOH+H2↑,2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
(2)说明沉淀中不含红色的铜
(3)K、Ca、Na盐溶液的反应先是和里面的水的反应生成碱和氢气
四、计算题。
22、20℃时,KNO3的溶解度为31.6g,将20g KNO3投进50g水中,充分搅拌,制成20℃时的溶液,求该溶液中溶质的质量分数。
【答案】24%
同课章节目录
