物质的分离与提纯
图片预览






文档简介
课件19张PPT。物质的分离与提纯-----粗盐提纯“吹尽黄沙始见金”
如何分离出铁铜混合物中的铁屑?常用的分离方法有那些?过滤、蒸发、结晶、洗气瓶洗气、用酸除去杂质、等等思考:这些方法是依据什么性质
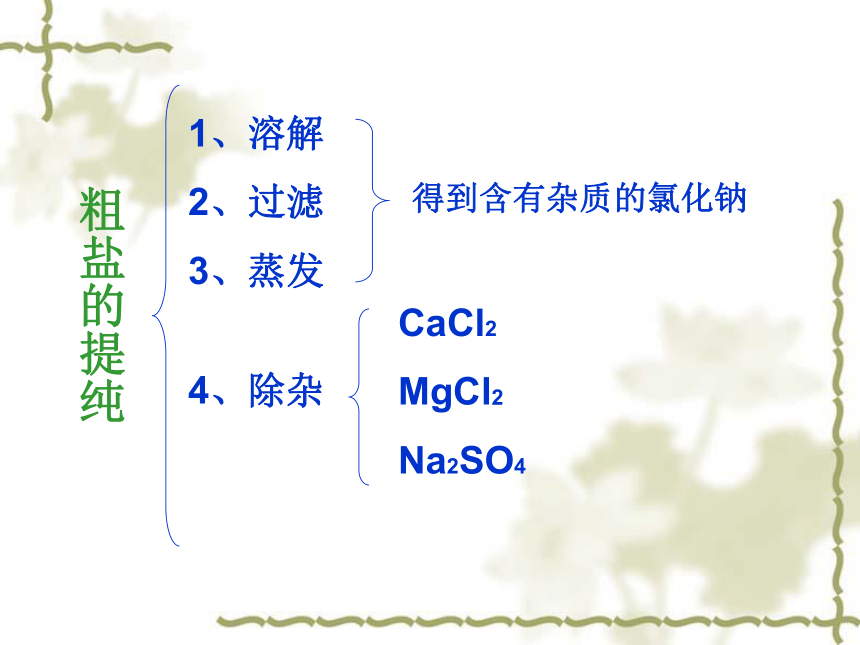
进行分离和提纯的?问题化学上的杂质都是有害和无价值的吗?用海水煮盐得到的粗盐中含有较多的杂质,如不溶性的泥沙,可溶性的CaCl2、MgCl2及一些硫酸盐。问题:如何除去食盐中的泥沙?通过溶解、过滤、蒸发操作之后,得到的固体就是纯净的食盐了吗? 过滤粗盐溶解悬浊液(泥沙、NaCl、MgCl2、CaCl2、硫酸盐)不溶性杂质NaCl、MgCl2、CaCl2、硫酸盐的溶液粗盐的提纯溶 解 主要的仪器:玻璃棒、烧杯玻璃棒的作用:搅拌、加速溶解过 滤主要仪器:玻璃棒、漏斗(滤纸)、铁架台(铁圈)、烧杯玻璃棒的作用:引流、一贴、两低、三靠
多次过滤使滤液澄清---用于分离固液混合物 蒸 发 主要的仪器:玻璃棒、蒸发皿、酒精灯、铁架台(铁圈)玻璃棒的作用:
搅拌、防止局部温度过高,
液滴飞溅---用于分离溶于溶剂中的溶质注意事项:
1、安装装置顺序:从下到上,从
左到右
2、2/3
3、直接加热
4、玻璃棒搅拌
5、加热到大量固体析出时,停止
加热,用余热来蒸干剩余的液体
6、热的蒸发皿不能放在试验台
上,要垫石棉网 思考与交流化学除杂除杂原则:
*不增(尽量少引入新杂质)
*不减(不损耗样品)
*易分(容易分离——生成完全不溶物)
*复原(除去各种过量杂质,还原到目标产物)注意:除杂试剂要适当过量;设计所加试剂的先后顺序!1、只要Na2CO3加在BaCl2之后便合理
2、最后加入的盐酸只能适量NaCl
CaCl2
MgCl2
Na2SO4
NaCl
CaCl2
MgCl2
BaCl2NaCl
MgCl2
Na2CO3NaCl
NaOH
Na2CO3
NaCl
HClNaCl过量NaOH过量HCl加热蒸发离子的检验:1、原理:
根据物质的物理性质(如颜色、状态、气味、密度等)或化学性质(生成气体↑、沉淀↓等特殊现象)2、步骤:
(1)先对试样的外观进行观察(颜色、状态)
(2)将试样(固体)配成溶液,取出少许进行检验
(3 )选择合理的试剂(反应灵敏、现象明显)
(4)注意排除某些共有现象的干扰。
SO42-的检验方法: 操作:先加入稀HCl 酸化,再加入可溶性钡盐(BaCl2)溶液。现象:出现不溶于稀盐酸的白色沉淀
(BaSO4)。结论:存在硫酸根离子。 注意排除CO32-等离子的干扰!Cl-的检验方法: 操作:先加入稀HNO3酸化,再加入几滴AgNO3溶液。现象:出现不溶于稀硝酸的白色沉淀
(AgCl)。结论:存在氯离子。 注意排除CO32-离子的干扰!例题:某KNO3溶液中含杂质KCl、K2SO4和Ca(NO3)2,现欲除去杂质,得到纯净的KNO3溶液,则加入试剂的正确顺序是:A.Ba(NO3)2、K2CO3、AgNO3、HNO3
B.K2CO3、Ba(NO3)2、AgNO3、HNO3
C.Ba(NO3)2、AgNO3、K2CO3、HNO3
D.AgNO3、Ba(NO3)2、K2CO3、HNO3答案:CD讨论:下列检验未知溶液中是否含有SO42-的操作,所得结论是否可靠?方法二:未知液 白↓ 不溶稀HNO3Ba(NO3)2方法一:未知液 白↓ 不溶稀HClBaCl2方法三:未知液 白↓HNO3酸化BaCl2方法四:未知液 白↓HCl酸化BaCl2或Ba(NO3)2方法五:未知液 白↓ 不溶Ba(NO3)2过滤洗涤沉淀中加HCl
如何分离出铁铜混合物中的铁屑?常用的分离方法有那些?过滤、蒸发、结晶、洗气瓶洗气、用酸除去杂质、等等思考:这些方法是依据什么性质
进行分离和提纯的?问题化学上的杂质都是有害和无价值的吗?用海水煮盐得到的粗盐中含有较多的杂质,如不溶性的泥沙,可溶性的CaCl2、MgCl2及一些硫酸盐。问题:如何除去食盐中的泥沙?通过溶解、过滤、蒸发操作之后,得到的固体就是纯净的食盐了吗? 过滤粗盐溶解悬浊液(泥沙、NaCl、MgCl2、CaCl2、硫酸盐)不溶性杂质NaCl、MgCl2、CaCl2、硫酸盐的溶液粗盐的提纯溶 解 主要的仪器:玻璃棒、烧杯玻璃棒的作用:搅拌、加速溶解过 滤主要仪器:玻璃棒、漏斗(滤纸)、铁架台(铁圈)、烧杯玻璃棒的作用:引流、一贴、两低、三靠
多次过滤使滤液澄清---用于分离固液混合物 蒸 发 主要的仪器:玻璃棒、蒸发皿、酒精灯、铁架台(铁圈)玻璃棒的作用:
搅拌、防止局部温度过高,
液滴飞溅---用于分离溶于溶剂中的溶质注意事项:
1、安装装置顺序:从下到上,从
左到右
2、2/3
3、直接加热
4、玻璃棒搅拌
5、加热到大量固体析出时,停止
加热,用余热来蒸干剩余的液体
6、热的蒸发皿不能放在试验台
上,要垫石棉网 思考与交流化学除杂除杂原则:
*不增(尽量少引入新杂质)
*不减(不损耗样品)
*易分(容易分离——生成完全不溶物)
*复原(除去各种过量杂质,还原到目标产物)注意:除杂试剂要适当过量;设计所加试剂的先后顺序!1、只要Na2CO3加在BaCl2之后便合理
2、最后加入的盐酸只能适量NaCl
CaCl2
MgCl2
Na2SO4
NaCl
CaCl2
MgCl2
BaCl2NaCl
MgCl2
Na2CO3NaCl
NaOH
Na2CO3
NaCl
HClNaCl过量NaOH过量HCl加热蒸发离子的检验:1、原理:
根据物质的物理性质(如颜色、状态、气味、密度等)或化学性质(生成气体↑、沉淀↓等特殊现象)2、步骤:
(1)先对试样的外观进行观察(颜色、状态)
(2)将试样(固体)配成溶液,取出少许进行检验
(3 )选择合理的试剂(反应灵敏、现象明显)
(4)注意排除某些共有现象的干扰。
SO42-的检验方法: 操作:先加入稀HCl 酸化,再加入可溶性钡盐(BaCl2)溶液。现象:出现不溶于稀盐酸的白色沉淀
(BaSO4)。结论:存在硫酸根离子。 注意排除CO32-等离子的干扰!Cl-的检验方法: 操作:先加入稀HNO3酸化,再加入几滴AgNO3溶液。现象:出现不溶于稀硝酸的白色沉淀
(AgCl)。结论:存在氯离子。 注意排除CO32-离子的干扰!例题:某KNO3溶液中含杂质KCl、K2SO4和Ca(NO3)2,现欲除去杂质,得到纯净的KNO3溶液,则加入试剂的正确顺序是:A.Ba(NO3)2、K2CO3、AgNO3、HNO3
B.K2CO3、Ba(NO3)2、AgNO3、HNO3
C.Ba(NO3)2、AgNO3、K2CO3、HNO3
D.AgNO3、Ba(NO3)2、K2CO3、HNO3答案:CD讨论:下列检验未知溶液中是否含有SO42-的操作,所得结论是否可靠?方法二:未知液 白↓ 不溶稀HNO3Ba(NO3)2方法一:未知液 白↓ 不溶稀HClBaCl2方法三:未知液 白↓HNO3酸化BaCl2方法四:未知液 白↓HCl酸化BaCl2或Ba(NO3)2方法五:未知液 白↓ 不溶Ba(NO3)2过滤洗涤沉淀中加HCl
同课章节目录
- 专题一 物质的分离与提纯
- 课题1 海带中碘元素的分离及检验
- 拓展课题1-1 茶叶中某些元素的鉴定
- 课题2 用纸层析法分离铁离子和铜离子
- 拓展课题1-2 菠菜的叶绿体中色素的提取和分离
- 拓展课题1-3 用粉笔进行层析分离
- 课题3 硝酸钾晶体的制备
- 拓展课题1-4 粗盐提纯
- 专题二 物质性质的研究
- 课题1 铝及其化合物的性质
- 拓展课题2-1 铝热反应
- 课题2 乙醇和苯酚的性质
- 拓展课题2-2 苯酚与甲醛的反应
- 专题三 物质的检验与鉴别
- 课题1 牙膏和火柴中某些成分的检验
- 拓展课题3-1 新装修居室内空气中甲醛浓度的检测
- 拓展课题3-2 汽车尾气成分的检验
- 课题2 亚硝酸钠和食盐的鉴别
- 拓展课题3-3 真假碘盐的鉴别
- 专题四 化学反应条件的控制
- 课题1 硫代硫酸钠与酸反应速率的影响因素
- 拓展课题4-1 “蓝瓶子”实验
- 课题2 催化剂对过氧化氢分解反应速率的影响
- 拓展课题4-2 过氧化氢酶的催化作用
- 拓展课题4-3 蔗糖的燃烧
- 课题3 反应条件对化学平衡的影响
- 拓展课题4-4 淀粉与碘显色现象的探究
- 拓展课题4-5 压强对化学平衡的影响
- 专题五 电化学问题研究
- 课题1 原电池
- 拓展课题5-1 干电池模拟实验
- 课题2 电解与电镀
- 拓展课题5-2 阿伏加德罗常数的测定
- 专题六 物质的定量分析
- 课题1 食醋总酸含量的测定
- 拓展课题6-1 配制并标定氢氧化钠溶液
- 课题2 镀锌铁皮锌镀层厚度的测定
- 拓展课题6-2 水果中维生素C含量的测定
- 专题七 物质的制备与合成
- 课题1 硫酸亚铁铵的制备
- 拓展课题7-1 用制氢废液制备硫酸锌晶体
- 课题2 阿司匹林的合成
- 拓展课题7-2 对氨基苯磺酸的合成
