高中化学人教版(2019)选择性必修3:4.2 蛋白质 第一课时 课件(共18张ppt)
文档属性
| 名称 | 高中化学人教版(2019)选择性必修3:4.2 蛋白质 第一课时 课件(共18张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-10 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
人教版化学选择性必修3
第四章 生物大分子
第二节 蛋白质
第1课时
一、氨基酸
氨基
氨基(—NH2)和羧基(—COOH)
α-氨基酸:羧基碳相连接的碳原子上的氢原子
被氨基取代的产物
组成蛋白质的氨基酸几乎都是α-氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
CH2—COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
(3)常见的氨基酸
无色
晶体
较高
2.物理性质
一般能溶于水
能溶于强酸、强碱溶液
难溶于乙醇、乙醚等有机溶剂
颜 色:
状 态:
熔 点:
溶解性
【想一想】
从氨基酸的结构分析,氨基酸可能具有怎样的化学性质?
R–CH–COOH
NH2
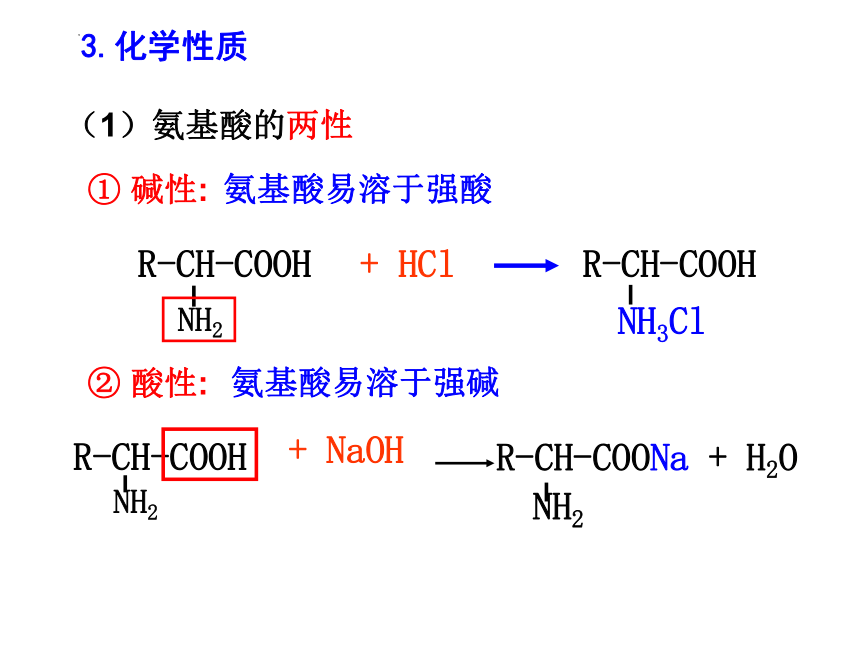
3.化学性质
(1)氨基酸的两性
① 碱性:
② 酸性:
R-CH-COOH
NH3Cl
R-CH-COOH
NH2
+ HCl
R-CH-COONa + H2O
NH2
R-CH-COOH
NH2
+ NaOH
氨基酸易溶于强碱
氨基酸易溶于强酸
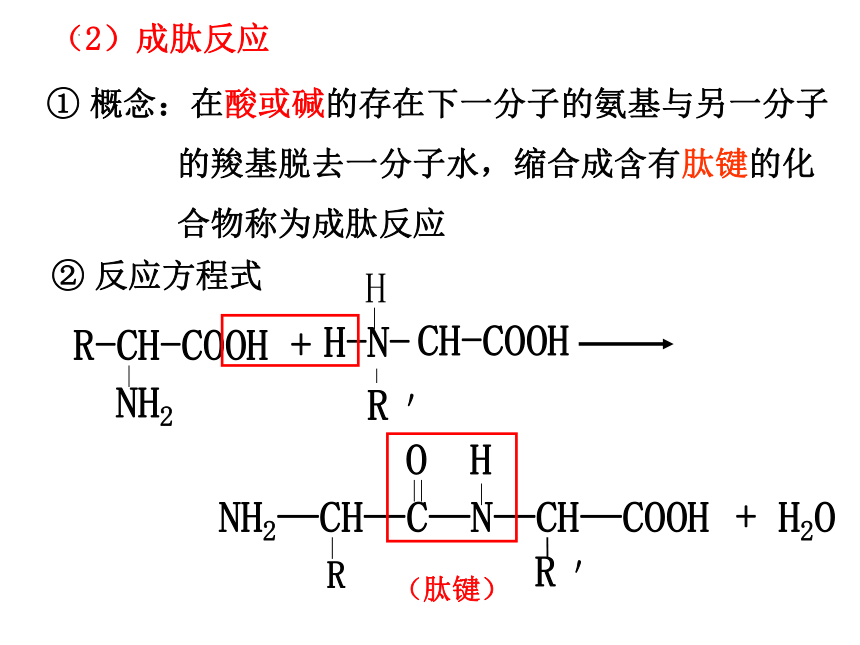
(2)成肽反应
① 概念:在酸或碱的存在下一分子的氨基与另一分子
的羧基脱去一分子水,缩合成含有肽键的化
合物称为成肽反应
② 反应方程式
R-CH-COOH +
NH2
CH-COOH
H-N-
R '
H
+ H2O
R '
NH2—CH—C—N—CH—COOH
R
O
H
(肽键)
二肽 :由二个氨基酸分子消去一个水分子而形成含
一个肽键的化合物
多肽:由许多个氨基酸分子消去多个水分子而形成含
许多个肽键的化合物
(M<1万)
(M>1万)
氨基酸
二肽
脱水
多肽
蛋白质
脱水
脱水
二、蛋白质
天然有机高分子化合物
胶体
—NH2
—COOH
能与酸反应又能与碱反应
两性分子
C、H、O、N
S、P
Fe、Cu、Zn、Mn
酸、碱或酶
多肽
氨基酸
α 氨基酸
氨基酸
二肽
脱水
多肽
蛋白质
脱水
脱水
水解
水解
水解
浓盐溶液
(NH4)2SO4
溶解度
分离、提纯蛋白质
(3)盐析 P112实验4-3
实验 操作
实验 现象 试管①中出现白色沉淀;试管②中白色沉淀消失
(4)变性 P112实验4-4
物理、化学性质和生理功能
加热
紫外线
超声波
强酸 强碱 重金属盐 乙醇 福尔马林
生理活性
不能再溶解
不可逆
【思考与讨论】(P113页)因误服铅、汞等重金属盐中毒的患者在急救时,为什么可口服牛奶、蛋清、或豆浆
提示:蛋清、牛奶、豆浆中含有丰富的蛋白质,重金属离子破坏这些食物中的蛋白质,而减少对病人本身蛋白质的损伤。
盐析 变性
变化条件
变化性质
变化过程
用 途
浓的无机盐溶液
受热、紫外线、酸、碱、
重金属盐和某些有机物
物理变化
(溶解度降低)
化学变化
(蛋白质性质改变)
可逆
不可逆
分离提纯
杀菌消毒
概念对比
(5)显色反应 实验4-5
实验结论:
显色反应:含有苯环的蛋白质遇到浓硝酸呈黄色。除了硝酸,其他一些试剂也可以与蛋白质作用,呈现特定的颜色,可用于蛋白质的分析检测。
(6)蛋白质灼烧有类似烧焦羽毛的气味。
细胞
催化
蛋白质
条件温和不需加热
专一性
高效催化
三、酶
课堂小结
一.氨基酸
结构
氨基(—NH2)
羧基(—COOH)
化学性质
氨基酸的两性
成肽反应
二. 蛋白质
蛋白质的存在与组成
蛋白质的结构
蛋白质的性质
两性
水解
盐析
变性
颜色反应
灼烧
水解
缩合
人教版化学选择性必修3
第四章 生物大分子
第二节 蛋白质
第1课时
一、氨基酸
氨基
氨基(—NH2)和羧基(—COOH)
α-氨基酸:羧基碳相连接的碳原子上的氢原子
被氨基取代的产物
组成蛋白质的氨基酸几乎都是α-氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
CH2—COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
(3)常见的氨基酸
无色
晶体
较高
2.物理性质
一般能溶于水
能溶于强酸、强碱溶液
难溶于乙醇、乙醚等有机溶剂
颜 色:
状 态:
熔 点:
溶解性
【想一想】
从氨基酸的结构分析,氨基酸可能具有怎样的化学性质?
R–CH–COOH
NH2
3.化学性质
(1)氨基酸的两性
① 碱性:
② 酸性:
R-CH-COOH
NH3Cl
R-CH-COOH
NH2
+ HCl
R-CH-COONa + H2O
NH2
R-CH-COOH
NH2
+ NaOH
氨基酸易溶于强碱
氨基酸易溶于强酸
(2)成肽反应
① 概念:在酸或碱的存在下一分子的氨基与另一分子
的羧基脱去一分子水,缩合成含有肽键的化
合物称为成肽反应
② 反应方程式
R-CH-COOH +
NH2
CH-COOH
H-N-
R '
H
+ H2O
R '
NH2—CH—C—N—CH—COOH
R
O
H
(肽键)
二肽 :由二个氨基酸分子消去一个水分子而形成含
一个肽键的化合物
多肽:由许多个氨基酸分子消去多个水分子而形成含
许多个肽键的化合物
(M<1万)
(M>1万)
氨基酸
二肽
脱水
多肽
蛋白质
脱水
脱水
二、蛋白质
天然有机高分子化合物
胶体
—NH2
—COOH
能与酸反应又能与碱反应
两性分子
C、H、O、N
S、P
Fe、Cu、Zn、Mn
酸、碱或酶
多肽
氨基酸
α 氨基酸
氨基酸
二肽
脱水
多肽
蛋白质
脱水
脱水
水解
水解
水解
浓盐溶液
(NH4)2SO4
溶解度
分离、提纯蛋白质
(3)盐析 P112实验4-3
实验 操作
实验 现象 试管①中出现白色沉淀;试管②中白色沉淀消失
(4)变性 P112实验4-4
物理、化学性质和生理功能
加热
紫外线
超声波
强酸 强碱 重金属盐 乙醇 福尔马林
生理活性
不能再溶解
不可逆
【思考与讨论】(P113页)因误服铅、汞等重金属盐中毒的患者在急救时,为什么可口服牛奶、蛋清、或豆浆
提示:蛋清、牛奶、豆浆中含有丰富的蛋白质,重金属离子破坏这些食物中的蛋白质,而减少对病人本身蛋白质的损伤。
盐析 变性
变化条件
变化性质
变化过程
用 途
浓的无机盐溶液
受热、紫外线、酸、碱、
重金属盐和某些有机物
物理变化
(溶解度降低)
化学变化
(蛋白质性质改变)
可逆
不可逆
分离提纯
杀菌消毒
概念对比
(5)显色反应 实验4-5
实验结论:
显色反应:含有苯环的蛋白质遇到浓硝酸呈黄色。除了硝酸,其他一些试剂也可以与蛋白质作用,呈现特定的颜色,可用于蛋白质的分析检测。
(6)蛋白质灼烧有类似烧焦羽毛的气味。
细胞
催化
蛋白质
条件温和不需加热
专一性
高效催化
三、酶
课堂小结
一.氨基酸
结构
氨基(—NH2)
羧基(—COOH)
化学性质
氨基酸的两性
成肽反应
二. 蛋白质
蛋白质的存在与组成
蛋白质的结构
蛋白质的性质
两性
水解
盐析
变性
颜色反应
灼烧
水解
缩合
