2021-2022学年人教版化学九年级上册第六单元碳和碳的氧化物专题测评试卷(word版 含解析)
文档属性
| 名称 | 2021-2022学年人教版化学九年级上册第六单元碳和碳的氧化物专题测评试卷(word版 含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 168.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-11 00:00:00 | ||
图片预览


文档简介
九年级上册第六单元碳和碳的氧化物专题测评
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、归纳和整理是化学学科的一种学习方法。在学习了碳和碳的氧化物的相关知识后,学习小组进行了如下知识整理,其中合理的是
A.金刚石和石墨都具有良好的导电性
B.二氧化碳和一氧化碳都具有还原性
C.二氧化碳用于灭火,既利用它的物理性质,又利用它的化学性质
D.一氧化碳和二氧化碳的组成元素相同,则二者的化学性质一定相同
2、化学与生产、生活密切相关,下列说法正确的是
A.食物的腐烂变质与动植物的新陈代谢均为氧化反应
B.进入菜窖前应先检验窖内二氧化碳的浓度,目的是防止二氧化碳中毒
C.用肥皂水检验硬水和软水,硬水泡沫多,软水泡沫少
D.石油的分馏得到多种化工产品,是利用各物质的熔点不同
3、物质的用途主要由其化学性质决定的是
A.活性炭吸附异味 B.干冰作制冷剂
C.稀有气体作保护气 D.金刚石切割玻璃
4、下列用途既利用其物理性质又利用其化学性质的是
A.活性炭用于防毒面具吸附毒气 B.干冰用于人工降雨
C.一氧化碳作燃料 D.二氧化碳用于灭火
5、 “碳中和”是指一定时间内排放的碳总量与吸收的碳总量相互抵消,实现“碳”零排放。下列不利于实现“碳中和”的是
A.大力植树造林 B.使用风能、太阳能等绿色能源
C.露天焚烧玉米桔梗 D.生活垃圾分类处理
6、鉴别与除杂是化学实验的重要内容,下列设计的方案不能达到实验目的是
A.鉴别蒸馏水和MgCl2溶液—加入肥皂水振荡,观察产生泡沫情况
B.除去CO2中混有的少量CO—通入过量氧气,点燃
C.除去氮气中混有的少量氧气—将混合气体缓慢通过灼热的铜网
D.鉴别水和过氧化氢溶液两种液体—加二氧化锰,观察产生气泡情况
7、为探究影响化学反应速度的因素,使用等量的同种钙片和同体积、同浓度的白醋开展四组实验,产生的二氧化碳的浓度随时间变化的关系如图所示。选取CO2的浓度从0-8%为研究对象,实验结果的分析错误的是
A.对比①③,温度越高,反应速率越快
B.对比②③,反应物接触面积越小,反应速率越慢
C.对比③④,反应物接触面积越大,反应速率越快
D.温度和反应物接触面积都会影响化学反应速度
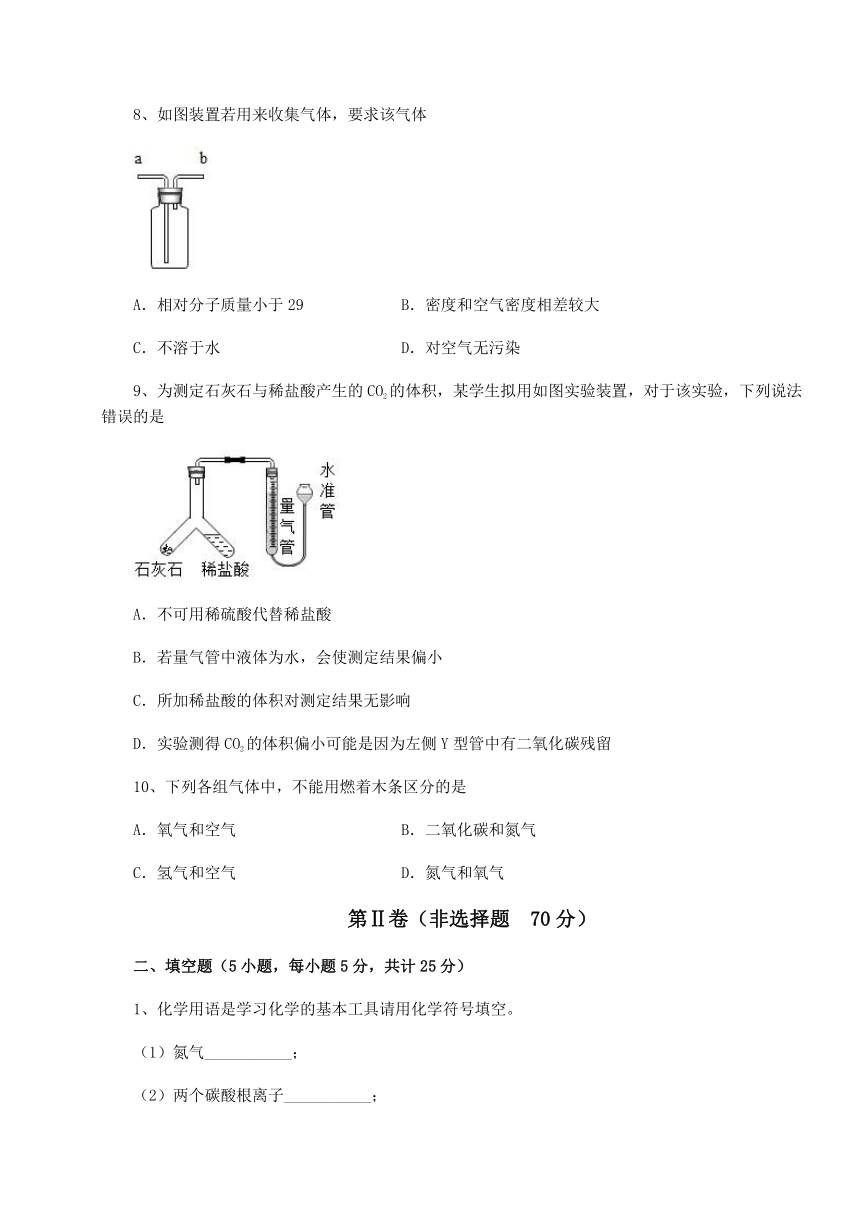
8、如图装置若用来收集气体,要求该气体
A.相对分子质量小于29 B.密度和空气密度相差较大
C.不溶于水 D.对空气无污染
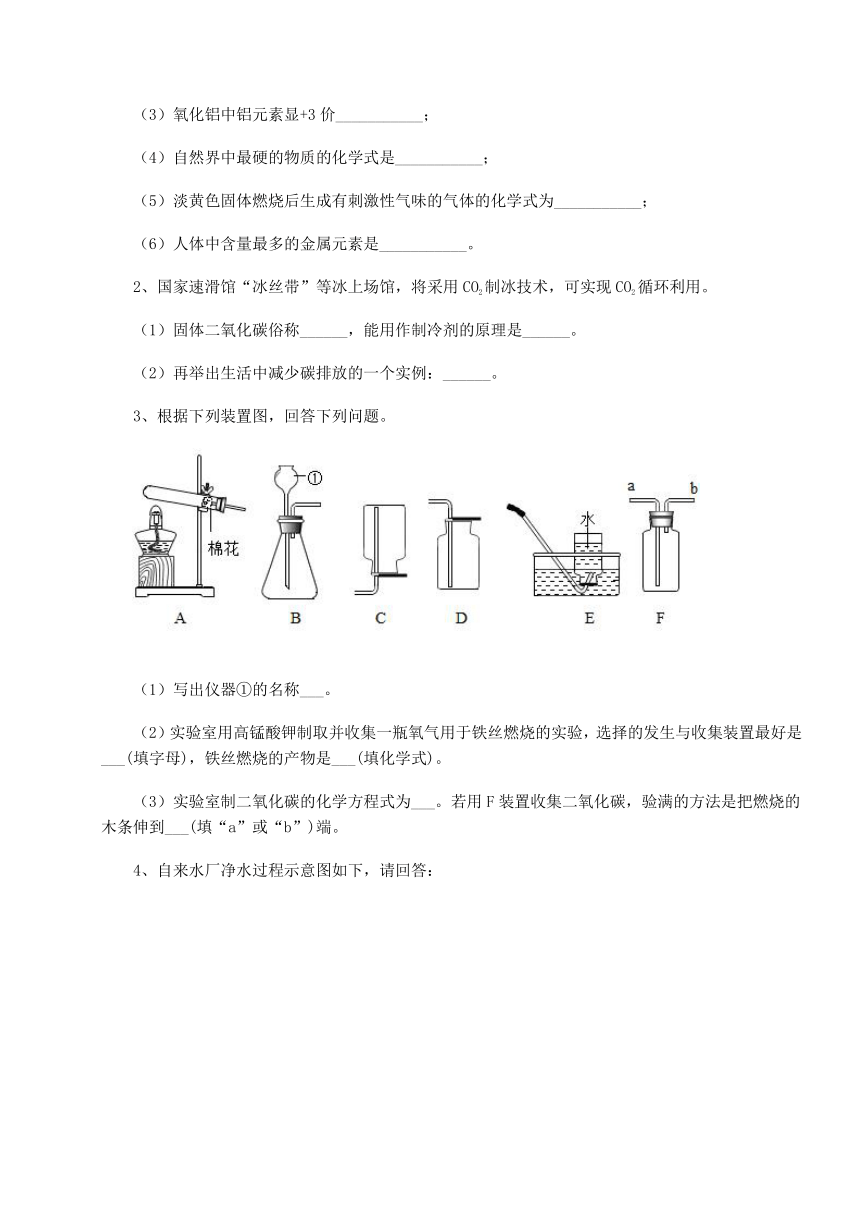
9、为测定石灰石与稀盐酸产生的CO2的体积,某学生拟用如图实验装置,对于该实验,下列说法错误的是
A.不可用稀硫酸代替稀盐酸
B.若量气管中液体为水,会使测定结果偏小
C.所加稀盐酸的体积对测定结果无影响
D.实验测得CO2的体积偏小可能是因为左侧Y型管中有二氧化碳残留
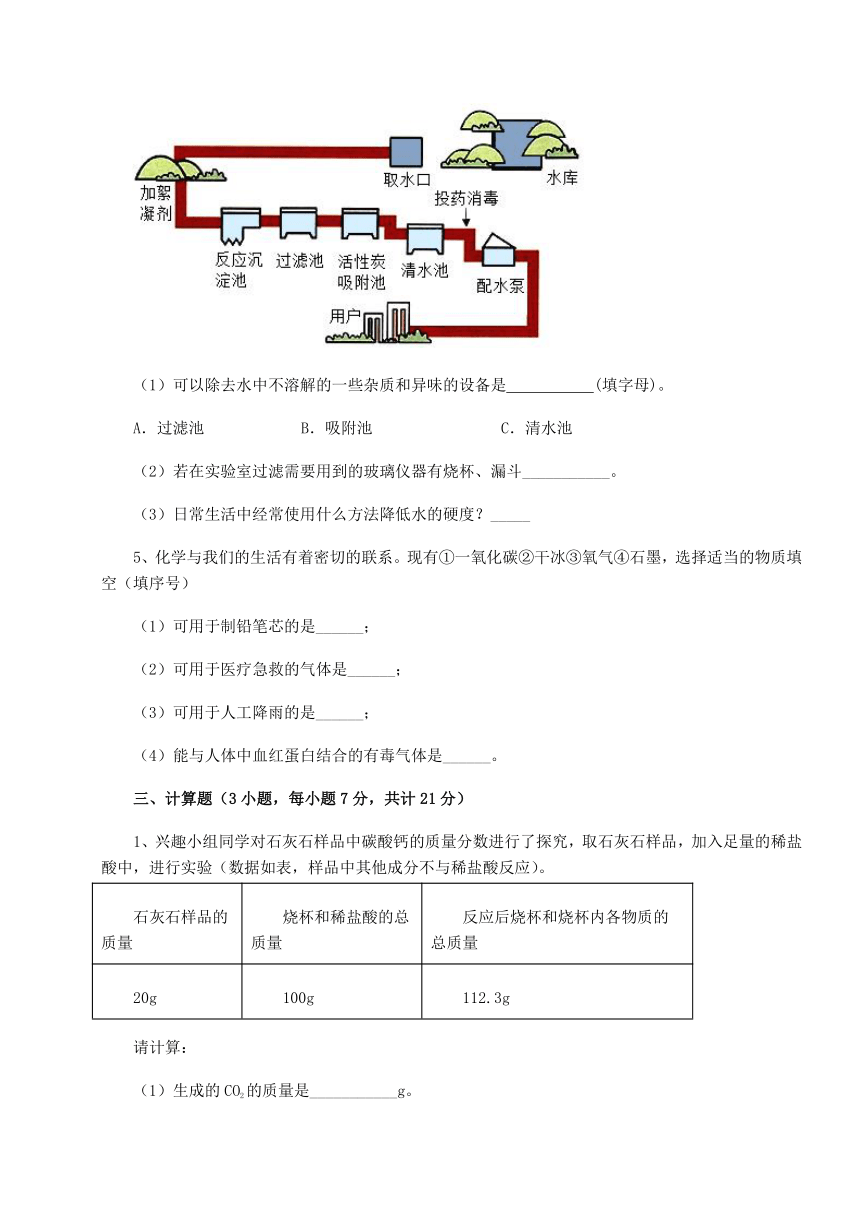
10、下列各组气体中,不能用燃着木条区分的是
A.氧气和空气 B.二氧化碳和氮气
C.氢气和空气 D.氮气和氧气
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题5分,共计25分)
1、化学用语是学习化学的基本工具请用化学符号填空。
(1)氮气___________;
(2)两个碳酸根离子___________;
(3)氧化铝中铝元素显+3价___________;
(4)自然界中最硬的物质的化学式是___________;
(5)淡黄色固体燃烧后生成有刺激性气味的气体的化学式为___________;
(6)人体中含量最多的金属元素是___________。
2、国家速滑馆“冰丝带”等冰上场馆,将采用CO2制冰技术,可实现CO2循环利用。
(1)固体二氧化碳俗称______,能用作制冷剂的原理是______。
(2)再举出生活中减少碳排放的一个实例:______。
3、根据下列装置图,回答下列问题。
(1)写出仪器①的名称___。
(2)实验室用高锰酸钾制取并收集一瓶氧气用于铁丝燃烧的实验,选择的发生与收集装置最好是___(填字母),铁丝燃烧的产物是___(填化学式)。
(3)实验室制二氧化碳的化学方程式为___。若用F装置收集二氧化碳,验满的方法是把燃烧的木条伸到___(填“a”或“b”)端。
4、自来水厂净水过程示意图如下,请回答:
(1)可以除去水中不溶解的一些杂质和异味的设备是 (填字母)。
A.过滤池 B.吸附池 C.清水池
(2)若在实验室过滤需要用到的玻璃仪器有烧杯、漏斗___________。
(3)日常生活中经常使用什么方法降低水的硬度?_____
5、化学与我们的生活有着密切的联系。现有①一氧化碳②干冰③氧气④石墨,选择适当的物质填空(填序号)
(1)可用于制铅笔芯的是______;
(2)可用于医疗急救的气体是______;
(3)可用于人工降雨的是______;
(4)能与人体中血红蛋白结合的有毒气体是______。
三、计算题(3小题,每小题7分,共计21分)
1、兴趣小组同学对石灰石样品中碳酸钙的质量分数进行了探究,取石灰石样品,加入足量的稀盐酸中,进行实验(数据如表,样品中其他成分不与稀盐酸反应)。
石灰石样品的质量 烧杯和稀盐酸的总质量 反应后烧杯和烧杯内各物质的总质量
20g 100g 112.3g
请计算:
(1)生成的CO2的质量是___________g。
(2)样品中碳酸钙的质量分数。(写出计算过程)
2、将16g氧化铜与足量的碳粉高温加热至完全反应后,可以得到多少克铜?(C:12, O:16, Cu:64)
3、某实验小组的同学为了测定大理石样品中碳酸钙的纯度,取了一定量的大理石样品放置于烧杯中(烧杯重50g)然后向烧杯中滴加一定溶质质量分数的稀盐酸。实验测得烧杯中物质的总质量与加入稀盐酸的质量关系如图所示。求:
(1)当加入___________g稀盐酸时,大理石中碳酸钙刚好反应完;
(2)大理石中碳酸钙的质量分数(写出计算过程,结果精确到0.1%)。
四、实验探究(2小题,每小题12分,共计24分)
1、在学习了“碳的化学性质”后,我校化学兴趣小组的同学在老师的指导下进行“用木炭还原氧化铜”的实验。装置如图所示,请你和他们一起完成下列探究任务。
(查阅资料)此实验最好使用酒精喷灯,也可以在酒精灯火焰上罩网罩,目的是___________。
(收集证据)右侧试管中观察到的现象是___________。
(提出问题)实验结束并冷却至室温后,试管内固体成分是什么?
(猜想与假设)甲同学的猜想:铜
乙同学的猜想:氧化铜和碳
丙同学的猜想:铜、氧化铜和碳
丁同学的猜想:铜和碳
你的猜想___________。
(收集证据)同学们一致认为,__________同学的猜想错误,原因是(用化学方程式表示)__________。在老师的帮助下,同学们确定了丙同学的猜想正确。
(反思与评价)通过对此次探究活动的分析可以得出:对反应后固体成分猜想的一般思路是___________一定存在、固体反应物可能存在、对于固体反应物是两种(或不是一种)且需要一定反应条件才能发生的反应,固体反应物可以同时剩余。
2、兴趣小组同学在做镁与盐反应的实验时,不小心将镁条加到饱和的碳酸氢钠溶液中,意外发现溶液中有白色不溶物生成。同学们对白色不溶物的成分产生了浓厚兴趣,于是在老师的帮助下进行了如下的探究。
(提出问题)白色不溶物是什么物质?
(猜想与假设)
猜想①是Mg(OH)2;猜想②是MgCO3;猜想③是Mg(OH)2和MgCO3的混合物
(查阅资料)
①MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
②白色无水硫酸铜遇水变蓝。
③碱石灰是固体氢氧化钠和氧化钙的混合物。
(实验验证)取适量干燥的白色不溶物,充分加热,并使分解产生的气体依次通过如图1所示装置(每步反应都完全)。
(实验现象)装置A中______,装置B中______。
(实验结论)猜想③正确。请写出Mg(OH)2受热分解的化学方程式______。
(拓展探究)直接向白色不溶物中滴加足量______,也能检验MgCO3的存在。
同学们为了进一步测定白色不溶物中各组分的质量关系,继续进行了下列探究。
称取干燥的白色不溶物36.8g,充分加热至不再产生气体,并使分解产生的气体全部被如图2所示装置C和D吸收。
(实验数据)实验后装置C增重3.6g,装置D增重13.2g。
(实验结论)若上述白色不溶物的组成用xMg(OH)2·yMgCO3表示,则x:y=______。
(反思评价)实验后,同学们经过讨论交流,发现实验方案可进一步优化,下列优化方案正确的是______(填序号)。
①只称量装置C、D增重的质量,不称量白色不溶物的质量
②去掉装置D,只称量白色不溶物和装置C增重的质量
③去掉装置C,只称量白色不溶物和装置D增重的质量
-参考答案-
一、单选题
1、C
【详解】
A、石墨具有良好的导电性,金刚石不具有导电性,不符合题意;
B、一氧化碳具有还原性,二氧化碳不具有还原性,不符合题意;
C、二氧化碳用于灭火,是因为二氧化碳不燃烧、不支持燃烧,密度比空气大,不燃烧、不支持燃烧属于化学性质,密度属于物理性质,符合题意;
D、一氧化碳和二氧化碳元素组成相同,但是分子构成不同,故化学性质不同,不符合题意。
故选C。
2、A
【详解】
A.食物的腐烂变质与动植物的新陈代谢均与氧气发生反应,故均为氧化反应,正确;
B.因为二氧化碳不能供给呼吸,所以进入菜窖前应先检验窖内二氧化碳的浓度,查看是否超标,错误;
C.用肥皂水检验硬水和软水,产生泡沫多、浮渣少的是软水,产生泡沫少、浮渣多的是硬水,错误;
D.石油的分馏得到多种化工产品,是利用各物质的沸点不同,而不是熔点,错误;
故选A。
【点睛】
3、C
【详解】
A、活性炭结构疏松多孔,具有吸附性,属于物理性质,故A错误;
B、干冰做制冷剂是利用其升华吸热的特点,属于物理性质,故B错误;
C、稀有气体化学性质很稳定,故用做保护气,是利用其化学性质,故C正确;
D、金刚石切割玻璃是利用其硬度大的特点,属于其物理性质,故D错误;
故选C。
4、D
【分析】
本题考查碳及其化合物的用途,结构决定性质,性质决定用途。
【详解】
A、活性炭疏松多孔,表面积大,吸附性强,用于防毒面具,只利用了物理性质,A不符合题意;
B、干冰是二氧化碳的固态形式,升华时能吸收大量热,用于人工降雨,只利用了物理性质,B不符合题意;
C、一氧化碳具有可燃性,可用作燃料,只利用了化学性质,C不符合题意;
D、二氧化碳用于灭火,既利用了二氧化碳密度比空气大的物理性质,又利用了二氧化碳不能燃烧,不支持燃烧的化学性质,D符合题意。
故选D。
5、C
【详解】
A. \大力植树造林,有利于实现“碳中和”,不符合题意;
B. 使用风能、太阳能等绿色能源,有利于实现“碳中和”,不符合题意;
C. 露天焚烧玉米桔梗产生大量二氧化碳,不利于实现“碳中和”,符合题意;
D. 生活垃圾分类处理,有利于实现“碳中和”,不符合题意。
故选C。
6、B
【详解】
A、蒸馏水是软水,加入肥皂水振荡,产生较多泡沫,MgCl2溶液中加入肥皂水振荡,产生较少泡沫,能达到实验目;
B、二氧化碳不燃烧,不支持燃烧,一氧化碳含量较少,通入过量氧气,一氧化碳不能点燃且引入新杂质氧气,不能达到实验目;
C、将混合气体缓慢通过灼热的铜网,铜和氧气反应生成氧化铜,氮气不参加反应,能达到实验目;
D、过氧化氢溶液中加二氧化锰生成水和氧气,产生较多气泡,水中加二氧化锰不反应,不产生气泡,可以鉴别,能达到实验目。
故选B。
7、B
【详解】
A、从图象对比①③可看出,①③其他条件相同,只有温度不同,在相同时间内,①生成二氧化碳的浓度大于③生成二氧化碳的浓度,由此说明温度越高,反应速率越快;故选项正确;
B、从图象对比②③可看出,钙片的形状不同,温度不同,因此无法比较;故选项错误;
C、从图象对比③④可看出,③④其他条件相同,只有钙片的形状不同,在相同时间内,③生成二氧化碳的浓度大于④生成二氧化碳的浓度,由此说明反应物接触面积越大,反应速率越快;故选项正确;
D、从图象可看出,温度和反应物接触面积都会影响化学反应速度;故选项正确。
故选:B。
8、B
【详解】
该收集方法为向上排空气法(长进短出)或向下排空气法(短进长出)收集气体,说明气体密度和空气密度相差较大且不和空气中成分反应;
故选B。
9、D
【详解】
A、硫酸和碳酸钙反应生成微溶于水的硫酸钙会覆盖在石灰石表面,阻止反应进行,所以不可用稀硫酸代替稀盐酸,说法正确,不符合题意;
B、若量气管中液体为水,二氧化碳能和水反应且能溶于水,会导致测定结果偏小,说法正确,不符合题意;
C、稀盐酸加入后会调整水准管,加入的多少不会对测定结果产生影响,说法正确,不符合题意;
D、只要一产生二氧化碳,装置中压强就会变大,量气管中的液体就会被下压,故Y型管中有二氧化碳不会对二氧化碳体积测定产生影响,说法错误,符合题意。
故选D。
【点睛】
10、B
【详解】
A、氧气具有助燃性,能使燃着的木条燃烧的更旺,燃着的木条在空气中继续安静燃烧,现象不同,可以区分,不符合题意;
B、二氧化碳和氮气均不燃烧、不支持燃烧,均能使燃着的木条熄灭,现象相同,无法区分,符合题意;
C、氢气具有可燃性,燃着的木条伸入氢气中,气体能燃烧,发出淡蓝色火焰,燃着的木条在空气中继续安静燃烧,现象不同,可以区分,不符合题意;
D、氮气不燃烧、不支持燃烧,能使燃着的木条熄灭,氧气具有助燃性,能使燃着的木条燃烧的更旺,现象不同,可以区分,不符合题意。
故选B。
二、填空题
1、
(1)N2
(2)2
(3)
(4)C
(5)SO2
(6)Ca
【解析】
(1)
氮气是由分子构成,化学式为元素符号+下标,即N2。
(2)
碳酸根离子为,个数放在离子符号之前,故两个碳酸根为:2
(3)
氧化铝中铝元素显+3价,氧元素显-2价,化学式为Al2O3,化合价标在元素符号的正上方即
(4)
自然界中最硬的物质是金刚石,金刚石由原子构成,化学式直接由元素符号表示,即C。
(5)
淡黄色固体是硫,硫燃烧生成的刺激性气味气体是二氧化硫,化学式为SO2。
(6)
人体中含量最多的元素是氧,最多的金属元素是钙,符号为Ca。
2、
(1) 干冰 升华吸热
(2)出行时乘公交车代替开私家车(合理即可)
【解析】
(1)
固体二氧化碳俗称干冰,能用作制冷剂的原理是干冰升华吸热,水蒸气凝结成液态水。
(2)
出行时乘公交车代替开私家车、植树种草等(合理即可)都可以减少碳排放。
3、
(1)长颈漏斗
(2) AE Fe3O4
(3) b
【解析】
(1)
由图示可知,装置为长颈漏斗。故填:长颈漏斗。
(2)
实验室用高锰酸钾制取氧气,需要加热,因此发生装置选择A,铁丝在氧气中燃烧会产生高温熔融物四氧化三铁,因此瓶底要放少量的水或细沙,收集装置最好选用E,可以提前预留部分水。产物四氧化三铁,化学式Fe3O4。故填:AE Fe3O4。
(3)
若用F装置收集二氧化碳,二氧化碳密度比空气大,应从a进b出,因此验满是把燃烧的木条伸到b端。故填:b。
4、
(1)AB
(2)玻璃棒
(3)煮沸
【解析】
(1)
除去水中不溶解的一些杂质属于固液分离,用过滤的方法,故除去不溶解的杂质需要将水通过过滤池,活性碳具有疏松多孔的结构,有吸附性,能吸附水的的色素和异味,所以除去异味需要将水通过吸附池,故答案选:AB。
(2)
实验室过滤装置如右图,需要用到的玻璃仪器有烧杯、漏斗和玻璃棒。
(3)
在对水进行加热煮沸的过程中,硬水中的可溶性钙镁化合物在受热时会转化为沉淀从水中分离出来,降低了水中可溶性钙镁化合物的含量,从而降低了水的硬度,故日常生中常用煮沸的方法降低水的硬度。
5、
(1)④
(2)③
(3)②
(4)①
【分析】
(1)
石墨质地较软,深灰色,能在纸上留下痕迹,可用于制铅笔芯,故选④。
(2)
氧气可供给呼吸,可用于医疗急救,故选③。
(3)
固体二氧化碳叫干冰,干冰升华吸热,使空气中的水蒸气冷凝成液体的水,所以干冰可用于人工降雨,故选②。
(4)
一氧化碳容易与携带氧气的血红蛋白结合,使其失去携带氧气的能力而发生中毒,故选①。
三、计算题
1、
(1)7.7
(2)设:样品中碳酸钙的质量为x
x=17.5g
样品中碳酸钙的质量分数=
答:样品中碳酸钙的质量分数是87.5%。
【解析】
(1)
碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳气体,开始时石灰石样品的质量为20g,烧杯和稀盐酸的总质量为100g,反应后烧杯和烧杯内各物质的总质量为112.3g,反应过程减少的质量即为反应生成二氧化碳的质量,故生成的CO2的质量=20g+100g-112.3g=7.7g;
(2)
见答案。
2、解:设可以得到铜的质量为x。
答:将16g氧化铜与足量的碳粉高温加热至完全反应后,可以得到12.8g铜。
【详解】
见答案。
3、
(1)50
(2)设大理石中碳酸钙的质量为x,依题意有:
所以大理石中碳酸钙的质量分数为
【解析】
(1)
由图分析,当加入50g稀盐酸时,产生二氧化碳的质量为65.0g+50g-112.8g=2.2g,当继续加入稀盐酸时产生的二氧化碳质量为112.8g+50g-162.8g=0,所以当加入50g稀盐酸时,大理石中碳酸钙刚好反应完。
(2)
见答案。
四、实验探究
1、使火焰集中并提高温度 液面下的导管口有气泡冒出,澄清石灰水变白色浑浊 铜和氧化铜
乙 固体生成物
【详解】
[查阅资料]
酒精灯火焰上罩网罩可以使火焰集中,提高温度;
[收集证据]
木炭和氧化铜反应生成铜和二氧化碳,所以右侧试管中观察到的现象是液面下的导管口有气泡冒出,澄清石灰水变白色浑浊;
[提出问题]
木炭和氧化铜反应生成铜和二氧化碳,生成物铜一定有;
若两种反应物都剩余,则试管内固体成分是铜、氧化铜和碳;
若反应物只有木炭剩余,则试管内固体成分是铜和碳;
若反应物只有氧化铜剩余,则试管内固体成分是铜、氧化铜;
若两种反应物恰好完全反应,则试管内固体成分是铜;
所以你的猜想是铜和氧化铜;
[收集证据]
木炭和氧化铜反应生成铜和二氧化碳,所以试管内固体铜一定有,所以乙同学的猜想错误,木炭和氧化铜反应生成铜和二氧化碳,化学反应方程式为:;
[反思与评价]
对反应后固体成分猜想的一般思路是生成的固体一定存在。
2、无水硫酸铜变蓝 澄清石灰水变浑浊 稀盐酸(或稀硝酸或稀硫酸) 2:3 ①、②
【详解】
实验现象:实验结论为:猜想③正确,故白色不溶物是氢氧化镁和碳酸镁的混合物,碳酸镁和氢氧化镁均加热易分解,分别生成两种氧化物,根据质量守恒定律,化学反应前后,元素的种类不变,氢氧化镁受热分解生成氧化镁和水,碳酸镁受热分解生成氧化镁和二氧化碳,故装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊;
实验结论:氢氧化镁受热分解生成氧化镁和水,该反应的化学方程式为:;
拓展探究:碳酸镁能与稀盐酸反应生成氯化镁、二氧化碳和水,故直接向白色不溶物中滴加足量稀盐酸,如产生白色沉淀,说明含碳酸镁;
实验结论:碱石灰增加的质量就是生成二氧化碳的质量,所以生成二氧化碳的质量为13.2g,设生成13.2g二氧化碳需要碳酸镁的质量为x
x=25.2g
所以含有氢氧化镁的质量为36.8g-25.2g=11.6g,x:y=;
反思评价:①只称量装置C、D增重的质量,可以计算出白色不溶物的质量,故选项正确;
②去掉装置D,根据水增加的质量计算出氢氧化镁的质量,再根据白色不溶物的质量计算出碳酸镁的质量,故选项正确;
③去掉装置C,只称量白色不溶物和装置D增重的质量,装置D既能吸收水分,又能吸收二氧化碳,不能计算出氢氧化镁或碳酸镁,故选项不正确。
故选①、②。
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、归纳和整理是化学学科的一种学习方法。在学习了碳和碳的氧化物的相关知识后,学习小组进行了如下知识整理,其中合理的是
A.金刚石和石墨都具有良好的导电性
B.二氧化碳和一氧化碳都具有还原性
C.二氧化碳用于灭火,既利用它的物理性质,又利用它的化学性质
D.一氧化碳和二氧化碳的组成元素相同,则二者的化学性质一定相同
2、化学与生产、生活密切相关,下列说法正确的是
A.食物的腐烂变质与动植物的新陈代谢均为氧化反应
B.进入菜窖前应先检验窖内二氧化碳的浓度,目的是防止二氧化碳中毒
C.用肥皂水检验硬水和软水,硬水泡沫多,软水泡沫少
D.石油的分馏得到多种化工产品,是利用各物质的熔点不同
3、物质的用途主要由其化学性质决定的是
A.活性炭吸附异味 B.干冰作制冷剂
C.稀有气体作保护气 D.金刚石切割玻璃
4、下列用途既利用其物理性质又利用其化学性质的是
A.活性炭用于防毒面具吸附毒气 B.干冰用于人工降雨
C.一氧化碳作燃料 D.二氧化碳用于灭火
5、 “碳中和”是指一定时间内排放的碳总量与吸收的碳总量相互抵消,实现“碳”零排放。下列不利于实现“碳中和”的是
A.大力植树造林 B.使用风能、太阳能等绿色能源
C.露天焚烧玉米桔梗 D.生活垃圾分类处理
6、鉴别与除杂是化学实验的重要内容,下列设计的方案不能达到实验目的是
A.鉴别蒸馏水和MgCl2溶液—加入肥皂水振荡,观察产生泡沫情况
B.除去CO2中混有的少量CO—通入过量氧气,点燃
C.除去氮气中混有的少量氧气—将混合气体缓慢通过灼热的铜网
D.鉴别水和过氧化氢溶液两种液体—加二氧化锰,观察产生气泡情况
7、为探究影响化学反应速度的因素,使用等量的同种钙片和同体积、同浓度的白醋开展四组实验,产生的二氧化碳的浓度随时间变化的关系如图所示。选取CO2的浓度从0-8%为研究对象,实验结果的分析错误的是
A.对比①③,温度越高,反应速率越快
B.对比②③,反应物接触面积越小,反应速率越慢
C.对比③④,反应物接触面积越大,反应速率越快
D.温度和反应物接触面积都会影响化学反应速度
8、如图装置若用来收集气体,要求该气体
A.相对分子质量小于29 B.密度和空气密度相差较大
C.不溶于水 D.对空气无污染
9、为测定石灰石与稀盐酸产生的CO2的体积,某学生拟用如图实验装置,对于该实验,下列说法错误的是
A.不可用稀硫酸代替稀盐酸
B.若量气管中液体为水,会使测定结果偏小
C.所加稀盐酸的体积对测定结果无影响
D.实验测得CO2的体积偏小可能是因为左侧Y型管中有二氧化碳残留
10、下列各组气体中,不能用燃着木条区分的是
A.氧气和空气 B.二氧化碳和氮气
C.氢气和空气 D.氮气和氧气
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题5分,共计25分)
1、化学用语是学习化学的基本工具请用化学符号填空。
(1)氮气___________;
(2)两个碳酸根离子___________;
(3)氧化铝中铝元素显+3价___________;
(4)自然界中最硬的物质的化学式是___________;
(5)淡黄色固体燃烧后生成有刺激性气味的气体的化学式为___________;
(6)人体中含量最多的金属元素是___________。
2、国家速滑馆“冰丝带”等冰上场馆,将采用CO2制冰技术,可实现CO2循环利用。
(1)固体二氧化碳俗称______,能用作制冷剂的原理是______。
(2)再举出生活中减少碳排放的一个实例:______。
3、根据下列装置图,回答下列问题。
(1)写出仪器①的名称___。
(2)实验室用高锰酸钾制取并收集一瓶氧气用于铁丝燃烧的实验,选择的发生与收集装置最好是___(填字母),铁丝燃烧的产物是___(填化学式)。
(3)实验室制二氧化碳的化学方程式为___。若用F装置收集二氧化碳,验满的方法是把燃烧的木条伸到___(填“a”或“b”)端。
4、自来水厂净水过程示意图如下,请回答:
(1)可以除去水中不溶解的一些杂质和异味的设备是 (填字母)。
A.过滤池 B.吸附池 C.清水池
(2)若在实验室过滤需要用到的玻璃仪器有烧杯、漏斗___________。
(3)日常生活中经常使用什么方法降低水的硬度?_____
5、化学与我们的生活有着密切的联系。现有①一氧化碳②干冰③氧气④石墨,选择适当的物质填空(填序号)
(1)可用于制铅笔芯的是______;
(2)可用于医疗急救的气体是______;
(3)可用于人工降雨的是______;
(4)能与人体中血红蛋白结合的有毒气体是______。
三、计算题(3小题,每小题7分,共计21分)
1、兴趣小组同学对石灰石样品中碳酸钙的质量分数进行了探究,取石灰石样品,加入足量的稀盐酸中,进行实验(数据如表,样品中其他成分不与稀盐酸反应)。
石灰石样品的质量 烧杯和稀盐酸的总质量 反应后烧杯和烧杯内各物质的总质量
20g 100g 112.3g
请计算:
(1)生成的CO2的质量是___________g。
(2)样品中碳酸钙的质量分数。(写出计算过程)
2、将16g氧化铜与足量的碳粉高温加热至完全反应后,可以得到多少克铜?(C:12, O:16, Cu:64)
3、某实验小组的同学为了测定大理石样品中碳酸钙的纯度,取了一定量的大理石样品放置于烧杯中(烧杯重50g)然后向烧杯中滴加一定溶质质量分数的稀盐酸。实验测得烧杯中物质的总质量与加入稀盐酸的质量关系如图所示。求:
(1)当加入___________g稀盐酸时,大理石中碳酸钙刚好反应完;
(2)大理石中碳酸钙的质量分数(写出计算过程,结果精确到0.1%)。
四、实验探究(2小题,每小题12分,共计24分)
1、在学习了“碳的化学性质”后,我校化学兴趣小组的同学在老师的指导下进行“用木炭还原氧化铜”的实验。装置如图所示,请你和他们一起完成下列探究任务。
(查阅资料)此实验最好使用酒精喷灯,也可以在酒精灯火焰上罩网罩,目的是___________。
(收集证据)右侧试管中观察到的现象是___________。
(提出问题)实验结束并冷却至室温后,试管内固体成分是什么?
(猜想与假设)甲同学的猜想:铜
乙同学的猜想:氧化铜和碳
丙同学的猜想:铜、氧化铜和碳
丁同学的猜想:铜和碳
你的猜想___________。
(收集证据)同学们一致认为,__________同学的猜想错误,原因是(用化学方程式表示)__________。在老师的帮助下,同学们确定了丙同学的猜想正确。
(反思与评价)通过对此次探究活动的分析可以得出:对反应后固体成分猜想的一般思路是___________一定存在、固体反应物可能存在、对于固体反应物是两种(或不是一种)且需要一定反应条件才能发生的反应,固体反应物可以同时剩余。
2、兴趣小组同学在做镁与盐反应的实验时,不小心将镁条加到饱和的碳酸氢钠溶液中,意外发现溶液中有白色不溶物生成。同学们对白色不溶物的成分产生了浓厚兴趣,于是在老师的帮助下进行了如下的探究。
(提出问题)白色不溶物是什么物质?
(猜想与假设)
猜想①是Mg(OH)2;猜想②是MgCO3;猜想③是Mg(OH)2和MgCO3的混合物
(查阅资料)
①MgCO3、Mg(OH)2加热易分解,分别生成两种氧化物。
②白色无水硫酸铜遇水变蓝。
③碱石灰是固体氢氧化钠和氧化钙的混合物。
(实验验证)取适量干燥的白色不溶物,充分加热,并使分解产生的气体依次通过如图1所示装置(每步反应都完全)。
(实验现象)装置A中______,装置B中______。
(实验结论)猜想③正确。请写出Mg(OH)2受热分解的化学方程式______。
(拓展探究)直接向白色不溶物中滴加足量______,也能检验MgCO3的存在。
同学们为了进一步测定白色不溶物中各组分的质量关系,继续进行了下列探究。
称取干燥的白色不溶物36.8g,充分加热至不再产生气体,并使分解产生的气体全部被如图2所示装置C和D吸收。
(实验数据)实验后装置C增重3.6g,装置D增重13.2g。
(实验结论)若上述白色不溶物的组成用xMg(OH)2·yMgCO3表示,则x:y=______。
(反思评价)实验后,同学们经过讨论交流,发现实验方案可进一步优化,下列优化方案正确的是______(填序号)。
①只称量装置C、D增重的质量,不称量白色不溶物的质量
②去掉装置D,只称量白色不溶物和装置C增重的质量
③去掉装置C,只称量白色不溶物和装置D增重的质量
-参考答案-
一、单选题
1、C
【详解】
A、石墨具有良好的导电性,金刚石不具有导电性,不符合题意;
B、一氧化碳具有还原性,二氧化碳不具有还原性,不符合题意;
C、二氧化碳用于灭火,是因为二氧化碳不燃烧、不支持燃烧,密度比空气大,不燃烧、不支持燃烧属于化学性质,密度属于物理性质,符合题意;
D、一氧化碳和二氧化碳元素组成相同,但是分子构成不同,故化学性质不同,不符合题意。
故选C。
2、A
【详解】
A.食物的腐烂变质与动植物的新陈代谢均与氧气发生反应,故均为氧化反应,正确;
B.因为二氧化碳不能供给呼吸,所以进入菜窖前应先检验窖内二氧化碳的浓度,查看是否超标,错误;
C.用肥皂水检验硬水和软水,产生泡沫多、浮渣少的是软水,产生泡沫少、浮渣多的是硬水,错误;
D.石油的分馏得到多种化工产品,是利用各物质的沸点不同,而不是熔点,错误;
故选A。
【点睛】
3、C
【详解】
A、活性炭结构疏松多孔,具有吸附性,属于物理性质,故A错误;
B、干冰做制冷剂是利用其升华吸热的特点,属于物理性质,故B错误;
C、稀有气体化学性质很稳定,故用做保护气,是利用其化学性质,故C正确;
D、金刚石切割玻璃是利用其硬度大的特点,属于其物理性质,故D错误;
故选C。
4、D
【分析】
本题考查碳及其化合物的用途,结构决定性质,性质决定用途。
【详解】
A、活性炭疏松多孔,表面积大,吸附性强,用于防毒面具,只利用了物理性质,A不符合题意;
B、干冰是二氧化碳的固态形式,升华时能吸收大量热,用于人工降雨,只利用了物理性质,B不符合题意;
C、一氧化碳具有可燃性,可用作燃料,只利用了化学性质,C不符合题意;
D、二氧化碳用于灭火,既利用了二氧化碳密度比空气大的物理性质,又利用了二氧化碳不能燃烧,不支持燃烧的化学性质,D符合题意。
故选D。
5、C
【详解】
A. \大力植树造林,有利于实现“碳中和”,不符合题意;
B. 使用风能、太阳能等绿色能源,有利于实现“碳中和”,不符合题意;
C. 露天焚烧玉米桔梗产生大量二氧化碳,不利于实现“碳中和”,符合题意;
D. 生活垃圾分类处理,有利于实现“碳中和”,不符合题意。
故选C。
6、B
【详解】
A、蒸馏水是软水,加入肥皂水振荡,产生较多泡沫,MgCl2溶液中加入肥皂水振荡,产生较少泡沫,能达到实验目;
B、二氧化碳不燃烧,不支持燃烧,一氧化碳含量较少,通入过量氧气,一氧化碳不能点燃且引入新杂质氧气,不能达到实验目;
C、将混合气体缓慢通过灼热的铜网,铜和氧气反应生成氧化铜,氮气不参加反应,能达到实验目;
D、过氧化氢溶液中加二氧化锰生成水和氧气,产生较多气泡,水中加二氧化锰不反应,不产生气泡,可以鉴别,能达到实验目。
故选B。
7、B
【详解】
A、从图象对比①③可看出,①③其他条件相同,只有温度不同,在相同时间内,①生成二氧化碳的浓度大于③生成二氧化碳的浓度,由此说明温度越高,反应速率越快;故选项正确;
B、从图象对比②③可看出,钙片的形状不同,温度不同,因此无法比较;故选项错误;
C、从图象对比③④可看出,③④其他条件相同,只有钙片的形状不同,在相同时间内,③生成二氧化碳的浓度大于④生成二氧化碳的浓度,由此说明反应物接触面积越大,反应速率越快;故选项正确;
D、从图象可看出,温度和反应物接触面积都会影响化学反应速度;故选项正确。
故选:B。
8、B
【详解】
该收集方法为向上排空气法(长进短出)或向下排空气法(短进长出)收集气体,说明气体密度和空气密度相差较大且不和空气中成分反应;
故选B。
9、D
【详解】
A、硫酸和碳酸钙反应生成微溶于水的硫酸钙会覆盖在石灰石表面,阻止反应进行,所以不可用稀硫酸代替稀盐酸,说法正确,不符合题意;
B、若量气管中液体为水,二氧化碳能和水反应且能溶于水,会导致测定结果偏小,说法正确,不符合题意;
C、稀盐酸加入后会调整水准管,加入的多少不会对测定结果产生影响,说法正确,不符合题意;
D、只要一产生二氧化碳,装置中压强就会变大,量气管中的液体就会被下压,故Y型管中有二氧化碳不会对二氧化碳体积测定产生影响,说法错误,符合题意。
故选D。
【点睛】
10、B
【详解】
A、氧气具有助燃性,能使燃着的木条燃烧的更旺,燃着的木条在空气中继续安静燃烧,现象不同,可以区分,不符合题意;
B、二氧化碳和氮气均不燃烧、不支持燃烧,均能使燃着的木条熄灭,现象相同,无法区分,符合题意;
C、氢气具有可燃性,燃着的木条伸入氢气中,气体能燃烧,发出淡蓝色火焰,燃着的木条在空气中继续安静燃烧,现象不同,可以区分,不符合题意;
D、氮气不燃烧、不支持燃烧,能使燃着的木条熄灭,氧气具有助燃性,能使燃着的木条燃烧的更旺,现象不同,可以区分,不符合题意。
故选B。
二、填空题
1、
(1)N2
(2)2
(3)
(4)C
(5)SO2
(6)Ca
【解析】
(1)
氮气是由分子构成,化学式为元素符号+下标,即N2。
(2)
碳酸根离子为,个数放在离子符号之前,故两个碳酸根为:2
(3)
氧化铝中铝元素显+3价,氧元素显-2价,化学式为Al2O3,化合价标在元素符号的正上方即
(4)
自然界中最硬的物质是金刚石,金刚石由原子构成,化学式直接由元素符号表示,即C。
(5)
淡黄色固体是硫,硫燃烧生成的刺激性气味气体是二氧化硫,化学式为SO2。
(6)
人体中含量最多的元素是氧,最多的金属元素是钙,符号为Ca。
2、
(1) 干冰 升华吸热
(2)出行时乘公交车代替开私家车(合理即可)
【解析】
(1)
固体二氧化碳俗称干冰,能用作制冷剂的原理是干冰升华吸热,水蒸气凝结成液态水。
(2)
出行时乘公交车代替开私家车、植树种草等(合理即可)都可以减少碳排放。
3、
(1)长颈漏斗
(2) AE Fe3O4
(3) b
【解析】
(1)
由图示可知,装置为长颈漏斗。故填:长颈漏斗。
(2)
实验室用高锰酸钾制取氧气,需要加热,因此发生装置选择A,铁丝在氧气中燃烧会产生高温熔融物四氧化三铁,因此瓶底要放少量的水或细沙,收集装置最好选用E,可以提前预留部分水。产物四氧化三铁,化学式Fe3O4。故填:AE Fe3O4。
(3)
若用F装置收集二氧化碳,二氧化碳密度比空气大,应从a进b出,因此验满是把燃烧的木条伸到b端。故填:b。
4、
(1)AB
(2)玻璃棒
(3)煮沸
【解析】
(1)
除去水中不溶解的一些杂质属于固液分离,用过滤的方法,故除去不溶解的杂质需要将水通过过滤池,活性碳具有疏松多孔的结构,有吸附性,能吸附水的的色素和异味,所以除去异味需要将水通过吸附池,故答案选:AB。
(2)
实验室过滤装置如右图,需要用到的玻璃仪器有烧杯、漏斗和玻璃棒。
(3)
在对水进行加热煮沸的过程中,硬水中的可溶性钙镁化合物在受热时会转化为沉淀从水中分离出来,降低了水中可溶性钙镁化合物的含量,从而降低了水的硬度,故日常生中常用煮沸的方法降低水的硬度。
5、
(1)④
(2)③
(3)②
(4)①
【分析】
(1)
石墨质地较软,深灰色,能在纸上留下痕迹,可用于制铅笔芯,故选④。
(2)
氧气可供给呼吸,可用于医疗急救,故选③。
(3)
固体二氧化碳叫干冰,干冰升华吸热,使空气中的水蒸气冷凝成液体的水,所以干冰可用于人工降雨,故选②。
(4)
一氧化碳容易与携带氧气的血红蛋白结合,使其失去携带氧气的能力而发生中毒,故选①。
三、计算题
1、
(1)7.7
(2)设:样品中碳酸钙的质量为x
x=17.5g
样品中碳酸钙的质量分数=
答:样品中碳酸钙的质量分数是87.5%。
【解析】
(1)
碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳气体,开始时石灰石样品的质量为20g,烧杯和稀盐酸的总质量为100g,反应后烧杯和烧杯内各物质的总质量为112.3g,反应过程减少的质量即为反应生成二氧化碳的质量,故生成的CO2的质量=20g+100g-112.3g=7.7g;
(2)
见答案。
2、解:设可以得到铜的质量为x。
答:将16g氧化铜与足量的碳粉高温加热至完全反应后,可以得到12.8g铜。
【详解】
见答案。
3、
(1)50
(2)设大理石中碳酸钙的质量为x,依题意有:
所以大理石中碳酸钙的质量分数为
【解析】
(1)
由图分析,当加入50g稀盐酸时,产生二氧化碳的质量为65.0g+50g-112.8g=2.2g,当继续加入稀盐酸时产生的二氧化碳质量为112.8g+50g-162.8g=0,所以当加入50g稀盐酸时,大理石中碳酸钙刚好反应完。
(2)
见答案。
四、实验探究
1、使火焰集中并提高温度 液面下的导管口有气泡冒出,澄清石灰水变白色浑浊 铜和氧化铜
乙 固体生成物
【详解】
[查阅资料]
酒精灯火焰上罩网罩可以使火焰集中,提高温度;
[收集证据]
木炭和氧化铜反应生成铜和二氧化碳,所以右侧试管中观察到的现象是液面下的导管口有气泡冒出,澄清石灰水变白色浑浊;
[提出问题]
木炭和氧化铜反应生成铜和二氧化碳,生成物铜一定有;
若两种反应物都剩余,则试管内固体成分是铜、氧化铜和碳;
若反应物只有木炭剩余,则试管内固体成分是铜和碳;
若反应物只有氧化铜剩余,则试管内固体成分是铜、氧化铜;
若两种反应物恰好完全反应,则试管内固体成分是铜;
所以你的猜想是铜和氧化铜;
[收集证据]
木炭和氧化铜反应生成铜和二氧化碳,所以试管内固体铜一定有,所以乙同学的猜想错误,木炭和氧化铜反应生成铜和二氧化碳,化学反应方程式为:;
[反思与评价]
对反应后固体成分猜想的一般思路是生成的固体一定存在。
2、无水硫酸铜变蓝 澄清石灰水变浑浊 稀盐酸(或稀硝酸或稀硫酸) 2:3 ①、②
【详解】
实验现象:实验结论为:猜想③正确,故白色不溶物是氢氧化镁和碳酸镁的混合物,碳酸镁和氢氧化镁均加热易分解,分别生成两种氧化物,根据质量守恒定律,化学反应前后,元素的种类不变,氢氧化镁受热分解生成氧化镁和水,碳酸镁受热分解生成氧化镁和二氧化碳,故装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊;
实验结论:氢氧化镁受热分解生成氧化镁和水,该反应的化学方程式为:;
拓展探究:碳酸镁能与稀盐酸反应生成氯化镁、二氧化碳和水,故直接向白色不溶物中滴加足量稀盐酸,如产生白色沉淀,说明含碳酸镁;
实验结论:碱石灰增加的质量就是生成二氧化碳的质量,所以生成二氧化碳的质量为13.2g,设生成13.2g二氧化碳需要碳酸镁的质量为x
x=25.2g
所以含有氢氧化镁的质量为36.8g-25.2g=11.6g,x:y=;
反思评价:①只称量装置C、D增重的质量,可以计算出白色不溶物的质量,故选项正确;
②去掉装置D,根据水增加的质量计算出氢氧化镁的质量,再根据白色不溶物的质量计算出碳酸镁的质量,故选项正确;
③去掉装置C,只称量白色不溶物和装置D增重的质量,装置D既能吸收水分,又能吸收二氧化碳,不能计算出氢氧化镁或碳酸镁,故选项不正确。
故选①、②。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
