浙教版科学九年级上第1章第二节探索酸的性质(酸的性质复习)
文档属性
| 名称 | 浙教版科学九年级上第1章第二节探索酸的性质(酸的性质复习) |

|
|
| 格式 | zip | ||
| 文件大小 | 342.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2013-03-31 00:00:00 | ||
图片预览







文档简介
课件21张PPT。 酸的性质
复习猜一猜[谜语]
我入水中较安全,水入我中有危险,我与水合多放热,实验牢记保平安谜底:浓硫酸写出几种常见的酸的化学式,
并写出它们的电离方程式电离通式:酸==H+ + 酸根阴离子 一、酸的含义:电离时所生成的阳离子全部是氢离子的化合物。问题:NaHSO4是不是酸?为什么?下列溶液,属于酸溶液的是( )
A、Na+ . H+. Cl-. SO42-
B、H+. K+. Cl-. NO3-
C、H+. Cl-. SO42- . NO3-
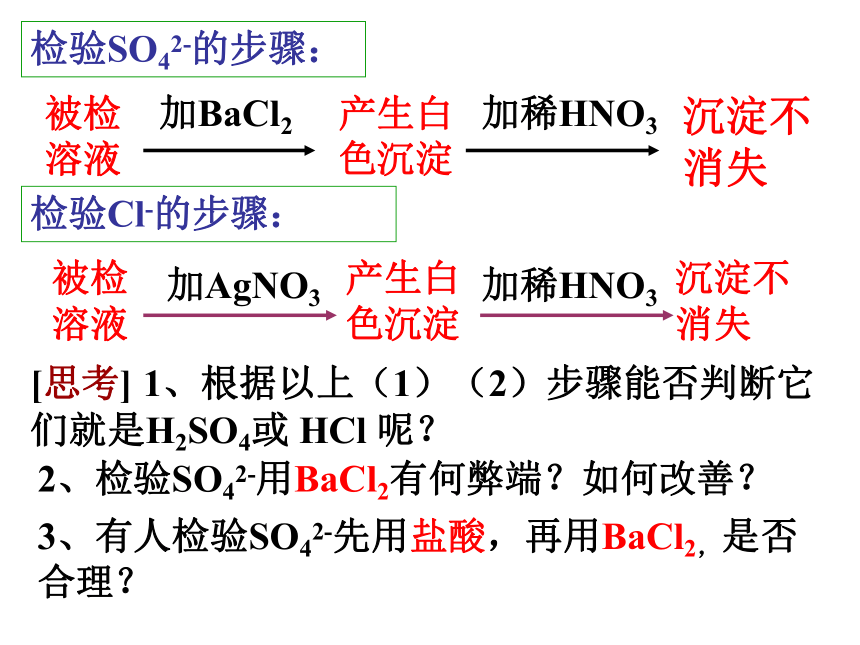
D、H+. NH4+. SO42- . NO3- 酸的共性都具有氢离子(H+)即(H+的性质)已知两瓶失去标签的无色液体,一瓶是浓盐酸,一瓶是浓硫酸,你能快速鉴别出这两种溶液吗?物理方法有哪些?化学方法有哪些?看谁设计得方法多。酸的个性无色无色(黄色)粘稠、液体液体无刺激性气味有有有(强)无无有(弱)浓硫酸与浓盐酸的区别被检溶液加BaCl2产生白色沉淀加稀HNO3沉淀不消失检验SO42-的步骤:检验Cl-的步骤:加AgNO3产生白色沉淀加稀HNO3沉淀不消失被检溶液[思考] 1、根据以上(1)(2)步骤能否判断它们就是H2SO4或 HCl 呢?2、检验SO42-用BaCl2有何弊端?如何改善?3、有人检验SO42-先用盐酸,再用BaCl2,是否合理?实验室有一瓶H2SO4 和 HCl的混酸。老师让同学们用实验的方法证明这一事实。三位同学的操作如下:
甲:①取少量混酸 ②加适量BaCl2溶液和稀HNO3
③过滤 ④向滤液中加AgNO3溶液
乙:①取少量混酸 ②加适量Ba(NO3)2溶液和稀HNO3
③过滤 ④向滤液中加AgNO3溶液
丙:①取少量混酸 ②加适量AgNO3 溶液
③过滤 ④向滤液中加BaCl2溶液
请回答:同学____的操作是正确的。其原因是 。例题用一用1、有这样一则报道:一辆满载硫酸的槽罐车在路上因车祸翻倒,浓硫酸大量泄漏,为了不污染旁边的水源和造成人身伤害事故,有人提议:(1)用大量的水冲洗泄漏的浓硫酸(2)紧急购买大量氯化钡撒在泄漏出的浓硫酸上(3)用土将泄漏出的浓硫酸掩埋(4)紧急购买熟石灰撒在泄漏出的浓硫酸上。你是一位初三学生,如果你在场,你同意何种建议呢?请陈述你的理由。2、常温下,氯气(Cl2)能溶于水,氯气的水溶液叫“氯水”。
溶解的氯气部分能够与水起反应,生成盐酸和次氯酸
(HClO)。次氯酸能杀死水里的病菌,所以自来水常用
氯气来杀菌消毒。次氯酸还能使某些染料和有机色素
褪色,可用作棉、麻和纸张等的漂白剂。请回答:
(1)氯气与水反应的化学方程式 。
次氯酸(HClO)中氯元素的化合价为 。
(2)若用自来水(密度视为1g/cm3)配制1%的下列
溶液,溶质质量分数不受影响的是( )
A、稀盐酸 B、纯碱溶液
C、烧碱溶液 D、硝酸钾溶液
(3)蓝色石蕊试纸(含有机色素)遇到新制氯水后,
首先变红,但很快又褪色,这是因为 。1、学校实验室的废液缸中收集了学生在实验室制取
CO2后残留的废液.小红同学想探究废液中溶质的
成分,请你一同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【作出猜想】小红认为废液中的溶质只有CaCl2
你认为还可能含有的溶质是 (填化学式)
【查阅资料】 CaCl2溶液呈中性①小红取少量CaCl2溶液分别加入到2支试管中,并向
其中分别滴入无色酚酞试液做对比实验,结果两试管
中溶液均无色,于是小红认为自己的猜想是正确的.
②你认为小红的实验 (填”能”或”不能”)证明
她的猜想,理由是 .不能酚酞遇盐酸也不变色,无法确定是否含有HClHCl探一探拓展与应用①若实验证明你的猜想是正确的,想要处理废液
只得到CaCl2溶液,应向废液中加入过量的 ,
反应完成后过虑.
②通过以上探究你认为实验室的废液未经处理
直接倒入下水道,可能造成的危害是 .可能腐蚀铁制下水管道或污染水质碳酸钙③如果要证明你的猜想是正确的,你选择的试剂是 ,
实验中可以看到的现象是 .
2、甲酸是一种无色、有刺激性气味的液体.有较强的腐蚀性。小明想知道甲酸是否具有酸性,做了如下探究:
??(1)他作出的猜想是“甲酸具有酸性”。你认为下列哪一项实验设计能够检验这?一猜想?请用图中字母表示 探一探?(2)若小明的猜想是正确的,则甲酸就会像盐酸那样,能与碳酸钠反应,产生 气体 。?(3)甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素“脱出”结合成水。利用浓硫酸的脱水性,实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会转变成 。 3、小明和小华进行盐酸与锌反应制取氢气的实验研究,小明用较稀盐酸,小华用较浓的盐酸,他们分别用相等质量的锌粒与足量盐酸在烧杯中反应,并将烧杯中物质总质量随时间变化的情况绘成图,试答:
(1)烧杯中物质总质量减小的原因是______
(2)请说明曲线①和②不同的原因_____
(3) 表明小明实验结果的曲线是_____
[反馈练习]1、现有两瓶无色试剂,分别是稀硫酸和稀盐酸,如果要鉴别它们最好用什么试剂?( )
A、氯化钡溶液 B、硝酸银溶液 C、紫色石蕊试液 D、无色酚酞试液
2、现有四瓶溶液,分别是①稀硫酸②稀盐酸③氯化钡溶液④硫酸铜溶液,如果不用任何试剂,你能把它们一一鉴别出来吗?鉴别出来的顺序怎样?3、下图表示加水稀释pH=10的溶液的是( )4、下列物质可以由金属单质和盐酸直接反应制得的有 ( )
A.FeCl3 B.AlCl3 C.CuCl2 D.AgCl
5、除去稀硝酸中的少量盐酸,可以选用( )
A.氢氧化钠溶液
B.足量硝酸银溶液
C.氯化钡溶液
D.适量硝酸银溶液6、20世纪20年代,丹麦和英国的一些化学家提出了新的酸碱理论质子论.质子论认为:凡能放出质子(即H+)的分子或离子都是酸,凡能结合z质子或离子都是碱.根据这个理论,试判断:①H2SO4; ②OH-; ③HCO3-;④NO3-; ⑤Na+中属于酸的是 ,属于碱的是 .① ③② ③④完成作业本
复习猜一猜[谜语]
我入水中较安全,水入我中有危险,我与水合多放热,实验牢记保平安谜底:浓硫酸写出几种常见的酸的化学式,
并写出它们的电离方程式电离通式:酸==H+ + 酸根阴离子 一、酸的含义:电离时所生成的阳离子全部是氢离子的化合物。问题:NaHSO4是不是酸?为什么?下列溶液,属于酸溶液的是( )
A、Na+ . H+. Cl-. SO42-
B、H+. K+. Cl-. NO3-
C、H+. Cl-. SO42- . NO3-
D、H+. NH4+. SO42- . NO3- 酸的共性都具有氢离子(H+)即(H+的性质)已知两瓶失去标签的无色液体,一瓶是浓盐酸,一瓶是浓硫酸,你能快速鉴别出这两种溶液吗?物理方法有哪些?化学方法有哪些?看谁设计得方法多。酸的个性无色无色(黄色)粘稠、液体液体无刺激性气味有有有(强)无无有(弱)浓硫酸与浓盐酸的区别被检溶液加BaCl2产生白色沉淀加稀HNO3沉淀不消失检验SO42-的步骤:检验Cl-的步骤:加AgNO3产生白色沉淀加稀HNO3沉淀不消失被检溶液[思考] 1、根据以上(1)(2)步骤能否判断它们就是H2SO4或 HCl 呢?2、检验SO42-用BaCl2有何弊端?如何改善?3、有人检验SO42-先用盐酸,再用BaCl2,是否合理?实验室有一瓶H2SO4 和 HCl的混酸。老师让同学们用实验的方法证明这一事实。三位同学的操作如下:
甲:①取少量混酸 ②加适量BaCl2溶液和稀HNO3
③过滤 ④向滤液中加AgNO3溶液
乙:①取少量混酸 ②加适量Ba(NO3)2溶液和稀HNO3
③过滤 ④向滤液中加AgNO3溶液
丙:①取少量混酸 ②加适量AgNO3 溶液
③过滤 ④向滤液中加BaCl2溶液
请回答:同学____的操作是正确的。其原因是 。例题用一用1、有这样一则报道:一辆满载硫酸的槽罐车在路上因车祸翻倒,浓硫酸大量泄漏,为了不污染旁边的水源和造成人身伤害事故,有人提议:(1)用大量的水冲洗泄漏的浓硫酸(2)紧急购买大量氯化钡撒在泄漏出的浓硫酸上(3)用土将泄漏出的浓硫酸掩埋(4)紧急购买熟石灰撒在泄漏出的浓硫酸上。你是一位初三学生,如果你在场,你同意何种建议呢?请陈述你的理由。2、常温下,氯气(Cl2)能溶于水,氯气的水溶液叫“氯水”。
溶解的氯气部分能够与水起反应,生成盐酸和次氯酸
(HClO)。次氯酸能杀死水里的病菌,所以自来水常用
氯气来杀菌消毒。次氯酸还能使某些染料和有机色素
褪色,可用作棉、麻和纸张等的漂白剂。请回答:
(1)氯气与水反应的化学方程式 。
次氯酸(HClO)中氯元素的化合价为 。
(2)若用自来水(密度视为1g/cm3)配制1%的下列
溶液,溶质质量分数不受影响的是( )
A、稀盐酸 B、纯碱溶液
C、烧碱溶液 D、硝酸钾溶液
(3)蓝色石蕊试纸(含有机色素)遇到新制氯水后,
首先变红,但很快又褪色,这是因为 。1、学校实验室的废液缸中收集了学生在实验室制取
CO2后残留的废液.小红同学想探究废液中溶质的
成分,请你一同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【作出猜想】小红认为废液中的溶质只有CaCl2
你认为还可能含有的溶质是 (填化学式)
【查阅资料】 CaCl2溶液呈中性①小红取少量CaCl2溶液分别加入到2支试管中,并向
其中分别滴入无色酚酞试液做对比实验,结果两试管
中溶液均无色,于是小红认为自己的猜想是正确的.
②你认为小红的实验 (填”能”或”不能”)证明
她的猜想,理由是 .不能酚酞遇盐酸也不变色,无法确定是否含有HClHCl探一探拓展与应用①若实验证明你的猜想是正确的,想要处理废液
只得到CaCl2溶液,应向废液中加入过量的 ,
反应完成后过虑.
②通过以上探究你认为实验室的废液未经处理
直接倒入下水道,可能造成的危害是 .可能腐蚀铁制下水管道或污染水质碳酸钙③如果要证明你的猜想是正确的,你选择的试剂是 ,
实验中可以看到的现象是 .
2、甲酸是一种无色、有刺激性气味的液体.有较强的腐蚀性。小明想知道甲酸是否具有酸性,做了如下探究:
??(1)他作出的猜想是“甲酸具有酸性”。你认为下列哪一项实验设计能够检验这?一猜想?请用图中字母表示 探一探?(2)若小明的猜想是正确的,则甲酸就会像盐酸那样,能与碳酸钠反应,产生 气体 。?(3)甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素“脱出”结合成水。利用浓硫酸的脱水性,实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会转变成 。 3、小明和小华进行盐酸与锌反应制取氢气的实验研究,小明用较稀盐酸,小华用较浓的盐酸,他们分别用相等质量的锌粒与足量盐酸在烧杯中反应,并将烧杯中物质总质量随时间变化的情况绘成图,试答:
(1)烧杯中物质总质量减小的原因是______
(2)请说明曲线①和②不同的原因_____
(3) 表明小明实验结果的曲线是_____
[反馈练习]1、现有两瓶无色试剂,分别是稀硫酸和稀盐酸,如果要鉴别它们最好用什么试剂?( )
A、氯化钡溶液 B、硝酸银溶液 C、紫色石蕊试液 D、无色酚酞试液
2、现有四瓶溶液,分别是①稀硫酸②稀盐酸③氯化钡溶液④硫酸铜溶液,如果不用任何试剂,你能把它们一一鉴别出来吗?鉴别出来的顺序怎样?3、下图表示加水稀释pH=10的溶液的是( )4、下列物质可以由金属单质和盐酸直接反应制得的有 ( )
A.FeCl3 B.AlCl3 C.CuCl2 D.AgCl
5、除去稀硝酸中的少量盐酸,可以选用( )
A.氢氧化钠溶液
B.足量硝酸银溶液
C.氯化钡溶液
D.适量硝酸银溶液6、20世纪20年代,丹麦和英国的一些化学家提出了新的酸碱理论质子论.质子论认为:凡能放出质子(即H+)的分子或离子都是酸,凡能结合z质子或离子都是碱.根据这个理论,试判断:①H2SO4; ②OH-; ③HCO3-;④NO3-; ⑤Na+中属于酸的是 ,属于碱的是 .① ③② ③④完成作业本
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
