4.1.2 化学电源课件2021-2022学年上学期高二化学人教版(2019)选择性必修1(共13张PPT)
文档属性
| 名称 | 4.1.2 化学电源课件2021-2022学年上学期高二化学人教版(2019)选择性必修1(共13张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 977.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-12 00:00:00 | ||
图片预览


文档简介
(共13张PPT)
第2课时 化学电源
第四章 第一节 化学反应与电能
学习目标
1.通过交流讨论了解一次电池、二次电池和燃料电池的基本构造,学会书写常见的电极反应式和电池反应。
2.通过相关的信息分析了解化学电源的工作原理,初步建立化学电源工作原理的认知模型。
3.通过学习各类电池的实际应用,感受化学给人类带来的进步和文明,通过了解废旧电池对环境的危害,树立环保意识。
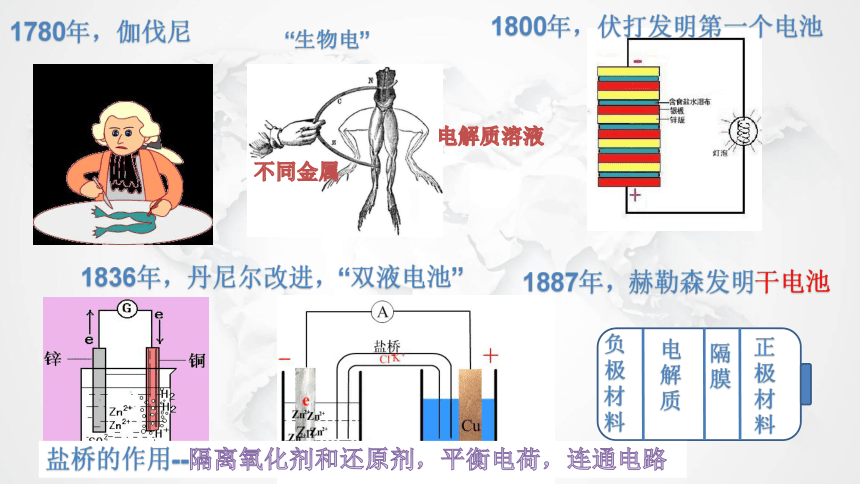
1780年,伽伐尼
“生物电”
不同金属
电解质溶液
1800年,伏打发明第一个电池
1836年,丹尼尔改进,“双液电池”
负极材料
电解质
隔膜
正极材料
1887年,赫勒森发明干电池
盐桥的作用--隔离氧化剂和还原剂,平衡电荷,连通电路
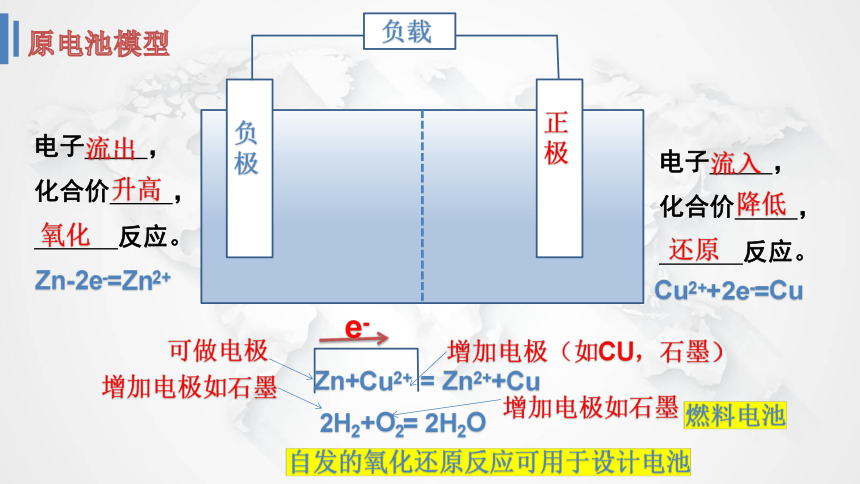
负极
正极
负载
电子 ,
化合价 ,
反应。
电子 ,
化合价 ,
反应。
Zn-2e-=Zn2+
Cu2++2e-=Cu
Zn+Cu2+ = Zn2++Cu
可做电极
增加电极(如CU,石墨)
2H2+O2= 2H2O
增加电极如石墨
增加电极如石墨
燃料电池
自发的氧化还原反应可用于设计电池
流出
升高
氧化
流入
降低
还原
原电池模型
e-
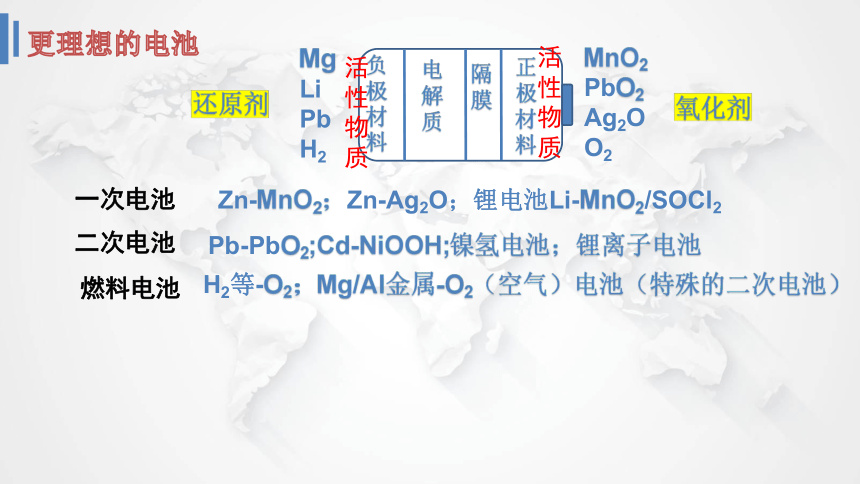
更理想的电池
负极材料
电解质
隔膜
正极材料
还原剂
氧化剂
Mg
Li
Pb
H2
MnO2
PbO2
Ag2O
O2
一次电池
二次电池
燃料电池
Zn-MnO2;Zn-Ag2O;锂电池Li-MnO2/SOCl2
Pb-PbO2;Cd-NiOOH;镍氢电池;锂离子电池
H2等-O2;Mg/Al金属-O2(空气)电池(特殊的二次电池)
活性物质
活性物质
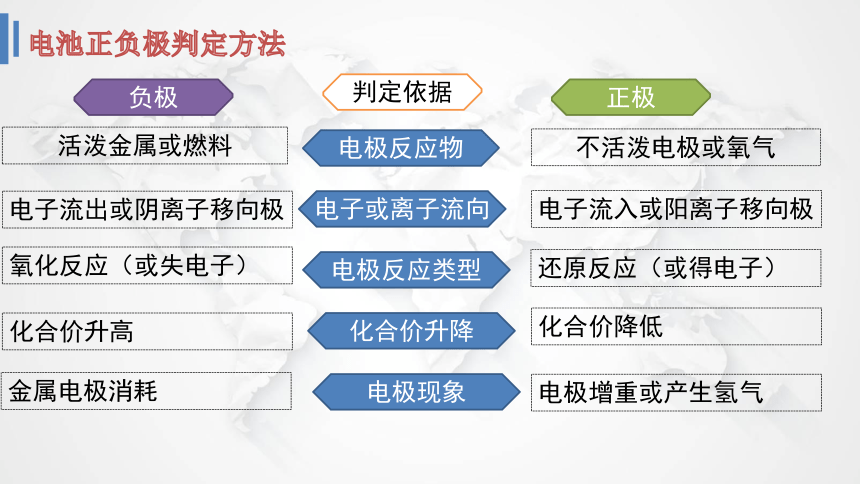
电池正负极判定方法
判定依据
电极反应物
电子或离子流向
电极反应类型
化合价升降
电极现象
负极
正极
活泼金属或燃料
不活泼电极或氧气
电子流出或阴离子移向极
电子流入或阳离子移向极
氧化反应(或失电子)
还原反应(或得电子)
化合价升高
化合价降低
金属电极消耗
电极增重或产生氢气
一次电池
碱性锌锰电池总反应式:Zn+2MnO2+H2O=2MnOOH+ZnO
1.定电极
2.标价态
3.配守恒
三步法
确定正负电极及其反应物(离子环境)
确定升降元素
(1)电子守恒 (2)电荷守恒 (3)原子守恒
负极反应式:Zn+2OH--2e-=ZnO+H2O;
正极反应式:2MnO2+2H2O+2e-=2MnOOH+2OH-。
二次电池
铅酸蓄电池是典型的二次电池,其性能优良、价格低廉、安全可靠、可多次充放电,所以在生产、生活中使用广泛,如汽车、电动自行车等都使用这种电池。其充、放电时的电池反应为
Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)。
负极:Pb(s)+SO42-(aq)-2e-=PbSO4(s);
正极:PbO2(s)+4H+(aq)+SO42-(aq)+2e-=PbSO4(s)+2H2O(l);
放电过程中,负极的质量增大,电解质溶液的pH升高。
燃料电池
将燃料和氧化剂的化学能直接转化为电能的化学电池
负极
H2,CO,烃类,醇类,其他有机物
失电子
不同电解质体系下的特定结构形式
正极
通常为氧气
得电子
不同电解质体系下的特定结构形式
如OH-,H2O,O2-
不同电解质体系下两极生成物结构
电解质体系 平衡电荷的离子 正极 负极
酸性溶液
碱性溶液 固体电解质 熔融碳酸盐 H+
OH-
O2-
CO32-
O2+4H++4e-=2H2O
O2+2H2O+4e-=4OH-
O2+4e-=2O2-
O2+CO2+4e=2CO32-
C、H类燃料
通常
C CO2
H H+
碱性
C CO32-
H H2O
当堂训练
负
4H2O+2O2+8e-=8OH-
减弱
大于
当堂训练
D
当堂训练
B
第2课时 化学电源
第四章 第一节 化学反应与电能
学习目标
1.通过交流讨论了解一次电池、二次电池和燃料电池的基本构造,学会书写常见的电极反应式和电池反应。
2.通过相关的信息分析了解化学电源的工作原理,初步建立化学电源工作原理的认知模型。
3.通过学习各类电池的实际应用,感受化学给人类带来的进步和文明,通过了解废旧电池对环境的危害,树立环保意识。
1780年,伽伐尼
“生物电”
不同金属
电解质溶液
1800年,伏打发明第一个电池
1836年,丹尼尔改进,“双液电池”
负极材料
电解质
隔膜
正极材料
1887年,赫勒森发明干电池
盐桥的作用--隔离氧化剂和还原剂,平衡电荷,连通电路
负极
正极
负载
电子 ,
化合价 ,
反应。
电子 ,
化合价 ,
反应。
Zn-2e-=Zn2+
Cu2++2e-=Cu
Zn+Cu2+ = Zn2++Cu
可做电极
增加电极(如CU,石墨)
2H2+O2= 2H2O
增加电极如石墨
增加电极如石墨
燃料电池
自发的氧化还原反应可用于设计电池
流出
升高
氧化
流入
降低
还原
原电池模型
e-
更理想的电池
负极材料
电解质
隔膜
正极材料
还原剂
氧化剂
Mg
Li
Pb
H2
MnO2
PbO2
Ag2O
O2
一次电池
二次电池
燃料电池
Zn-MnO2;Zn-Ag2O;锂电池Li-MnO2/SOCl2
Pb-PbO2;Cd-NiOOH;镍氢电池;锂离子电池
H2等-O2;Mg/Al金属-O2(空气)电池(特殊的二次电池)
活性物质
活性物质
电池正负极判定方法
判定依据
电极反应物
电子或离子流向
电极反应类型
化合价升降
电极现象
负极
正极
活泼金属或燃料
不活泼电极或氧气
电子流出或阴离子移向极
电子流入或阳离子移向极
氧化反应(或失电子)
还原反应(或得电子)
化合价升高
化合价降低
金属电极消耗
电极增重或产生氢气
一次电池
碱性锌锰电池总反应式:Zn+2MnO2+H2O=2MnOOH+ZnO
1.定电极
2.标价态
3.配守恒
三步法
确定正负电极及其反应物(离子环境)
确定升降元素
(1)电子守恒 (2)电荷守恒 (3)原子守恒
负极反应式:Zn+2OH--2e-=ZnO+H2O;
正极反应式:2MnO2+2H2O+2e-=2MnOOH+2OH-。
二次电池
铅酸蓄电池是典型的二次电池,其性能优良、价格低廉、安全可靠、可多次充放电,所以在生产、生活中使用广泛,如汽车、电动自行车等都使用这种电池。其充、放电时的电池反应为
Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)。
负极:Pb(s)+SO42-(aq)-2e-=PbSO4(s);
正极:PbO2(s)+4H+(aq)+SO42-(aq)+2e-=PbSO4(s)+2H2O(l);
放电过程中,负极的质量增大,电解质溶液的pH升高。
燃料电池
将燃料和氧化剂的化学能直接转化为电能的化学电池
负极
H2,CO,烃类,醇类,其他有机物
失电子
不同电解质体系下的特定结构形式
正极
通常为氧气
得电子
不同电解质体系下的特定结构形式
如OH-,H2O,O2-
不同电解质体系下两极生成物结构
电解质体系 平衡电荷的离子 正极 负极
酸性溶液
碱性溶液 固体电解质 熔融碳酸盐 H+
OH-
O2-
CO32-
O2+4H++4e-=2H2O
O2+2H2O+4e-=4OH-
O2+4e-=2O2-
O2+CO2+4e=2CO32-
C、H类燃料
通常
C CO2
H H+
碱性
C CO32-
H H2O
当堂训练
负
4H2O+2O2+8e-=8OH-
减弱
大于
当堂训练
D
当堂训练
B
