专题8有机化合物的获得与应用——提升训练(word版 含解析)
文档属性
| 名称 | 专题8有机化合物的获得与应用——提升训练(word版 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 272.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-13 00:00:00 | ||
图片预览




文档简介
专题8有机化合物的获得与应用
一、选择题(共16题)
1.下列说法正确的是
A.蛋白质加热后会变性,这种变化是不可逆的
B.人体中的氨基酸不能由自身合成的属于非必需氨基酸
C.牛奶中含量最多的物质是蛋白质,不是水
D.所有蛋白质均含有C、H、O、N、S五种元素
2.下列能源可以再生的是
A.煤 B.石油 C.生物质能 D.可燃冰
3.下列说法不正确的是
A.CH3COOCH2CH3和CH3CH2COOCH3是不同种物质
B.医药中常用酒精来消毒,是因为酒精能够使细菌蛋白质发生变性
C.淀粉和蛋白质都为高分子化合物,在一定条件下均可水解
D.聚氯乙烯的单体是—CH2CH2C1—
4.化学与生产。生活。环境等息息相关,下列说法错误的是( )
A.港珠澳大桥采用的超高相对分子质量聚乙烯纤维吊绳属于有机高分子化合物
B.“玉兔二号”月球车首次实现在月球背面着陆,其帆板太阳能电池的材料是硅
C.《周礼》中“煤饼烧蛎房成灰”(蛎房即牡蛎壳),“灰”的主要成分为
D.《本草纲目》中“凡酸坏之酒,皆可蒸烧”,所用的分离方法是蒸馏
5.下列说法正确的是
A.医用酒精和双氧水杀灭病毒的原理相同
B.84消毒液的有效成分为次氯酸钠
C.用醋熏的方法杀死空气中潜在的新冠肺炎病毒
D.生产口罩的重要原料由丙烯发生缩聚反应生成
6.下列说法不正确的是
A.可以用溴的四氯化碳溶液除去甲烷中的乙烯
B.普通玻璃的主要成分为Na2SiO3、CaSiO3和SiO2,原料为纯碱、石灰石和石英
C.蛋白质存在于各类生命体内,一切重要的生命现象都与蛋白质密切而关
D.石油在加热和催化剂的作用下,可以通过结构调整,使链状烃变成环状烃
7.设NA为阿伏伽德罗常数的值,则下列说法正确的是
A.标准状况下,2.24L CH2Cl2中含氯原子数目为0.2NA
B.14 g聚乙烯中所含原子数为3NA
C.0.1 mol苯乙烯中含有碳碳双键的数目为0.4NA
D.常温常压下,100 g质量分数为46%的酒精水溶液中含氧原子总数为NA
8.下列有关化学用语的表达正确的是
A.Cl-的结构示意图: B.甲烷分子的空间填充模型:
C.丙烯的结构简式:CH2CHCH3 D.乙醇的分子式:C2H5OH
9.某学生进行的下列家庭小实验不合理的是( )
A.用食醋检验牙膏中的摩擦剂是否是碳酸钙
B.炒菜时滴加少量食醋和料酒可增加香味
C.在一瓣橘子上插入两根铜线并与小灯泡连接,验证电流的产生
D.用灼烧并闻气味的方法区别纯棉织物和羊毛织物
10.某高吸水性树脂P的结构片段如图所示。其中X为,Y起交联作用,由在合成P的过程中形成。下列说法不正确的是
A.合成P的反应可能是加聚反应
B.P的高吸水性与“—COONa”结构有关
C.由Y的结构推测CH2=CH2也可起到类似的交联作用
D.合成P的过程中用到的一种原料可能是CH2=CH—COONa
11.下列有机反应属于取代反应的是
A.CH2=CH2+
B.CH3CH=CH2+Cl2CH2=CHCH2Cl+HCl
C.2CH3CH2OH+O22CH3CHO+2H2O
D.CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
12.下列与有机物结构、性质相关的叙述中,正确的是
A.煤的干馏,煤的气化和液化是化学变化
B.肥皂可以通过高分子化合物油脂发生皂化反应制得
C.鸡蛋清中加入CuSO4溶液会产生盐析现象,析出的蛋白质可再溶于水
D.淀粉、纤维素完全水解的产物互为同分异构体,且都可与新制氢氧化铜反应
13.下列说法正确的是
A.葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体
B.淀粉、纤维素都属于天然高分子
C.油脂、淀粉、蔗糖和葡萄糖在一定条件下都能发生水解反应
D.肌醇()与葡萄糖()的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此均属于糖类化合物
14.工业上用X( )合成Y( ),下列有关分析正确的是
A.由X合成Y的反应为加聚反应
B.若Y的相对分子质量(平均值)为19600,则
C.Y的相对分子质量为X的n倍
D.Y能使溴的溶液褪色
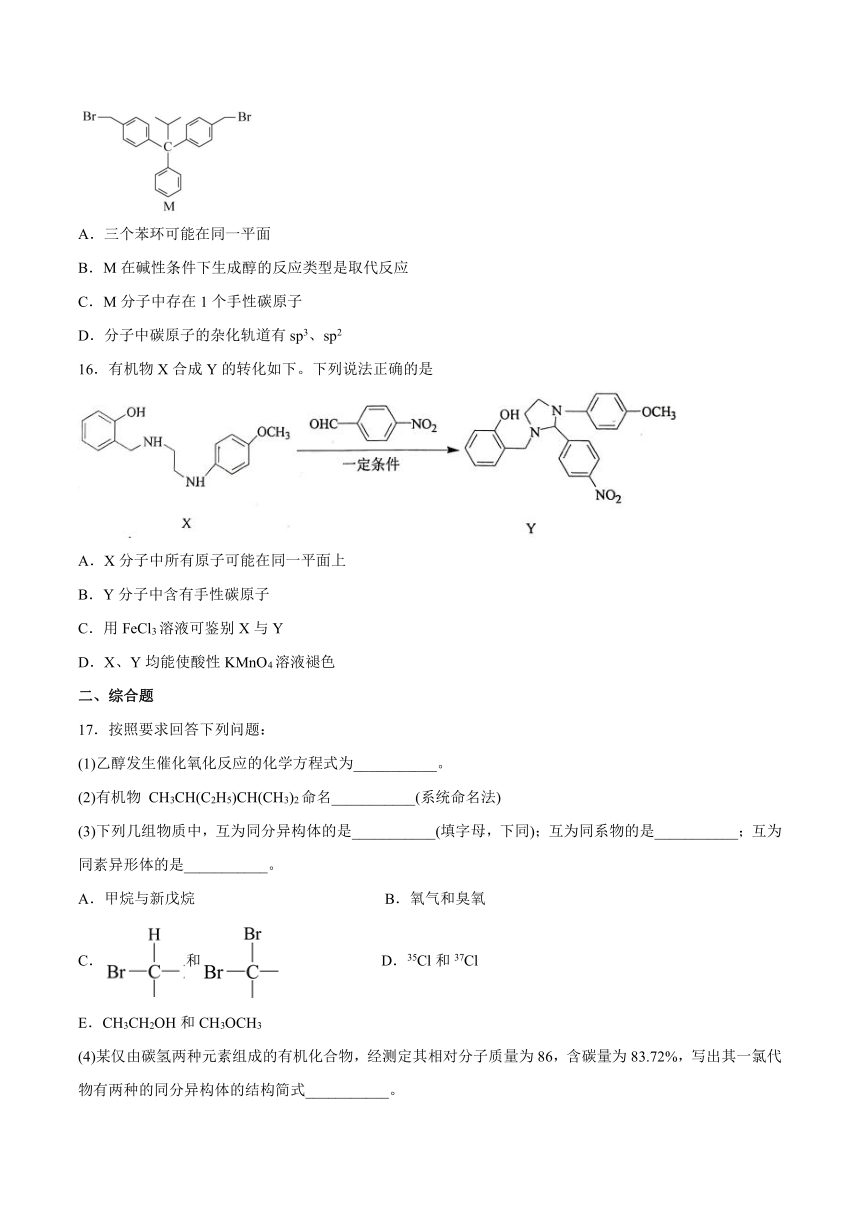
15.有机化合物M结构简式如图所示,下列说法不正确的是
A.三个苯环可能在同一平面
B.M在碱性条件下生成醇的反应类型是取代反应
C.M分子中存在1个手性碳原子
D.分子中碳原子的杂化轨道有sp3、sp2
16.有机物X合成Y的转化如下。下列说法正确的是
A.X分子中所有原子可能在同一平面上
B.Y分子中含有手性碳原子
C.用FeCl3溶液可鉴别X与Y
D.X、Y均能使酸性KMnO4溶液褪色
二、综合题
17.按照要求回答下列问题:
(1)乙醇发生催化氧化反应的化学方程式为___________。
(2)有机物 CH3CH(C2H5)CH(CH3)2命名___________(系统命名法)
(3)下列几组物质中,互为同分异构体的是___________(填字母,下同);互为同系物的是___________;互为同素异形体的是___________。
A.甲烷与新戊烷 B.氧气和臭氧
C.和 D.35Cl和37Cl
E.CH3CH2OH和CH3OCH3
(4)某仅由碳氢两种元素组成的有机化合物,经测定其相对分子质量为86,含碳量为83.72%,写出其一氯代物有两种的同分异构体的结构简式___________。
18.石油的主要炼制过程如图所示。
完成下列填空:
(1)上述过程属于物理变化的是______(填写序号);工业上利用步骤③获得短链气态不饱和烃,该步操作的名称是______。
(2)步骤④是工业制乙醇(CH3CH2OH)的方法之一,该反应的化学方程式是_______,反应类型属于_____(选填“加成”或“取代”)反应。
(3)乙烯(CH2=CH2)的产量是衡量一个国家石油化工发展水平的标志。实验室利用步骤⑤制取乙烯,该反应的化学方程式是____________。
19.我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。请回答下列问题:
(1)乙醇的官能团名称是 ___________ (填“羧基”或“羟基”);
(2)使用K2Cr2O7酸性溶液检测酒驾,利用了乙醇的___________(填“氧化性”或“还原性”)。
(3)乙醇在铜或银作催化剂的条件下,可以被空气中的氧气氧化。完成相应的反应方程式: 2CH3CH2OH + O22___________ + 2CH3CHO
20.按要求填空:
(1)下列物质中属于天然有机高分子化合物的是(填序号)____________________
①淀粉 ②油脂 ③高级脂肪酸 ④纤维素 ⑤蚕丝 ⑥聚乙烯塑料 ⑦涤纶
(2)写出该有机物的结构简式______________________________________它所属的类别为____________________(填序号)
①卤代烃 ②脂肪族化合物 ③脂环化合物 ④烯烃 ⑤烃的衍生物
(3)0.lmol某烃在足量的O2中燃烧,生成13.2gCO2和5.4gH2O,该烃的分子式为_______
(4)写出丙烯发生加聚反应的化学方程式_________________________________________
21.为了探究乙醇和钠反应的原理,做如下实验:
甲:向试管中加入3mL乙醇,放入一小块钠,观察现象,并收集,检验产生的气体。
乙:向试管中加入3mL乙醚(),放入一小块钠,无气体产生。
回答以下问题:
(1)简述检验实验甲中产生的气体的方法及作出判断的依据:_________。
(2)从结构上分析,选取乙醚作参照物的原因是_________。
(3)实验甲说明________;实验乙说明_______;根据实验结果,乙醇和金属钠反应的化学方程式应为_________。
22.阅读下列科普短文,回答问题。
国家卫健委公布的《新型冠状病毒肺炎诊疗方案(试行)》中提到:在相对封闭环境中,长时间暴露于高浓度气溶胶情况下,新冠病毒存在经气溶胶传播的可能。佩戴医用外科口罩可起到防护作用,含有病毒的飞沫会被口罩中间层熔喷无纺布(主要材质是聚丙烯)吸附。消毒也是控制病毒传播的有效措施,《新型冠状病毒肺炎流行期间预防性消毒指引》建议:表面消毒可选择含氯消毒剂、75%酒精, 食饮具需要煮沸消毒15分钟以上。
(1)气溶胶中粒子的大小为____________。
a. < l nm b. > 100 nm c.1 nm~100 nm
(2)丙烯在催化剂条件下制备聚丙烯,化学反应方程式为_________________。
(3) 75%酒精的有效成分是乙醇,乙醇的一种同分异构体的结构简式为________________。
(4)食饮具可通过煮沸消毒,病毒蛋白质在加热条件下发生了_______________。
(5)环氧乙烷是一种低温灭菌剂,经典的生产方法是氯代乙醇法,包括两步反应:
i. CH2=CH2+Cl2+H2O→ClCH2CH2OH+HCl
ii. ClCH2CH2OH+HCl+Ca(OH)2→+CaCl2+2H2O
现代石油化工采用低温催化法:2CH2=CH2+O2与氯代乙醇法相比,低温催化法的优点有__________、_____________。(答两点)
参考答案:
1.A
【详解】
A.蛋白质在加热后会变性,这种变化是不可逆的,例如煮熟的蛋白不会变成蛋清,A正确;
B.人体中的必需氨基酸不能由自身合成,必须从外界摄取,B错误;
C.牛奶中含量最多的是水,其次是蛋白质,C错误;
D.蛋白质由氨基酸构成,并不是所有的氨基酸均含有S元素,但一定含有C、H、O、N这四种元素,D错误;
故选A。
2.C
【详解】
A.煤属于化石燃料,是不可再生能源,A不符合题意;
B.石油属于化石燃料,是不可再生能源,B不符合题意;
C.生物质燃烧产物经过光合作用,又可转化为生物质,所以生物质能属于可再生能源,C符合题意;
D.可燃冰的主要成分为甲烷,不能再生,所以可燃冰不属于可再生能源,C不符合题意;
故选C。
3.D
【详解】
A.CH3COOCH2CH3是乙酸乙酯,CH3CH2COOCH3是丙酸甲酯,二者是不同的物质,A正确;
B.酒精可以使细菌的蛋白质变性,故可以用酒精来消毒,B正确;
C.淀粉和蛋白质都是高分子化合物,二者在一定条件下都可以水解,淀粉水解的最终产物为葡萄糖,蛋白质水解的最终产物为氨基酸,C正确;
D.聚氯乙烯的单体是CH2=CHCl,D错误;
故选D。
4.C
【详解】
A.聚乙烯属于有机高分子化合物,A项正确,不符合题意。
B.太阳能电池的材料是单晶硅,B项正确,不符合题意。
C.牡蛎壳的主要成分为碳酸钙,受热分解为氧化钙和二氧化碳,C项错误,符合题意;
D.“酸坏”是指少量乙醇被氧化为乙酸,分离乙醇和乙酸的方法为蒸馏,D项正确,不符合题意。
故选C。
5.B
【详解】
A.双氧水和乙醇的杀菌原理不同,双氧水是强氧化剂,会迅速分解产生新生氧,可以通过氧化作用破坏微生物表面的蛋白质,从而杀灭微生物;酒精可以使蛋白质凝固,从而丧失生物活性,从而杀灭微生物,A项错误;
B.84消毒液的有效成分为次氯酸钠,B项正确;
C.醋的主要成分是乙酸,可使蛋白质变性,但在空气中用量太大,少量醋不能杀灭病毒,C项错误;
D.生产口罩的重要原料由丙烯发生加聚反应生成,D项错误;
答案选B。
6.A
【详解】
A.甲烷易溶于四氯化碳,应用溴水除杂,A错误;
B.生产普通玻璃的反应为:Na2CO3+SiO2Na2SiO3+CO2↑,CaCO3+SiO2CaSiO3+CO2↑,故普通玻璃的主要成分为Na2SiO3、CaSiO3和SiO2,原料为纯碱、石灰石和石英,B正确;
C.蛋白质是构成细胞的基本物质,存在于各类生物体内,一切重要的生命现象都与蛋白质密切相关,C正确;
D.石油在加热和催化剂的作用下,可以通过结构调整,即催化重整,使链状烃变成环状烃,以提高芳香烃的产量,D正确;
故答案为:A。
7.B
【详解】
A.标准状况下,CH2Cl2为液态,无法用气体摩尔体积进行计算其物质的量,A错误;
B. 聚乙烯的最简式为CH2,14g聚乙烯中含有1molCH2,所含原子数为3NA,B正确;
C. 苯乙烯分子中含有1个碳碳双键,0.1mol苯乙烯中含有双键的数目为0.1NA,C错误;
D. 常温常压下,100g46%酒精水溶液中46g乙醇中含有01mol氧原子,54g水中含有3mol氧原子,则含氧原子总数为4NA,D错误;
答案为B
8.B
【详解】
A.Cl-的核电荷数为17,核外电子数为18,结构示意图为 ,A不正确;
B.甲烷分子的电子式为,则其空间填充模型为:,B正确;
C.丙烯分子中含有碳碳双键,不能省略,则其结构简式为CH2=CHCH3,C不正确;
D.乙醇的结构简式为C2H5OH,分子式为C2H6O,D不正确;
故选B。
9.C
【详解】
A.食醋的主要成分为醋酸,能够与牙膏中的碳酸钙反应生成二氧化碳气体,可以通过是否有气体生成,作为判断的依据,故A合理;
B.料酒中醇和食醋中的乙酸发生了酯化反应,生成了有香味的乙酸乙酯,因此炒菜时滴加少量食醋和料酒可增加香味,故B合理;
C.形成原电池反应时,两极金属不能相同,否则不能形成原电池反应,故C不合理;
D.毛织物的主要成分是蛋白质,灼烧时有烧焦羽毛的气味;纯棉织物中不含有蛋白质,灼烧时没有烧焦羽毛的气味,故D合理;
故选C。
10.C
【详解】
A.由分析可知,合成P的反应为CH2=CH—COONa和Y以2:1的物质的量比发生加聚反应生成P,故A正确;
B.由结构片段可知,P分子中含有许多—COONa,—COONa可以发生水解反应生成亲水基—COOH,则P的高吸水性与分子中含有—COONa结构有关,故B正确;
C.由结构简式可知,Y的结构中含有2个碳碳双键,在形成P的反应中CH2=CH—COONa和Y以2:1的物质的量比发生加聚反应,Y分子中的2个碳碳双键起到了交联作用,而CH2=CH2分子中只含有1个碳碳双键,无法起到类似的交联作用,故C错误;
D.由分析可知,生成P的单体为CH2=CH—COONa和Y,故D正确;
故选C。
11.B
【详解】
A.乙烯与苯发生加成反应产生乙苯,反应类型属于加成反应,A不符合题意;
B.CH3CH=CH2与Cl2在500℃时发生甲基上的取代反应产生CH2=CHCH2Cl,同时产生HCl,B符合题意;
C.CH3CH2OH与Cu在催化剂存在条件下被O2氧化产生CH3CHO,发生的反应属于氧化反应,C不符合题意;
D.CH3CH2Br与NaOH的乙醇溶液共热,发生消去反应,产生CH2=CH2,反应类型为消去反应,D不符合题意;
故选B。
12.A
【详解】
A、煤的干馏,是加强热使煤中的成分分解成气体、液体和固体;煤的气化,是通过化学反应使煤变成气体燃料;煤的液化,是通过化学反应使煤变成液体燃料;所以都是化学变化,选项A正确;
B、油脂不是高分子化合物,选项B错误;
C、鸡蛋清中加入硫酸铜溶液会变性,而不是发生盐析,选项C错误;
D、淀粉、纤维素完全水解的产物都是葡萄糖,不是同分异构体,选项D错误。
答案选A。
13.AB
【详解】
A.葡萄糖、果糖的分子式均为C6H12O6,葡萄糖为六碳醛糖,果糖为六碳酮糖,两者结构不同,二者互为同分异构体,A正确;
B.淀粉、纤维素的分子式都为(C6H10O5)n,都属于天然高分子化合物,B正确;
C.葡萄糖为单糖,不能水解,C错误;
D.糖类是多羟基醛、多羟基酮和它们的脱水缩合物,肌醇()不是糖类化合物,D错误;
答案选AB。
14.AC
【详解】
A.由X合成Y的反应为加聚反应,A项正确;
B.X的相对分子质量为56,Y的相对分子质量为,,则,B项错误;
C.X的相对分子质量为56,Y的相对分子质量为,Y的相对分子质量为X的n倍,C项正确;
D.Y的重复结构单元中不存在碳碳双键,故Y不能使溴的溶液褪色,D项错误;
答案选AC。
15.AC
【详解】
A.根据M结构简式分析可知,分子中的三个苯环可以看作取代甲烷上的3个H原子,甲烷上最多2个H原子与C原子共平面,因此M中三个苯环不可能在同一平面,A项错误;
B.M分子中的Br在碱性条件下水解生成醇,卤代烃的碱性水解属于取代反应,B项正确;
C.有机化合物M不存在手性碳原子,C项错误;
D.M中和三个苯环直接相连的碳原子以及甲基、亚甲基中的碳原子都是sp3杂化,苯环中的碳原子都是sp2杂化, D项正确;
故选AC。
16.BD
【详解】
A. X分子中含有氮原子,与其它3个原子以3根单键相结合呈三角锥形、分子内有单键碳原子是四面体结构,故分子内所有原子不可能在同一平面上,A错误;
B. Y分子中有一个碳原子分别连有不等同的氮原子、苯环和氢原子,故该碳原子为手性碳原子,B正确;
C. X和Y中均含酚羟基,故不能用FeCl3溶液鉴别,C错误;
D. X和Y中均含酚羟基,均能使酸性KMnO4溶液褪色,D正确;
答案选BD。
17.(1)2CH3CH2OH+O22CH3CHO+2H2O
(2)2,3-二甲基戊烷
(3) E A B
(4)(CH3)2CHCH(CH3)2
【详解】
(1)
乙醇催化氧化,生成乙醛和水,反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;
(2)
CH3CH(C2H5)CH(CH3)2主链上有5个碳原子,即戊烷,从离支链近的一端开始编号,则在2号碳和3号碳上分别均有2个甲基,故名称为:2,3-二甲基戊烷;
(3)
A.甲烷与新戊烷都是烷烃,属于同系物;
B.氧气和臭氧都是氧元素的单质,属于同素异形体;
C. 和结构相同,分子式相同,属于同种物质;
D.35Cl和37Cl质子数都是17,是氯元素的不同原子,属于同位素;
E.CH3CH2OH和CH3OCH3,分子式相同而结构不同,属于同分异构体;
所以互为同分异构体的是 E;互为同系物的是 A;互为同素异形体的是B;
(4)
该有机物只含碳氢两种元素,含碳量为83.72%,则含氢量为1-83.72%=16.28%,碳原子的个数为,氢原子的个数为,该有机物分子为C6H14,其一氯代物有两种的同分异构体的结构简式为(CH3)2CHCH(CH3)2。
18. ① 裂解 CH2=CH2+H2OCH3CH2OH 加成 CH3CH2OHCH2=CH2↑+H2O
【详解】
(1)分馏过程中没有新物质产生,因此上述过程属于物理变化的是①;工业上利用步骤③获得短链气态不饱和烃乙烯,因此该步操作的名称是裂解。
(2)步骤④是工业制乙醇(CH3CH2OH)的方法之一,原理是利用乙烯和水加成,则该反应的化学方程式是CH2=CH2+H2OCH3CH2OH,反应类型属于加成反应。
(3)乙烯(CH2=CH2)的产量是衡量一个国家石油化工发展水平的标志。实验室利用乙醇的消去反应制取乙烯,该反应的化学方程式是CH3CH2OHCH2=CH2↑+H2O。
19.(1)羟基
(2)还原性
(3)H2O
【详解】
(1)
乙醇的结构简式是C2H5OH,含有的官能团是-OH,名称是羟基;
(2)
K2Cr2O7具有强氧化性,使用K2Cr2O7酸性溶液检测酒驾,利用了乙醇的还原性;
(3)
乙醇在铜或银作催化剂的条件下,可以和空气中的氧气反应生成乙醛和水,反应的化学方程式是 2CH3CH2OH + O22H2O+ 2CH3CHO。
20. ①④⑤ CH2=CH-CH=CH-CH2Cl2 ①②⑤ C3H6 n CH2=CH-CH3
【详解】
(1) 天然有机高分子化合物是指自然界存在的高分子化合物,所以①淀粉④纤维素⑤蚕丝属于天然有机高分子化合物,②油脂③高级脂肪酸不属于高分子化合物;⑥聚乙烯塑料 ⑦涤纶属于合成有机高分子化合物。故答案为①④⑤。
(2) 根据上述分析可知:有机物的结构简式CH2=CH-CH=CH-CHCl2;分子内含有的官能团为-Cl和碳碳双键,属于①卤代烃②脂肪族化合物⑤烃的衍生物,没有苯环,也没有其他的环,不属于③脂环化合物,故答案为CH2=CH-CH=CH-CHCl2;①②⑤;
(3) 13.2gCO2的物质的量为0.3mol;5.4gH2O的物质的量为0.3mol,含H为0.6 mol ,所以0.lmol某烃含碳原子0.3 mol,含H为0.6 mol,所以生成该烃的分子式为C3H6,故答案为C3H6。
(4) 丙烯发生加聚反应的化学方程式n CH2=CH-CH3。
21. 将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则证明该气体是氢气 乙醇分子中含有乙基和羟基,乙醚分子中含有乙基 羟基氢可与钠发生置换反应 乙基上的氢不能与钠发生反应
【详解】
(1)试管中加入乙醇,放入一小块钠,二者会发生反应得到乙醇钠和氢气,氢气的检验方法:将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则证明该气体是氢气,故答案:将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则证明该气体是氢气。
(2)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基,故选取乙醚作参照物,说明与钠发生反应的为羟基,故答案:乙醇分子中含有乙基和羟基,乙醚分子中含有乙基。
(3)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基,向试管中加入3mL乙醚,放入一小块钠,不发生反应,说明与钠反应的物质中需含有羟基氢,乙基上的氢不能与钠发生反应,羟基中的氢原子能和金属钠反应得到氢气,其反应的化学方程式应为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故答案:羟基氢可与钠发生置换反应;乙基上的氢不能与钠发生反应;2CH3CH2OH+2Na→2CH3CH2ONa+H2↑。
22. c nCH3CH=CH2 CH3OCH3 变性 原子利用率100% (或原子经济性高),不产生CaCl2等工业废渣 对设备腐蚀性小、低温催化能耗低
【详解】
(1)分散质粒子直径在1nm~100nm之间的分散系为胶体,气溶胶中粒子的大小为1nm~100nm;故答案为:c;
(2)丙烯在催化剂条件下制备聚丙烯,化学反应方程式为:nCH3CH=CH2;
(3)乙醇的分子式是C2H6O,饱和一元醇和饱和一元醚属于类别异构,乙醇的同分异构体是甲醚,其结构简式是CH3OCH3;故答案为:CH3OCH3;
(4)加热可以使蛋白质变性,所以病毒蛋白质在加热条件下发生了变性;故答案为:变性;
(5)氯代乙醇法生产环氧乙烷,原子利用率没有达到100%,并且有CaCl2等工业废渣产生;现代石油化工采用低温催化法:2CH2=CH2+O2,原子利用率100% (或原子经济性高),没有副产物,与氯代乙醇法相比,低温催化法的优点是原子利用率100% (或原子经济性高),不产生CaCl2等工业废渣、对设备腐蚀性小、低温催化能耗低等优点;故答案为:原子利用率100% (或原子经济性高),不产生CaCl2等工业废渣;对设备腐蚀性小、低温催化能耗低。
一、选择题(共16题)
1.下列说法正确的是
A.蛋白质加热后会变性,这种变化是不可逆的
B.人体中的氨基酸不能由自身合成的属于非必需氨基酸
C.牛奶中含量最多的物质是蛋白质,不是水
D.所有蛋白质均含有C、H、O、N、S五种元素
2.下列能源可以再生的是
A.煤 B.石油 C.生物质能 D.可燃冰
3.下列说法不正确的是
A.CH3COOCH2CH3和CH3CH2COOCH3是不同种物质
B.医药中常用酒精来消毒,是因为酒精能够使细菌蛋白质发生变性
C.淀粉和蛋白质都为高分子化合物,在一定条件下均可水解
D.聚氯乙烯的单体是—CH2CH2C1—
4.化学与生产。生活。环境等息息相关,下列说法错误的是( )
A.港珠澳大桥采用的超高相对分子质量聚乙烯纤维吊绳属于有机高分子化合物
B.“玉兔二号”月球车首次实现在月球背面着陆,其帆板太阳能电池的材料是硅
C.《周礼》中“煤饼烧蛎房成灰”(蛎房即牡蛎壳),“灰”的主要成分为
D.《本草纲目》中“凡酸坏之酒,皆可蒸烧”,所用的分离方法是蒸馏
5.下列说法正确的是
A.医用酒精和双氧水杀灭病毒的原理相同
B.84消毒液的有效成分为次氯酸钠
C.用醋熏的方法杀死空气中潜在的新冠肺炎病毒
D.生产口罩的重要原料由丙烯发生缩聚反应生成
6.下列说法不正确的是
A.可以用溴的四氯化碳溶液除去甲烷中的乙烯
B.普通玻璃的主要成分为Na2SiO3、CaSiO3和SiO2,原料为纯碱、石灰石和石英
C.蛋白质存在于各类生命体内,一切重要的生命现象都与蛋白质密切而关
D.石油在加热和催化剂的作用下,可以通过结构调整,使链状烃变成环状烃
7.设NA为阿伏伽德罗常数的值,则下列说法正确的是
A.标准状况下,2.24L CH2Cl2中含氯原子数目为0.2NA
B.14 g聚乙烯中所含原子数为3NA
C.0.1 mol苯乙烯中含有碳碳双键的数目为0.4NA
D.常温常压下,100 g质量分数为46%的酒精水溶液中含氧原子总数为NA
8.下列有关化学用语的表达正确的是
A.Cl-的结构示意图: B.甲烷分子的空间填充模型:
C.丙烯的结构简式:CH2CHCH3 D.乙醇的分子式:C2H5OH
9.某学生进行的下列家庭小实验不合理的是( )
A.用食醋检验牙膏中的摩擦剂是否是碳酸钙
B.炒菜时滴加少量食醋和料酒可增加香味
C.在一瓣橘子上插入两根铜线并与小灯泡连接,验证电流的产生
D.用灼烧并闻气味的方法区别纯棉织物和羊毛织物
10.某高吸水性树脂P的结构片段如图所示。其中X为,Y起交联作用,由在合成P的过程中形成。下列说法不正确的是
A.合成P的反应可能是加聚反应
B.P的高吸水性与“—COONa”结构有关
C.由Y的结构推测CH2=CH2也可起到类似的交联作用
D.合成P的过程中用到的一种原料可能是CH2=CH—COONa
11.下列有机反应属于取代反应的是
A.CH2=CH2+
B.CH3CH=CH2+Cl2CH2=CHCH2Cl+HCl
C.2CH3CH2OH+O22CH3CHO+2H2O
D.CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
12.下列与有机物结构、性质相关的叙述中,正确的是
A.煤的干馏,煤的气化和液化是化学变化
B.肥皂可以通过高分子化合物油脂发生皂化反应制得
C.鸡蛋清中加入CuSO4溶液会产生盐析现象,析出的蛋白质可再溶于水
D.淀粉、纤维素完全水解的产物互为同分异构体,且都可与新制氢氧化铜反应
13.下列说法正确的是
A.葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体
B.淀粉、纤维素都属于天然高分子
C.油脂、淀粉、蔗糖和葡萄糖在一定条件下都能发生水解反应
D.肌醇()与葡萄糖()的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此均属于糖类化合物
14.工业上用X( )合成Y( ),下列有关分析正确的是
A.由X合成Y的反应为加聚反应
B.若Y的相对分子质量(平均值)为19600,则
C.Y的相对分子质量为X的n倍
D.Y能使溴的溶液褪色
15.有机化合物M结构简式如图所示,下列说法不正确的是
A.三个苯环可能在同一平面
B.M在碱性条件下生成醇的反应类型是取代反应
C.M分子中存在1个手性碳原子
D.分子中碳原子的杂化轨道有sp3、sp2
16.有机物X合成Y的转化如下。下列说法正确的是
A.X分子中所有原子可能在同一平面上
B.Y分子中含有手性碳原子
C.用FeCl3溶液可鉴别X与Y
D.X、Y均能使酸性KMnO4溶液褪色
二、综合题
17.按照要求回答下列问题:
(1)乙醇发生催化氧化反应的化学方程式为___________。
(2)有机物 CH3CH(C2H5)CH(CH3)2命名___________(系统命名法)
(3)下列几组物质中,互为同分异构体的是___________(填字母,下同);互为同系物的是___________;互为同素异形体的是___________。
A.甲烷与新戊烷 B.氧气和臭氧
C.和 D.35Cl和37Cl
E.CH3CH2OH和CH3OCH3
(4)某仅由碳氢两种元素组成的有机化合物,经测定其相对分子质量为86,含碳量为83.72%,写出其一氯代物有两种的同分异构体的结构简式___________。
18.石油的主要炼制过程如图所示。
完成下列填空:
(1)上述过程属于物理变化的是______(填写序号);工业上利用步骤③获得短链气态不饱和烃,该步操作的名称是______。
(2)步骤④是工业制乙醇(CH3CH2OH)的方法之一,该反应的化学方程式是_______,反应类型属于_____(选填“加成”或“取代”)反应。
(3)乙烯(CH2=CH2)的产量是衡量一个国家石油化工发展水平的标志。实验室利用步骤⑤制取乙烯,该反应的化学方程式是____________。
19.我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。请回答下列问题:
(1)乙醇的官能团名称是 ___________ (填“羧基”或“羟基”);
(2)使用K2Cr2O7酸性溶液检测酒驾,利用了乙醇的___________(填“氧化性”或“还原性”)。
(3)乙醇在铜或银作催化剂的条件下,可以被空气中的氧气氧化。完成相应的反应方程式: 2CH3CH2OH + O22___________ + 2CH3CHO
20.按要求填空:
(1)下列物质中属于天然有机高分子化合物的是(填序号)____________________
①淀粉 ②油脂 ③高级脂肪酸 ④纤维素 ⑤蚕丝 ⑥聚乙烯塑料 ⑦涤纶
(2)写出该有机物的结构简式______________________________________它所属的类别为____________________(填序号)
①卤代烃 ②脂肪族化合物 ③脂环化合物 ④烯烃 ⑤烃的衍生物
(3)0.lmol某烃在足量的O2中燃烧,生成13.2gCO2和5.4gH2O,该烃的分子式为_______
(4)写出丙烯发生加聚反应的化学方程式_________________________________________
21.为了探究乙醇和钠反应的原理,做如下实验:
甲:向试管中加入3mL乙醇,放入一小块钠,观察现象,并收集,检验产生的气体。
乙:向试管中加入3mL乙醚(),放入一小块钠,无气体产生。
回答以下问题:
(1)简述检验实验甲中产生的气体的方法及作出判断的依据:_________。
(2)从结构上分析,选取乙醚作参照物的原因是_________。
(3)实验甲说明________;实验乙说明_______;根据实验结果,乙醇和金属钠反应的化学方程式应为_________。
22.阅读下列科普短文,回答问题。
国家卫健委公布的《新型冠状病毒肺炎诊疗方案(试行)》中提到:在相对封闭环境中,长时间暴露于高浓度气溶胶情况下,新冠病毒存在经气溶胶传播的可能。佩戴医用外科口罩可起到防护作用,含有病毒的飞沫会被口罩中间层熔喷无纺布(主要材质是聚丙烯)吸附。消毒也是控制病毒传播的有效措施,《新型冠状病毒肺炎流行期间预防性消毒指引》建议:表面消毒可选择含氯消毒剂、75%酒精, 食饮具需要煮沸消毒15分钟以上。
(1)气溶胶中粒子的大小为____________。
a. < l nm b. > 100 nm c.1 nm~100 nm
(2)丙烯在催化剂条件下制备聚丙烯,化学反应方程式为_________________。
(3) 75%酒精的有效成分是乙醇,乙醇的一种同分异构体的结构简式为________________。
(4)食饮具可通过煮沸消毒,病毒蛋白质在加热条件下发生了_______________。
(5)环氧乙烷是一种低温灭菌剂,经典的生产方法是氯代乙醇法,包括两步反应:
i. CH2=CH2+Cl2+H2O→ClCH2CH2OH+HCl
ii. ClCH2CH2OH+HCl+Ca(OH)2→+CaCl2+2H2O
现代石油化工采用低温催化法:2CH2=CH2+O2与氯代乙醇法相比,低温催化法的优点有__________、_____________。(答两点)
参考答案:
1.A
【详解】
A.蛋白质在加热后会变性,这种变化是不可逆的,例如煮熟的蛋白不会变成蛋清,A正确;
B.人体中的必需氨基酸不能由自身合成,必须从外界摄取,B错误;
C.牛奶中含量最多的是水,其次是蛋白质,C错误;
D.蛋白质由氨基酸构成,并不是所有的氨基酸均含有S元素,但一定含有C、H、O、N这四种元素,D错误;
故选A。
2.C
【详解】
A.煤属于化石燃料,是不可再生能源,A不符合题意;
B.石油属于化石燃料,是不可再生能源,B不符合题意;
C.生物质燃烧产物经过光合作用,又可转化为生物质,所以生物质能属于可再生能源,C符合题意;
D.可燃冰的主要成分为甲烷,不能再生,所以可燃冰不属于可再生能源,C不符合题意;
故选C。
3.D
【详解】
A.CH3COOCH2CH3是乙酸乙酯,CH3CH2COOCH3是丙酸甲酯,二者是不同的物质,A正确;
B.酒精可以使细菌的蛋白质变性,故可以用酒精来消毒,B正确;
C.淀粉和蛋白质都是高分子化合物,二者在一定条件下都可以水解,淀粉水解的最终产物为葡萄糖,蛋白质水解的最终产物为氨基酸,C正确;
D.聚氯乙烯的单体是CH2=CHCl,D错误;
故选D。
4.C
【详解】
A.聚乙烯属于有机高分子化合物,A项正确,不符合题意。
B.太阳能电池的材料是单晶硅,B项正确,不符合题意。
C.牡蛎壳的主要成分为碳酸钙,受热分解为氧化钙和二氧化碳,C项错误,符合题意;
D.“酸坏”是指少量乙醇被氧化为乙酸,分离乙醇和乙酸的方法为蒸馏,D项正确,不符合题意。
故选C。
5.B
【详解】
A.双氧水和乙醇的杀菌原理不同,双氧水是强氧化剂,会迅速分解产生新生氧,可以通过氧化作用破坏微生物表面的蛋白质,从而杀灭微生物;酒精可以使蛋白质凝固,从而丧失生物活性,从而杀灭微生物,A项错误;
B.84消毒液的有效成分为次氯酸钠,B项正确;
C.醋的主要成分是乙酸,可使蛋白质变性,但在空气中用量太大,少量醋不能杀灭病毒,C项错误;
D.生产口罩的重要原料由丙烯发生加聚反应生成,D项错误;
答案选B。
6.A
【详解】
A.甲烷易溶于四氯化碳,应用溴水除杂,A错误;
B.生产普通玻璃的反应为:Na2CO3+SiO2Na2SiO3+CO2↑,CaCO3+SiO2CaSiO3+CO2↑,故普通玻璃的主要成分为Na2SiO3、CaSiO3和SiO2,原料为纯碱、石灰石和石英,B正确;
C.蛋白质是构成细胞的基本物质,存在于各类生物体内,一切重要的生命现象都与蛋白质密切相关,C正确;
D.石油在加热和催化剂的作用下,可以通过结构调整,即催化重整,使链状烃变成环状烃,以提高芳香烃的产量,D正确;
故答案为:A。
7.B
【详解】
A.标准状况下,CH2Cl2为液态,无法用气体摩尔体积进行计算其物质的量,A错误;
B. 聚乙烯的最简式为CH2,14g聚乙烯中含有1molCH2,所含原子数为3NA,B正确;
C. 苯乙烯分子中含有1个碳碳双键,0.1mol苯乙烯中含有双键的数目为0.1NA,C错误;
D. 常温常压下,100g46%酒精水溶液中46g乙醇中含有01mol氧原子,54g水中含有3mol氧原子,则含氧原子总数为4NA,D错误;
答案为B
8.B
【详解】
A.Cl-的核电荷数为17,核外电子数为18,结构示意图为 ,A不正确;
B.甲烷分子的电子式为,则其空间填充模型为:,B正确;
C.丙烯分子中含有碳碳双键,不能省略,则其结构简式为CH2=CHCH3,C不正确;
D.乙醇的结构简式为C2H5OH,分子式为C2H6O,D不正确;
故选B。
9.C
【详解】
A.食醋的主要成分为醋酸,能够与牙膏中的碳酸钙反应生成二氧化碳气体,可以通过是否有气体生成,作为判断的依据,故A合理;
B.料酒中醇和食醋中的乙酸发生了酯化反应,生成了有香味的乙酸乙酯,因此炒菜时滴加少量食醋和料酒可增加香味,故B合理;
C.形成原电池反应时,两极金属不能相同,否则不能形成原电池反应,故C不合理;
D.毛织物的主要成分是蛋白质,灼烧时有烧焦羽毛的气味;纯棉织物中不含有蛋白质,灼烧时没有烧焦羽毛的气味,故D合理;
故选C。
10.C
【详解】
A.由分析可知,合成P的反应为CH2=CH—COONa和Y以2:1的物质的量比发生加聚反应生成P,故A正确;
B.由结构片段可知,P分子中含有许多—COONa,—COONa可以发生水解反应生成亲水基—COOH,则P的高吸水性与分子中含有—COONa结构有关,故B正确;
C.由结构简式可知,Y的结构中含有2个碳碳双键,在形成P的反应中CH2=CH—COONa和Y以2:1的物质的量比发生加聚反应,Y分子中的2个碳碳双键起到了交联作用,而CH2=CH2分子中只含有1个碳碳双键,无法起到类似的交联作用,故C错误;
D.由分析可知,生成P的单体为CH2=CH—COONa和Y,故D正确;
故选C。
11.B
【详解】
A.乙烯与苯发生加成反应产生乙苯,反应类型属于加成反应,A不符合题意;
B.CH3CH=CH2与Cl2在500℃时发生甲基上的取代反应产生CH2=CHCH2Cl,同时产生HCl,B符合题意;
C.CH3CH2OH与Cu在催化剂存在条件下被O2氧化产生CH3CHO,发生的反应属于氧化反应,C不符合题意;
D.CH3CH2Br与NaOH的乙醇溶液共热,发生消去反应,产生CH2=CH2,反应类型为消去反应,D不符合题意;
故选B。
12.A
【详解】
A、煤的干馏,是加强热使煤中的成分分解成气体、液体和固体;煤的气化,是通过化学反应使煤变成气体燃料;煤的液化,是通过化学反应使煤变成液体燃料;所以都是化学变化,选项A正确;
B、油脂不是高分子化合物,选项B错误;
C、鸡蛋清中加入硫酸铜溶液会变性,而不是发生盐析,选项C错误;
D、淀粉、纤维素完全水解的产物都是葡萄糖,不是同分异构体,选项D错误。
答案选A。
13.AB
【详解】
A.葡萄糖、果糖的分子式均为C6H12O6,葡萄糖为六碳醛糖,果糖为六碳酮糖,两者结构不同,二者互为同分异构体,A正确;
B.淀粉、纤维素的分子式都为(C6H10O5)n,都属于天然高分子化合物,B正确;
C.葡萄糖为单糖,不能水解,C错误;
D.糖类是多羟基醛、多羟基酮和它们的脱水缩合物,肌醇()不是糖类化合物,D错误;
答案选AB。
14.AC
【详解】
A.由X合成Y的反应为加聚反应,A项正确;
B.X的相对分子质量为56,Y的相对分子质量为,,则,B项错误;
C.X的相对分子质量为56,Y的相对分子质量为,Y的相对分子质量为X的n倍,C项正确;
D.Y的重复结构单元中不存在碳碳双键,故Y不能使溴的溶液褪色,D项错误;
答案选AC。
15.AC
【详解】
A.根据M结构简式分析可知,分子中的三个苯环可以看作取代甲烷上的3个H原子,甲烷上最多2个H原子与C原子共平面,因此M中三个苯环不可能在同一平面,A项错误;
B.M分子中的Br在碱性条件下水解生成醇,卤代烃的碱性水解属于取代反应,B项正确;
C.有机化合物M不存在手性碳原子,C项错误;
D.M中和三个苯环直接相连的碳原子以及甲基、亚甲基中的碳原子都是sp3杂化,苯环中的碳原子都是sp2杂化, D项正确;
故选AC。
16.BD
【详解】
A. X分子中含有氮原子,与其它3个原子以3根单键相结合呈三角锥形、分子内有单键碳原子是四面体结构,故分子内所有原子不可能在同一平面上,A错误;
B. Y分子中有一个碳原子分别连有不等同的氮原子、苯环和氢原子,故该碳原子为手性碳原子,B正确;
C. X和Y中均含酚羟基,故不能用FeCl3溶液鉴别,C错误;
D. X和Y中均含酚羟基,均能使酸性KMnO4溶液褪色,D正确;
答案选BD。
17.(1)2CH3CH2OH+O22CH3CHO+2H2O
(2)2,3-二甲基戊烷
(3) E A B
(4)(CH3)2CHCH(CH3)2
【详解】
(1)
乙醇催化氧化,生成乙醛和水,反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;
(2)
CH3CH(C2H5)CH(CH3)2主链上有5个碳原子,即戊烷,从离支链近的一端开始编号,则在2号碳和3号碳上分别均有2个甲基,故名称为:2,3-二甲基戊烷;
(3)
A.甲烷与新戊烷都是烷烃,属于同系物;
B.氧气和臭氧都是氧元素的单质,属于同素异形体;
C. 和结构相同,分子式相同,属于同种物质;
D.35Cl和37Cl质子数都是17,是氯元素的不同原子,属于同位素;
E.CH3CH2OH和CH3OCH3,分子式相同而结构不同,属于同分异构体;
所以互为同分异构体的是 E;互为同系物的是 A;互为同素异形体的是B;
(4)
该有机物只含碳氢两种元素,含碳量为83.72%,则含氢量为1-83.72%=16.28%,碳原子的个数为,氢原子的个数为,该有机物分子为C6H14,其一氯代物有两种的同分异构体的结构简式为(CH3)2CHCH(CH3)2。
18. ① 裂解 CH2=CH2+H2OCH3CH2OH 加成 CH3CH2OHCH2=CH2↑+H2O
【详解】
(1)分馏过程中没有新物质产生,因此上述过程属于物理变化的是①;工业上利用步骤③获得短链气态不饱和烃乙烯,因此该步操作的名称是裂解。
(2)步骤④是工业制乙醇(CH3CH2OH)的方法之一,原理是利用乙烯和水加成,则该反应的化学方程式是CH2=CH2+H2OCH3CH2OH,反应类型属于加成反应。
(3)乙烯(CH2=CH2)的产量是衡量一个国家石油化工发展水平的标志。实验室利用乙醇的消去反应制取乙烯,该反应的化学方程式是CH3CH2OHCH2=CH2↑+H2O。
19.(1)羟基
(2)还原性
(3)H2O
【详解】
(1)
乙醇的结构简式是C2H5OH,含有的官能团是-OH,名称是羟基;
(2)
K2Cr2O7具有强氧化性,使用K2Cr2O7酸性溶液检测酒驾,利用了乙醇的还原性;
(3)
乙醇在铜或银作催化剂的条件下,可以和空气中的氧气反应生成乙醛和水,反应的化学方程式是 2CH3CH2OH + O22H2O+ 2CH3CHO。
20. ①④⑤ CH2=CH-CH=CH-CH2Cl2 ①②⑤ C3H6 n CH2=CH-CH3
【详解】
(1) 天然有机高分子化合物是指自然界存在的高分子化合物,所以①淀粉④纤维素⑤蚕丝属于天然有机高分子化合物,②油脂③高级脂肪酸不属于高分子化合物;⑥聚乙烯塑料 ⑦涤纶属于合成有机高分子化合物。故答案为①④⑤。
(2) 根据上述分析可知:有机物的结构简式CH2=CH-CH=CH-CHCl2;分子内含有的官能团为-Cl和碳碳双键,属于①卤代烃②脂肪族化合物⑤烃的衍生物,没有苯环,也没有其他的环,不属于③脂环化合物,故答案为CH2=CH-CH=CH-CHCl2;①②⑤;
(3) 13.2gCO2的物质的量为0.3mol;5.4gH2O的物质的量为0.3mol,含H为0.6 mol ,所以0.lmol某烃含碳原子0.3 mol,含H为0.6 mol,所以生成该烃的分子式为C3H6,故答案为C3H6。
(4) 丙烯发生加聚反应的化学方程式n CH2=CH-CH3。
21. 将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则证明该气体是氢气 乙醇分子中含有乙基和羟基,乙醚分子中含有乙基 羟基氢可与钠发生置换反应 乙基上的氢不能与钠发生反应
【详解】
(1)试管中加入乙醇,放入一小块钠,二者会发生反应得到乙醇钠和氢气,氢气的检验方法:将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则证明该气体是氢气,故答案:将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则证明该气体是氢气。
(2)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基,故选取乙醚作参照物,说明与钠发生反应的为羟基,故答案:乙醇分子中含有乙基和羟基,乙醚分子中含有乙基。
(3)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基,向试管中加入3mL乙醚,放入一小块钠,不发生反应,说明与钠反应的物质中需含有羟基氢,乙基上的氢不能与钠发生反应,羟基中的氢原子能和金属钠反应得到氢气,其反应的化学方程式应为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故答案:羟基氢可与钠发生置换反应;乙基上的氢不能与钠发生反应;2CH3CH2OH+2Na→2CH3CH2ONa+H2↑。
22. c nCH3CH=CH2 CH3OCH3 变性 原子利用率100% (或原子经济性高),不产生CaCl2等工业废渣 对设备腐蚀性小、低温催化能耗低
【详解】
(1)分散质粒子直径在1nm~100nm之间的分散系为胶体,气溶胶中粒子的大小为1nm~100nm;故答案为:c;
(2)丙烯在催化剂条件下制备聚丙烯,化学反应方程式为:nCH3CH=CH2;
(3)乙醇的分子式是C2H6O,饱和一元醇和饱和一元醚属于类别异构,乙醇的同分异构体是甲醚,其结构简式是CH3OCH3;故答案为:CH3OCH3;
(4)加热可以使蛋白质变性,所以病毒蛋白质在加热条件下发生了变性;故答案为:变性;
(5)氯代乙醇法生产环氧乙烷,原子利用率没有达到100%,并且有CaCl2等工业废渣产生;现代石油化工采用低温催化法:2CH2=CH2+O2,原子利用率100% (或原子经济性高),没有副产物,与氯代乙醇法相比,低温催化法的优点是原子利用率100% (或原子经济性高),不产生CaCl2等工业废渣、对设备腐蚀性小、低温催化能耗低等优点;故答案为:原子利用率100% (或原子经济性高),不产生CaCl2等工业废渣;对设备腐蚀性小、低温催化能耗低。
