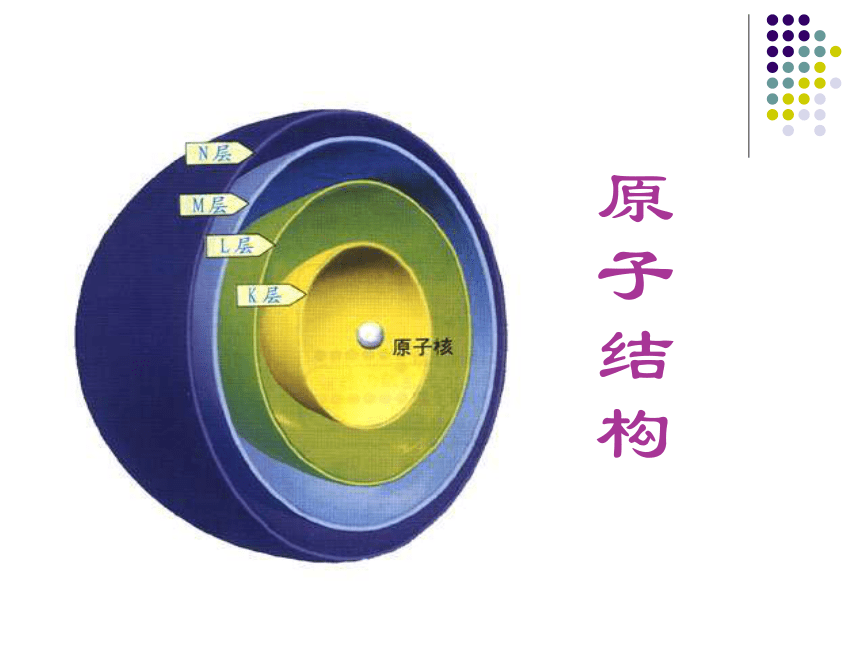
原子结构
图片预览






文档简介
课件19张PPT。
原子结构1.质量数(A) 质子数(Z) 中子数(N) 2.原子 :核电荷数 质子数 核外电子数3. 阳离子 :核电荷数 质子数 核外电子数,4. 阴离子 :核电荷数 质子数 核外电子数,原子核核外电子质子中子复习=+===>核外电子数=a-m=<核外电子数=b+n原子只是构成物质的一种粒子。原子是化学变化中不可再分的粒子,并不是不可分割的。原子并不是实心的,原子核只占原子体积的几千亿分之一。由碳原子构成由CO2分子构成由Na+和Cl-构成由铜原子构成5、关于钠原子和钠离子的认识不正确的是
A.它们的质子数相同
B.它们的电性不同
C.Na比Na+少1个电子
D.钠原子变为钠离子后,质量几乎不变C1.某元素的阳离子Rn+,核外共用x个电子,原子的质
量数为A,则该元素原子里的中子数为( )
(A)A-x-n (B)A-x+n
(C)A+x-n (D)A+x+n A2.某微粒 用表示,下列关于该微粒的叙述
正确的是( )
(A)所含质子数=A-n (B)所含中子数=A-Z
(C)所含电子数=Z+n (D)质量数=Z+A
B 练习练习3、与OH–具有相同质子数和电子数的微粒是
A、F– B、NH3 C、H2O D、Na+元素:具有相同质子数的同一类原子的总称。同位素:质子数相同而中子数不同的核
素互称为同位素。核素:具有一定质子数和一定中子数的一种原子。Cl 、 C 、 H 、O理解要点:同位素在周期表中位于同一位置,具有相同的元素符号
决定元素种类的是质子数,决定核素种类的是质子数和中子数
同一元素中,可以有若干种互为同位素的不同核素,故核素
(原子)种类远多于元素种类
天然存在的某种元素,各同位素所占的原子百分比一般是不变的
同位素质量数不同,物理性质不同,核外电子数相同,化学性质几乎相同 决定元素种类的是原子中的 ;
决定原子种类的是原子中的 ;
决定原子质量的主要是原子中的 ;
决定原子所带电荷的是原子中的 ;
决定元素的化学性质的是原子中的 。质子数质子数和中子数质子数和中子数质子数和电子数核外电子数思考:1.关于H+、H-、1H、2H、3H五种微粒,以
下说法正确的是
A.是五种氢元素
B.是氢元素的五种同位素
C.是氢元素的五种不同微粒
D.它们的数均质子相等
(CD)练习2、下列各组物质中,互为同位素的是( )
A. O2、O3、O4 B . H2 D2 T2
C . H2O、 D2O、T2O D D 1)1H、2H、3H可形成几种分子?最多有几种
相对分子质量?(6种、5种)能力考查2) 某元素X所形成的分子X2,其相对分子质量共有三
种,分别为158、160、162;
问: X元素有几种同位素? 二种能力考查(3)化学反应中,下列数据发生变化的是
A. 质子数 B. 中子数
C. 电子数 D. 质量数 (C)2.已知X,Y原子的核电荷数分别为a和b,Xm+和Yn-的核外电子排布相同,下列正确的是:
A a=b+m+n B a=b-m+n
C a=b+m-n D a=b-n-m练习(A)1、核电荷数分别为16的元素和4的元素的原子相比较,前者的下列数据是后者的4倍的是
A 电子数 B 最外层电子数
C 电子层数 D 次外层电子数 (AD)3.已知R2+核内共有N个中子,R的质量数
为A,m g R2+中含电子的物质的量为
A. mol
B. mol
C. mol
D. mol(D)能力考查已知A2-、B-、C+、D2+、E3+五种简单离子的核外电子数相等,与它们对应的原子的核电荷数由大到小的顺序是:
练习答案:E、D、C、B、A练习:
符合示意图 的粒子不
可能是
A、Ar B、k+ C、Cl- D、Cl(5)最外层电子数是次外层电子数的2倍的元素:_____
是次外层3倍的是:_ _;是次外层4倍的是:___.(9)内层电子数之和是最外层电子数2倍的元素:________(8)次外层电子数是最外层电子数的2倍的元素:_________(7)电子总数为最外层电子数的2倍的是:_________(6)电子层数与最外层电子数相等的元素:___________(4)最外层电子数等于次外层电子数的元素:________ (3)最外层有2个电子的元素:_________________(2)最外层有1个电子的元素:___________(1)原子核中无中子的原子:_______前20号元素的原子结构的特殊性Li 、Na 、K 、 HBe、Mg、Ca、HeBe、ArCNeH、Be、Al。BeSi、LiLi、PO③阴离子:核外有10个电子的微粒①分子:②阳离子:Ne、HF、H2O、NH3、CH4Na+、Mg2+、Al3+、NH4+、H3O+N3-、O2-、F-、OH-、NH2-能力考查
原子结构1.质量数(A) 质子数(Z) 中子数(N) 2.原子 :核电荷数 质子数 核外电子数3. 阳离子 :核电荷数 质子数 核外电子数,4. 阴离子 :核电荷数 质子数 核外电子数,原子核核外电子质子中子复习=+===>核外电子数=a-m=<核外电子数=b+n原子只是构成物质的一种粒子。原子是化学变化中不可再分的粒子,并不是不可分割的。原子并不是实心的,原子核只占原子体积的几千亿分之一。由碳原子构成由CO2分子构成由Na+和Cl-构成由铜原子构成5、关于钠原子和钠离子的认识不正确的是
A.它们的质子数相同
B.它们的电性不同
C.Na比Na+少1个电子
D.钠原子变为钠离子后,质量几乎不变C1.某元素的阳离子Rn+,核外共用x个电子,原子的质
量数为A,则该元素原子里的中子数为( )
(A)A-x-n (B)A-x+n
(C)A+x-n (D)A+x+n A2.某微粒 用表示,下列关于该微粒的叙述
正确的是( )
(A)所含质子数=A-n (B)所含中子数=A-Z
(C)所含电子数=Z+n (D)质量数=Z+A
B 练习练习3、与OH–具有相同质子数和电子数的微粒是
A、F– B、NH3 C、H2O D、Na+元素:具有相同质子数的同一类原子的总称。同位素:质子数相同而中子数不同的核
素互称为同位素。核素:具有一定质子数和一定中子数的一种原子。Cl 、 C 、 H 、O理解要点:同位素在周期表中位于同一位置,具有相同的元素符号
决定元素种类的是质子数,决定核素种类的是质子数和中子数
同一元素中,可以有若干种互为同位素的不同核素,故核素
(原子)种类远多于元素种类
天然存在的某种元素,各同位素所占的原子百分比一般是不变的
同位素质量数不同,物理性质不同,核外电子数相同,化学性质几乎相同 决定元素种类的是原子中的 ;
决定原子种类的是原子中的 ;
决定原子质量的主要是原子中的 ;
决定原子所带电荷的是原子中的 ;
决定元素的化学性质的是原子中的 。质子数质子数和中子数质子数和中子数质子数和电子数核外电子数思考:1.关于H+、H-、1H、2H、3H五种微粒,以
下说法正确的是
A.是五种氢元素
B.是氢元素的五种同位素
C.是氢元素的五种不同微粒
D.它们的数均质子相等
(CD)练习2、下列各组物质中,互为同位素的是( )
A. O2、O3、O4 B . H2 D2 T2
C . H2O、 D2O、T2O D D 1)1H、2H、3H可形成几种分子?最多有几种
相对分子质量?(6种、5种)能力考查2) 某元素X所形成的分子X2,其相对分子质量共有三
种,分别为158、160、162;
问: X元素有几种同位素? 二种能力考查(3)化学反应中,下列数据发生变化的是
A. 质子数 B. 中子数
C. 电子数 D. 质量数 (C)2.已知X,Y原子的核电荷数分别为a和b,Xm+和Yn-的核外电子排布相同,下列正确的是:
A a=b+m+n B a=b-m+n
C a=b+m-n D a=b-n-m练习(A)1、核电荷数分别为16的元素和4的元素的原子相比较,前者的下列数据是后者的4倍的是
A 电子数 B 最外层电子数
C 电子层数 D 次外层电子数 (AD)3.已知R2+核内共有N个中子,R的质量数
为A,m g R2+中含电子的物质的量为
A. mol
B. mol
C. mol
D. mol(D)能力考查已知A2-、B-、C+、D2+、E3+五种简单离子的核外电子数相等,与它们对应的原子的核电荷数由大到小的顺序是:
练习答案:E、D、C、B、A练习:
符合示意图 的粒子不
可能是
A、Ar B、k+ C、Cl- D、Cl(5)最外层电子数是次外层电子数的2倍的元素:_____
是次外层3倍的是:_ _;是次外层4倍的是:___.(9)内层电子数之和是最外层电子数2倍的元素:________(8)次外层电子数是最外层电子数的2倍的元素:_________(7)电子总数为最外层电子数的2倍的是:_________(6)电子层数与最外层电子数相等的元素:___________(4)最外层电子数等于次外层电子数的元素:________ (3)最外层有2个电子的元素:_________________(2)最外层有1个电子的元素:___________(1)原子核中无中子的原子:_______前20号元素的原子结构的特殊性Li 、Na 、K 、 HBe、Mg、Ca、HeBe、ArCNeH、Be、Al。BeSi、LiLi、PO③阴离子:核外有10个电子的微粒①分子:②阳离子:Ne、HF、H2O、NH3、CH4Na+、Mg2+、Al3+、NH4+、H3O+N3-、O2-、F-、OH-、NH2-能力考查
