初中科学实验专题(常见气体制备)
图片预览


文档简介
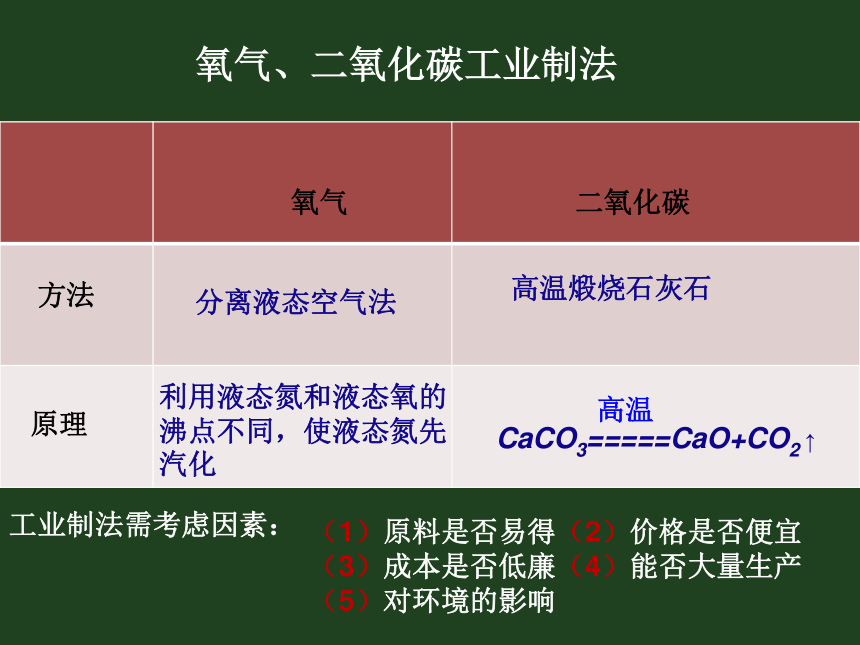
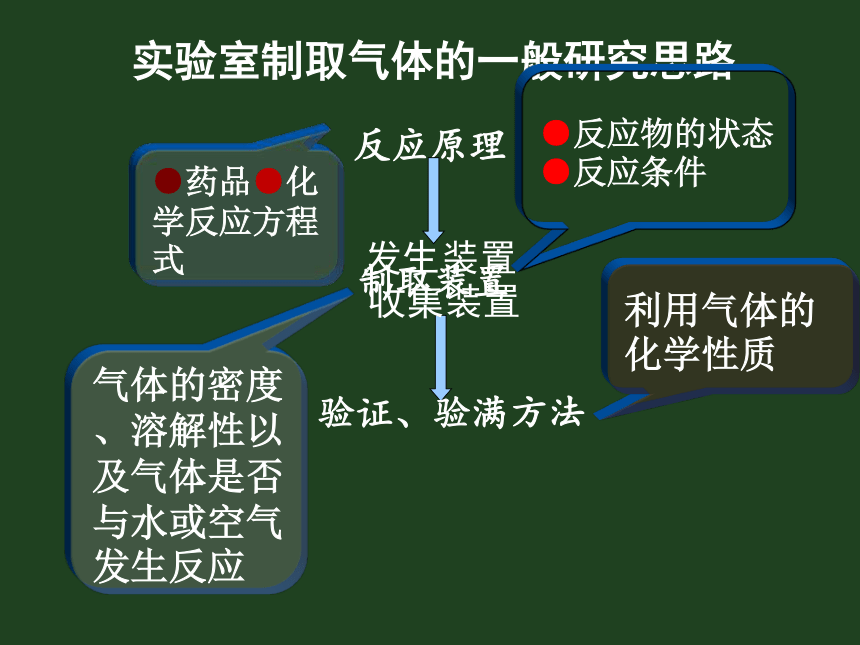
课件26张PPT。实验专题 常见气体制备氧气、二氧化碳工业制法 氧气二氧化碳方法原理分离液态空气法高温煅烧石灰石利用液态氮和液态氧的沸点不同,使液态氮先汽化工业制法需考虑因素:(1)原料是否易得(2)价格是否便宜 (3)成本是否低廉(4)能否大量生产(5)对环境的影响 实验室制取气体的一般研究思路反应原理制取装置验证、验满方法●药品●化学反应方程式发生装置收集装置●反应物的状态●反应条件气体的密度、溶解性以及气体是否与水或空气发生反应利用气体的化学性质一、实验室制取气体的药品和反应原理想一想
下列三种方法用于实验室制取气体是否理想?为什么?
1.用镁和盐酸反应或铁和盐酸反应制氢气
2.用木炭与氧气反应制取二氧化碳
3.在高温高压的条件下用氮气和氢气反应制取氨气小结:选择药品和反应时必须要考虑的因素药品的成本:廉价易得反应速率:适中反应条件:节能、易实现
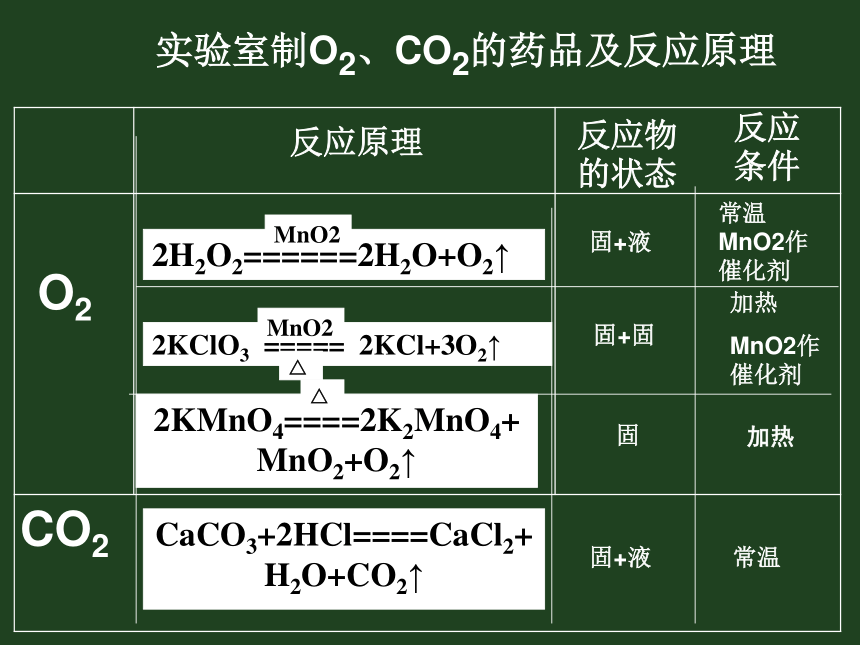
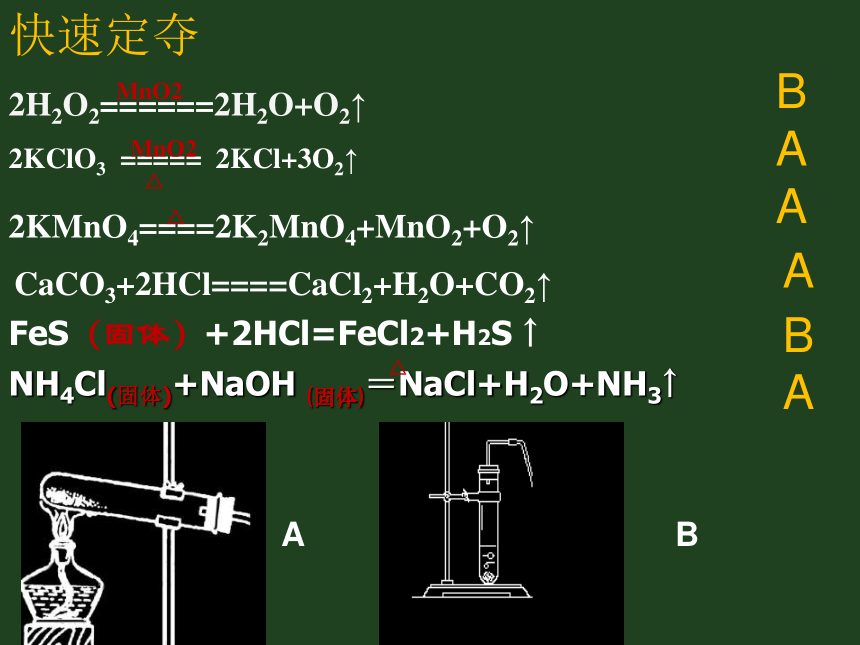
生成物:纯度高、便于收集、污染少实验室制O2、CO2的药品及反应原理反应物的状态反应条件O2CO22H2O2======2H2O+O2↑MnO22KClO3 ===== 2KCl+3O2↑MnO2△2KMnO4====2K2MnO4+
MnO2+O2↑△CaCO3+2HCl====CaCl2+H2O+CO2↑固+液常温 MnO2作催化剂固+固固固+液加热
MnO2作催化剂
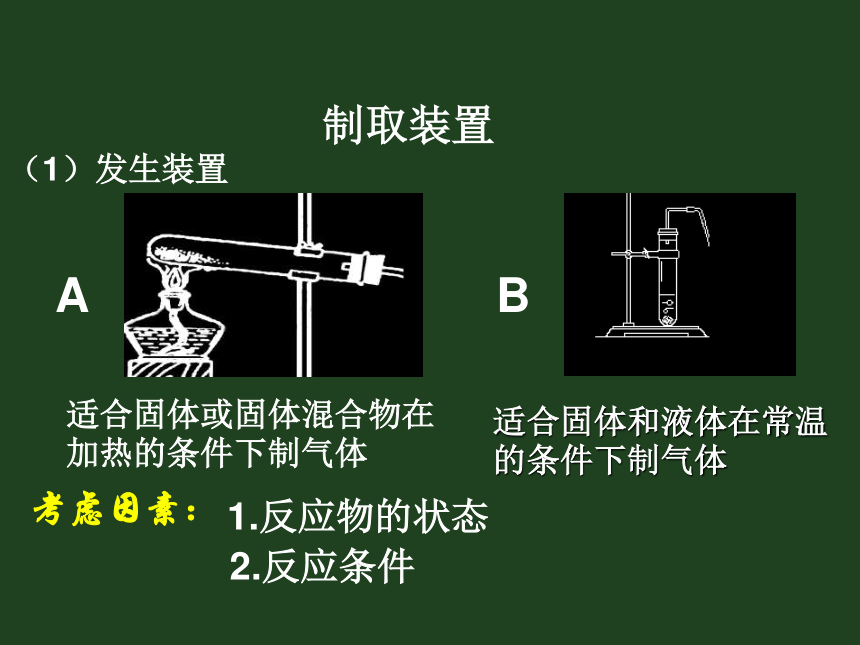
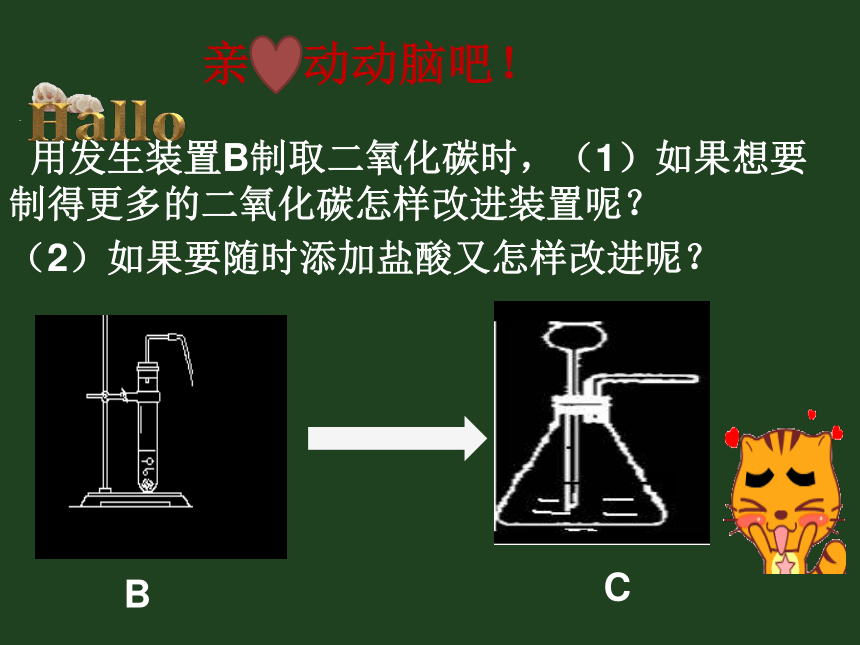
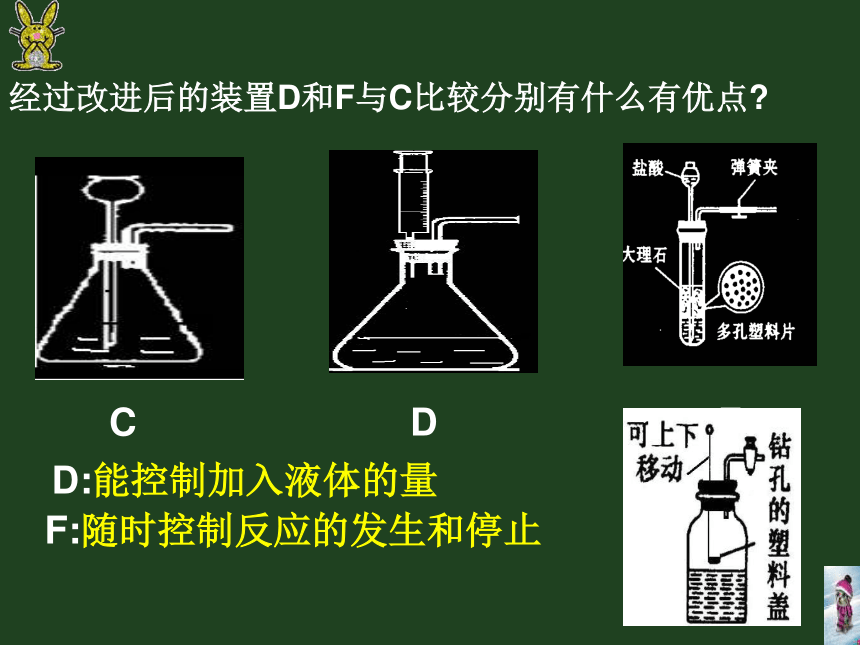
加热常温制取装置(1)发生装置适合固体或固体混合物在加热的条件下制气体适合固体和液体在常温的条件下制气体考虑因素:1.反应物的状态2.反应条件2KClO3 ===== 2KCl+3O2↑MnO2△2H2O2======2H2O+O2↑MnO22KMnO4====2K2MnO4+MnO2+O2↑△CaCO3+2HCl====CaCl2+H2O+CO2↑快速定夺FeS(固体)+2HCl=FeCl2+H2S ↑NH4Cl(固体)+NaOH (固体)=NaCl+H2O+NH3↑ABBAAAB△A亲 动动脑吧! 用发生装置B制取二氧化碳时,(1)如果想要 制得更多的二氧化碳怎样改进装置呢?(2)如果要随时添加盐酸又怎样改进呢?BCCDF经过改进后的装置D和F与C比较分别有什么有优点?D:能控制加入液体的量F:随时控制反应的发生和停止收集装置的选择难溶于水且不与水反应密度比空气大且不与空气发生反应密度比空气小且不与空气发生反应
思考:1.排水法和排空气法收集所用的导气管有什么不同?排空气时导气管为何要伸入到接近瓶底的地方?
2.收集气体选用上述何种装置是由气体的哪些性质决定的?
3.若用排水法收集气体什么时候开始收集呢?
哇塞!你最棒?♀如果要收集CO2, H2,O2,CO,CH4等分别可使用上述哪些装置?
CO2 :选BH2 :选A,CO2 :选A,BCO :选ACH4 :选AC思维拓展!你会吗?
1、如果改用①装置来收集CO2, H2, 气体应该如何进出? 小结:若要从a端进气,该气体要满足密度比空气大,若要从b端进气,该气体要满足密度比空气小。 ?2、若用图②排水法收集气体,气体应该有哪些性质,又如何进出呢?图③有何用途?
气体的验满将带火星的木条靠近集气瓶口,若木条复燃,说明已收集满 。将燃着的木条靠近集气瓶口,若木条熄灭,说明已收集满 。用排水法收集时,当瓶口向外冒出气泡时说明收集的气体满了。气体的检验将带火星的木条插入集气瓶内,若复燃,说明是氧气 。将气体通入澄清的石灰水,振荡,若澄清的石灰水变浑浊,说明是二氧化碳 。气体发生气体净化气体收集尾气处理 ①除杂 ②干燥 性质验证部分一套完整的制气装置气体净化气体除杂气体干燥洗气瓶
进气管应“长进短出”液体试剂如果在制取CO时,气体中含有CO2 ,将采用什么试剂除去CO2 ? 不能引来新的气体干燥剂的选择及使用原则1、选择原则①气体在被干燥的过程中要不能被减少
②不要引入新的杂质。2、选择方法:根据气体的 酸、碱性气体的酸碱性 干燥剂的酸碱性 保持一致3、常见干燥剂酸性干燥剂碱性干燥剂中性干燥剂如:浓硫酸如:碱石灰、生石灰、固体NaOH等如CaCl2固体(不能干燥NH3)常见干燥剂及使用装置 → →浓硫酸无水CaCl2碱石灰H2,O2,SO2, CO, CH4H2,O2, N2,
CH4, NH3
NH3NH3SO2,CO2……常见除尾气装置除去尾气的方法(1)燃烧法(2)气囊收集法(3)碱液吸收法 (4)水溶解法 如CH4、H2、CO等如CO2,SO2如HCl、NH3等防止水倒吸的原理是:当液体被吸收时,液面上升到漏斗中,由于漏斗容积大,导致烧杯内液面明显下降,使漏斗口脱离液面,因为重力作用,漏斗中液体又回流到烧杯中,从而防止倒吸。总 结常见气体制备(1)气体发生装置(2)气体收集装置(3)气体的除杂装置(4)气体的干燥装置(5)气体尾气处理装置1,下列是实验室氧气的制备、收集、验满、验证的操作,其中正确的( )A2,如图所示的四个装置图及其使用方法的说明中,错误的一项是( )
A 硫化氢(H2S)是一种有毒气体,其密度比空气大且能溶于水形成氢硫酸。能与氢氧化钠溶液反应,实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下通过发生复分解反应制得硫化氢气体。试回答:①制取硫化氢气体的发生装置可以选用??????????
②若用C装置收集硫化氢气体,进气口应为?????? ,原因是?????? ? 。
③为了验证硫化氢的水溶液呈酸性,可以将该气体通入装置D,D中所盛的试剂应该是????????? ? __,现象是???? ??? ????
④做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置E吸收,E中的试剂应该为????????? ???溶液。
Bb硫化氢气体密度比空气的密度大紫色石蕊试液氢氧化钠变红变式训练
甲 乙 丙 丁 戊练一练:稀盐酸和锌粒反应制取氢气
利用下列仪器制取一定量氢气并测定其在该温度和压强下的体积(假定制得氢气的体积不超过100毫升),请设计实验装置。df各仪器的连接顺序是(按接口字母)________________________a→c→d→b
25判断下图是否有错误?如果有,请指出错误并加以改正。试管口要略向下倾斜导气管只需稍出橡胶塞铁夹应夹在试管中上部导管口只能插在集气瓶口附近应加酒精长颈漏斗应该插入液面以下。伸入反应容器中的导气管不宜过长。谢大家
下列三种方法用于实验室制取气体是否理想?为什么?
1.用镁和盐酸反应或铁和盐酸反应制氢气
2.用木炭与氧气反应制取二氧化碳
3.在高温高压的条件下用氮气和氢气反应制取氨气小结:选择药品和反应时必须要考虑的因素药品的成本:廉价易得反应速率:适中反应条件:节能、易实现
生成物:纯度高、便于收集、污染少实验室制O2、CO2的药品及反应原理反应物的状态反应条件O2CO22H2O2======2H2O+O2↑MnO22KClO3 ===== 2KCl+3O2↑MnO2△2KMnO4====2K2MnO4+
MnO2+O2↑△CaCO3+2HCl====CaCl2+H2O+CO2↑固+液常温 MnO2作催化剂固+固固固+液加热
MnO2作催化剂
加热常温制取装置(1)发生装置适合固体或固体混合物在加热的条件下制气体适合固体和液体在常温的条件下制气体考虑因素:1.反应物的状态2.反应条件2KClO3 ===== 2KCl+3O2↑MnO2△2H2O2======2H2O+O2↑MnO22KMnO4====2K2MnO4+MnO2+O2↑△CaCO3+2HCl====CaCl2+H2O+CO2↑快速定夺FeS(固体)+2HCl=FeCl2+H2S ↑NH4Cl(固体)+NaOH (固体)=NaCl+H2O+NH3↑ABBAAAB△A亲 动动脑吧! 用发生装置B制取二氧化碳时,(1)如果想要 制得更多的二氧化碳怎样改进装置呢?(2)如果要随时添加盐酸又怎样改进呢?BCCDF经过改进后的装置D和F与C比较分别有什么有优点?D:能控制加入液体的量F:随时控制反应的发生和停止收集装置的选择难溶于水且不与水反应密度比空气大且不与空气发生反应密度比空气小且不与空气发生反应
思考:1.排水法和排空气法收集所用的导气管有什么不同?排空气时导气管为何要伸入到接近瓶底的地方?
2.收集气体选用上述何种装置是由气体的哪些性质决定的?
3.若用排水法收集气体什么时候开始收集呢?
哇塞!你最棒?♀如果要收集CO2, H2,O2,CO,CH4等分别可使用上述哪些装置?
CO2 :选BH2 :选A,CO2 :选A,BCO :选ACH4 :选AC思维拓展!你会吗?
1、如果改用①装置来收集CO2, H2, 气体应该如何进出? 小结:若要从a端进气,该气体要满足密度比空气大,若要从b端进气,该气体要满足密度比空气小。 ?2、若用图②排水法收集气体,气体应该有哪些性质,又如何进出呢?图③有何用途?
气体的验满将带火星的木条靠近集气瓶口,若木条复燃,说明已收集满 。将燃着的木条靠近集气瓶口,若木条熄灭,说明已收集满 。用排水法收集时,当瓶口向外冒出气泡时说明收集的气体满了。气体的检验将带火星的木条插入集气瓶内,若复燃,说明是氧气 。将气体通入澄清的石灰水,振荡,若澄清的石灰水变浑浊,说明是二氧化碳 。气体发生气体净化气体收集尾气处理 ①除杂 ②干燥 性质验证部分一套完整的制气装置气体净化气体除杂气体干燥洗气瓶
进气管应“长进短出”液体试剂如果在制取CO时,气体中含有CO2 ,将采用什么试剂除去CO2 ? 不能引来新的气体干燥剂的选择及使用原则1、选择原则①气体在被干燥的过程中要不能被减少
②不要引入新的杂质。2、选择方法:根据气体的 酸、碱性气体的酸碱性 干燥剂的酸碱性 保持一致3、常见干燥剂酸性干燥剂碱性干燥剂中性干燥剂如:浓硫酸如:碱石灰、生石灰、固体NaOH等如CaCl2固体(不能干燥NH3)常见干燥剂及使用装置 → →浓硫酸无水CaCl2碱石灰H2,O2,SO2, CO, CH4H2,O2, N2,
CH4, NH3
NH3NH3SO2,CO2……常见除尾气装置除去尾气的方法(1)燃烧法(2)气囊收集法(3)碱液吸收法 (4)水溶解法 如CH4、H2、CO等如CO2,SO2如HCl、NH3等防止水倒吸的原理是:当液体被吸收时,液面上升到漏斗中,由于漏斗容积大,导致烧杯内液面明显下降,使漏斗口脱离液面,因为重力作用,漏斗中液体又回流到烧杯中,从而防止倒吸。总 结常见气体制备(1)气体发生装置(2)气体收集装置(3)气体的除杂装置(4)气体的干燥装置(5)气体尾气处理装置1,下列是实验室氧气的制备、收集、验满、验证的操作,其中正确的( )A2,如图所示的四个装置图及其使用方法的说明中,错误的一项是( )
A 硫化氢(H2S)是一种有毒气体,其密度比空气大且能溶于水形成氢硫酸。能与氢氧化钠溶液反应,实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下通过发生复分解反应制得硫化氢气体。试回答:①制取硫化氢气体的发生装置可以选用??????????
②若用C装置收集硫化氢气体,进气口应为?????? ,原因是?????? ? 。
③为了验证硫化氢的水溶液呈酸性,可以将该气体通入装置D,D中所盛的试剂应该是????????? ? __,现象是???? ??? ????
④做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置E吸收,E中的试剂应该为????????? ???溶液。
Bb硫化氢气体密度比空气的密度大紫色石蕊试液氢氧化钠变红变式训练
甲 乙 丙 丁 戊练一练:稀盐酸和锌粒反应制取氢气
利用下列仪器制取一定量氢气并测定其在该温度和压强下的体积(假定制得氢气的体积不超过100毫升),请设计实验装置。df各仪器的连接顺序是(按接口字母)________________________a→c→d→b
25判断下图是否有错误?如果有,请指出错误并加以改正。试管口要略向下倾斜导气管只需稍出橡胶塞铁夹应夹在试管中上部导管口只能插在集气瓶口附近应加酒精长颈漏斗应该插入液面以下。伸入反应容器中的导气管不宜过长。谢大家
