化学人教版(2019)必修第二册8.3环境保护与绿色化学(共27张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册8.3环境保护与绿色化学(共27张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-17 00:00:00 | ||
图片预览








文档简介
(共27张PPT)
学
习
目
标
学
习
重
点
第三节 环境保护与绿色化学
1.能列举常见的大气、水体和土襄的污染物及其危害,说明常见污染的成因和防治措施的化学原理,树立“绿水青山就是金山银山”的理念。
2.以酸雨防治和污水处理为例,设计简单的防治方案,体会化学原理的应用对环境保护的作用,说明化学科学在生产、生活中的应用价值。
3.通过环氧乙烷两种制备方法的讨论,树立“绿色化学”的观念,并能运用“绿色化学”思想分析和讨论化工生产的相关问题,形成节约和循环利用的可持续发展意识。
SO2等污染物的控制、消除和回收利用;污水处理的流程、方法及原理。
学
习
难
点
“绿色化学”观念的形成和“绿色化学”思想的运用。
1.环境保护
(1)环境问题:主要是指由于人类_______地开发和利用_________而造成的_________破坏,以及___________和_________所造成的环境污染。
一、化学与环境保护
不合理
自然资源
生态环境
工农业生产
人类生活
存在形态
含量
分析
测定
(2)环境保护的任务
①环境监测:对污染物的_________、_____等进行_____和_____,为控制和消除污染提供可靠的数据。
②治理工业“三废”(废水、废气、废渣)。
③寻找源头治理环境污染的生产工艺:杜绝污染物的排放,能从根本上解决环境问题。
练习1.“保护环境”是我国的基本国策。下列做法不应该提倡的是( )
A.采取低碳、节俭的生活方式
B.按照规定对生活废弃物进行分类放置
C.深入农村和社区宣传环保知识
D.经常使用一次性筷子、纸杯、塑料袋等
D
环境污染
大气污染
水污染
土壤污染
工业“三废”
废气
废水
废渣
化石燃料的燃烧和工业生产
废气和颗粒物
工农业生产和日常生活中
农药、化肥、生活污水
2.污染分类及污染物的来源
(1)大气污染及其治理
①污染物主要来源:化石燃料的燃烧和工业生产过程产生的废气及其携带的颗粒物。
②污染物主要成分:CO、SO2、氮氧化物、挥发性有机物、烟尘等。
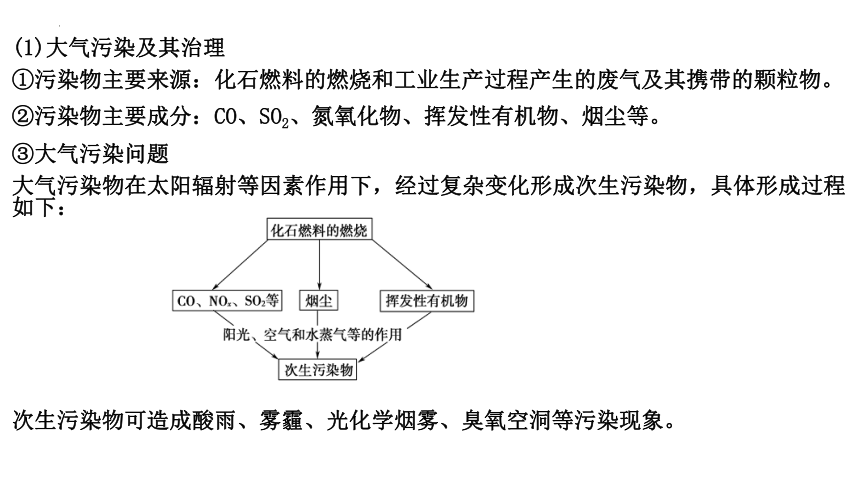
③大气污染问题
大气污染物在太阳辐射等因素作用下,经过复杂变化形成次生污染物,具体形成过程如下:
次生污染物可造成酸雨、雾霾、光化学烟雾、臭氧空洞等污染现象。
环境问题 主要污染物 主要危害
酸雨(pH<5.6) SO2及氮氧化物(NOx) 土壤酸化、水源污染、建筑物被腐蚀等
温室效应 CO2、CH4 造成全球气候变暖,水位上升,陆地面积减小
臭氧空洞 氟氯代烃、氮氧化物(NOx) 到达地球表面的紫外线明显增多,给人类健康(皮肤癌)及生态环境带来多方面危害
光化学烟雾 碳氢化合物、氮氧化物(NOx) 刺激人体器官,特别是人的呼吸系统,使人生病甚至死亡
PM2.5 直径小于或等于2.5微米颗粒物 污染空气,形成雾霾天气,增加交通事故,危害人体健康
1.CO2能引起温室效应,故CO2属于大气污染物之一,所以应最大限度地杜绝CO2的排放。这种观点对吗?
不对。CO2不属于大气污染物,CO2参与光合作用,所以CO2还是有一定作用的。当然,为减少温室效应,应该减少CO2的排放。
【思考与讨论】
2. 常温下pH小于7的雨水就是酸雨,对吗?为什么?
不对。正常雨水因溶解了空气中的CO2而使雨水的pH小于7。pH小于5.6的雨水称为酸雨。
3.酸雨是如何形成的?又如何治理?
a.硫酸型酸雨及治理
(1)形成原理:_____________________________________________。
课本P119【思考与讨论】(1)
(2)治理:可在煤中添加生石灰、熟石灰、石灰石,或用氨水为脱硫剂。反应原理如下:
①生石灰:________________________________________________。
②熟石灰:________________________________________________。
③石灰石:__________________________________________________。
④氨水:_______________________________________________________。
(1)形成原理:____________________________________________。
(2)治理:工业尾气中的NOx一般用烧碱吸收,汽车尾气一般进行催化转化。
①碱液吸收:2NO2+2NaOH===NaNO3+NaNO2+H2O
NO2+NO+2NaOH===2NaNO2+H2O
②催化转化:2NO2+4CO N2+4CO2
2NO+O2===2NO2 3NO2+H2O===HNO3+NO
b.硝酸型酸雨及治理
练习3.将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧,这样处理的目的是( )
①使煤充分燃烧,提高煤的利用率。②减少SO2的产生,避免造成“酸雨”。
③减少有毒的CO产生,避免污染空气④减少CO2的产生,避免“温室效应”。
A.①②③ B.②③④ C.①③④ D.①②③④
A
练习4.为了防治酸雨,工业上采用生石灰和含硫的煤混合使用以“固硫”
(避免硫的化合物进入大气),最后生成石膏。试回答下列问题:(1)比较此法与石灰石粉末与含硫的煤混合法哪个更好些?___(填字母)。A.生石灰 B.石灰石
原因是 。(2)你认为减少酸雨产生可采取的措施是_________(填字母)。①少用煤作燃料 ②把工厂的烟囱造高 ③先将燃料煤脱硫 ④在土壤中加熟石灰防止酸化 ⑤开发新能源,避免含S、N的氧化物的大量排放A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
A
石灰石分解为CaO需消耗能量,浪费煤,使生产成本提高。
C
练习5.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(2)写出一氧化碳与一氧化氮反应的化学方程式_______________________。
(3)在“催化转化器”转化后的气体中有CO2、SO2,下列不能鉴别这两种气体的是_________。
A.KMnO4溶液 B.石灰水 C.BaCl2溶液 D.品红溶液
(4)有效减少城市污染的方法可以有_________。
A.开发氢能源 B.使用电动车 C.植树造林 D.戴上呼吸面具
BC
ABC
2CO+2NO = 2CO2+N2
④大气污染的治理措施
限制和减少污染物的排放,吸收和处理大气污染物。
a.通过改善燃料质量、改进燃烧裝置和燃烧技术、改进排烟设备、发展洁净煤技术降低燃煤在能源结构中的比例等措施,减少煤等化石燃料燃烧产生的污染;
b.通过推广使用无铅汽油、在汽车尾气系统中安装催化转化器、使用燃料电池、乙醇汽油作为汽油代用品、发展电动车等措施,减少汽车等机动车尾气污染;
c.停止氟氯代烷的生产和使用以保护臭氧层;
d.通过合理使用煤气、石油气或天然气等家用燃料、使用合格的环保型建筑材料和装饰材料、禁止在公共场所吸烟等措施降低CO、CO2、NO、NO2、SO2、尼古丁、甲醛、苯及其同系物、氡等污染物含量,改善室内空气质量等。
(2)水污染及其治理
①工农业生产和生活中产生的污水,任意排放会导致土壤、水体污染,必须经过多步处理才能达到排放标准。
环境问题 主要污染物 主要危害
赤潮和水华 含氮、磷元素的废水 使水体富营养化,导致水中藻类疯长,消耗水中溶解的氧,使水质恶化
②废水污染造成的环境问题:
课本P119【思考与讨论】(2)
练习6.我国近海海域海水中一些元素含量普遍超标,富营养化十分严重,经常发生“赤潮”现象。下列生活用品中能引起“赤潮”的是( )
A.肥皂 B.含磷洗涤剂 C.加酶洗衣粉 D.化妆品
B
③污水处理流程
a.一级处理:通常采用____方法,即用格栅间、沉淀池等除去污水中不溶解的污染物。经一级处理后的水一般达不到排放标准,一级处理作为预处理。
b.二级处理:采用____方法(或______法)及某些化学方法,除去水中的可降解有机物等污染物。经二级处理后的水一般可以达到国家规定的排放标
c.三级处理:主要采用_________、__________、__________和________等,对污水进行深度处理和净化。经三级处理后水可用于绿化和景观用水等。
物理
生物
微生物
化学沉淀法
氧化还原法
离子交换法
反渗透法
练习7.高铁酸钠(Na2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe3+。
(1)高铁酸钠中铁元素的化合价为_____;高铁酸钠能消毒杀菌,这是基于它的什么性质:__________。
(2)高铁酸钠用于水处理,除了能消毒杀菌外,它还能沉降水中的悬浮杂质,起到净水作用,请说明其净水原理:
____________________________________________________________________________________________________________________________________________________________
高铁酸钠的还原产物是Fe3+,Fe3+可发生水解,生成Fe(OH)3胶体,它可吸附水中悬浮的杂质或泥沙胶粒等一起凝聚而沉降,达到净水的效果
+6
强氧化性
(3)固体废弃物造成的污染及其治理
主要指生活垃圾、工业废料随意堆放造成的污染。目前最引入注意的是由塑料制品造成的白色污染及废旧电池造成的重金属污染。垃圾污染范围广泛,对环境及生物的不良影响途径多样。
①处理原则:_______、_______和_______。
②目的:_____________和_____________。
无害化
减量化
资源化
减少环境污染
资源回收利用
练习8.为了保护自然环境,提高人民的生活质量,必须重视处理“白色污染”。该“白色污染”指的是( )
A.冶炼厂的白色烟尘 B.石灰窑的白色粉末
C.聚氯乙烯等塑料垃圾 D.白色建筑材料
C
(1)化学工作者进行的环境质量监测工作可有可无,有污染治理就行( )
提示 环境质量监测工作是进行环境质量评价和污染治理的基础,非常必要。
(2)化石燃料燃烧产生的CO、NOx、SO2为次生污染物( )
提示 CO、NOx、SO2为一次污染物,其形成的酸雨、光化学烟雾等为次生污染物。
(3)“燃煤固硫”“汽车尾气催化净化”都能提高空气质量( )
提示 “燃煤固硫”可以减少SO2的污染,汽车尾气催化净化可以减少CO、NOx及某些有机物的污染。
1.判断正误
×
×
√
(4)工业废渣和生活垃圾等固体废弃物对环境影响不大,可不必处理( )
提示 处理固体废弃物要遵循无害化、减量化和资源化原则,达到减少环境污染和资源回收利用两个重要目的。
(5)污水的一级处理通常采用化学法和生物法将难溶解的污染物除去( )
提示 一级处理通常采用物理方法,用格栅间、沉淀池等去除不溶性污染物。
×
×
【课堂检测】
2.活性炭联合脱硫脱硝技术(AC)是一种比较成熟的脱硫脱硝技术,可以在较低的温度下,将废气中的SO2、NOx通过一系列反应生成铵盐,从而变废为宝,其工作示意图如右所示:
(1)SO2在活性炭表面被氧化最终生成硫酸,反应方程式为:
_____________________________________________________________。
2SO2+O2
2SO3、SO3+H2O===H2SO4(或2SO2+O2+2H2O===2H2SO4)
(2)吸收塔加入NH3后,可脱除废气中的NO、NO2,写出NO和NO2分别和NH3反应的化学方程式:_________________________、___________________________。
4NH3+6NO===5N2+6H2O
8NH3+6NO2===7N2+12H2O
(3)NH3和吸收塔中生成的H2SO4反应,会生成铵盐,写出反应的化学方程式:_________________________________________________________。
2NH3+
H2SO4===(NH4)2SO4(或NH3+H2SO4===
NH4HSO4)
(4)活性炭的造价较高,工业上一般选用活性焦作为吸附剂来脱硫脱硝,活性炭来自煤干馏产品,煤的干馏为_____(填“物理”或“化学”)变化,从煤干馏产品中获取苯、二甲苯的操作方法为:____________。
化学
蒸馏(或分馏)
二、绿色化学
1.绿色化学也称_________化学。
2.核心思想:改变“先污染后治理”的观念和做法,利用化学原理和技术手段,减少或消除产品在生产和应用中涉及的有害化学物质,实现从_________或_____环境污染。
3.原子经济性反应:反应物的原子全部转化为期望的最终产物,原子利用率达到______。
环境友好
源头减少
消除
100%
练习1.“绿色化学”要求从经济、环保和技术上设计可行的化学反应。据此,由单质镁制硝酸镁的下列4个方案中,你认为可行而且符合“绿色化学”要求的方案是( )
C
期望产物的总质量
生成物的总质量
原子利用率=
X100%
①计算两种生产工艺原子利用率
③原子利用率为100%的化学反应类型有哪些?
④试从反应物、产物对环境的影响,生产工艺,原子经济性反应,催化剂选择性等角度分析两方法的优劣。
方法一:反应物Cl2和Ca(OH)2对环境及设备有很大的污染性和腐蚀性,生产工艺分二步,产率和原子利用率低,成本高,反应的选择性低,产物中有大量的非期望物质。
方法二:反应物中O2无毒无污染、生产工艺简单,原子利用率为100%,催化剂选择性高、产率高、成本低,因此方法二更优。
化合反应、加聚反应、加成反应
某产物的实际产量
该产物的理论产量
产率=
X100%
原子利用率和产率不一样
②原子利用率和产率一样吗?
原料、溶剂
反应路线
资源、能源
无毒、无害,应致力于开发无溶剂存在下的反应;在起始端就采用实现污染预防的科学手段
开发、应用“原子经济性”的反应路线,最大限度地利用反应物分子中的每一个原子,充分利用资源,实现废物的零排放。
绿色化学要求充分利用可再生资源,合理利用资源和能源,降低生产成本,使之符合可持续发展的理念。
反应条件
尽量在温和的温度和压力下进行。节约能源;寻找新型、高效、对环境友好、可回收、高选择性的催化剂。
⑤绿色化学对化学研究和化工生产的提出的新的挑战
4.绿色化学对化学反应的要求
5.开发和利用自然资源遵循的原则
减量化(Reduce) 减少原料、节约能源
再利用(Reuse) 如催化剂、反应载体
再循环(Recycle) 物质循环、能量循环
(1)“绿色化学”就是污染后有效治理的化学思想( )
提示 “绿色化学”思想是从源头上减少或消除污染的化学。
(2)“绿色化学”就是指在化工生产中不排放任何有害物质( )
(3)在汽车排气管上安装“催化转化器”把CO、NO催化生成N2和CO2,符合绿色化学的理念( )
提示 “绿色化学”理念是从源头上减少或消除污染。
1.判断正误
×
√
×
(4)“3R”原则(减量化、再利用和再循环)是开发和利用自然资源的基本原则( )
(5)植物秸秆含大量钾元素,焚烧后作钾肥符合“绿色化学”的思想( )
提示 植物秸秆燃烧会产生大量的污染物,不符合“绿色化学”的思想。
(6)利用阳光发电,光解水制氢气是解决能源危机,实现可持续发展的有效途径( )
√
×
√
【课堂检测】
2.某工厂利用铜屑制硝酸铜。你认为可以用哪些方法?哪种最好?
① 铜与浓硝酸反应;② 铜与稀硝酸反应;③ 铜与氧气反应后,再与硝酸反应。
从原子经济性的角度考虑,从最大限度地减少废物的排放的角度考虑,方法③是最好的。
3.“绿色商品”是指对环境无污染的商品,下列商品能称为“绿色商品”的是( )
A.含铅汽油 B.含磷洗涤剂 C.含氟冰箱 D.加碘食盐
D
4.在绿色化学工艺中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子的利用率为100%。在用CH3CH===CH2合成CH2===C(CH3)COOCH3的过程中,欲使原子的利用率达到最高,还需要其他的反应物有( )
A.CO2和H2O B.CO和HCHO C.CH3OH和H2 D.H2和CO2
B
学
习
目
标
学
习
重
点
第三节 环境保护与绿色化学
1.能列举常见的大气、水体和土襄的污染物及其危害,说明常见污染的成因和防治措施的化学原理,树立“绿水青山就是金山银山”的理念。
2.以酸雨防治和污水处理为例,设计简单的防治方案,体会化学原理的应用对环境保护的作用,说明化学科学在生产、生活中的应用价值。
3.通过环氧乙烷两种制备方法的讨论,树立“绿色化学”的观念,并能运用“绿色化学”思想分析和讨论化工生产的相关问题,形成节约和循环利用的可持续发展意识。
SO2等污染物的控制、消除和回收利用;污水处理的流程、方法及原理。
学
习
难
点
“绿色化学”观念的形成和“绿色化学”思想的运用。
1.环境保护
(1)环境问题:主要是指由于人类_______地开发和利用_________而造成的_________破坏,以及___________和_________所造成的环境污染。
一、化学与环境保护
不合理
自然资源
生态环境
工农业生产
人类生活
存在形态
含量
分析
测定
(2)环境保护的任务
①环境监测:对污染物的_________、_____等进行_____和_____,为控制和消除污染提供可靠的数据。
②治理工业“三废”(废水、废气、废渣)。
③寻找源头治理环境污染的生产工艺:杜绝污染物的排放,能从根本上解决环境问题。
练习1.“保护环境”是我国的基本国策。下列做法不应该提倡的是( )
A.采取低碳、节俭的生活方式
B.按照规定对生活废弃物进行分类放置
C.深入农村和社区宣传环保知识
D.经常使用一次性筷子、纸杯、塑料袋等
D
环境污染
大气污染
水污染
土壤污染
工业“三废”
废气
废水
废渣
化石燃料的燃烧和工业生产
废气和颗粒物
工农业生产和日常生活中
农药、化肥、生活污水
2.污染分类及污染物的来源
(1)大气污染及其治理
①污染物主要来源:化石燃料的燃烧和工业生产过程产生的废气及其携带的颗粒物。
②污染物主要成分:CO、SO2、氮氧化物、挥发性有机物、烟尘等。
③大气污染问题
大气污染物在太阳辐射等因素作用下,经过复杂变化形成次生污染物,具体形成过程如下:
次生污染物可造成酸雨、雾霾、光化学烟雾、臭氧空洞等污染现象。
环境问题 主要污染物 主要危害
酸雨(pH<5.6) SO2及氮氧化物(NOx) 土壤酸化、水源污染、建筑物被腐蚀等
温室效应 CO2、CH4 造成全球气候变暖,水位上升,陆地面积减小
臭氧空洞 氟氯代烃、氮氧化物(NOx) 到达地球表面的紫外线明显增多,给人类健康(皮肤癌)及生态环境带来多方面危害
光化学烟雾 碳氢化合物、氮氧化物(NOx) 刺激人体器官,特别是人的呼吸系统,使人生病甚至死亡
PM2.5 直径小于或等于2.5微米颗粒物 污染空气,形成雾霾天气,增加交通事故,危害人体健康
1.CO2能引起温室效应,故CO2属于大气污染物之一,所以应最大限度地杜绝CO2的排放。这种观点对吗?
不对。CO2不属于大气污染物,CO2参与光合作用,所以CO2还是有一定作用的。当然,为减少温室效应,应该减少CO2的排放。
【思考与讨论】
2. 常温下pH小于7的雨水就是酸雨,对吗?为什么?
不对。正常雨水因溶解了空气中的CO2而使雨水的pH小于7。pH小于5.6的雨水称为酸雨。
3.酸雨是如何形成的?又如何治理?
a.硫酸型酸雨及治理
(1)形成原理:_____________________________________________。
课本P119【思考与讨论】(1)
(2)治理:可在煤中添加生石灰、熟石灰、石灰石,或用氨水为脱硫剂。反应原理如下:
①生石灰:________________________________________________。
②熟石灰:________________________________________________。
③石灰石:__________________________________________________。
④氨水:_______________________________________________________。
(1)形成原理:____________________________________________。
(2)治理:工业尾气中的NOx一般用烧碱吸收,汽车尾气一般进行催化转化。
①碱液吸收:2NO2+2NaOH===NaNO3+NaNO2+H2O
NO2+NO+2NaOH===2NaNO2+H2O
②催化转化:2NO2+4CO N2+4CO2
2NO+O2===2NO2 3NO2+H2O===HNO3+NO
b.硝酸型酸雨及治理
练习3.将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧,这样处理的目的是( )
①使煤充分燃烧,提高煤的利用率。②减少SO2的产生,避免造成“酸雨”。
③减少有毒的CO产生,避免污染空气④减少CO2的产生,避免“温室效应”。
A.①②③ B.②③④ C.①③④ D.①②③④
A
练习4.为了防治酸雨,工业上采用生石灰和含硫的煤混合使用以“固硫”
(避免硫的化合物进入大气),最后生成石膏。试回答下列问题:(1)比较此法与石灰石粉末与含硫的煤混合法哪个更好些?___(填字母)。A.生石灰 B.石灰石
原因是 。(2)你认为减少酸雨产生可采取的措施是_________(填字母)。①少用煤作燃料 ②把工厂的烟囱造高 ③先将燃料煤脱硫 ④在土壤中加熟石灰防止酸化 ⑤开发新能源,避免含S、N的氧化物的大量排放A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
A
石灰石分解为CaO需消耗能量,浪费煤,使生产成本提高。
C
练习5.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(2)写出一氧化碳与一氧化氮反应的化学方程式_______________________。
(3)在“催化转化器”转化后的气体中有CO2、SO2,下列不能鉴别这两种气体的是_________。
A.KMnO4溶液 B.石灰水 C.BaCl2溶液 D.品红溶液
(4)有效减少城市污染的方法可以有_________。
A.开发氢能源 B.使用电动车 C.植树造林 D.戴上呼吸面具
BC
ABC
2CO+2NO = 2CO2+N2
④大气污染的治理措施
限制和减少污染物的排放,吸收和处理大气污染物。
a.通过改善燃料质量、改进燃烧裝置和燃烧技术、改进排烟设备、发展洁净煤技术降低燃煤在能源结构中的比例等措施,减少煤等化石燃料燃烧产生的污染;
b.通过推广使用无铅汽油、在汽车尾气系统中安装催化转化器、使用燃料电池、乙醇汽油作为汽油代用品、发展电动车等措施,减少汽车等机动车尾气污染;
c.停止氟氯代烷的生产和使用以保护臭氧层;
d.通过合理使用煤气、石油气或天然气等家用燃料、使用合格的环保型建筑材料和装饰材料、禁止在公共场所吸烟等措施降低CO、CO2、NO、NO2、SO2、尼古丁、甲醛、苯及其同系物、氡等污染物含量,改善室内空气质量等。
(2)水污染及其治理
①工农业生产和生活中产生的污水,任意排放会导致土壤、水体污染,必须经过多步处理才能达到排放标准。
环境问题 主要污染物 主要危害
赤潮和水华 含氮、磷元素的废水 使水体富营养化,导致水中藻类疯长,消耗水中溶解的氧,使水质恶化
②废水污染造成的环境问题:
课本P119【思考与讨论】(2)
练习6.我国近海海域海水中一些元素含量普遍超标,富营养化十分严重,经常发生“赤潮”现象。下列生活用品中能引起“赤潮”的是( )
A.肥皂 B.含磷洗涤剂 C.加酶洗衣粉 D.化妆品
B
③污水处理流程
a.一级处理:通常采用____方法,即用格栅间、沉淀池等除去污水中不溶解的污染物。经一级处理后的水一般达不到排放标准,一级处理作为预处理。
b.二级处理:采用____方法(或______法)及某些化学方法,除去水中的可降解有机物等污染物。经二级处理后的水一般可以达到国家规定的排放标
c.三级处理:主要采用_________、__________、__________和________等,对污水进行深度处理和净化。经三级处理后水可用于绿化和景观用水等。
物理
生物
微生物
化学沉淀法
氧化还原法
离子交换法
反渗透法
练习7.高铁酸钠(Na2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe3+。
(1)高铁酸钠中铁元素的化合价为_____;高铁酸钠能消毒杀菌,这是基于它的什么性质:__________。
(2)高铁酸钠用于水处理,除了能消毒杀菌外,它还能沉降水中的悬浮杂质,起到净水作用,请说明其净水原理:
____________________________________________________________________________________________________________________________________________________________
高铁酸钠的还原产物是Fe3+,Fe3+可发生水解,生成Fe(OH)3胶体,它可吸附水中悬浮的杂质或泥沙胶粒等一起凝聚而沉降,达到净水的效果
+6
强氧化性
(3)固体废弃物造成的污染及其治理
主要指生活垃圾、工业废料随意堆放造成的污染。目前最引入注意的是由塑料制品造成的白色污染及废旧电池造成的重金属污染。垃圾污染范围广泛,对环境及生物的不良影响途径多样。
①处理原则:_______、_______和_______。
②目的:_____________和_____________。
无害化
减量化
资源化
减少环境污染
资源回收利用
练习8.为了保护自然环境,提高人民的生活质量,必须重视处理“白色污染”。该“白色污染”指的是( )
A.冶炼厂的白色烟尘 B.石灰窑的白色粉末
C.聚氯乙烯等塑料垃圾 D.白色建筑材料
C
(1)化学工作者进行的环境质量监测工作可有可无,有污染治理就行( )
提示 环境质量监测工作是进行环境质量评价和污染治理的基础,非常必要。
(2)化石燃料燃烧产生的CO、NOx、SO2为次生污染物( )
提示 CO、NOx、SO2为一次污染物,其形成的酸雨、光化学烟雾等为次生污染物。
(3)“燃煤固硫”“汽车尾气催化净化”都能提高空气质量( )
提示 “燃煤固硫”可以减少SO2的污染,汽车尾气催化净化可以减少CO、NOx及某些有机物的污染。
1.判断正误
×
×
√
(4)工业废渣和生活垃圾等固体废弃物对环境影响不大,可不必处理( )
提示 处理固体废弃物要遵循无害化、减量化和资源化原则,达到减少环境污染和资源回收利用两个重要目的。
(5)污水的一级处理通常采用化学法和生物法将难溶解的污染物除去( )
提示 一级处理通常采用物理方法,用格栅间、沉淀池等去除不溶性污染物。
×
×
【课堂检测】
2.活性炭联合脱硫脱硝技术(AC)是一种比较成熟的脱硫脱硝技术,可以在较低的温度下,将废气中的SO2、NOx通过一系列反应生成铵盐,从而变废为宝,其工作示意图如右所示:
(1)SO2在活性炭表面被氧化最终生成硫酸,反应方程式为:
_____________________________________________________________。
2SO2+O2
2SO3、SO3+H2O===H2SO4(或2SO2+O2+2H2O===2H2SO4)
(2)吸收塔加入NH3后,可脱除废气中的NO、NO2,写出NO和NO2分别和NH3反应的化学方程式:_________________________、___________________________。
4NH3+6NO===5N2+6H2O
8NH3+6NO2===7N2+12H2O
(3)NH3和吸收塔中生成的H2SO4反应,会生成铵盐,写出反应的化学方程式:_________________________________________________________。
2NH3+
H2SO4===(NH4)2SO4(或NH3+H2SO4===
NH4HSO4)
(4)活性炭的造价较高,工业上一般选用活性焦作为吸附剂来脱硫脱硝,活性炭来自煤干馏产品,煤的干馏为_____(填“物理”或“化学”)变化,从煤干馏产品中获取苯、二甲苯的操作方法为:____________。
化学
蒸馏(或分馏)
二、绿色化学
1.绿色化学也称_________化学。
2.核心思想:改变“先污染后治理”的观念和做法,利用化学原理和技术手段,减少或消除产品在生产和应用中涉及的有害化学物质,实现从_________或_____环境污染。
3.原子经济性反应:反应物的原子全部转化为期望的最终产物,原子利用率达到______。
环境友好
源头减少
消除
100%
练习1.“绿色化学”要求从经济、环保和技术上设计可行的化学反应。据此,由单质镁制硝酸镁的下列4个方案中,你认为可行而且符合“绿色化学”要求的方案是( )
C
期望产物的总质量
生成物的总质量
原子利用率=
X100%
①计算两种生产工艺原子利用率
③原子利用率为100%的化学反应类型有哪些?
④试从反应物、产物对环境的影响,生产工艺,原子经济性反应,催化剂选择性等角度分析两方法的优劣。
方法一:反应物Cl2和Ca(OH)2对环境及设备有很大的污染性和腐蚀性,生产工艺分二步,产率和原子利用率低,成本高,反应的选择性低,产物中有大量的非期望物质。
方法二:反应物中O2无毒无污染、生产工艺简单,原子利用率为100%,催化剂选择性高、产率高、成本低,因此方法二更优。
化合反应、加聚反应、加成反应
某产物的实际产量
该产物的理论产量
产率=
X100%
原子利用率和产率不一样
②原子利用率和产率一样吗?
原料、溶剂
反应路线
资源、能源
无毒、无害,应致力于开发无溶剂存在下的反应;在起始端就采用实现污染预防的科学手段
开发、应用“原子经济性”的反应路线,最大限度地利用反应物分子中的每一个原子,充分利用资源,实现废物的零排放。
绿色化学要求充分利用可再生资源,合理利用资源和能源,降低生产成本,使之符合可持续发展的理念。
反应条件
尽量在温和的温度和压力下进行。节约能源;寻找新型、高效、对环境友好、可回收、高选择性的催化剂。
⑤绿色化学对化学研究和化工生产的提出的新的挑战
4.绿色化学对化学反应的要求
5.开发和利用自然资源遵循的原则
减量化(Reduce) 减少原料、节约能源
再利用(Reuse) 如催化剂、反应载体
再循环(Recycle) 物质循环、能量循环
(1)“绿色化学”就是污染后有效治理的化学思想( )
提示 “绿色化学”思想是从源头上减少或消除污染的化学。
(2)“绿色化学”就是指在化工生产中不排放任何有害物质( )
(3)在汽车排气管上安装“催化转化器”把CO、NO催化生成N2和CO2,符合绿色化学的理念( )
提示 “绿色化学”理念是从源头上减少或消除污染。
1.判断正误
×
√
×
(4)“3R”原则(减量化、再利用和再循环)是开发和利用自然资源的基本原则( )
(5)植物秸秆含大量钾元素,焚烧后作钾肥符合“绿色化学”的思想( )
提示 植物秸秆燃烧会产生大量的污染物,不符合“绿色化学”的思想。
(6)利用阳光发电,光解水制氢气是解决能源危机,实现可持续发展的有效途径( )
√
×
√
【课堂检测】
2.某工厂利用铜屑制硝酸铜。你认为可以用哪些方法?哪种最好?
① 铜与浓硝酸反应;② 铜与稀硝酸反应;③ 铜与氧气反应后,再与硝酸反应。
从原子经济性的角度考虑,从最大限度地减少废物的排放的角度考虑,方法③是最好的。
3.“绿色商品”是指对环境无污染的商品,下列商品能称为“绿色商品”的是( )
A.含铅汽油 B.含磷洗涤剂 C.含氟冰箱 D.加碘食盐
D
4.在绿色化学工艺中,理想状态是反应物中的原子全部转化为欲制得的产物,即原子的利用率为100%。在用CH3CH===CH2合成CH2===C(CH3)COOCH3的过程中,欲使原子的利用率达到最高,还需要其他的反应物有( )
A.CO2和H2O B.CO和HCHO C.CH3OH和H2 D.H2和CO2
B
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
