6.4 珍惜和保护金属资源 导学案(学生版+教师版)
文档属性
| 名称 | 6.4 珍惜和保护金属资源 导学案(学生版+教师版) |

|
|
| 格式 | doc | ||
| 文件大小 | 238.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-17 00:00:00 | ||
图片预览



文档简介
设计: 审核:
6.4珍惜和保护金属资源
课前复习:
下列关于金属资源的说法中,不正确的是( )
A. 自然界中除少数不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在
B. 自然界中的金属资源是取之不尽的
C. 人类大规模利用铁、铝、铜三种金属的先后顺序是铜、铁、铝,主要原因是它们的活动性差异
D. 地壳中含量最多的且目前被人们利用逐渐增多的金属元素是铝元素
下列说法正确的是( )
A. CO和CO2组成元素相同,具有相同的化学性质
B. 氢气和一氧化碳都是气体,都可以用向下排空气法收集
C. 生铁和钢都属于铁合金,含有相同的元素种类
D. 金刚石和金都是由原子构成的,都属于金属单质
一种无色气体X通过灼热的碳,得到另一种气体Y,Y和灼热的CuO反应又得到铜和X,X和Y是下列各组物( )
A. X是CO,Y是CO2 B. X是O2,Y是CO C. X是CO2,Y是CO D. X是O2,Y是CO2
铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由______组成;从微观看,铁由______构成。
(2)生活中:如图是常用的铁锅。把铁制成铁锅利用了铁的延展性和______性。 为防止铁制品锈蚀,可采用的一种防锈方法是______。
(3)实验室:细铁丝在氧气中燃烧的现象是______,放热。该反应的化学方程式是______。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是______,该反应利用了一氧化碳的哪种化学性质:______。
炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图:
对实验进行分析并回答:
(1)给玻璃管加热的仪器叫酒精喷灯,要用其 ______ (填“外焰”、“内焰”或“焰心”)进行加热。
(2)实验中玻璃管里氧化铁粉末的颜色变化是 ______ ,观察到澄清石灰水的现象是 ______ 。
(3)实验中应 ______ 通CO气体 ______ (填“先”或“后”)点燃酒精灯对氧化铁加热,作用是 ______ 。
(4)实验后应 ______ 熄灭对氧化铁加热的酒精灯 ______ (填“先”或“后”)停止通CO气体,作用是 ______ 。
(5)实验要在装置末端a处燃着一盏酒精灯,其作用是 ______ 。
学习目标:
1.知道地球上的金属资源是有限的,关注金属资源的消耗情况;
2.了解铁锈生成的条件,体验铁生锈条件探究活动的过程和方法;
3.认识防锈的几类简单方法;
4.初步形成保护金属资源的意识。
新课讲授:
一、探究点:钢铁锈蚀因素的探究
问题:钢铁锈蚀的因素有哪些?
假设:钢铁生锈肯定与氧气有关,
还可能与水分,盐分有关。
实验事实:将3 枚无锈的铁钉,分装在
不同条件下的试管内,观察一段时间后:
现象:A:: ; B: ;C: 。
解释与结论:铁在有 等物质存在的条件下,发生复杂的化学反应,生成铁锈,其主要成分是 (化学式: )。由于铁锈是一种疏松多孔的物质,水分子和氧分子能穿过它的空隙,不断向里面渗透,继续跟铁反应,直至全部被锈蚀。当铁接触易跟它发生反应的化学物质(如:酸)时,就更容易被锈蚀了。
拓展与迁移:根据以上结论,你认为防止钢铁生锈的基本原理是什么?
1、防止钢铁生锈的方法:
(1)保持铁制品表面的 ;
(2)在铁制品表面覆盖 ,如在钢铁制品上 、 、 等;
(3)改善铁的内部结构:把铁制成 。
2、除锈方法:
(1)物理方法: 、 等。
(2)化学方法:稀盐酸除铁锈: 稀硫酸除铁锈:
(写出上述两个化学方程式)
二、金属保护
(1)从资源的采掘与开发方面保护金属资源:
① ;
②
③ 。
(2)从保护金属材料和制品方面保护金属资源:防止 。
课堂检测:
埋在地下的铸铁管道在下列哪种情况下腐蚀最慢的是( )
A.在干燥、致密的土壤中 B.在干燥、疏松的土壤中
C.在潮湿、致密的土壤中 D.在潮湿、疏松的土壤中
2.为了防止家中的菜刀生锈,某同学设计了以下几种方案:合理可行的方案 ( )
① 每天用机油擦拭一遍 ② 用完后保存在水中
③ 擦干后用植物油涂抹④ 用干布把它擦干
⑤ 用食醋涂抹 ⑥ 用酱油涂抹 ⑦ 用清水洗干净后迅速放进塑料袋中,并包裹好。
A、①②③④⑥⑦ B、②③④ C、③ ④ D、⑤⑥⑦
3.如图5-3所示,在盛水的试管中放一根洁净的铁钉,用带U型管的胶塞塞紧,U型管内水面处于同一高度。数天后观察到U型管内的水面 ( )
A、a 比 b 高 B、 b 比 a 高 C、一样高 D、无法判断
4.如图是探究铁制品锈蚀的条件时设计的实验。下列对比实验设计与探究的条件,对应关系正确的是( )
A.甲和丁:水 B.乙和丙:空气
C.甲和丙:空气 D.甲和乙:水
5、下列有关金属材料的说法中,正确的是( )
A.地壳中含量最多的金属元素是铁
B.在日常生活中,大量使用的常常不是纯金属,而是它们的合金
C.“真金不怕火炼”说明黄金的硬度非常大
D.铁制品生锈产生的铁锈是一种疏松多孔的物质,铁锈的主要成分是 Fe3O4
6.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐 B.寻找金属代用品
C.防止金属的腐蚀 D.过度开采金属矿物
7.如图是教材中的几个实验,结合实验回答问题:
(1)A实验中,一段时间后可根据观察到 的现象,得出铁生锈需要与氧气接触的结论;
(2)B实验中,铜片两侧分别放有同样大小的乒乓球碎片和滤纸碎片,观察到乒乓球碎片燃烧,而滤纸碎片不燃烧,由此可以得出燃烧的条件之一是 ;
(3)C实验中,实验成功可得到的结论是 ;
(4)D实验中,向水中加入少量硫酸钠或氢氧化钠的目的是 。
8、在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整.铁生锈条件的探究.
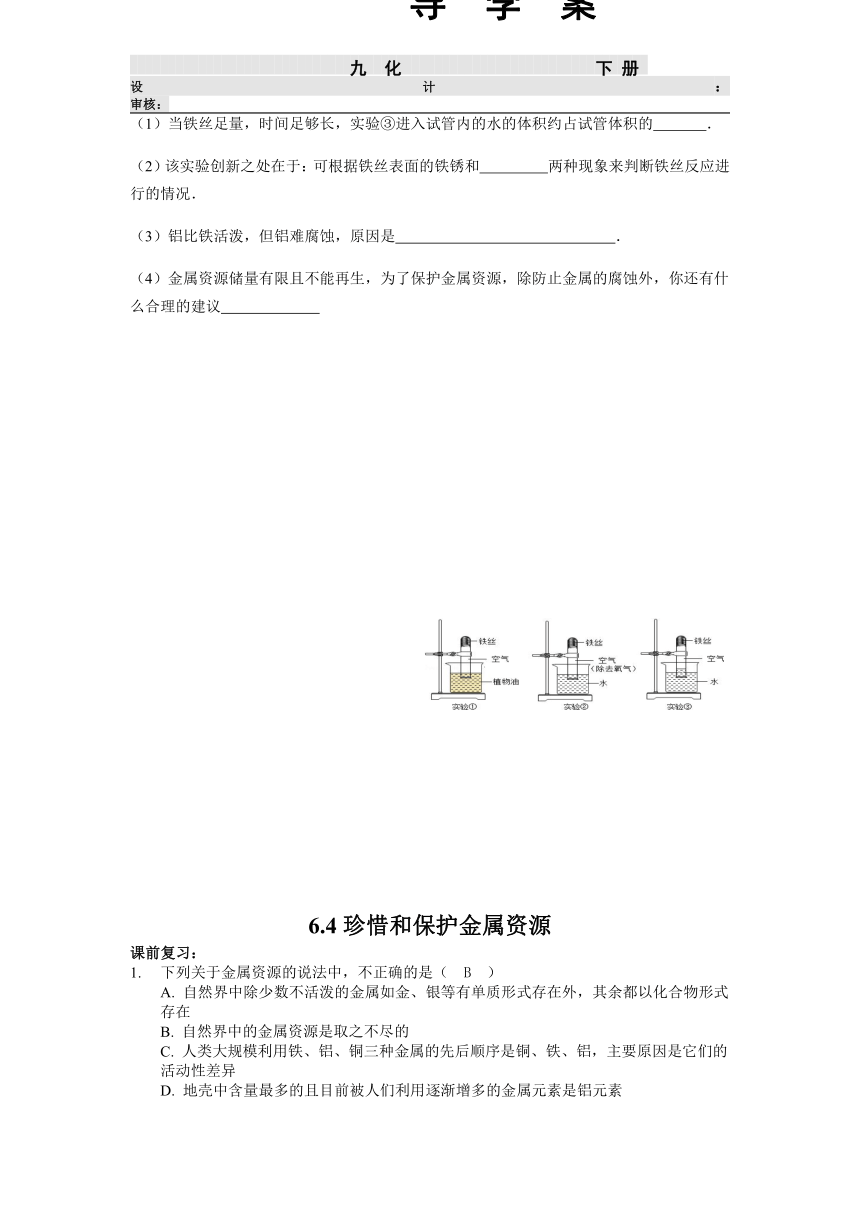
取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象.
实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小.铁生锈实际上是铁与空气中的 (填名称)发生反应的结果.
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 .
(2)该实验创新之处在于:可根据铁丝表面的铁锈和 两种现象来判断铁丝反应进行的情况.
(3)铝比铁活泼,但铝难腐蚀,原因是 .
(4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议
6.4珍惜和保护金属资源
课前复习:
下列关于金属资源的说法中,不正确的是( B )
A. 自然界中除少数不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在
B. 自然界中的金属资源是取之不尽的
C. 人类大规模利用铁、铝、铜三种金属的先后顺序是铜、铁、铝,主要原因是它们的活动性差异
D. 地壳中含量最多的且目前被人们利用逐渐增多的金属元素是铝元素
下列说法正确的是( C )
A. CO和CO2组成元素相同,具有相同的化学性质
B. 氢气和一氧化碳都是气体,都可以用向下排空气法收集
C. 生铁和钢都属于铁合金,含有相同的元素种类
D. 金刚石和金都是由原子构成的,都属于金属单质
一种无色气体X通过灼热的碳,得到另一种气体Y,Y和灼热的CuO反应又得到铜和X,X和Y是下列各组物( C )
A. X是CO,Y是CO2 B. X是O2,Y是CO C. X是CO2,Y是CO D. X是O2,Y是CO2
铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由___铁元素___组成;从微观看,铁由_铁原子_____构成。
(2)生活中:如图是常用的铁锅。把铁制成铁锅利用了铁的延展性和__导热____性。 为防止铁制品锈蚀,可采用的一种防锈方法是_喷漆_____。
(3)实验室:细铁丝在氧气中燃烧的现象是_剧烈燃烧,火星四射,生成黑色固体_____,放热。该反应的化学方程式是__3_Fe+2O2_ _Fe3O4_____。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是__3CO+Fe2O3_2Fe+_ 3CO2_____,该反应利用了一氧化碳的哪种化学性质:_还原性_____。
炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图:
对实验进行分析并回答:
(1)给玻璃管加热的仪器叫酒精喷灯,要用其 __外焰____ (填“外焰”、“内焰”或“焰心”)进行加热。
(2)实验中玻璃管里氧化铁粉末的颜色变化是 _由红色变黑色_____ ,观察到澄清石灰水的现象是 _澄清石灰水变浑浊_____ 。
(3)实验中应 __先____ 通CO气体 ___后___ (填“先”或“后”)点燃酒精灯对氧化铁加热,作用是 _排净玻璃管中的空气,避免加热时发生爆炸_____ 。
(4)实验后应 __先____ 熄灭对氧化铁加热的酒精灯 __后____ (填“先”或“后”)停止通CO气体,作用是 _防止高温的铁被氧化_____ 。
(5)实验要在装置末端a处燃着一盏酒精灯,其作用是 __点燃多余一氧化碳,防治污染空气____ 。
学习目标:
1.知道地球上的金属资源是有限的,关注金属资源的消耗情况;
2.了解铁锈生成的条件,体验铁生锈条件探究活动的过程和方法;
3.认识防锈的几类简单方法;
4.初步形成保护金属资源的意识。
新课讲授:
一、探究点:钢铁锈蚀因素的探究
问题:钢铁锈蚀的因素有哪些?
假设:钢铁生锈肯定与氧气有关,
还可能与水分,盐分有关。
实验事实:将3 枚无锈的铁钉,分装在
不同条件下的试管内,观察一段时间后:
现象:A:: 不生锈 ; B: 生锈 ;C: 不生锈 。
解释与结论:铁在有 水和氧气 等物质存在的条件下,发生复杂的化学反应,生成铁锈,其主要成分是 (化学式: Fe2O3 )。由于铁锈是一种疏松多孔的物质,水分子和氧分子能穿过它的空隙,不断向里面渗透,继续跟铁反应,直至全部被锈蚀。当铁接触易跟它发生反应的化学物质(如:酸)时,就更容易被锈蚀了。
拓展与迁移:根据以上结论,你认为防止钢铁生锈的基本原理是什么?
1、防止钢铁生锈的方法:
(1)保持铁制品表面的 清洁和干燥 ;
(2)在铁制品表面覆盖 一层保护膜 ,如在钢铁制品上 涂油 、 喷漆 、 电镀 等;
(3)改善铁的内部结构:把铁制成 合金 。
2、除锈方法:
(1)物理方法: 砂纸打磨 、 刀刮 等。
(2)化学方法:稀盐酸除铁锈:6HCl+ Fe2O3=2FeCl3+3H2O 稀硫酸除铁锈:3H2SO4+ Fe2O3=Fe2(SO4)3+3H2O
(写出上述两个化学方程式)
二、金属保护
(1)从资源的采掘与开发方面保护金属资源:
① 废旧金属回收再利用 ;
② 合理有计划开采
③ 积极寻找金属替代品 。
(2)从保护金属材料和制品方面保护金属资源:防止 金属生锈 。
课堂检测:
埋在地下的铸铁管道在下列哪种情况下腐蚀最慢的是( A )
A.在干燥、致密的土壤中 B.在干燥、疏松的土壤中
C.在潮湿、致密的土壤中 D.在潮湿、疏松的土壤中
2.为了防止家中的菜刀生锈,某同学设计了以下几种方案:合理可行的方案 ( C )
① 每天用机油擦拭一遍 ② 用完后保存在水中
③ 擦干后用植物油涂抹④ 用干布把它擦干
⑤ 用食醋涂抹 ⑥ 用酱油涂抹 ⑦ 用清水洗干净后迅速放进塑料袋中,并包裹好。
A、①②③④⑥⑦ B、②③④ C、③ ④ D、⑤⑥⑦
3.如图5-3所示,在盛水的试管中放一根洁净的铁钉,用带U型管的胶塞塞紧,U型管内水面处于同一高度。数天后观察到U型管内的水面 ( A )
A、a 比 b 高 B、 b 比 a 高 C、一样高 D、无法判断
4.如图是探究铁制品锈蚀的条件时设计的实验。下列对比实验设计与探究的条件,对应关系正确的是( A )
A.甲和丁:水 B.乙和丙:空气
C.甲和丙:空气 D.甲和乙:水
5、下列有关金属材料的说法中,正确的是( B )
A.地壳中含量最多的金属元素是铁
B.在日常生活中,大量使用的常常不是纯金属,而是它们的合金
C.“真金不怕火炼”说明黄金的硬度非常大
D.铁制品生锈产生的铁锈是一种疏松多孔的物质,铁锈的主要成分是 Fe3O4
6.下列做法中,不利于保护金属资源的是( D )
A.回收易拉罐 B.寻找金属代用品
C.防止金属的腐蚀 D.过度开采金属矿物
7.如图是教材中的几个实验,结合实验回答问题:
(1)A实验中,一段时间后可根据观察到 1中铁钉生锈,2中铁钉不生锈 的现象,得出铁生锈需要与氧气接触的结论;
(2)B实验中,铜片两侧分别放有同样大小的乒乓球碎片和滤纸碎片,观察到乒乓球碎片燃烧,而滤纸碎片不燃烧,由此可以得出燃烧的条件之一是 温度达到可燃物着火点 ;
(3)C实验中,实验成功可得到的结论是 氧气约赞空气体积的五分之一 ;
(4)D实验中,向水中加入少量硫酸钠或氢氧化钠的目的是 增强水的导电性 。
8、在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整.铁生锈条件的探究.
取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象.
实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小.铁生锈实际上是铁与空气中的 水和氧气 (填名称)发生反应的结果.
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 1/5 .
(2)该实验创新之处在于:可根据铁丝表面的铁锈和 液面上升 两种现象来判断铁丝反应进行的情况.
(3)铝比铁活泼,但铝难腐蚀,原因是常温下, 铝易与空气中氧气反应生成一层致密的氧化膜起到保护作用 .
(4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议 废旧金属回收再利用
6.4珍惜和保护金属资源
课前复习:
下列关于金属资源的说法中,不正确的是( )
A. 自然界中除少数不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在
B. 自然界中的金属资源是取之不尽的
C. 人类大规模利用铁、铝、铜三种金属的先后顺序是铜、铁、铝,主要原因是它们的活动性差异
D. 地壳中含量最多的且目前被人们利用逐渐增多的金属元素是铝元素
下列说法正确的是( )
A. CO和CO2组成元素相同,具有相同的化学性质
B. 氢气和一氧化碳都是气体,都可以用向下排空气法收集
C. 生铁和钢都属于铁合金,含有相同的元素种类
D. 金刚石和金都是由原子构成的,都属于金属单质
一种无色气体X通过灼热的碳,得到另一种气体Y,Y和灼热的CuO反应又得到铜和X,X和Y是下列各组物( )
A. X是CO,Y是CO2 B. X是O2,Y是CO C. X是CO2,Y是CO D. X是O2,Y是CO2
铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由______组成;从微观看,铁由______构成。
(2)生活中:如图是常用的铁锅。把铁制成铁锅利用了铁的延展性和______性。 为防止铁制品锈蚀,可采用的一种防锈方法是______。
(3)实验室:细铁丝在氧气中燃烧的现象是______,放热。该反应的化学方程式是______。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是______,该反应利用了一氧化碳的哪种化学性质:______。
炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图:
对实验进行分析并回答:
(1)给玻璃管加热的仪器叫酒精喷灯,要用其 ______ (填“外焰”、“内焰”或“焰心”)进行加热。
(2)实验中玻璃管里氧化铁粉末的颜色变化是 ______ ,观察到澄清石灰水的现象是 ______ 。
(3)实验中应 ______ 通CO气体 ______ (填“先”或“后”)点燃酒精灯对氧化铁加热,作用是 ______ 。
(4)实验后应 ______ 熄灭对氧化铁加热的酒精灯 ______ (填“先”或“后”)停止通CO气体,作用是 ______ 。
(5)实验要在装置末端a处燃着一盏酒精灯,其作用是 ______ 。
学习目标:
1.知道地球上的金属资源是有限的,关注金属资源的消耗情况;
2.了解铁锈生成的条件,体验铁生锈条件探究活动的过程和方法;
3.认识防锈的几类简单方法;
4.初步形成保护金属资源的意识。
新课讲授:
一、探究点:钢铁锈蚀因素的探究
问题:钢铁锈蚀的因素有哪些?
假设:钢铁生锈肯定与氧气有关,
还可能与水分,盐分有关。
实验事实:将3 枚无锈的铁钉,分装在
不同条件下的试管内,观察一段时间后:
现象:A:: ; B: ;C: 。
解释与结论:铁在有 等物质存在的条件下,发生复杂的化学反应,生成铁锈,其主要成分是 (化学式: )。由于铁锈是一种疏松多孔的物质,水分子和氧分子能穿过它的空隙,不断向里面渗透,继续跟铁反应,直至全部被锈蚀。当铁接触易跟它发生反应的化学物质(如:酸)时,就更容易被锈蚀了。
拓展与迁移:根据以上结论,你认为防止钢铁生锈的基本原理是什么?
1、防止钢铁生锈的方法:
(1)保持铁制品表面的 ;
(2)在铁制品表面覆盖 ,如在钢铁制品上 、 、 等;
(3)改善铁的内部结构:把铁制成 。
2、除锈方法:
(1)物理方法: 、 等。
(2)化学方法:稀盐酸除铁锈: 稀硫酸除铁锈:
(写出上述两个化学方程式)
二、金属保护
(1)从资源的采掘与开发方面保护金属资源:
① ;
②
③ 。
(2)从保护金属材料和制品方面保护金属资源:防止 。
课堂检测:
埋在地下的铸铁管道在下列哪种情况下腐蚀最慢的是( )
A.在干燥、致密的土壤中 B.在干燥、疏松的土壤中
C.在潮湿、致密的土壤中 D.在潮湿、疏松的土壤中
2.为了防止家中的菜刀生锈,某同学设计了以下几种方案:合理可行的方案 ( )
① 每天用机油擦拭一遍 ② 用完后保存在水中
③ 擦干后用植物油涂抹④ 用干布把它擦干
⑤ 用食醋涂抹 ⑥ 用酱油涂抹 ⑦ 用清水洗干净后迅速放进塑料袋中,并包裹好。
A、①②③④⑥⑦ B、②③④ C、③ ④ D、⑤⑥⑦
3.如图5-3所示,在盛水的试管中放一根洁净的铁钉,用带U型管的胶塞塞紧,U型管内水面处于同一高度。数天后观察到U型管内的水面 ( )
A、a 比 b 高 B、 b 比 a 高 C、一样高 D、无法判断
4.如图是探究铁制品锈蚀的条件时设计的实验。下列对比实验设计与探究的条件,对应关系正确的是( )
A.甲和丁:水 B.乙和丙:空气
C.甲和丙:空气 D.甲和乙:水
5、下列有关金属材料的说法中,正确的是( )
A.地壳中含量最多的金属元素是铁
B.在日常生活中,大量使用的常常不是纯金属,而是它们的合金
C.“真金不怕火炼”说明黄金的硬度非常大
D.铁制品生锈产生的铁锈是一种疏松多孔的物质,铁锈的主要成分是 Fe3O4
6.下列做法中,不利于保护金属资源的是( )
A.回收易拉罐 B.寻找金属代用品
C.防止金属的腐蚀 D.过度开采金属矿物
7.如图是教材中的几个实验,结合实验回答问题:
(1)A实验中,一段时间后可根据观察到 的现象,得出铁生锈需要与氧气接触的结论;
(2)B实验中,铜片两侧分别放有同样大小的乒乓球碎片和滤纸碎片,观察到乒乓球碎片燃烧,而滤纸碎片不燃烧,由此可以得出燃烧的条件之一是 ;
(3)C实验中,实验成功可得到的结论是 ;
(4)D实验中,向水中加入少量硫酸钠或氢氧化钠的目的是 。
8、在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整.铁生锈条件的探究.
取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象.
实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小.铁生锈实际上是铁与空气中的 (填名称)发生反应的结果.
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 .
(2)该实验创新之处在于:可根据铁丝表面的铁锈和 两种现象来判断铁丝反应进行的情况.
(3)铝比铁活泼,但铝难腐蚀,原因是 .
(4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议
6.4珍惜和保护金属资源
课前复习:
下列关于金属资源的说法中,不正确的是( B )
A. 自然界中除少数不活泼的金属如金、银等有单质形式存在外,其余都以化合物形式存在
B. 自然界中的金属资源是取之不尽的
C. 人类大规模利用铁、铝、铜三种金属的先后顺序是铜、铁、铝,主要原因是它们的活动性差异
D. 地壳中含量最多的且目前被人们利用逐渐增多的金属元素是铝元素
下列说法正确的是( C )
A. CO和CO2组成元素相同,具有相同的化学性质
B. 氢气和一氧化碳都是气体,都可以用向下排空气法收集
C. 生铁和钢都属于铁合金,含有相同的元素种类
D. 金刚石和金都是由原子构成的,都属于金属单质
一种无色气体X通过灼热的碳,得到另一种气体Y,Y和灼热的CuO反应又得到铜和X,X和Y是下列各组物( C )
A. X是CO,Y是CO2 B. X是O2,Y是CO C. X是CO2,Y是CO D. X是O2,Y是CO2
铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由___铁元素___组成;从微观看,铁由_铁原子_____构成。
(2)生活中:如图是常用的铁锅。把铁制成铁锅利用了铁的延展性和__导热____性。 为防止铁制品锈蚀,可采用的一种防锈方法是_喷漆_____。
(3)实验室:细铁丝在氧气中燃烧的现象是_剧烈燃烧,火星四射,生成黑色固体_____,放热。该反应的化学方程式是__3_Fe+2O2_ _Fe3O4_____。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是__3CO+Fe2O3_2Fe+_ 3CO2_____,该反应利用了一氧化碳的哪种化学性质:_还原性_____。
炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图:
对实验进行分析并回答:
(1)给玻璃管加热的仪器叫酒精喷灯,要用其 __外焰____ (填“外焰”、“内焰”或“焰心”)进行加热。
(2)实验中玻璃管里氧化铁粉末的颜色变化是 _由红色变黑色_____ ,观察到澄清石灰水的现象是 _澄清石灰水变浑浊_____ 。
(3)实验中应 __先____ 通CO气体 ___后___ (填“先”或“后”)点燃酒精灯对氧化铁加热,作用是 _排净玻璃管中的空气,避免加热时发生爆炸_____ 。
(4)实验后应 __先____ 熄灭对氧化铁加热的酒精灯 __后____ (填“先”或“后”)停止通CO气体,作用是 _防止高温的铁被氧化_____ 。
(5)实验要在装置末端a处燃着一盏酒精灯,其作用是 __点燃多余一氧化碳,防治污染空气____ 。
学习目标:
1.知道地球上的金属资源是有限的,关注金属资源的消耗情况;
2.了解铁锈生成的条件,体验铁生锈条件探究活动的过程和方法;
3.认识防锈的几类简单方法;
4.初步形成保护金属资源的意识。
新课讲授:
一、探究点:钢铁锈蚀因素的探究
问题:钢铁锈蚀的因素有哪些?
假设:钢铁生锈肯定与氧气有关,
还可能与水分,盐分有关。
实验事实:将3 枚无锈的铁钉,分装在
不同条件下的试管内,观察一段时间后:
现象:A:: 不生锈 ; B: 生锈 ;C: 不生锈 。
解释与结论:铁在有 水和氧气 等物质存在的条件下,发生复杂的化学反应,生成铁锈,其主要成分是 (化学式: Fe2O3 )。由于铁锈是一种疏松多孔的物质,水分子和氧分子能穿过它的空隙,不断向里面渗透,继续跟铁反应,直至全部被锈蚀。当铁接触易跟它发生反应的化学物质(如:酸)时,就更容易被锈蚀了。
拓展与迁移:根据以上结论,你认为防止钢铁生锈的基本原理是什么?
1、防止钢铁生锈的方法:
(1)保持铁制品表面的 清洁和干燥 ;
(2)在铁制品表面覆盖 一层保护膜 ,如在钢铁制品上 涂油 、 喷漆 、 电镀 等;
(3)改善铁的内部结构:把铁制成 合金 。
2、除锈方法:
(1)物理方法: 砂纸打磨 、 刀刮 等。
(2)化学方法:稀盐酸除铁锈:6HCl+ Fe2O3=2FeCl3+3H2O 稀硫酸除铁锈:3H2SO4+ Fe2O3=Fe2(SO4)3+3H2O
(写出上述两个化学方程式)
二、金属保护
(1)从资源的采掘与开发方面保护金属资源:
① 废旧金属回收再利用 ;
② 合理有计划开采
③ 积极寻找金属替代品 。
(2)从保护金属材料和制品方面保护金属资源:防止 金属生锈 。
课堂检测:
埋在地下的铸铁管道在下列哪种情况下腐蚀最慢的是( A )
A.在干燥、致密的土壤中 B.在干燥、疏松的土壤中
C.在潮湿、致密的土壤中 D.在潮湿、疏松的土壤中
2.为了防止家中的菜刀生锈,某同学设计了以下几种方案:合理可行的方案 ( C )
① 每天用机油擦拭一遍 ② 用完后保存在水中
③ 擦干后用植物油涂抹④ 用干布把它擦干
⑤ 用食醋涂抹 ⑥ 用酱油涂抹 ⑦ 用清水洗干净后迅速放进塑料袋中,并包裹好。
A、①②③④⑥⑦ B、②③④ C、③ ④ D、⑤⑥⑦
3.如图5-3所示,在盛水的试管中放一根洁净的铁钉,用带U型管的胶塞塞紧,U型管内水面处于同一高度。数天后观察到U型管内的水面 ( A )
A、a 比 b 高 B、 b 比 a 高 C、一样高 D、无法判断
4.如图是探究铁制品锈蚀的条件时设计的实验。下列对比实验设计与探究的条件,对应关系正确的是( A )
A.甲和丁:水 B.乙和丙:空气
C.甲和丙:空气 D.甲和乙:水
5、下列有关金属材料的说法中,正确的是( B )
A.地壳中含量最多的金属元素是铁
B.在日常生活中,大量使用的常常不是纯金属,而是它们的合金
C.“真金不怕火炼”说明黄金的硬度非常大
D.铁制品生锈产生的铁锈是一种疏松多孔的物质,铁锈的主要成分是 Fe3O4
6.下列做法中,不利于保护金属资源的是( D )
A.回收易拉罐 B.寻找金属代用品
C.防止金属的腐蚀 D.过度开采金属矿物
7.如图是教材中的几个实验,结合实验回答问题:
(1)A实验中,一段时间后可根据观察到 1中铁钉生锈,2中铁钉不生锈 的现象,得出铁生锈需要与氧气接触的结论;
(2)B实验中,铜片两侧分别放有同样大小的乒乓球碎片和滤纸碎片,观察到乒乓球碎片燃烧,而滤纸碎片不燃烧,由此可以得出燃烧的条件之一是 温度达到可燃物着火点 ;
(3)C实验中,实验成功可得到的结论是 氧气约赞空气体积的五分之一 ;
(4)D实验中,向水中加入少量硫酸钠或氢氧化钠的目的是 增强水的导电性 。
8、在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整.铁生锈条件的探究.
取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象.
实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小.铁生锈实际上是铁与空气中的 水和氧气 (填名称)发生反应的结果.
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 1/5 .
(2)该实验创新之处在于:可根据铁丝表面的铁锈和 液面上升 两种现象来判断铁丝反应进行的情况.
(3)铝比铁活泼,但铝难腐蚀,原因是常温下, 铝易与空气中氧气反应生成一层致密的氧化膜起到保护作用 .
(4)金属资源储量有限且不能再生,为了保护金属资源,除防止金属的腐蚀外,你还有什么合理的建议 废旧金属回收再利用
