课题 1 质量守恒定律
图片预览





文档简介
课件25张PPT。质量守恒定律(1)建湖县上冈实验初中 杜朔南>=<猜想科学探究实验一:白磷燃烧注意观察:
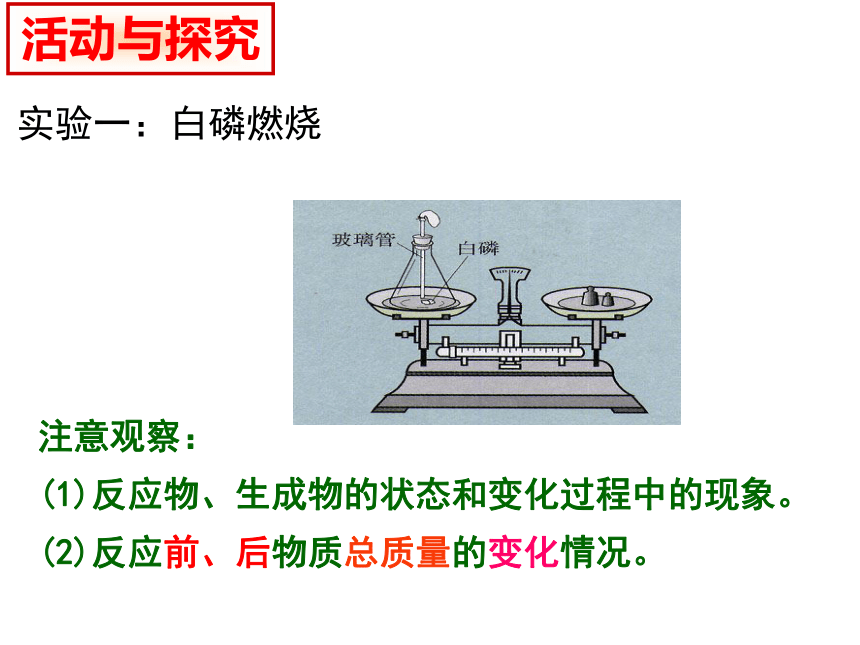
(1)反应物、生成物的状态和变化过程中的现象。
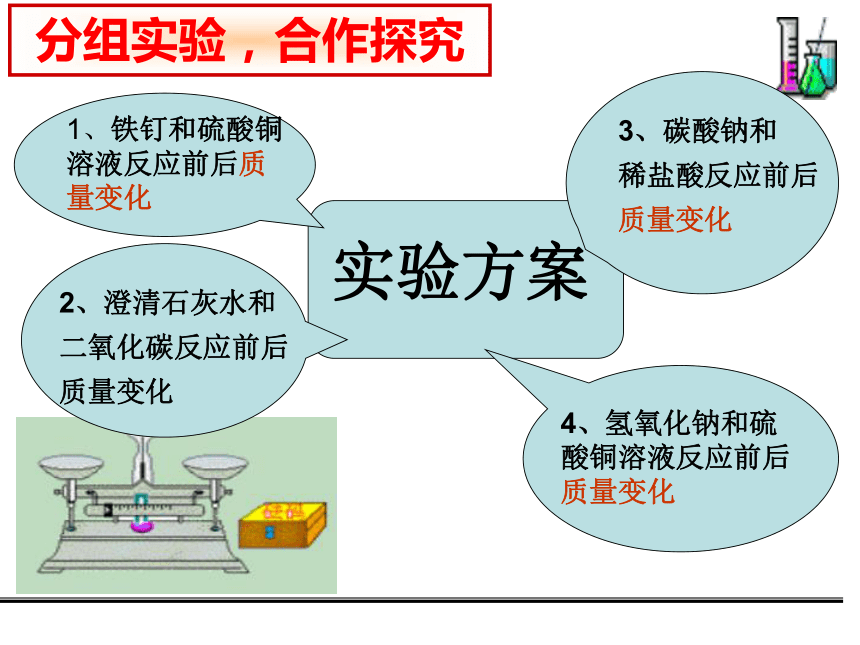
(2)反应前、后物质总质量的变化情况。 活动与探究对比思考:反应前物质(或物体)反应后物质(或物体)锥形瓶细砂气球(空气)氧气氮气白磷锥形瓶细砂气球五氧化二磷(剩余气体)氮气稀有气体等稀有气体等白磷五氧化二磷氧气m(P)+m(O2)=m(P2O5)实验方案1、铁钉和硫酸铜溶液反应前后质量变化2、澄清石灰水和二氧化碳反应前后质量变化3、碳酸钠和
稀盐酸反应前后
质量变化4、氢氧化钠和硫
酸铜溶液反应前后质量变化分组实验,合作探究实验步骤:
1.称量
2.发生反应
3.称量—反应前各物质的总质量—反应后各物质的总质量温馨提示:
1、反应装置放在左托盘正中央的位置。
2、用镊子夹取砝码、移动游码使天平平衡。
3、第一次称量后,砝码游码不必归位。
4、反应发生时,装置要放在实验台上。
5、反应发生后,将装置放在左托盘上,观察
天平是否平衡。
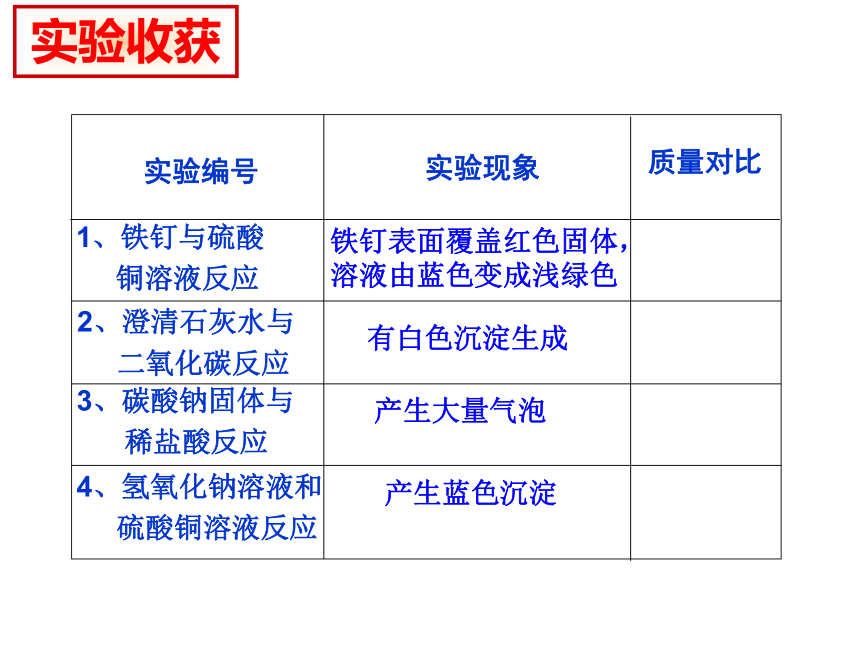
6、实验后,仪器、药品要摆放整齐。实验收获实验编号
实验现象质量对比1、铁钉与硫酸
铜溶液反应铁钉表面覆盖红色固体,
溶液由蓝色变成浅绿色2、澄清石灰水与
二氧化碳反应有白色沉淀生成3、碳酸钠固体与
稀盐酸反应产生大量气泡4、氢氧化钠溶液和
硫酸铜溶液反应产生蓝色沉淀2、氢氧化钙+二氧化碳 碳酸钙+水类比推理m(Fe)+m(CuSO4) = m(CuSO4) + m(Cu)m(Ca(OH)2)+m(CO2)=m(CaCO3)+m(H2O)3. 盐酸+碳酸钠 氯化钠+二氧化碳+水类比推理m(HCl)+m(Na2CO3) = m(NaCl)+m(CO2) + m(H2O)m(CuSO4)+m(NaOH) = m(Cu(OH) 2)+m(Na2SO4) 质量守恒定律
把握质量守恒定律应注意几点1、只有化学变化才遵守质量守恒定律,物理变化不用质量守恒定律解释!
2、守恒的是“总质量”,即“参加反应的各反应物的总质量”和“生成物的总质量”。 ( 如沉淀、气体等都应考虑进去。)
3、 “参加”,意味着没有参加反应(剩余)的物质的质量不能算在内。参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。质量化学反应碳酸钠与稀盐酸反应后质量减小的原因是什么?碳酸钠与稀盐酸的反应
参加化学反应的反应物有:
生成物有:
我们漏称了: 二氧化碳气体碳酸钠和稀盐酸氯化钠、水和二氧化碳讨论:14交流讨论密闭的环境下如何将所有的反应物和生成物都称量在内呢?如何改进?改进实验仪器
橡皮塞、锥形瓶、导管
双孔橡皮塞、注射器、
气球、带盖的矿泉水瓶、小试管、带支管的试管锥形瓶、小试管碳酸钠和稀盐酸的反应为什么化学反应前后质量守恒呢?溯本求源:水电解的微观过程 从分子、原子的变化情况说明为什么化学反应一定遵守质量守恒定律?1、镁带在氧气中完全燃烧后,生成物的质量比原来镁带的质量大。试用质量守恒定律解释原因。学以致用: 根据质量守恒定律,参加反应的镁和氧气的质量之和等于生成氧化镁的质量。所以氧化镁的质量大于镁带的质量。镁燃烧,产生耀眼的白光,生成一种白色固体。天平不平衡。①参加反应的氧气没有称量。②生成物白烟跑掉一部分。 ③坩埚钳上粘掉一部分等等。巩固延伸 所有的化学反应都遵守质量守恒定律,该定律具有普遍意义。因为有时考虑问题不全面或实验方案不完善,而导致表面上的不相等。镁的质量+参加反应的氧气质量==氧化镁的质量牛刀小试:2、细铁丝在氧气中完全燃烧后,生成物的质量比原来铁丝的质量大。试用质量守恒定律解释原因1、“点石成金”符合质量守恒定律吗?3、小明同学用10g高锰酸钾做加热制取氧气的实验,完全反应后称量剩余固体,质量为9.2g.符合质量守恒定律吗? 符合。根据质量守恒定律参加
反应的高锰酸钾的质量等于生成固体和氧气的质量总和。 质量减轻,证明生成了0.8g氧气。 某物质A在一定条件下分解后只生成二氧化碳和水,则该物质由 种元素组成。
若物质A的一个分子分解生成一个二氧化碳分子和一个水分子,则一个A分子是怎么构成?碳、氢、氧三一个A分子由一个碳原子、两个氢原子和三个氧原子构成。畅谈收获,交流解疑家庭小实验
(1)反应物、生成物的状态和变化过程中的现象。
(2)反应前、后物质总质量的变化情况。 活动与探究对比思考:反应前物质(或物体)反应后物质(或物体)锥形瓶细砂气球(空气)氧气氮气白磷锥形瓶细砂气球五氧化二磷(剩余气体)氮气稀有气体等稀有气体等白磷五氧化二磷氧气m(P)+m(O2)=m(P2O5)实验方案1、铁钉和硫酸铜溶液反应前后质量变化2、澄清石灰水和二氧化碳反应前后质量变化3、碳酸钠和
稀盐酸反应前后
质量变化4、氢氧化钠和硫
酸铜溶液反应前后质量变化分组实验,合作探究实验步骤:
1.称量
2.发生反应
3.称量—反应前各物质的总质量—反应后各物质的总质量温馨提示:
1、反应装置放在左托盘正中央的位置。
2、用镊子夹取砝码、移动游码使天平平衡。
3、第一次称量后,砝码游码不必归位。
4、反应发生时,装置要放在实验台上。
5、反应发生后,将装置放在左托盘上,观察
天平是否平衡。
6、实验后,仪器、药品要摆放整齐。实验收获实验编号
实验现象质量对比1、铁钉与硫酸
铜溶液反应铁钉表面覆盖红色固体,
溶液由蓝色变成浅绿色2、澄清石灰水与
二氧化碳反应有白色沉淀生成3、碳酸钠固体与
稀盐酸反应产生大量气泡4、氢氧化钠溶液和
硫酸铜溶液反应产生蓝色沉淀2、氢氧化钙+二氧化碳 碳酸钙+水类比推理m(Fe)+m(CuSO4) = m(CuSO4) + m(Cu)m(Ca(OH)2)+m(CO2)=m(CaCO3)+m(H2O)3. 盐酸+碳酸钠 氯化钠+二氧化碳+水类比推理m(HCl)+m(Na2CO3) = m(NaCl)+m(CO2) + m(H2O)m(CuSO4)+m(NaOH) = m(Cu(OH) 2)+m(Na2SO4) 质量守恒定律
把握质量守恒定律应注意几点1、只有化学变化才遵守质量守恒定律,物理变化不用质量守恒定律解释!
2、守恒的是“总质量”,即“参加反应的各反应物的总质量”和“生成物的总质量”。 ( 如沉淀、气体等都应考虑进去。)
3、 “参加”,意味着没有参加反应(剩余)的物质的质量不能算在内。参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。质量化学反应碳酸钠与稀盐酸反应后质量减小的原因是什么?碳酸钠与稀盐酸的反应
参加化学反应的反应物有:
生成物有:
我们漏称了: 二氧化碳气体碳酸钠和稀盐酸氯化钠、水和二氧化碳讨论:14交流讨论密闭的环境下如何将所有的反应物和生成物都称量在内呢?如何改进?改进实验仪器
橡皮塞、锥形瓶、导管
双孔橡皮塞、注射器、
气球、带盖的矿泉水瓶、小试管、带支管的试管锥形瓶、小试管碳酸钠和稀盐酸的反应为什么化学反应前后质量守恒呢?溯本求源:水电解的微观过程 从分子、原子的变化情况说明为什么化学反应一定遵守质量守恒定律?1、镁带在氧气中完全燃烧后,生成物的质量比原来镁带的质量大。试用质量守恒定律解释原因。学以致用: 根据质量守恒定律,参加反应的镁和氧气的质量之和等于生成氧化镁的质量。所以氧化镁的质量大于镁带的质量。镁燃烧,产生耀眼的白光,生成一种白色固体。天平不平衡。①参加反应的氧气没有称量。②生成物白烟跑掉一部分。 ③坩埚钳上粘掉一部分等等。巩固延伸 所有的化学反应都遵守质量守恒定律,该定律具有普遍意义。因为有时考虑问题不全面或实验方案不完善,而导致表面上的不相等。镁的质量+参加反应的氧气质量==氧化镁的质量牛刀小试:2、细铁丝在氧气中完全燃烧后,生成物的质量比原来铁丝的质量大。试用质量守恒定律解释原因1、“点石成金”符合质量守恒定律吗?3、小明同学用10g高锰酸钾做加热制取氧气的实验,完全反应后称量剩余固体,质量为9.2g.符合质量守恒定律吗? 符合。根据质量守恒定律参加
反应的高锰酸钾的质量等于生成固体和氧气的质量总和。 质量减轻,证明生成了0.8g氧气。 某物质A在一定条件下分解后只生成二氧化碳和水,则该物质由 种元素组成。
若物质A的一个分子分解生成一个二氧化碳分子和一个水分子,则一个A分子是怎么构成?碳、氢、氧三一个A分子由一个碳原子、两个氢原子和三个氧原子构成。畅谈收获,交流解疑家庭小实验
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
