化学能与电能
图片预览








文档简介
课件20张PPT。化学能与电能教学重点:原电池的构成条件及工作原理教学难点:电极反应物的确定及电极方程式的书写教学目标1、知识与技能:
了解原电池的定义、工作原理、构成条件、判断正负极;初步养成学生利用实验进行科学探究的能力。2、过程与方法:
通过模拟动画、实验探究原电池的形成及原理,充分运用观察法、实验法、归纳法、对比法等方法。 3、情感态度与价值观:
通过对火力发电和原电池的学习,感受化学给社会带来的进步和文明,激发学生学习兴趣。一、火力发电2001年我国发电总量构成图 火电,又称为火力发电。那么,火究竟是如何转化为电? 电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源,又称为电力。1、原理分析2、化学本质分析氧化还原反应火力发电将化学能经一系列能量转化为电能旧键断裂和新键形成、体系能量变化3、利弊分析 利:化学能转化为电能,社会应用最广泛、使用最方便。弊:温室效应;导致酸雨;废料废水;煤储量有限,不可再生;能量转换效率低。a、改进火力发电效能 直接将化学能转化为电能,减少中间环节能损,高效、 清洁利用燃料,不浪费能源,更方便、环保。 b、研究新的发电方式4、改进分析 化学史:化学能转变为电能的探索1791年他在解剖时在实验室将悬有去了皮的青蛙腿的铜钩挂在铁架台上,当青蛙碰到铁杆时,发现蛙腿会有肌肉抽搐的现象。伽伏尼认为动物的组织会产生电流,而金属是传递电流的导体。 他从独特的角度认为电流是由两种不同的金属产生的,经过一系列的实验,终于在1800年成功研制了世界上第一个能产生稳定电流的电池(见右图)。 (意大利生物学家伽伏尼)(法国物理学家、化学家伏特)【实验一】
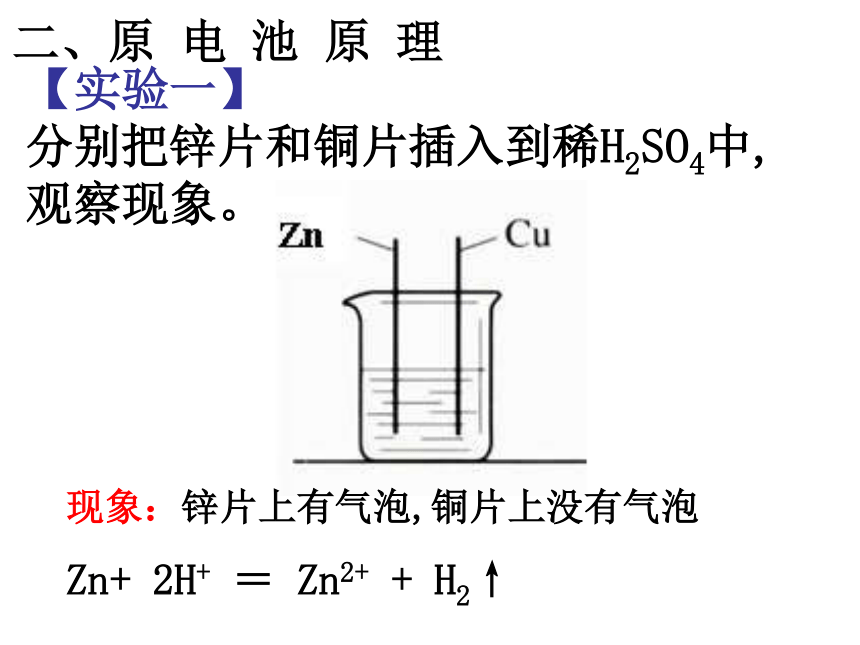
分别把锌片和铜片插入到稀H2SO4中,
观察现象。二、原 电 池 原 理现象:锌片上有气泡,铜片上没有气泡Zn+ 2H+ = Zn2+ + H2↑【实验二】
再用导线把锌片和铜片连接起来,观察铜片上有无气泡产生?在导线中间接入一个电流表,
观察电流表的指针是否偏转? [实验现象]:铜片上有气泡产生,锌片不断溶解,电流表的指针发生偏转。[实验结论]:导线中有电流通过1、原电池定义:把化学能转变为电能的装置.失得Zn-2e-= Zn2+2H++ 2e-= H2↑负极正极Zn+ 2H+ = Zn2+ + H2↑生成气体Zn片溶解本质:氧化还原反应2、原电池电极反应3、原电池的构成条件:极-两种活动性不同的金属(或一种非金属导体)作电极
液-电极材料均插入电解质溶液中
路-两极相连形成闭合电路
自-一个自发进行的氧化还原反应4、原电池的正、负极的判断方法: ①电极材料②电流方向或电子方向 ③溶液离子的移动方向 ④电极反应 ⑤电极的增重或减轻,
产生气体 — +e-还原反应氧化反应阳离子阴离子电极质量电极质量5、电极方程式的书写方法⑴首先判断正负极
较活泼的金属(负极)失电子,发生氧化反应
溶液中阳离子在正极上得电子,发生还原反应⑵两电极方程式中要满足得失电子数守恒学以致用:写出电极反应和总反应方程式练习1:把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱的为: ( )
A.a > b > c > d B.a > c > d > b
C.c > a > b .> d D.b > d > c > a B
练习2:根据反应2Fe3+ + Fe = 3 Fe 2+设计原电池,你有哪些可行方案? FeCu
C
AgFeCl3
Fe(NO3)3
Fe2(SO4)3练习3:一个原电池的总反应的离子方程式是
Zn + Cu2+ = Zn2+ + Cu,该反应的原电池的组成正确的是( )C 在巴格达博物馆中,有一只简陋的约有两千年历史的小陶罐—内有一根铜管,管内有一根下端由沥青包裹的铁棒。外观虽不起眼,却被誉为考古学领域最令人吃惊的发现。英国物理学家沃尔特·温顿对它做了仔细研究。他说: “在铜制容器内放上一些酸,随便什么,醋也可以。”于是他把这根管子放入出土的陶罐里,再向瓶里倒进了酸性葡萄酒,在铜管和铁棒间连上有电流计的导线,奇迹出现了……巴格达之谜化学趣话 自由女神的外壳为铜,内层支架为铁,中间用油毛毡隔开。时间长了,设计者预先没想到的事发生了:那层油毛毡失去了隔离作用,而大西洋潮湿的夹带盐分的空气向女神不断地吹来,无数的 在女神身上形成,结果加速了铁的腐蚀。尽管女神有万般灵验,现在也自身难保。怎样免除她的厄运呢?
面对自由女神的腐蚀,应采取什么措施和方法?把你好的建议上网发给美国纽约市长吧!原电池救救自由女神!化学趣话CuZnZn2+H+H+Zn-2e-=Zn2+2H++2e-=H2↑ 氧化反应还原反应负极正极电子沿导线传递,产生电流阳离子失去电子溶液中阳离子得到电子阴离子正极负极SO42-原电池小结较活泼金属不活泼金属或石墨工作原理:较活泼的金属发生氧化反应,电子从较活泼的金属(负极)通过外电路流向较不活泼的金属(正极)。 再见
了解原电池的定义、工作原理、构成条件、判断正负极;初步养成学生利用实验进行科学探究的能力。2、过程与方法:
通过模拟动画、实验探究原电池的形成及原理,充分运用观察法、实验法、归纳法、对比法等方法。 3、情感态度与价值观:
通过对火力发电和原电池的学习,感受化学给社会带来的进步和文明,激发学生学习兴趣。一、火力发电2001年我国发电总量构成图 火电,又称为火力发电。那么,火究竟是如何转化为电? 电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源,又称为电力。1、原理分析2、化学本质分析氧化还原反应火力发电将化学能经一系列能量转化为电能旧键断裂和新键形成、体系能量变化3、利弊分析 利:化学能转化为电能,社会应用最广泛、使用最方便。弊:温室效应;导致酸雨;废料废水;煤储量有限,不可再生;能量转换效率低。a、改进火力发电效能 直接将化学能转化为电能,减少中间环节能损,高效、 清洁利用燃料,不浪费能源,更方便、环保。 b、研究新的发电方式4、改进分析 化学史:化学能转变为电能的探索1791年他在解剖时在实验室将悬有去了皮的青蛙腿的铜钩挂在铁架台上,当青蛙碰到铁杆时,发现蛙腿会有肌肉抽搐的现象。伽伏尼认为动物的组织会产生电流,而金属是传递电流的导体。 他从独特的角度认为电流是由两种不同的金属产生的,经过一系列的实验,终于在1800年成功研制了世界上第一个能产生稳定电流的电池(见右图)。 (意大利生物学家伽伏尼)(法国物理学家、化学家伏特)【实验一】
分别把锌片和铜片插入到稀H2SO4中,
观察现象。二、原 电 池 原 理现象:锌片上有气泡,铜片上没有气泡Zn+ 2H+ = Zn2+ + H2↑【实验二】
再用导线把锌片和铜片连接起来,观察铜片上有无气泡产生?在导线中间接入一个电流表,
观察电流表的指针是否偏转? [实验现象]:铜片上有气泡产生,锌片不断溶解,电流表的指针发生偏转。[实验结论]:导线中有电流通过1、原电池定义:把化学能转变为电能的装置.失得Zn-2e-= Zn2+2H++ 2e-= H2↑负极正极Zn+ 2H+ = Zn2+ + H2↑生成气体Zn片溶解本质:氧化还原反应2、原电池电极反应3、原电池的构成条件:极-两种活动性不同的金属(或一种非金属导体)作电极
液-电极材料均插入电解质溶液中
路-两极相连形成闭合电路
自-一个自发进行的氧化还原反应4、原电池的正、负极的判断方法: ①电极材料②电流方向或电子方向 ③溶液离子的移动方向 ④电极反应 ⑤电极的增重或减轻,
产生气体 — +e-还原反应氧化反应阳离子阴离子电极质量电极质量5、电极方程式的书写方法⑴首先判断正负极
较活泼的金属(负极)失电子,发生氧化反应
溶液中阳离子在正极上得电子,发生还原反应⑵两电极方程式中要满足得失电子数守恒学以致用:写出电极反应和总反应方程式练习1:把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱的为: ( )
A.a > b > c > d B.a > c > d > b
C.c > a > b .> d D.b > d > c > a B
练习2:根据反应2Fe3+ + Fe = 3 Fe 2+设计原电池,你有哪些可行方案? FeCu
C
AgFeCl3
Fe(NO3)3
Fe2(SO4)3练习3:一个原电池的总反应的离子方程式是
Zn + Cu2+ = Zn2+ + Cu,该反应的原电池的组成正确的是( )C 在巴格达博物馆中,有一只简陋的约有两千年历史的小陶罐—内有一根铜管,管内有一根下端由沥青包裹的铁棒。外观虽不起眼,却被誉为考古学领域最令人吃惊的发现。英国物理学家沃尔特·温顿对它做了仔细研究。他说: “在铜制容器内放上一些酸,随便什么,醋也可以。”于是他把这根管子放入出土的陶罐里,再向瓶里倒进了酸性葡萄酒,在铜管和铁棒间连上有电流计的导线,奇迹出现了……巴格达之谜化学趣话 自由女神的外壳为铜,内层支架为铁,中间用油毛毡隔开。时间长了,设计者预先没想到的事发生了:那层油毛毡失去了隔离作用,而大西洋潮湿的夹带盐分的空气向女神不断地吹来,无数的 在女神身上形成,结果加速了铁的腐蚀。尽管女神有万般灵验,现在也自身难保。怎样免除她的厄运呢?
面对自由女神的腐蚀,应采取什么措施和方法?把你好的建议上网发给美国纽约市长吧!原电池救救自由女神!化学趣话CuZnZn2+H+H+Zn-2e-=Zn2+2H++2e-=H2↑ 氧化反应还原反应负极正极电子沿导线传递,产生电流阳离子失去电子溶液中阳离子得到电子阴离子正极负极SO42-原电池小结较活泼金属不活泼金属或石墨工作原理:较活泼的金属发生氧化反应,电子从较活泼的金属(负极)通过外电路流向较不活泼的金属(正极)。 再见
