人教版九年级化学 第十单元 课题1 常见的酸和碱 课时2 常见的酸的性质和用途课件(共24张PPT)
文档属性
| 名称 | 人教版九年级化学 第十单元 课题1 常见的酸和碱 课时2 常见的酸的性质和用途课件(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 474.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-22 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
课题1 常见的酸和碱
第十单元 酸和碱
课时2 常见的酸的性质和用途
目录
01
课程要求
02
课前预习
03
知识点精讲
04
课堂检测
课程要求
认识硫酸、盐酸等常见酸的主要性质和用途;知道浓硫酸有腐蚀性;初步学会浓硫酸的稀释方法。
课前预习
写出下列物质的化学式。
氯化铵
氯化亚铁
氯化铜
硫酸铝
硫酸钠
碳酸钙
碳酸钠
NH4Cl
FeCl2
CuCl2
Al2(SO4)3
Na2SO4
CaCO3
Na2CO3
知识点精讲
知识点1
浓盐酸和浓硫酸的性质及用途
酸 浓盐酸(HCl) 浓硫酸(H2SO4)
颜色、状态、气味 ______色、有__________气味的______体 ______色黏稠的________
打开试剂瓶后的现象 有______生成,说明浓盐酸具有______性 无明显现象
密度 常用浓盐酸(37%~38%)1.19 g/cm3 常用浓硫酸(98%)1.84 g/cm3
完成课本P52“实验10-2”,填写下表。
无
刺激性
液
无
油状液体
白雾
挥发
用途 ①金属________、制造药物等; ②人体胃液中含有盐酸,可帮助消化 ①用于化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等;
②浓硫酸有________性,在实验室常用它做________
除锈
吸水
干燥剂
注意:①浓硫酸可干燥CO2、SO2、HCl等酸性气体和O2、H2、CO等中性气体,但不能干燥NH3,常放入洗气瓶中使用。②浓盐酸具有________性,敞口放置,盐酸会挥发到空气中,使得溶液的质量________,溶质的质量分数________;浓硫酸具有________性,敞口放置,浓硫酸会吸收空气中的水分,使得溶液的质量________,溶质的质量分数________。所以浓盐酸和浓硫酸都应该________保存。
挥发
变小
变小
吸水
变大
变小
密封
课堂练习
1. 硫酸是一种重要的工业原料,下列说法不正确的是( )
A. 浓硫酸可用于干燥O2
B. 浓硫酸是无色油状黏稠液体
C. 实验室可用块状石灰石与稀硫酸制备CO2
D. 稀硫酸可用于金属表面除锈
C
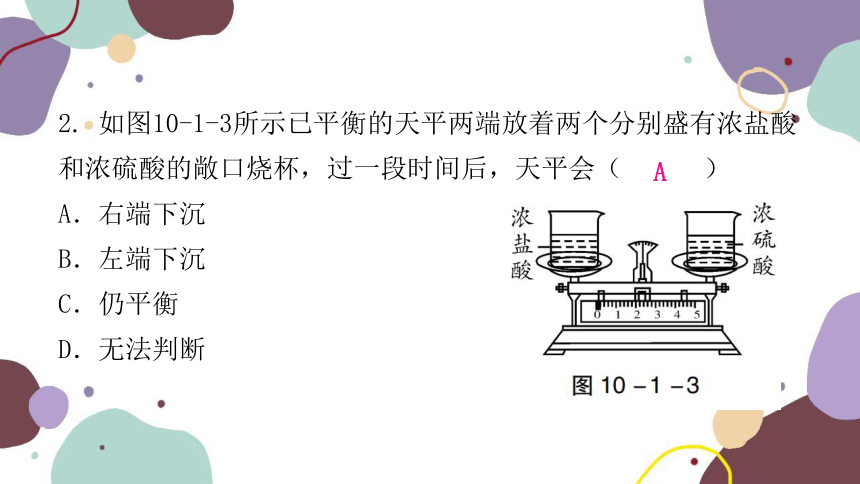
2. 如图10-1-3所示已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯,过一段时间后,天平会( )
A.右端下沉
B.左端下沉
C.仍平衡
D.无法判断
A
3. 下列有关酸的说法错误的是( )
A.浓硫酸要密封保存,这与浓硫酸的挥发性有关
B.浓硫酸、浓盐酸都具有强烈的腐蚀性
C.浓盐酸在空气中会形成白雾
D.浓盐酸和浓硫酸敞口放置,溶质质量分数均减小
A
思路点拨
浓盐酸和浓硫酸敞口放置于空气中溶质质量分数都减小,但前者是因为溶质质量减小,后者是因为溶剂质量增加。
知识点2
浓硫酸的腐蚀性及稀释
实验操作 放置一会儿后的现象 实验结论
用玻璃棒蘸浓硫酸在纸上写字 字迹________ 浓硫酸具有________性
用小木棍蘸少量浓硫酸 蘸浓硫酸的小木棍________
将浓硫酸滴到一小块布上 滴浓硫酸的布__________________
1. 观察课本P53“实验10-3”,填写下表。
黑色
变黑
变黑甚至成洞
强腐蚀
【归纳】浓硫酸能夺取纸张、木材、布料、皮肤里的________(脱水性),生成黑色的________,因此不要将浓硫酸沾到皮肤或衣服上。
水分
炭
2. 观察课本P53“实验10-4”,填写下表。
实验图示 操作步骤 现象 实验结论
①将________沿着器壁________注入盛有水的烧杯中,并用________(作用:_____________)不断搅拌; ②用手触摸烧杯外壁 烧杯外壁________ 浓硫酸溶于水________________
浓硫酸
缓慢
玻璃棒
帮助散热
发热
放出大量热
注意:①稀释浓硫酸时,一定要把浓硫酸沿容器壁慢慢注入水里,并不断搅拌。切不可将水倒入浓硫酸。如果将水注入浓硫酸中,由于____________________,会浮在浓硫酸上面,溶解时放出的________能使水立刻________,使浓硫酸液滴_____________,这是非常危险的!
②如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量________冲洗,然后再涂上_________________________溶液。
水的密度较小
热
沸腾
向四周飞溅
水
3%~5%的NaHCO3
课堂练习
4. 下列图示的实验操作,正确的是( )
A
5. 用玻璃棒蘸取硫酸在白纸上写字,如图10-1-4。
(1)现象:放置一会儿发现用________(填“浓”或“稀”)硫酸在白纸上写的字变黑。
(2)结论:同种酸由于______________________不同,它们的性质不完全相同。
浓
溶质的质量分数
思路点拨
浓硫酸的脱水性:把有机物中的氢、氧元素按水的组成脱去,从而使有机物碳化,属于化学性质;浓硫酸的吸水性:把物质中的水分吸收,从而使物质变得干燥,属于物理性质,常用于干燥气体。
课堂检测
1. 如图是些常见危险品安全标志,装运浓硫酸槽罐车上应贴的图标是( )
A
2. 下列关于盐酸的描述,错误的是( )
A. 盐酸中的溶质是HCl
B. 盐酸能使紫色石蕊溶液变蓝
C. 人体胃液中含有盐酸,可帮助消化
D. 打开装有浓盐酸的试剂瓶瓶盖,瓶口处有白雾出现
B
3. 小明同学想除去卫生间地面瓷砖上的铁锈痕迹,他选择了一种最适宜的物质对铁锈进行了预先处理,你认为这种物质是( )
A.食盐水
B.汽油
C.白醋
D.洗衣粉
C
4. 用玻璃棒蘸取下列溶液在石蕊试纸上写字,字迹先变红后变黑,则蘸取的溶液是( )
A. 浓盐酸
B. 稀盐酸
C. 浓硫酸
D. 稀硫酸
C
5. 如图10-1-5该装置可用来洗气。向其中装入足量浓硫酸,将氧气和水蒸气的混合气体由________端进,________端出,出来的气体就只有________。这说明浓硫酸具有________性。这属于________(填“物理”或“化学”)性质。
a
b
氧气
吸水
物理
酸 性质 溶质的质量 溶剂的质量 溶液的质量 溶质的质量分数
浓盐酸 _________ _________ _________ _________ _________
浓硫酸 _________ _________ _________ _________ _________
挥发性
吸水性
变小
不变
不变
变大
变小
变大
变小
变小
6. 将盛放浓盐酸和浓硫酸的两只试剂瓶敞口放置一段时间,用“变大”“变小”或“不变”等词填写下列变化。
以上变化都属于__________________,浓盐酸、浓硫酸都需要____________________。
物理变化
密封保存
课题1 常见的酸和碱
第十单元 酸和碱
课时2 常见的酸的性质和用途
目录
01
课程要求
02
课前预习
03
知识点精讲
04
课堂检测
课程要求
认识硫酸、盐酸等常见酸的主要性质和用途;知道浓硫酸有腐蚀性;初步学会浓硫酸的稀释方法。
课前预习
写出下列物质的化学式。
氯化铵
氯化亚铁
氯化铜
硫酸铝
硫酸钠
碳酸钙
碳酸钠
NH4Cl
FeCl2
CuCl2
Al2(SO4)3
Na2SO4
CaCO3
Na2CO3
知识点精讲
知识点1
浓盐酸和浓硫酸的性质及用途
酸 浓盐酸(HCl) 浓硫酸(H2SO4)
颜色、状态、气味 ______色、有__________气味的______体 ______色黏稠的________
打开试剂瓶后的现象 有______生成,说明浓盐酸具有______性 无明显现象
密度 常用浓盐酸(37%~38%)1.19 g/cm3 常用浓硫酸(98%)1.84 g/cm3
完成课本P52“实验10-2”,填写下表。
无
刺激性
液
无
油状液体
白雾
挥发
用途 ①金属________、制造药物等; ②人体胃液中含有盐酸,可帮助消化 ①用于化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等;
②浓硫酸有________性,在实验室常用它做________
除锈
吸水
干燥剂
注意:①浓硫酸可干燥CO2、SO2、HCl等酸性气体和O2、H2、CO等中性气体,但不能干燥NH3,常放入洗气瓶中使用。②浓盐酸具有________性,敞口放置,盐酸会挥发到空气中,使得溶液的质量________,溶质的质量分数________;浓硫酸具有________性,敞口放置,浓硫酸会吸收空气中的水分,使得溶液的质量________,溶质的质量分数________。所以浓盐酸和浓硫酸都应该________保存。
挥发
变小
变小
吸水
变大
变小
密封
课堂练习
1. 硫酸是一种重要的工业原料,下列说法不正确的是( )
A. 浓硫酸可用于干燥O2
B. 浓硫酸是无色油状黏稠液体
C. 实验室可用块状石灰石与稀硫酸制备CO2
D. 稀硫酸可用于金属表面除锈
C
2. 如图10-1-3所示已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯,过一段时间后,天平会( )
A.右端下沉
B.左端下沉
C.仍平衡
D.无法判断
A
3. 下列有关酸的说法错误的是( )
A.浓硫酸要密封保存,这与浓硫酸的挥发性有关
B.浓硫酸、浓盐酸都具有强烈的腐蚀性
C.浓盐酸在空气中会形成白雾
D.浓盐酸和浓硫酸敞口放置,溶质质量分数均减小
A
思路点拨
浓盐酸和浓硫酸敞口放置于空气中溶质质量分数都减小,但前者是因为溶质质量减小,后者是因为溶剂质量增加。
知识点2
浓硫酸的腐蚀性及稀释
实验操作 放置一会儿后的现象 实验结论
用玻璃棒蘸浓硫酸在纸上写字 字迹________ 浓硫酸具有________性
用小木棍蘸少量浓硫酸 蘸浓硫酸的小木棍________
将浓硫酸滴到一小块布上 滴浓硫酸的布__________________
1. 观察课本P53“实验10-3”,填写下表。
黑色
变黑
变黑甚至成洞
强腐蚀
【归纳】浓硫酸能夺取纸张、木材、布料、皮肤里的________(脱水性),生成黑色的________,因此不要将浓硫酸沾到皮肤或衣服上。
水分
炭
2. 观察课本P53“实验10-4”,填写下表。
实验图示 操作步骤 现象 实验结论
①将________沿着器壁________注入盛有水的烧杯中,并用________(作用:_____________)不断搅拌; ②用手触摸烧杯外壁 烧杯外壁________ 浓硫酸溶于水________________
浓硫酸
缓慢
玻璃棒
帮助散热
发热
放出大量热
注意:①稀释浓硫酸时,一定要把浓硫酸沿容器壁慢慢注入水里,并不断搅拌。切不可将水倒入浓硫酸。如果将水注入浓硫酸中,由于____________________,会浮在浓硫酸上面,溶解时放出的________能使水立刻________,使浓硫酸液滴_____________,这是非常危险的!
②如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量________冲洗,然后再涂上_________________________溶液。
水的密度较小
热
沸腾
向四周飞溅
水
3%~5%的NaHCO3
课堂练习
4. 下列图示的实验操作,正确的是( )
A
5. 用玻璃棒蘸取硫酸在白纸上写字,如图10-1-4。
(1)现象:放置一会儿发现用________(填“浓”或“稀”)硫酸在白纸上写的字变黑。
(2)结论:同种酸由于______________________不同,它们的性质不完全相同。
浓
溶质的质量分数
思路点拨
浓硫酸的脱水性:把有机物中的氢、氧元素按水的组成脱去,从而使有机物碳化,属于化学性质;浓硫酸的吸水性:把物质中的水分吸收,从而使物质变得干燥,属于物理性质,常用于干燥气体。
课堂检测
1. 如图是些常见危险品安全标志,装运浓硫酸槽罐车上应贴的图标是( )
A
2. 下列关于盐酸的描述,错误的是( )
A. 盐酸中的溶质是HCl
B. 盐酸能使紫色石蕊溶液变蓝
C. 人体胃液中含有盐酸,可帮助消化
D. 打开装有浓盐酸的试剂瓶瓶盖,瓶口处有白雾出现
B
3. 小明同学想除去卫生间地面瓷砖上的铁锈痕迹,他选择了一种最适宜的物质对铁锈进行了预先处理,你认为这种物质是( )
A.食盐水
B.汽油
C.白醋
D.洗衣粉
C
4. 用玻璃棒蘸取下列溶液在石蕊试纸上写字,字迹先变红后变黑,则蘸取的溶液是( )
A. 浓盐酸
B. 稀盐酸
C. 浓硫酸
D. 稀硫酸
C
5. 如图10-1-5该装置可用来洗气。向其中装入足量浓硫酸,将氧气和水蒸气的混合气体由________端进,________端出,出来的气体就只有________。这说明浓硫酸具有________性。这属于________(填“物理”或“化学”)性质。
a
b
氧气
吸水
物理
酸 性质 溶质的质量 溶剂的质量 溶液的质量 溶质的质量分数
浓盐酸 _________ _________ _________ _________ _________
浓硫酸 _________ _________ _________ _________ _________
挥发性
吸水性
变小
不变
不变
变大
变小
变大
变小
变小
6. 将盛放浓盐酸和浓硫酸的两只试剂瓶敞口放置一段时间,用“变大”“变小”或“不变”等词填写下列变化。
以上变化都属于__________________,浓盐酸、浓硫酸都需要____________________。
物理变化
密封保存
同课章节目录
