铁及其化合物的性质与转化(20张PPT)
文档属性
| 名称 | 铁及其化合物的性质与转化(20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 922.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-25 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
高二 专题复习
铁及其化合物的性质和转化
学习目标
1.复习铁的原子结构和化学性质,铁的氧化物和氢氧化物性质,掌握Fe2+和
Fe3+的检验方法。
2.复习Fe2+和Fe3+间的相互转化,掌握变价金属阳离子的氧化性和还原性。
3.认识铁及其重要化合物相互转化等方面的实际应用。
知识梳理一:铁的原子结构
铁
原子结构示意图
在周期表中位置
第四周期第VIII族,属过渡元素
存在
游离态:少量存在于陨石中
化合态:赤铁矿、磁铁矿、黄铁矿等
基态原子核外电子排布式
1s22s22p63s23p63d64s2
1. Fe2+基态核外电子排布式为_______________。
Fe3+基态核外电子排布式为_______________。
2.下列说法正确的是 ( )
铁位于元素周期表中第4周期ⅧB族。
Fe分别与氯气、盐酸反应得到相同的氯化物。
常温下,浓硫酸、浓硝酸能使铁发生钝化,故可在常温下用铁制容器贮藏运输浓硫酸、浓硝酸。
Fe2O3是红棕色固体,可以制成红色的油漆、涂料。
CD
巩固练习
FeCl3
FeCl2
[Ar]3d6
1s22s22p63s23p63d6
或
[Ar]3d5
1s22s22p63s23p63d5
或
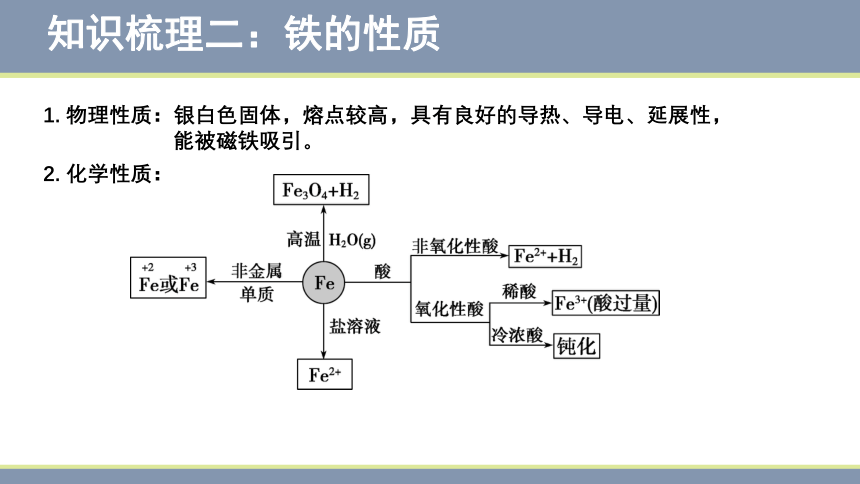
知识梳理二:铁的性质
1. 物理性质:银白色固体,熔点较高,具有良好的导热、导电、延展性,
能被磁铁吸引。
2. 化学性质:
知识梳理二:铁的性质
棕黄
黑
黑
2FeCl3
Fe3O4
FeS
Fe3O4 + 4H2
知识梳理二:铁的性质
3FeCl2
FeSO4 + Cu
铁、铝
浓硫酸、浓硝酸
铁制或铝制容器
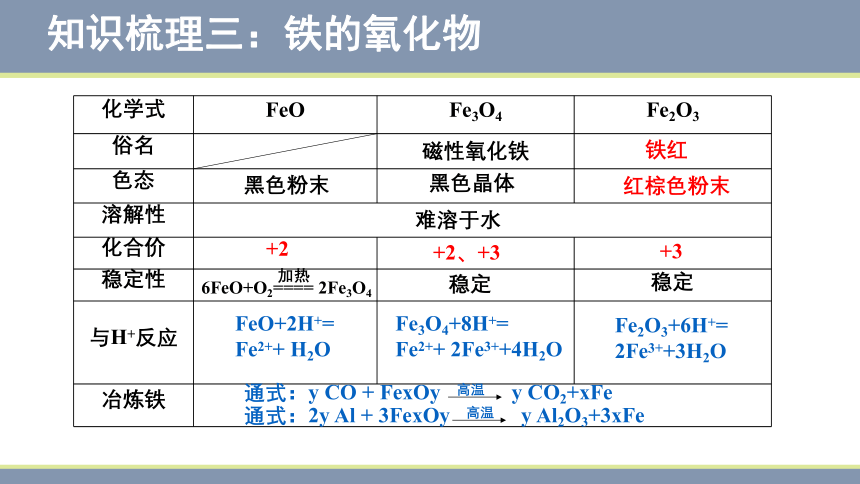
化学式 FeO Fe3O4 Fe2O3
俗名
色态
溶解性 化合价
稳定性
与H+反应
冶炼铁 通式:2y Al + 3FexOy 高温 y Al2O3+3xFe
磁性氧化铁
铁红
黑色粉末
黑色晶体
红棕色粉末
难溶于水
+2
+2、+3
+3
加热
6FeO+O2==== 2Fe3O4
稳定
稳定
FeO+2H+=
Fe2++ H2O
Fe3O4+8H+=
Fe2++ 2Fe3++4H2O
Fe2O3+6H+=
2Fe3++3H2O
知识梳理三:铁的氧化物
通式:y CO + FexOy 高温 y CO2+xFe
知识梳理四:铁的氢氧化物
化学式 Fe(OH)2 Fe(OH)3
色态
与盐酸反应
受热分解 —
制法 可溶性亚铁盐与碱溶液反应 可溶性铁盐与碱溶液反应
二者的关系 在空气中,Fe(OH)2能够非常迅速地被氧气氧化成Fe(OH)3,现象是 , 反应方程式 。 4Fe(OH)2+O2+2H2O=4Fe(OH)3
白色沉淀迅速转化为灰绿色,最后转化为红褐色
白色固体
红褐色固体
Fe(OH)2+2H+= Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
Fe2++2OH-=Fe(OH)2↓
Fe3++3OH-=Fe(OH)3↓
2Fe(OH)3= Fe2O3+3H2O
错
错
对
对
对
错
错
错
3. 判断正误:
巩固练习
4.下列离子方程式正确的是( )
A.FeO溶于硝酸:FeO + 2H+ = Fe2+ + H2O
B.FeCl3溶液与Cu的反应:Cu+Fe3+ = Cu2++Fe2+
C.过量的Fe与稀硝酸反应:
Fe+4H+ + NO3― = Fe3++NO↑+2H2O
D.Fe(OH)3溶于氢碘酸:
Fe(OH)3+3H+ = Fe3++3H2O
E.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
F.向FeBr2溶液中通入足量氯气:
2Fe2++4Br-+3Cl2 = 2Fe3++2Br2+6Cl–
F
硝酸有强氧化性
Fe2+ 、Fe3+
Fe3+与I–发生氧化还原反应
巩固练习
未配平
Fe2+
Fe3+
知识梳理五:Fe2+与 Fe3+的相互转化
Fe2+→Fe3+的氧化剂:
Zn、Fe、Cu、I-、S2-、SO32-等
Cl2、Br2、O2、HNO3、H2O2、KMnO4(H+)等
Fe3+→Fe2+的还原剂:
归纳提升:Fe、Fe2+ 和 Fe3+ 的转化关系图
强氧化剂
还原剂
强氧化剂
弱氧化剂
还原剂
还原剂
知识梳理六:Fe2+、 Fe3+的检验
1.Fe2+的检验
①含有Fe2+的溶液呈 ;
②向待检液中滴加NaOH溶液或氨水,产生白色絮状沉淀,露置在空气中
一段时间后,沉淀变为灰绿色,最后变为红褐色,说明含Fe2+
③向待检液中先滴加 ,无变化,再滴加 ,溶液显 ,
说明含Fe2+
④滴入赤血盐(K3[Fe(CN)6])溶液,出现滕氏蓝沉淀的是Fe2+
3Fe2+ +2[Fe(CN)6]3- =Fe3[Fe(CN)6]2↓(铁氰化亚铁),滕氏蓝
浅绿色
血红色
KSCN溶液
新制的氯水
知识梳理六:Fe2+、 Fe3+的检验
2.Fe3+的检验
①含有Fe3+的溶液呈 ;
②向待检液中滴加NaOH溶液或氨水,产生 沉淀,说明含Fe3+
③向待检液中滴加 ,溶液呈血红色,说明含Fe3+
④向待检液中滴加 ,溶液呈紫色,说明含Fe3+
⑤滴入黄血盐(K4[Fe(CN)6])溶液,出现普鲁士蓝沉淀的是Fe3+
4Fe3+ +3[Fe(CN)6]4- =Fe4[Fe(CN)6]3↓(亚铁氰化铁) 普鲁士蓝
黄色
红褐色
KSCN溶液
苯酚溶液
5. 判断下列各组物质充分反应后,一定能使KSCN溶液显红色的是 ,
一定能使酸性KMnO4褪色的是 。
Fe2+
Fe3+
不确定
√
√
√
√
√
√
③④
②④⑤⑥
巩固练习
Fe + HNO3(稀)
Fe(含少量铁锈) + 足量H2SO4(稀)
FeO + 过量HNO3(稀)
Fe + 水蒸气(高温)→ 稀盐酸
Fe(OH)3 + 足量 HI 溶液
Fe、Cu、Fe3+、Cu2+在溶液中充分反 应后有固体剩余
D
巩固练习
OH-
H+
H+或OH-
链接高考:2021第二次适应性考试
17题(部分)
BD
Fe2O3
CuO
SiO2
4FeS2 + 11O2 === 2Fe2O3 + 8SO2
高温
链接高考:2021第二次适应性考试
17题(部分)
Fe2O3
CuO
SiO2
Fe2(SO4)3
CuSO4
H2SO4
SiO2
Fe + Cu2+ = Fe2+ + Cu
Fe + 2H+ = Fe2+ +H2↑
将Cu2+
转化为
Cu
取少量还原后的上层清液,向其中滴加KSCN溶液,
若溶液不变红,则Fe3+已完全被还原
Fe + 2Fe3+ = 3Fe2+
课堂小结:铁及其化合物的价类二维图
Fe
FeO
Fe2O3
Fe3O4
Fe2+
Fe3+
Fe(OH)2
Fe(OH)3
高二 专题复习
铁及其化合物的性质和转化
学习目标
1.复习铁的原子结构和化学性质,铁的氧化物和氢氧化物性质,掌握Fe2+和
Fe3+的检验方法。
2.复习Fe2+和Fe3+间的相互转化,掌握变价金属阳离子的氧化性和还原性。
3.认识铁及其重要化合物相互转化等方面的实际应用。
知识梳理一:铁的原子结构
铁
原子结构示意图
在周期表中位置
第四周期第VIII族,属过渡元素
存在
游离态:少量存在于陨石中
化合态:赤铁矿、磁铁矿、黄铁矿等
基态原子核外电子排布式
1s22s22p63s23p63d64s2
1. Fe2+基态核外电子排布式为_______________。
Fe3+基态核外电子排布式为_______________。
2.下列说法正确的是 ( )
铁位于元素周期表中第4周期ⅧB族。
Fe分别与氯气、盐酸反应得到相同的氯化物。
常温下,浓硫酸、浓硝酸能使铁发生钝化,故可在常温下用铁制容器贮藏运输浓硫酸、浓硝酸。
Fe2O3是红棕色固体,可以制成红色的油漆、涂料。
CD
巩固练习
FeCl3
FeCl2
[Ar]3d6
1s22s22p63s23p63d6
或
[Ar]3d5
1s22s22p63s23p63d5
或
知识梳理二:铁的性质
1. 物理性质:银白色固体,熔点较高,具有良好的导热、导电、延展性,
能被磁铁吸引。
2. 化学性质:
知识梳理二:铁的性质
棕黄
黑
黑
2FeCl3
Fe3O4
FeS
Fe3O4 + 4H2
知识梳理二:铁的性质
3FeCl2
FeSO4 + Cu
铁、铝
浓硫酸、浓硝酸
铁制或铝制容器
化学式 FeO Fe3O4 Fe2O3
俗名
色态
溶解性 化合价
稳定性
与H+反应
冶炼铁 通式:2y Al + 3FexOy 高温 y Al2O3+3xFe
磁性氧化铁
铁红
黑色粉末
黑色晶体
红棕色粉末
难溶于水
+2
+2、+3
+3
加热
6FeO+O2==== 2Fe3O4
稳定
稳定
FeO+2H+=
Fe2++ H2O
Fe3O4+8H+=
Fe2++ 2Fe3++4H2O
Fe2O3+6H+=
2Fe3++3H2O
知识梳理三:铁的氧化物
通式:y CO + FexOy 高温 y CO2+xFe
知识梳理四:铁的氢氧化物
化学式 Fe(OH)2 Fe(OH)3
色态
与盐酸反应
受热分解 —
制法 可溶性亚铁盐与碱溶液反应 可溶性铁盐与碱溶液反应
二者的关系 在空气中,Fe(OH)2能够非常迅速地被氧气氧化成Fe(OH)3,现象是 , 反应方程式 。 4Fe(OH)2+O2+2H2O=4Fe(OH)3
白色沉淀迅速转化为灰绿色,最后转化为红褐色
白色固体
红褐色固体
Fe(OH)2+2H+= Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
Fe2++2OH-=Fe(OH)2↓
Fe3++3OH-=Fe(OH)3↓
2Fe(OH)3= Fe2O3+3H2O
错
错
对
对
对
错
错
错
3. 判断正误:
巩固练习
4.下列离子方程式正确的是( )
A.FeO溶于硝酸:FeO + 2H+ = Fe2+ + H2O
B.FeCl3溶液与Cu的反应:Cu+Fe3+ = Cu2++Fe2+
C.过量的Fe与稀硝酸反应:
Fe+4H+ + NO3― = Fe3++NO↑+2H2O
D.Fe(OH)3溶于氢碘酸:
Fe(OH)3+3H+ = Fe3++3H2O
E.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
F.向FeBr2溶液中通入足量氯气:
2Fe2++4Br-+3Cl2 = 2Fe3++2Br2+6Cl–
F
硝酸有强氧化性
Fe2+ 、Fe3+
Fe3+与I–发生氧化还原反应
巩固练习
未配平
Fe2+
Fe3+
知识梳理五:Fe2+与 Fe3+的相互转化
Fe2+→Fe3+的氧化剂:
Zn、Fe、Cu、I-、S2-、SO32-等
Cl2、Br2、O2、HNO3、H2O2、KMnO4(H+)等
Fe3+→Fe2+的还原剂:
归纳提升:Fe、Fe2+ 和 Fe3+ 的转化关系图
强氧化剂
还原剂
强氧化剂
弱氧化剂
还原剂
还原剂
知识梳理六:Fe2+、 Fe3+的检验
1.Fe2+的检验
①含有Fe2+的溶液呈 ;
②向待检液中滴加NaOH溶液或氨水,产生白色絮状沉淀,露置在空气中
一段时间后,沉淀变为灰绿色,最后变为红褐色,说明含Fe2+
③向待检液中先滴加 ,无变化,再滴加 ,溶液显 ,
说明含Fe2+
④滴入赤血盐(K3[Fe(CN)6])溶液,出现滕氏蓝沉淀的是Fe2+
3Fe2+ +2[Fe(CN)6]3- =Fe3[Fe(CN)6]2↓(铁氰化亚铁),滕氏蓝
浅绿色
血红色
KSCN溶液
新制的氯水
知识梳理六:Fe2+、 Fe3+的检验
2.Fe3+的检验
①含有Fe3+的溶液呈 ;
②向待检液中滴加NaOH溶液或氨水,产生 沉淀,说明含Fe3+
③向待检液中滴加 ,溶液呈血红色,说明含Fe3+
④向待检液中滴加 ,溶液呈紫色,说明含Fe3+
⑤滴入黄血盐(K4[Fe(CN)6])溶液,出现普鲁士蓝沉淀的是Fe3+
4Fe3+ +3[Fe(CN)6]4- =Fe4[Fe(CN)6]3↓(亚铁氰化铁) 普鲁士蓝
黄色
红褐色
KSCN溶液
苯酚溶液
5. 判断下列各组物质充分反应后,一定能使KSCN溶液显红色的是 ,
一定能使酸性KMnO4褪色的是 。
Fe2+
Fe3+
不确定
√
√
√
√
√
√
③④
②④⑤⑥
巩固练习
Fe + HNO3(稀)
Fe(含少量铁锈) + 足量H2SO4(稀)
FeO + 过量HNO3(稀)
Fe + 水蒸气(高温)→ 稀盐酸
Fe(OH)3 + 足量 HI 溶液
Fe、Cu、Fe3+、Cu2+在溶液中充分反 应后有固体剩余
D
巩固练习
OH-
H+
H+或OH-
链接高考:2021第二次适应性考试
17题(部分)
BD
Fe2O3
CuO
SiO2
4FeS2 + 11O2 === 2Fe2O3 + 8SO2
高温
链接高考:2021第二次适应性考试
17题(部分)
Fe2O3
CuO
SiO2
Fe2(SO4)3
CuSO4
H2SO4
SiO2
Fe + Cu2+ = Fe2+ + Cu
Fe + 2H+ = Fe2+ +H2↑
将Cu2+
转化为
Cu
取少量还原后的上层清液,向其中滴加KSCN溶液,
若溶液不变红,则Fe3+已完全被还原
Fe + 2Fe3+ = 3Fe2+
课堂小结:铁及其化合物的价类二维图
Fe
FeO
Fe2O3
Fe3O4
Fe2+
Fe3+
Fe(OH)2
Fe(OH)3
同课章节目录
