铁及其化合物的应用(19张ppt)
文档属性
| 名称 | 铁及其化合物的应用(19张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-25 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
高二 专题复习
铁及其化合物的应用
学习目标
1.复习新情境下铁及其化合物反应方程式书写的方法。
2.复习水解平衡、沉淀溶解平衡、电化学等原理在铁及其化合物转化中的应用。
3. 通过铁及其化合物重要应用的探究,提升问题解决能力。
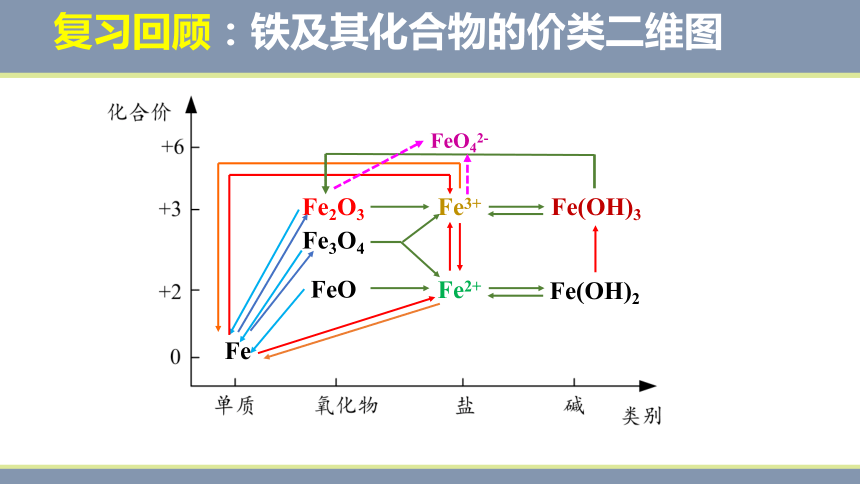
复习回顾:铁及其化合物的价类二维图
Fe
FeO
Fe2O3
Fe3O4
Fe2+
Fe3+
Fe(OH)2
Fe(OH)3
FeO42-
Fe2O3 = 2FeO42-
一、陌生情境中的氧化还原反应
高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。
(1)工业上可以通过在碱性条件下次氯酸钠氧化铁盐法制备高铁酸钠,
离子反应方程式: 。
(2)通过电解方法,用Fe2O3为阳极,石墨为阴极,NaOH溶液为电解质溶液
制备高铁酸钠(Na2FeO4)。写出阳极的电极反应式:
。
Fe3+ + ClO- = FeO42- + Cl-
2. 铁酸锌(ZnFe2O4)是一种脱硫剂,可用于脱除煤气中的H2S。400℃时,
ZnFe2O4与H2、H2S反应生成ZnS和FeS。其化学方程式
为 。
ZnFe2O4 + 3H2S +H2 ==== ZnS + 2FeS +4H2O
400℃
2 3 2 3
+3
+6
+1
-1
2
3
+ 5H2O
+ 10OH-
+10OH-
+ 5H2O
+3
+2
0
- 6e-
②已知:FeSO4+Na2CO3=== FeCO3↓+Na2SO4
制备FeCO3时,选用的加料方式是 (填字母),原因是 。
a.将FeSO4溶液与Na2CO3 溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
二、水解原理相关的应用
Fe(OH)2是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈酸性。
① 配制硫酸亚铁溶液时常加少量 抑制Fe2+的水解,加少量 防止
Fe2+被氧化。
硫酸
铁屑
防止生成Fe(OH)2沉淀
c
Na2CO3溶液呈碱性
二、水解原理的相关应用
2. Fe(OH)3是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强
的溶液中。
① 实验室可用FeCl3滴入沸水中制取氢氧化铁胶体,反应的化学方程式:
。
② 工业上常用调节pH方法除去溶液中的Fe3+。
③ 实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的 中,然后再稀释至所需浓度。
④ Fe3+与 HCO3-、 CO32- 、AlO2- 等水解呈碱性的离子不能大量共存。
⑤ FeCl3溶液蒸干并灼烧后的产物为 。
FeCl3 + 3H2O (沸水) === Fe(OH)3(胶体) + 3HCl
盐酸
Fe2O3
Fe3+、 Fe2+、 Cu2+ 开始沉淀的pH至沉淀完全的pH范围分别为
(1.1~3.2)、(5.8~8.8)和(5.0~6.7)。
(1)除去CuCl2溶液中Fe3+,应调节溶液的pH范围为 。
(2)CuCl2溶液中含有少量Fe3+和 Fe2+杂质,如何除去?
3.2~5.0
三、沉淀溶解平衡的应用
向溶液中加入稍过量的H2O2,并不断搅拌,将Fe2+全部氧化为Fe3+,
加入适量的CuO,并不断搅拌,调节溶液pH为3.2~5.0之间,过滤。
2. MnSO4溶液中混有Fe2(SO4)3、Al2(SO4)3的杂质。向混合溶液中滴加氨水,调节pH进行除杂。若溶液中c(Mn2+) = 0.2 mol L-1,欲使溶液中Fe3+、 Al3+的浓度均小于1ⅹ10-6mol L-1,需控制的pH范围为 。
(已知:室温下 Ksp[Al(OH)3] = 1ⅹ10-33,Ksp[Fe(OH)3] = 3ⅹ10-39,Ksp[Mn(OH)2] = 2 ⅹ10-13。)
5 < pH < 8
三、沉淀溶解平衡的应用
Ksp[Mn(OH)2] = 2 ⅹ10-13 c(OH-) <(2 ⅹ10-13 /0.2 ) 2 = 10-6
Ksp[Fe(OH)3] = 3ⅹ10-39 c(OH-) >(3 ⅹ10-39 /1ⅹ10-6 ) 3 ≈ 10-11
Ksp[Al(OH)3] = 1ⅹ10-33 c(OH-) >(1 ⅹ10-33 /1ⅹ10-6 ) 3 = 10-9
c(H+) < 10-5 pH > 5
c(H+) < 10-3 pH > 3
c(H+) > 10-8 pH < 8
四、电化学中的“铁”
铁的腐蚀
析氢腐蚀
吸氧腐蚀
1. 电化学腐蚀
条 件
正极反应
负极反应
电池反应
后续反应 水膜酸性较强
水膜酸性很弱或呈中性
2H++2e- = H2↑
O2+2H2O+4e- =4OH-
析氢腐蚀
吸氧腐蚀
Fe - 2e- = Fe2+
Fe - 2e- = Fe2+
2Fe+O2+2H2O = 2Fe(OH)2
Fe +2H+ = Fe2++H2↑
铁锈的形成:4Fe(OH)2+O2+2H2O = 4Fe(OH)3
2Fe(OH)3 = Fe2O3·nH2O+(3-n)H2O
2. 电化学防护
牺牲阳极的阴极保护法示意图
辅助阳极(不溶性)
外加电流的阴极保护法示意图
判断正误:
(1) 用牺牲阳极的阴极保护法保护钢铁水闸时,将钢铁水闸与石墨相连( )
(2) 镀锌铁板是利用牺牲阳极的阴极保护法来达到防止腐蚀的目的( )
(3) 镀铜铁制品镀层受损后,铁制品比没有镀层前更容易生锈( )
(4) 若在海轮外壳上附着一些锌块,则可以减缓海轮外壳的腐蚀( )
(5) 用下图所示方法可保护钢闸门不被腐蚀( )
×
√
√
√
×
C
Fe-6e-+8OH-===FeO42- +4H2O
2H2O+2e- ===2OH- +H2↑
阴离子移向阳极,
Fe电极是阳极
没有指明温度和压强
当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_______________________________________。
链接高考:2016江苏高考
1. 铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物。
(1) 在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示。
铁的质量分数增加,铁炭混合物中微电池数目减少
Fe + Cu2+ = Fe2+ + Cu Fe + Pb2+ = Fe2+ + Pb
纳米铁粉与H+反应生成H2
Fe2++BH4- === Fe+B(OH)4- + H2↑
2 2 2
2
1ⅹ4
-1
0
+4OH-
c(H+) ↑
影响反应速率的因素?
Ⅱ有没有其他反应?
Fe + Cu2+ = Fe2+ + Cu
温度
浓度
压强
催化剂
……
4Fe+NO3- +10H+===4Fe2++NH4++3H2O
链接高考:2021第二次适应性考试
+6
+3
3
2ⅹ2
HFeO4- = Fe(OH)3↓ + O2↑
4 4 3
+ 4H+
+ 2H2O
酸性条件下,会发生其他反应吗?
防止FeO42-氧化废水中的Cl- 而被消耗,防止FeO42-分解
FeO42-分解
FeO42-氧化Cl-生成Cl2
链接高考:2021第二次适应性考试
酸性条件下 ClO- 与 Cl- 反应生成Cl2逸出
pH ↑ c(OH-) ↑
会有其他反应发生吗?
随着废水pH的增大,Fe3+与ClO-反应生成的FeO42-浓度增大,
FeO42-氧化废水中有机物的反应速率更大。
对有机物氧化率有影响吗?
同学们再见!
高二 专题复习
铁及其化合物的应用
学习目标
1.复习新情境下铁及其化合物反应方程式书写的方法。
2.复习水解平衡、沉淀溶解平衡、电化学等原理在铁及其化合物转化中的应用。
3. 通过铁及其化合物重要应用的探究,提升问题解决能力。
复习回顾:铁及其化合物的价类二维图
Fe
FeO
Fe2O3
Fe3O4
Fe2+
Fe3+
Fe(OH)2
Fe(OH)3
FeO42-
Fe2O3 = 2FeO42-
一、陌生情境中的氧化还原反应
高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。
(1)工业上可以通过在碱性条件下次氯酸钠氧化铁盐法制备高铁酸钠,
离子反应方程式: 。
(2)通过电解方法,用Fe2O3为阳极,石墨为阴极,NaOH溶液为电解质溶液
制备高铁酸钠(Na2FeO4)。写出阳极的电极反应式:
。
Fe3+ + ClO- = FeO42- + Cl-
2. 铁酸锌(ZnFe2O4)是一种脱硫剂,可用于脱除煤气中的H2S。400℃时,
ZnFe2O4与H2、H2S反应生成ZnS和FeS。其化学方程式
为 。
ZnFe2O4 + 3H2S +H2 ==== ZnS + 2FeS +4H2O
400℃
2 3 2 3
+3
+6
+1
-1
2
3
+ 5H2O
+ 10OH-
+10OH-
+ 5H2O
+3
+2
0
- 6e-
②已知:FeSO4+Na2CO3=== FeCO3↓+Na2SO4
制备FeCO3时,选用的加料方式是 (填字母),原因是 。
a.将FeSO4溶液与Na2CO3 溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
二、水解原理相关的应用
Fe(OH)2是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈酸性。
① 配制硫酸亚铁溶液时常加少量 抑制Fe2+的水解,加少量 防止
Fe2+被氧化。
硫酸
铁屑
防止生成Fe(OH)2沉淀
c
Na2CO3溶液呈碱性
二、水解原理的相关应用
2. Fe(OH)3是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强
的溶液中。
① 实验室可用FeCl3滴入沸水中制取氢氧化铁胶体,反应的化学方程式:
。
② 工业上常用调节pH方法除去溶液中的Fe3+。
③ 实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的 中,然后再稀释至所需浓度。
④ Fe3+与 HCO3-、 CO32- 、AlO2- 等水解呈碱性的离子不能大量共存。
⑤ FeCl3溶液蒸干并灼烧后的产物为 。
FeCl3 + 3H2O (沸水) === Fe(OH)3(胶体) + 3HCl
盐酸
Fe2O3
Fe3+、 Fe2+、 Cu2+ 开始沉淀的pH至沉淀完全的pH范围分别为
(1.1~3.2)、(5.8~8.8)和(5.0~6.7)。
(1)除去CuCl2溶液中Fe3+,应调节溶液的pH范围为 。
(2)CuCl2溶液中含有少量Fe3+和 Fe2+杂质,如何除去?
3.2~5.0
三、沉淀溶解平衡的应用
向溶液中加入稍过量的H2O2,并不断搅拌,将Fe2+全部氧化为Fe3+,
加入适量的CuO,并不断搅拌,调节溶液pH为3.2~5.0之间,过滤。
2. MnSO4溶液中混有Fe2(SO4)3、Al2(SO4)3的杂质。向混合溶液中滴加氨水,调节pH进行除杂。若溶液中c(Mn2+) = 0.2 mol L-1,欲使溶液中Fe3+、 Al3+的浓度均小于1ⅹ10-6mol L-1,需控制的pH范围为 。
(已知:室温下 Ksp[Al(OH)3] = 1ⅹ10-33,Ksp[Fe(OH)3] = 3ⅹ10-39,Ksp[Mn(OH)2] = 2 ⅹ10-13。)
5 < pH < 8
三、沉淀溶解平衡的应用
Ksp[Mn(OH)2] = 2 ⅹ10-13 c(OH-) <(2 ⅹ10-13 /0.2 ) 2 = 10-6
Ksp[Fe(OH)3] = 3ⅹ10-39 c(OH-) >(3 ⅹ10-39 /1ⅹ10-6 ) 3 ≈ 10-11
Ksp[Al(OH)3] = 1ⅹ10-33 c(OH-) >(1 ⅹ10-33 /1ⅹ10-6 ) 3 = 10-9
c(H+) < 10-5 pH > 5
c(H+) < 10-3 pH > 3
c(H+) > 10-8 pH < 8
四、电化学中的“铁”
铁的腐蚀
析氢腐蚀
吸氧腐蚀
1. 电化学腐蚀
条 件
正极反应
负极反应
电池反应
后续反应 水膜酸性较强
水膜酸性很弱或呈中性
2H++2e- = H2↑
O2+2H2O+4e- =4OH-
析氢腐蚀
吸氧腐蚀
Fe - 2e- = Fe2+
Fe - 2e- = Fe2+
2Fe+O2+2H2O = 2Fe(OH)2
Fe +2H+ = Fe2++H2↑
铁锈的形成:4Fe(OH)2+O2+2H2O = 4Fe(OH)3
2Fe(OH)3 = Fe2O3·nH2O+(3-n)H2O
2. 电化学防护
牺牲阳极的阴极保护法示意图
辅助阳极(不溶性)
外加电流的阴极保护法示意图
判断正误:
(1) 用牺牲阳极的阴极保护法保护钢铁水闸时,将钢铁水闸与石墨相连( )
(2) 镀锌铁板是利用牺牲阳极的阴极保护法来达到防止腐蚀的目的( )
(3) 镀铜铁制品镀层受损后,铁制品比没有镀层前更容易生锈( )
(4) 若在海轮外壳上附着一些锌块,则可以减缓海轮外壳的腐蚀( )
(5) 用下图所示方法可保护钢闸门不被腐蚀( )
×
√
√
√
×
C
Fe-6e-+8OH-===FeO42- +4H2O
2H2O+2e- ===2OH- +H2↑
阴离子移向阳极,
Fe电极是阳极
没有指明温度和压强
当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_______________________________________。
链接高考:2016江苏高考
1. 铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物。
(1) 在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示。
铁的质量分数增加,铁炭混合物中微电池数目减少
Fe + Cu2+ = Fe2+ + Cu Fe + Pb2+ = Fe2+ + Pb
纳米铁粉与H+反应生成H2
Fe2++BH4- === Fe+B(OH)4- + H2↑
2 2 2
2
1ⅹ4
-1
0
+4OH-
c(H+) ↑
影响反应速率的因素?
Ⅱ有没有其他反应?
Fe + Cu2+ = Fe2+ + Cu
温度
浓度
压强
催化剂
……
4Fe+NO3- +10H+===4Fe2++NH4++3H2O
链接高考:2021第二次适应性考试
+6
+3
3
2ⅹ2
HFeO4- = Fe(OH)3↓ + O2↑
4 4 3
+ 4H+
+ 2H2O
酸性条件下,会发生其他反应吗?
防止FeO42-氧化废水中的Cl- 而被消耗,防止FeO42-分解
FeO42-分解
FeO42-氧化Cl-生成Cl2
链接高考:2021第二次适应性考试
酸性条件下 ClO- 与 Cl- 反应生成Cl2逸出
pH ↑ c(OH-) ↑
会有其他反应发生吗?
随着废水pH的增大,Fe3+与ClO-反应生成的FeO42-浓度增大,
FeO42-氧化废水中有机物的反应速率更大。
对有机物氧化率有影响吗?
同学们再见!
同课章节目录
