湖南省岳阳市湘阴县2021-2022学年高三下学期期中考试化学试题(Word版含答案)
文档属性
| 名称 | 湖南省岳阳市湘阴县2021-2022学年高三下学期期中考试化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 756.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-27 00:00:00 | ||
图片预览



文档简介
湘阴县2021-2022学年高三下学期期中考试
化学
(时间75分钟 满分100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cu 64 Ba 137
一、单项选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项符合题目要求。
1. 2020年11月24日,嫦娥五号探测器发射圆满成功,开启我国首次地外天体采样返回之旅。探月工程所选用的新材料与化学有密切相关。下列叙述正确的是
A. 登月中,所用北斗系统的导航卫星,其计算机的芯片材料是高纯度二氧化硅
B. 用于光学望远镜的高致密碳化硅特种陶瓷材料,是一种传统无机非金属材料
C. 面对高空低压的环境,所使用的碳纤维是一种有机高分子材料
D. 嫦娥五号探测器在月球表面展示的国旗,其材料要求具有耐高低温、防静电等多种特性,所用的高性能芳纶纤维材料是复合材料
2. 已知NA是阿伏加德罗常数的值,下列说法正确的是
A. D218O和T2O的混合物1.1 g,含有的质子数为0.5NA
B. 0.1mol·L-1Na2CO3溶液中阴离子总数大于0.2NA
C. 5.6g Fe与足量的S反应转移的电子数为0.3NA
D. 0.1 mol H2和0.2 mol I2充分反应后分子总数小于0.3NA
3.常温下,用0.1mol·L-1氨水滴定10mL浓度均为0.1mol·L-1的HCl和CH3COOH的混合液,
已知醋酸的电离常数为Ka=1.8×10-5, 下列说法错误的是
A. 在氨水滴定前,混合溶液c(Cl-)> c(CH3COOH)
B. 在氨水滴定前,混合溶液c(CH3COO-) ≈ Ka
C. 当滴入氨水10mL时,c(NH4+)+c(NH3·H2O)= c(CH3COOH)+ c(CH3COO-)
D. 当溶液呈中性时,氨水滴入量等于20mL,且c(NH4+)4. 如图所示,铁有δ、γ、α三种晶体,三种晶体在不同温度下能发生转化。下列说法正确的是
δ-Fe γ-Fe α-Fe
A.γ-Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
B.α-Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
C.将铁加热到1 500 ℃分别急速冷却和缓慢冷却,得到的晶体类型相同
D.若α-Fe晶胞边长为a cm,γ-Fe晶胞边长为b cm,则两种晶体的密度比为b3∶a3
5. 常温下,向1 LpH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示。下列叙述不正确的是
A c点溶液中:c(Na+)>c(HCO)>c(CO)
B. a点溶液中:水电离出的c(H+)=1×10-10 mol·L-1
C. b点溶液中:c(H+)=1×10-10 mol·L-1
D. d点溶液中:c(Na+)+c(H+)=2c(CO)+c(HCO)+c(OH-)
6. 正确认识化学物质是学好化学的关键,下列各组物质前后对应正确的是
A. 浓硫酸:电解质 B. :与 互为同系物
C. :硬脂酸甘油酯 D. 氯化铵的电子式:
7. 类比法是化学上研究物质的重要方法之一,下列类比的结果正确是
A. N2分子中存在,化学性质稳定,则的化学性质稳定
B. CH4的空间构型为正四面体型,则C(CH3)4碳骨架的空间构型为正四面体型
C. 工业上电解熔融的MgCl2冶炼镁,则电解熔融的AlCl3冶炼铝
D. 镁和铝与稀硫酸所形成的原电池中镁作负极,则镁和铝与氢氧化钠溶液所形成的原电池中镁作负极
8. 下列各组澄清溶液中的离子能大量共存,且加入(或通入)X试剂后发生反应的离子方程式书写正确的是
选项 离子组 X试剂 离子方程式
A Ca2+、Na+、HCO、Cl- NaOH 溶液 HCO+OH-=== CO+H2O
B Fe3+、Na+、I-、SO 过量氨水 Fe3++3NH3·H2O===Fe(OH)3↓+ 3NH
C K+、Na+、AlO、CO 少量盐酸 AlO+H++H2O ===Al(OH)3↓
D K+、Na+、ClO-、SO 足量SO2 SO2+3ClO-+H2O=== SO+Cl-+2HClO
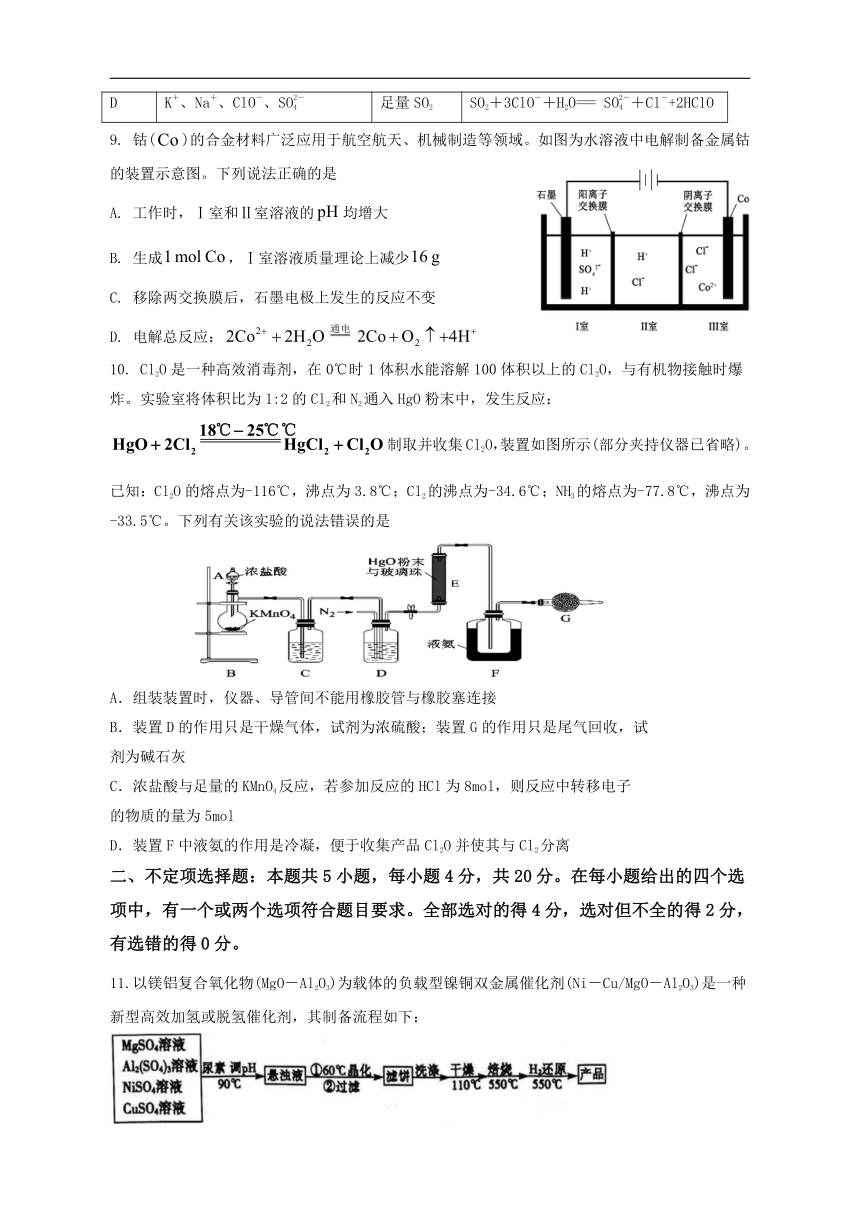
9. 钴()的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
A. 工作时,Ⅰ室和Ⅱ室溶液的均增大
B. 生成,Ⅰ室溶液质量理论上减少
C. 移除两交换膜后,石墨电极上发生的反应不变
D. 电解总反应:
10. Cl2O是一种高效消毒剂,在0℃时1体积水能溶解100体积以上的Cl2O,与有机物接触时爆炸。实验室将体积比为1:2的Cl2和N2通入HgO粉末中,发生反应:制取并收集Cl2O,装置如图所示(部分夹持仪器已省略)。已知:Cl2O的熔点为-116℃,沸点为3.8℃;Cl2的沸点为-34.6℃;NH3的熔点为-77.8℃,沸点为-33.5℃。下列有关该实验的说法错误的是
A.组装装置时,仪器、导管间不能用橡胶管与橡胶塞连接
B.装置D的作用只是干燥气体,试剂为浓硫酸;装置G的作用只是尾气回收,试
剂为碱石灰
C.浓盐酸与足量的KMnO4反应,若参加反应的HCl为8mol,则反应中转移电子
的物质的量为5mol
D.装置F中液氨的作用是冷凝,便于收集产品Cl2O并使其与Cl2分离
二、不定项选择题:本题共5小题,每小题4分,共20分。在每小题给出的四个选项中,有一个或两个选项符合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
11.以镁铝复合氧化物(MgO-Al2O3)为载体的负载型镍铜双金属催化剂(Ni-Cu/MgO-Al2O3)是一种新型高效加氢或脱氢催化剂,其制备流程如下:
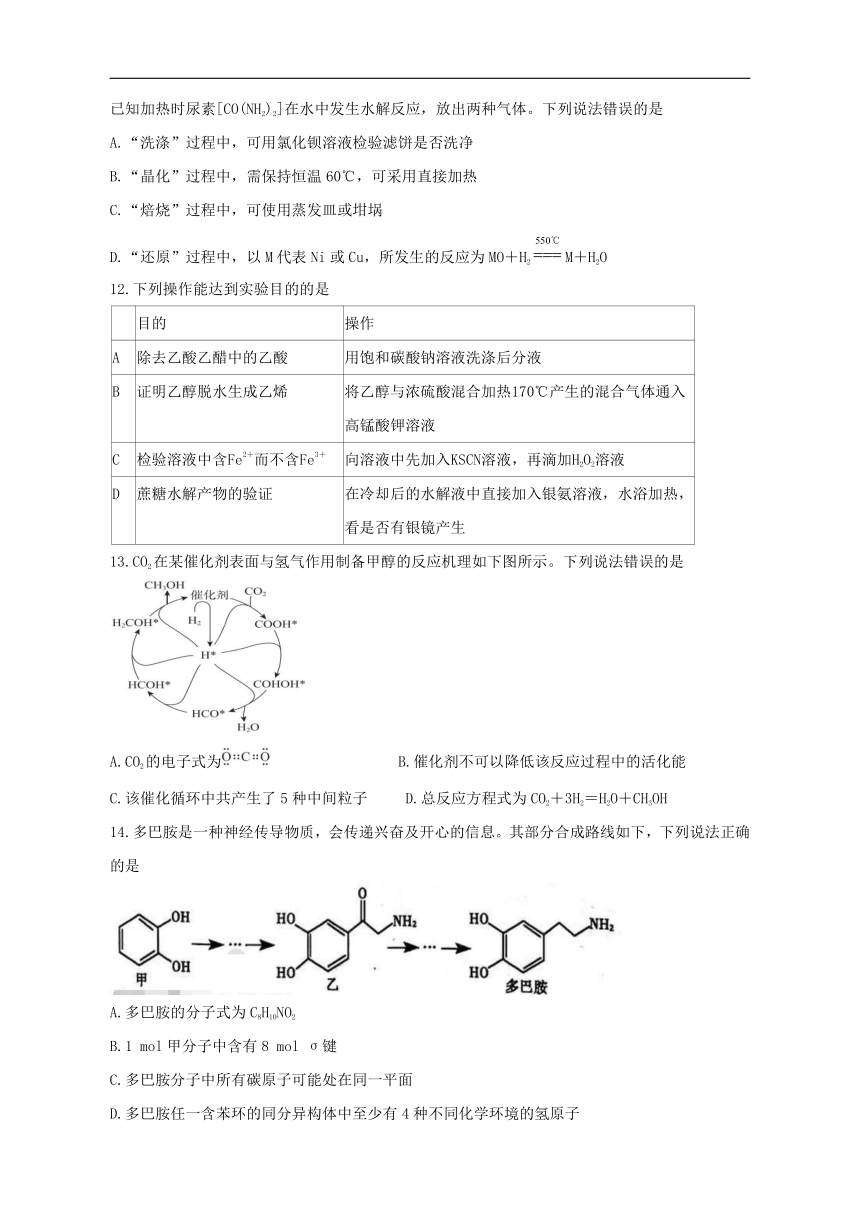
已知加热时尿素[CO(NH2)2]在水中发生水解反应,放出两种气体。下列说法错误的是
A.“洗涤”过程中,可用氯化钡溶液检验滤饼是否洗净
B.“晶化”过程中,需保持恒温60℃,可采用直接加热
C.“焙烧”过程中,可使用蒸发皿或坩埚
D.“还原”过程中,以M代表Ni或Cu,所发生的反应为MO+H2M+H2O
12.下列操作能达到实验目的的是
目的 操作
A 除去乙酸乙醋中的乙酸 用饱和碳酸钠溶液洗涤后分液
B 证明乙醇脱水生成乙烯 将乙醇与浓硫酸混合加热170℃产生的混合气体通入高锰酸钾溶液
C 检验溶液中含Fe2+而不含Fe3+ 向溶液中先加入KSCN溶液,再滴加H2O2溶液
D 蔗糖水解产物的验证 在冷却后的水解液中直接加入银氨溶液,水浴加热,看是否有银镜产生
13.CO2在某催化剂表面与氢气作用制备甲醇的反应机理如下图所示。下列说法错误的是
A.CO2的电子式为 B.催化剂不可以降低该反应过程中的活化能
C.该催化循环中共产生了5种中间粒子 D.总反应方程式为CO2+3H2=H2O+CH3OH
14.多巴胺是一种神经传导物质,会传递兴奋及开心的信息。其部分合成路线如下,下列说法正确的是
A.多巴胺的分子式为C8H10NO2
B.1 mol甲分子中含有8 mol σ键
C.多巴胺分子中所有碳原子可能处在同一平面
D.多巴胺任一含苯环的同分异构体中至少有4种不同化学环境的氢原子
15.常温下,用0.100 mol·L-1 NaOH溶液滴定10 mL 0.100 mol·L-1 H3PO4溶液,pH随滴入NaOH溶液体积的变化曲线如图所示。下列说法错误的是
A.Ka1(H3PO4)的数量级为10-3
B.a点溶液中c(H2PO4-)>c(HPO42-)>c(H3PO4)
C.c点溶液中c(H+)+2c(H3PO4)+c(H2PO4-)=c(OH-)+c(PO43-)
D.随着NaOH溶液的滴加,水的电离程度逐渐增大
三、非选择题:本题共5小题,共50分
16.(12分)碲(Te)为第VIA元素,其单质凭借优良的性能成为制作合金添加剂、半导体、光电元件的主体材料,并被广泛应用于冶金、航空航天、电子等领域。可从精炼铜的阳极泥(主要成分为Cu2Te)中回收碲,工艺流程如下 :
(1)“焙烧”后,碲主要以TeO2 形式存在,写出相应反应的化学方程式:_________(2分)。
(2)为了选择最佳的焙烧工艺,进行了温度和硫酸加入量的条件实验,结果如下表所示:
则实验中应选择的条件为_______________(1分),原因为_______________(2分)。
(3)工艺( I)中,“还原”时发生的总的化学方程式为_______________(2分)。
(4)由于工艺(I)中“氧化”对溶液和物料条件要求高,有研究者采用工艺(II)获得碲。则“电积”过程中,阴极的电极反应式为_______________(2分)。
(5)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合并,进入铜电积系统。该处理措施优点为_____________(2分)。
②滤渣3中若含Au和Ag,可用__________将二者分离。(填字母)(2分)
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸
17.(14分)2020年春节前后,新型冠状病毒严重影响了人们正常生活。含次氯酸钠的水溶液具备良好的杀菌消毒效果。某化学兴趣小组拟利用实验室的常见药品制备次氯酸钠消毒液,并探讨提高消毒液中次氯酸钠百分比的方法。
Ⅰ该小组同学采用了高锰酸钾和浓盐酸在图1所示装置中制氯气,请回答下列问题:
中反应的化学方程式为______。
甲同学利用图1中的装置证明从a出来的氯气潮湿且含有氯化氢,则接口的连接顺序为______填接口编号,中放入______。乙同学认为甲同学的装置太复杂,可去掉装置,同时将中的溶液换成W,溶液W及实验中对应的现象为______。
Ⅱ,该小组同学将氯气通入含氢氧化钠溶液的烧杯中,发现反应放热明显,查阅资料获悉,氯气与碱溶液反应,产物会随反应温度的不同而不同。具体如下:
该小组利用该信息又设计了如图2所示的装置制取和NaClO。
该小组应控制的实验条件是______。反应后,从装置中溶液蒸发浓缩获得晶体,将该晶体与二氧化锰共热,生成了能使带火星的木条复燃气体。
处发生反应的离子方程式为______。
根据上述Ⅰ、Ⅱ两个实验过程,你认为在实验室制取消毒液并提高次氯酸钠的质量分数,应该注意的事项有列举两条。______;______。
18.(12分)砷化镓(GaAs)是优良的半导体材料,其晶体结构与单晶硅相似。
(1)基态Ga原子的价电子排布式为 ,其同周期元素中未成对电子数
最多的是 (填元素符号)。
(2)GaAs可用Ga(CH3)3(常温下为无色液体)和AsH3高温反应制得,同时生成另一种产物,写出反应方程式 ,另一种产物中心原子的杂化类型为 。
(3)沸点AsH3 NH3(填“>”、“<”、“=”),
原因是 。
(4)GaAs的晶胞结构如图所示,键角 ,若晶胞中距离最近的两个Ga原子距离为a nm,阿伏加德罗常数的值为NA,则GaAs的密度为 g/cm3。
19.(12分)某研究小组合成抗心绞痛药物雷诺嗪,设计合成路线如下:
已知:(1)
(2)
(3)
请回答:
(1)下列说法正确的是 。
A.1H-NMR谱显示化合物F中有3种不同化学环境的氢原子
B.1mol E与足量NaOH反应,最多消耗NaOH 4 mol
C.F→G的反应类型是氧化反应
D.雷诺嗪的分子式是C24H33N3O4
(2)化合物X的结构简式是 ;化合物Y的结构简式是 。
(3)B + C → D的化学方程式是 。
(4)写出化合物B同时符合下列条件的同分异构体的结构简式 。
①包含 ;
②包含碳氧双键和—NH-Cl结构。
以苯和丙烯为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂任选)
。
化学参考答案
一、单项选择题:本题共10小题,每小题3分,共30分。
题号 1 2 3 4 5 6 7 8 9 10
答案 D A C B A C B C D B
二、不定项选择题:本题共5小题,每小题4分,共20分。
题号 11 12 13 14 15
答案 BC AC BC CD D
三、非选择题:本题共4小题,共50分
16.(12分)(1) Cu2Te+2H2SO4+2O22CuSO4+TeO2+2H2O
(2) 460℃、硫酸用量为理论量的1.25 倍 该条件下,铜的浸出率高且碲的损失较低
(3)Na2TeO4+3Na2SO3+H2SO4=4Na2SO4+Te+H2O (4)TeO32-+ 4e-+ 3H2O=Te+6OH-
(5) ①CuSO4 溶液回收利用,提高经济效益 ②B
17. (14分)(1)浓
(2)efdchgb或fedchgb 湿润的淀粉碘化钾试纸 紫色石蕊试液,溶液变红色且不褪色
(3)装置放入热水浴中,装置放入冰水浴中
(4)
(5)氯气通入氢氧化钠溶液前要除去HCl,以免产物中氯化钠较多 要在较低温度下反应,以免产物中氯酸钠较多
18.(12分)(1)4S24P1 Cr
(2)Ga(CH3)3 +AsH3=GaAs+3CH4
SP3杂化
(3)< NH3分子间可以形成氢键
(4)109 28 ×1021
19.(12分)(1)ABD
(2)
(3)
(4)
(5)
化学
(时间75分钟 满分100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cu 64 Ba 137
一、单项选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项符合题目要求。
1. 2020年11月24日,嫦娥五号探测器发射圆满成功,开启我国首次地外天体采样返回之旅。探月工程所选用的新材料与化学有密切相关。下列叙述正确的是
A. 登月中,所用北斗系统的导航卫星,其计算机的芯片材料是高纯度二氧化硅
B. 用于光学望远镜的高致密碳化硅特种陶瓷材料,是一种传统无机非金属材料
C. 面对高空低压的环境,所使用的碳纤维是一种有机高分子材料
D. 嫦娥五号探测器在月球表面展示的国旗,其材料要求具有耐高低温、防静电等多种特性,所用的高性能芳纶纤维材料是复合材料
2. 已知NA是阿伏加德罗常数的值,下列说法正确的是
A. D218O和T2O的混合物1.1 g,含有的质子数为0.5NA
B. 0.1mol·L-1Na2CO3溶液中阴离子总数大于0.2NA
C. 5.6g Fe与足量的S反应转移的电子数为0.3NA
D. 0.1 mol H2和0.2 mol I2充分反应后分子总数小于0.3NA
3.常温下,用0.1mol·L-1氨水滴定10mL浓度均为0.1mol·L-1的HCl和CH3COOH的混合液,
已知醋酸的电离常数为Ka=1.8×10-5, 下列说法错误的是
A. 在氨水滴定前,混合溶液c(Cl-)> c(CH3COOH)
B. 在氨水滴定前,混合溶液c(CH3COO-) ≈ Ka
C. 当滴入氨水10mL时,c(NH4+)+c(NH3·H2O)= c(CH3COOH)+ c(CH3COO-)
D. 当溶液呈中性时,氨水滴入量等于20mL,且c(NH4+)
δ-Fe γ-Fe α-Fe
A.γ-Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
B.α-Fe晶体中与每个铁原子距离相等且最近的铁原子有6个
C.将铁加热到1 500 ℃分别急速冷却和缓慢冷却,得到的晶体类型相同
D.若α-Fe晶胞边长为a cm,γ-Fe晶胞边长为b cm,则两种晶体的密度比为b3∶a3
5. 常温下,向1 LpH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示。下列叙述不正确的是
A c点溶液中:c(Na+)>c(HCO)>c(CO)
B. a点溶液中:水电离出的c(H+)=1×10-10 mol·L-1
C. b点溶液中:c(H+)=1×10-10 mol·L-1
D. d点溶液中:c(Na+)+c(H+)=2c(CO)+c(HCO)+c(OH-)
6. 正确认识化学物质是学好化学的关键,下列各组物质前后对应正确的是
A. 浓硫酸:电解质 B. :与 互为同系物
C. :硬脂酸甘油酯 D. 氯化铵的电子式:
7. 类比法是化学上研究物质的重要方法之一,下列类比的结果正确是
A. N2分子中存在,化学性质稳定,则的化学性质稳定
B. CH4的空间构型为正四面体型,则C(CH3)4碳骨架的空间构型为正四面体型
C. 工业上电解熔融的MgCl2冶炼镁,则电解熔融的AlCl3冶炼铝
D. 镁和铝与稀硫酸所形成的原电池中镁作负极,则镁和铝与氢氧化钠溶液所形成的原电池中镁作负极
8. 下列各组澄清溶液中的离子能大量共存,且加入(或通入)X试剂后发生反应的离子方程式书写正确的是
选项 离子组 X试剂 离子方程式
A Ca2+、Na+、HCO、Cl- NaOH 溶液 HCO+OH-=== CO+H2O
B Fe3+、Na+、I-、SO 过量氨水 Fe3++3NH3·H2O===Fe(OH)3↓+ 3NH
C K+、Na+、AlO、CO 少量盐酸 AlO+H++H2O ===Al(OH)3↓
D K+、Na+、ClO-、SO 足量SO2 SO2+3ClO-+H2O=== SO+Cl-+2HClO
9. 钴()的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
A. 工作时,Ⅰ室和Ⅱ室溶液的均增大
B. 生成,Ⅰ室溶液质量理论上减少
C. 移除两交换膜后,石墨电极上发生的反应不变
D. 电解总反应:
10. Cl2O是一种高效消毒剂,在0℃时1体积水能溶解100体积以上的Cl2O,与有机物接触时爆炸。实验室将体积比为1:2的Cl2和N2通入HgO粉末中,发生反应:制取并收集Cl2O,装置如图所示(部分夹持仪器已省略)。已知:Cl2O的熔点为-116℃,沸点为3.8℃;Cl2的沸点为-34.6℃;NH3的熔点为-77.8℃,沸点为-33.5℃。下列有关该实验的说法错误的是
A.组装装置时,仪器、导管间不能用橡胶管与橡胶塞连接
B.装置D的作用只是干燥气体,试剂为浓硫酸;装置G的作用只是尾气回收,试
剂为碱石灰
C.浓盐酸与足量的KMnO4反应,若参加反应的HCl为8mol,则反应中转移电子
的物质的量为5mol
D.装置F中液氨的作用是冷凝,便于收集产品Cl2O并使其与Cl2分离
二、不定项选择题:本题共5小题,每小题4分,共20分。在每小题给出的四个选项中,有一个或两个选项符合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
11.以镁铝复合氧化物(MgO-Al2O3)为载体的负载型镍铜双金属催化剂(Ni-Cu/MgO-Al2O3)是一种新型高效加氢或脱氢催化剂,其制备流程如下:
已知加热时尿素[CO(NH2)2]在水中发生水解反应,放出两种气体。下列说法错误的是
A.“洗涤”过程中,可用氯化钡溶液检验滤饼是否洗净
B.“晶化”过程中,需保持恒温60℃,可采用直接加热
C.“焙烧”过程中,可使用蒸发皿或坩埚
D.“还原”过程中,以M代表Ni或Cu,所发生的反应为MO+H2M+H2O
12.下列操作能达到实验目的的是
目的 操作
A 除去乙酸乙醋中的乙酸 用饱和碳酸钠溶液洗涤后分液
B 证明乙醇脱水生成乙烯 将乙醇与浓硫酸混合加热170℃产生的混合气体通入高锰酸钾溶液
C 检验溶液中含Fe2+而不含Fe3+ 向溶液中先加入KSCN溶液,再滴加H2O2溶液
D 蔗糖水解产物的验证 在冷却后的水解液中直接加入银氨溶液,水浴加热,看是否有银镜产生
13.CO2在某催化剂表面与氢气作用制备甲醇的反应机理如下图所示。下列说法错误的是
A.CO2的电子式为 B.催化剂不可以降低该反应过程中的活化能
C.该催化循环中共产生了5种中间粒子 D.总反应方程式为CO2+3H2=H2O+CH3OH
14.多巴胺是一种神经传导物质,会传递兴奋及开心的信息。其部分合成路线如下,下列说法正确的是
A.多巴胺的分子式为C8H10NO2
B.1 mol甲分子中含有8 mol σ键
C.多巴胺分子中所有碳原子可能处在同一平面
D.多巴胺任一含苯环的同分异构体中至少有4种不同化学环境的氢原子
15.常温下,用0.100 mol·L-1 NaOH溶液滴定10 mL 0.100 mol·L-1 H3PO4溶液,pH随滴入NaOH溶液体积的变化曲线如图所示。下列说法错误的是
A.Ka1(H3PO4)的数量级为10-3
B.a点溶液中c(H2PO4-)>c(HPO42-)>c(H3PO4)
C.c点溶液中c(H+)+2c(H3PO4)+c(H2PO4-)=c(OH-)+c(PO43-)
D.随着NaOH溶液的滴加,水的电离程度逐渐增大
三、非选择题:本题共5小题,共50分
16.(12分)碲(Te)为第VIA元素,其单质凭借优良的性能成为制作合金添加剂、半导体、光电元件的主体材料,并被广泛应用于冶金、航空航天、电子等领域。可从精炼铜的阳极泥(主要成分为Cu2Te)中回收碲,工艺流程如下 :
(1)“焙烧”后,碲主要以TeO2 形式存在,写出相应反应的化学方程式:_________(2分)。
(2)为了选择最佳的焙烧工艺,进行了温度和硫酸加入量的条件实验,结果如下表所示:
则实验中应选择的条件为_______________(1分),原因为_______________(2分)。
(3)工艺( I)中,“还原”时发生的总的化学方程式为_______________(2分)。
(4)由于工艺(I)中“氧化”对溶液和物料条件要求高,有研究者采用工艺(II)获得碲。则“电积”过程中,阴极的电极反应式为_______________(2分)。
(5)工业生产中,滤渣2经硫酸酸浸后得滤液3和滤渣3。
①滤液3 与滤液1合并,进入铜电积系统。该处理措施优点为_____________(2分)。
②滤渣3中若含Au和Ag,可用__________将二者分离。(填字母)(2分)
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.浓盐酸
17.(14分)2020年春节前后,新型冠状病毒严重影响了人们正常生活。含次氯酸钠的水溶液具备良好的杀菌消毒效果。某化学兴趣小组拟利用实验室的常见药品制备次氯酸钠消毒液,并探讨提高消毒液中次氯酸钠百分比的方法。
Ⅰ该小组同学采用了高锰酸钾和浓盐酸在图1所示装置中制氯气,请回答下列问题:
中反应的化学方程式为______。
甲同学利用图1中的装置证明从a出来的氯气潮湿且含有氯化氢,则接口的连接顺序为______填接口编号,中放入______。乙同学认为甲同学的装置太复杂,可去掉装置,同时将中的溶液换成W,溶液W及实验中对应的现象为______。
Ⅱ,该小组同学将氯气通入含氢氧化钠溶液的烧杯中,发现反应放热明显,查阅资料获悉,氯气与碱溶液反应,产物会随反应温度的不同而不同。具体如下:
该小组利用该信息又设计了如图2所示的装置制取和NaClO。
该小组应控制的实验条件是______。反应后,从装置中溶液蒸发浓缩获得晶体,将该晶体与二氧化锰共热,生成了能使带火星的木条复燃气体。
处发生反应的离子方程式为______。
根据上述Ⅰ、Ⅱ两个实验过程,你认为在实验室制取消毒液并提高次氯酸钠的质量分数,应该注意的事项有列举两条。______;______。
18.(12分)砷化镓(GaAs)是优良的半导体材料,其晶体结构与单晶硅相似。
(1)基态Ga原子的价电子排布式为 ,其同周期元素中未成对电子数
最多的是 (填元素符号)。
(2)GaAs可用Ga(CH3)3(常温下为无色液体)和AsH3高温反应制得,同时生成另一种产物,写出反应方程式 ,另一种产物中心原子的杂化类型为 。
(3)沸点AsH3 NH3(填“>”、“<”、“=”),
原因是 。
(4)GaAs的晶胞结构如图所示,键角 ,若晶胞中距离最近的两个Ga原子距离为a nm,阿伏加德罗常数的值为NA,则GaAs的密度为 g/cm3。
19.(12分)某研究小组合成抗心绞痛药物雷诺嗪,设计合成路线如下:
已知:(1)
(2)
(3)
请回答:
(1)下列说法正确的是 。
A.1H-NMR谱显示化合物F中有3种不同化学环境的氢原子
B.1mol E与足量NaOH反应,最多消耗NaOH 4 mol
C.F→G的反应类型是氧化反应
D.雷诺嗪的分子式是C24H33N3O4
(2)化合物X的结构简式是 ;化合物Y的结构简式是 。
(3)B + C → D的化学方程式是 。
(4)写出化合物B同时符合下列条件的同分异构体的结构简式 。
①包含 ;
②包含碳氧双键和—NH-Cl结构。
以苯和丙烯为原料,设计下图所示化合物的合成路线(用流程图表示,无机试剂任选)
。
化学参考答案
一、单项选择题:本题共10小题,每小题3分,共30分。
题号 1 2 3 4 5 6 7 8 9 10
答案 D A C B A C B C D B
二、不定项选择题:本题共5小题,每小题4分,共20分。
题号 11 12 13 14 15
答案 BC AC BC CD D
三、非选择题:本题共4小题,共50分
16.(12分)(1) Cu2Te+2H2SO4+2O22CuSO4+TeO2+2H2O
(2) 460℃、硫酸用量为理论量的1.25 倍 该条件下,铜的浸出率高且碲的损失较低
(3)Na2TeO4+3Na2SO3+H2SO4=4Na2SO4+Te+H2O (4)TeO32-+ 4e-+ 3H2O=Te+6OH-
(5) ①CuSO4 溶液回收利用,提高经济效益 ②B
17. (14分)(1)浓
(2)efdchgb或fedchgb 湿润的淀粉碘化钾试纸 紫色石蕊试液,溶液变红色且不褪色
(3)装置放入热水浴中,装置放入冰水浴中
(4)
(5)氯气通入氢氧化钠溶液前要除去HCl,以免产物中氯化钠较多 要在较低温度下反应,以免产物中氯酸钠较多
18.(12分)(1)4S24P1 Cr
(2)Ga(CH3)3 +AsH3=GaAs+3CH4
SP3杂化
(3)< NH3分子间可以形成氢键
(4)109 28 ×1021
19.(12分)(1)ABD
(2)
(3)
(4)
(5)
同课章节目录
