1.1物质的分类及转化(33张ppt)
文档属性
| 名称 | 1.1物质的分类及转化(33张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-28 16:51:55 | ||
图片预览









文档简介
(共33张PPT)
第一节 物质的分类及转化
第一课时 物质的分类
学习目标
1
2
了解“树状分类法”和“交叉分类法”
学会从不同角度对常见无机化合物进行分类
学习目标
重难点
常见无机化合物的分类
1.同素异形体
自主阅读课本第6页,完成导纲上基础感知中同素异形体的相关内容。
同素异形体:
(1)概念:
(2)举例:
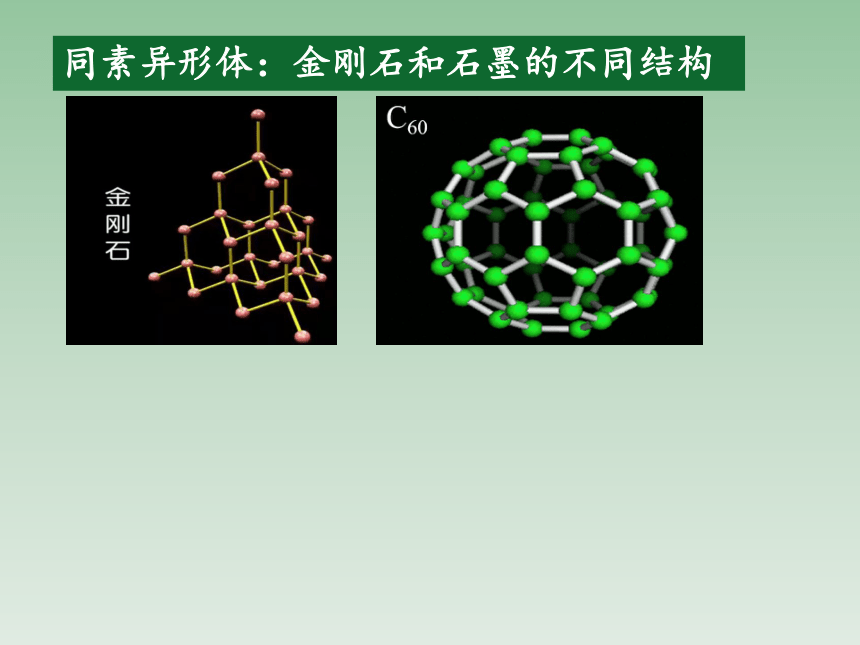
金刚石、石墨、C60是碳元素的同素异形体;O2和O3是氧元素的同素异形体;
红磷和白磷是磷元素的同素异形体。
由同一种元素形成的几种性质不同的单质,叫做这种元素的同素异形体。
同素异形体:金刚石和石墨的不同结构
同素异形体之间的转化属于物理变化还是化学变化?
化学变化。比如:金刚石和石墨的转化过程中,虽然元素的种类没有变,但它们的结构却发生了转变。
2.分类法
自主阅读课本第7页,完成导纲上基础感知中分类法的相关内容。
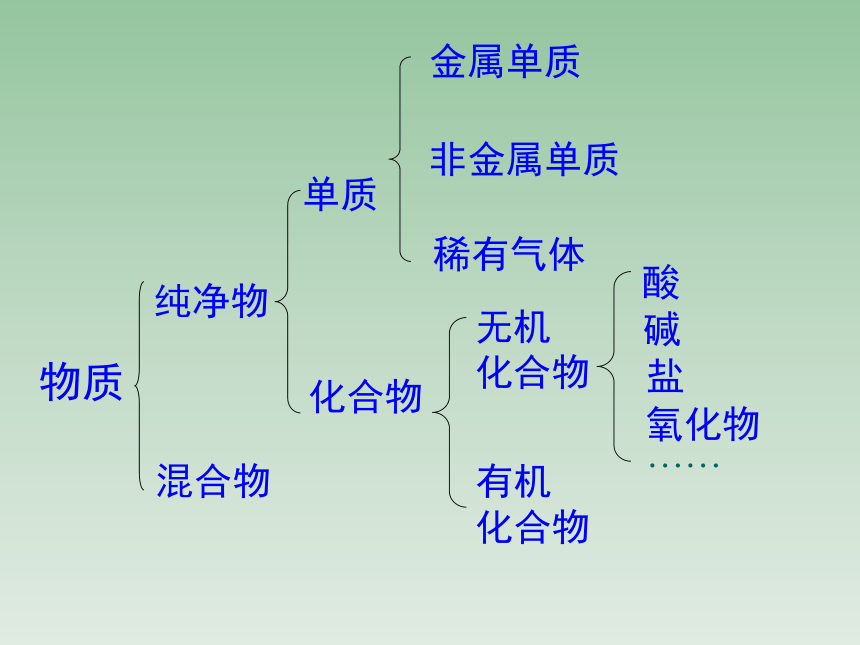
物质
纯净物
非金属单质
化合物
酸
碱
盐
氧化物
单质
混合物
金属单质
无机
化合物
有机
化合物
……
稀有气体
金属单质的化学性质
4.与水反应
2Na+2H2O=2NaOH+H2↑
1.活泼金属与酸反应
Fe+HCl=FeCl2+H2↑
2.与非金属单质发生反应
Fe+S=FeS
Fe+O2=Fe2O3
3.与其他金属盐溶液反应置换金属
(金属活动性顺序)
Fe+CuSO4=FeSO4+Cu
非金属单质的化学性质
3.大多数能够与水反应
Cl2+H2O=HCl+HClO
2.大多数能与金属反应
Fe+Cl2 = FeCl3+H2↑
1.与O2发生反应
C+O2 ═ CO2
4.活泼非金属置换不活泼的非金属Cl2+2HBr=2HCl+Br2
点燃
物质
纯净物
非金属单质
化合物
酸
碱
盐
氧化物
单质
混合物
金属单质
无机
化合物
有机
化合物
……
稀有气体
树状分类法
含义:采用树状形式,对同类事物进行再分类。
特点:同一层次的物质类别间一般是相互独立,没有交叉的。
酸
碱
盐
氧化物
纯净物
混合物
混合物
混合物
单质
化合物
物质
Na2CO3
K2SO4
钾盐
硫酸盐
钠盐
碳酸盐
Na2SO4
K2CO3
对于纯净物Na2CO3、Na2SO4、K2SO4、K2CO3,从其组成的阳离子来看,它们属于什么盐?从阴离子来看,又属于什么盐?
含义:对同一事物,以不同的标准进行分类。
特点:
1、从不同的角度分析物质有不同的分类方法
2、物质类别之间有部分交叉
交叉分类法
不一定。该物质有可能是同素异形体的混合物,比如:金刚石、石墨与C60的混合物。
1.只含有一种元素的物质一定是纯净物吗?
2.结晶水合物(如CuSO4·5H2O)属于纯净物还是混合物?
结晶水合物是纯净物。
注:只要能写出化学式的物质都是纯净物。
3.常见无机化合物
的分类
自主完成导纲上基础感知中酸、碱、盐、氧化物的分类。
组议:
讨论导纲上基础感知中酸、碱、盐、氧化物的分类。
酸的分类
按是否
含氧元素
酸
按有无
挥发性
挥发性酸:HNO3 、HCl 、 CH3COOH等
含氧酸:H2SO4、HNO3、H3PO4等
无氧酸:HCl、H2S(氢硫酸)等
按水溶液中H+的个数
一元酸:HCl、HNO3等
二元酸:H2SO4、H2CO3等
按酸性强弱
三元酸:H3PO4等
强酸:HNO3 、HCl 、H2SO4等
弱酸:HF、CH3COOH 等
难挥发性酸:H2SO4、 H3PO4等
碱的分类
碱
强碱:NaOH、KOH、Ba(OH)2等
可溶性碱:NaOH、KOH、Ba(OH)2等
难溶性碱:Mg(OH)2、Cu(OH)2等
弱碱:NH3·H2O等
按溶解性
按碱性强弱
盐的分类
按组成
盐
按溶解性
正盐:BaSO4、KNO3、NH4Cl等
碱式盐:Cu2(OH)2CO3等
难溶性盐:CaCO3、AgCl等
按酸根离子中是否含有氧元素
酸式盐:NaHCO3、KHSO4等
含氧酸盐:Na2SO4、KNO3等
无氧酸盐:NaCl、ZnS等
可溶性盐:Na2SO4、KNO3等
下列盐:①Na2CO3 ②NH4HCO3 ③BaSO4 ④NaH2PO3 ⑤Cu(OH)2CO3 ⑥NaHS ⑦Mg(OH)Cl
属于正盐的有 ,
酸式盐的有 ,
碱式盐的有 。
① ③
② ④ ⑥
⑤ ⑦
氧化物
酸性氧化物
碱性氧化物
两性氧化物
CO2、SiO2、SO3、Mn2O7 等
CaO、CuO、K2O 等
Al2O3、ZnO 等
依据组成元素
非金属氧化物
金属氧化物
依据性质
氧化物的分类
CO、NO 等
成盐氧化物
特殊氧化物
NO2、Na2O2、Fe3O4等
不成盐氧化物
Al2O3 + 2NaOH = 2NaAlO2 + H2O
Al2O3 + 6HCl =2 AlCl3 + 3H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
2Na2O2+4HCl=4NaCl+2H2O+O2↑
(偏铝酸钠)
自主完成导纲第2页的思考题。
对议:
互检导纲第2页的思考题。
1.所有的酸性氧化物都能溶于水,与水化合成酸吗?
不能,如:SiO2难溶于水。
不能,如:CuO难溶于水。
2.所有的碱性氧化物都能溶于水,与水化合成碱吗?
3.碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物吗?
4.酸性氧化物一定是非金属氧化物,非金属氧化物一定是酸性氧化物吗?
碱性氧化物
金属氧化物
一定
不一定,如Mn2O7
酸性氧化物
非金属氧化物
不一定,如Mn2O7
不一定,如CO
一定 三 不 定
小 结:
1、同素异形体
2、分类法
3、常见无机化合物的分类
同学们再见!
第一节 物质的分类及转化
第一课时 物质的分类
学习目标
1
2
了解“树状分类法”和“交叉分类法”
学会从不同角度对常见无机化合物进行分类
学习目标
重难点
常见无机化合物的分类
1.同素异形体
自主阅读课本第6页,完成导纲上基础感知中同素异形体的相关内容。
同素异形体:
(1)概念:
(2)举例:
金刚石、石墨、C60是碳元素的同素异形体;O2和O3是氧元素的同素异形体;
红磷和白磷是磷元素的同素异形体。
由同一种元素形成的几种性质不同的单质,叫做这种元素的同素异形体。
同素异形体:金刚石和石墨的不同结构
同素异形体之间的转化属于物理变化还是化学变化?
化学变化。比如:金刚石和石墨的转化过程中,虽然元素的种类没有变,但它们的结构却发生了转变。
2.分类法
自主阅读课本第7页,完成导纲上基础感知中分类法的相关内容。
物质
纯净物
非金属单质
化合物
酸
碱
盐
氧化物
单质
混合物
金属单质
无机
化合物
有机
化合物
……
稀有气体
金属单质的化学性质
4.与水反应
2Na+2H2O=2NaOH+H2↑
1.活泼金属与酸反应
Fe+HCl=FeCl2+H2↑
2.与非金属单质发生反应
Fe+S=FeS
Fe+O2=Fe2O3
3.与其他金属盐溶液反应置换金属
(金属活动性顺序)
Fe+CuSO4=FeSO4+Cu
非金属单质的化学性质
3.大多数能够与水反应
Cl2+H2O=HCl+HClO
2.大多数能与金属反应
Fe+Cl2 = FeCl3+H2↑
1.与O2发生反应
C+O2 ═ CO2
4.活泼非金属置换不活泼的非金属Cl2+2HBr=2HCl+Br2
点燃
物质
纯净物
非金属单质
化合物
酸
碱
盐
氧化物
单质
混合物
金属单质
无机
化合物
有机
化合物
……
稀有气体
树状分类法
含义:采用树状形式,对同类事物进行再分类。
特点:同一层次的物质类别间一般是相互独立,没有交叉的。
酸
碱
盐
氧化物
纯净物
混合物
混合物
混合物
单质
化合物
物质
Na2CO3
K2SO4
钾盐
硫酸盐
钠盐
碳酸盐
Na2SO4
K2CO3
对于纯净物Na2CO3、Na2SO4、K2SO4、K2CO3,从其组成的阳离子来看,它们属于什么盐?从阴离子来看,又属于什么盐?
含义:对同一事物,以不同的标准进行分类。
特点:
1、从不同的角度分析物质有不同的分类方法
2、物质类别之间有部分交叉
交叉分类法
不一定。该物质有可能是同素异形体的混合物,比如:金刚石、石墨与C60的混合物。
1.只含有一种元素的物质一定是纯净物吗?
2.结晶水合物(如CuSO4·5H2O)属于纯净物还是混合物?
结晶水合物是纯净物。
注:只要能写出化学式的物质都是纯净物。
3.常见无机化合物
的分类
自主完成导纲上基础感知中酸、碱、盐、氧化物的分类。
组议:
讨论导纲上基础感知中酸、碱、盐、氧化物的分类。
酸的分类
按是否
含氧元素
酸
按有无
挥发性
挥发性酸:HNO3 、HCl 、 CH3COOH等
含氧酸:H2SO4、HNO3、H3PO4等
无氧酸:HCl、H2S(氢硫酸)等
按水溶液中H+的个数
一元酸:HCl、HNO3等
二元酸:H2SO4、H2CO3等
按酸性强弱
三元酸:H3PO4等
强酸:HNO3 、HCl 、H2SO4等
弱酸:HF、CH3COOH 等
难挥发性酸:H2SO4、 H3PO4等
碱的分类
碱
强碱:NaOH、KOH、Ba(OH)2等
可溶性碱:NaOH、KOH、Ba(OH)2等
难溶性碱:Mg(OH)2、Cu(OH)2等
弱碱:NH3·H2O等
按溶解性
按碱性强弱
盐的分类
按组成
盐
按溶解性
正盐:BaSO4、KNO3、NH4Cl等
碱式盐:Cu2(OH)2CO3等
难溶性盐:CaCO3、AgCl等
按酸根离子中是否含有氧元素
酸式盐:NaHCO3、KHSO4等
含氧酸盐:Na2SO4、KNO3等
无氧酸盐:NaCl、ZnS等
可溶性盐:Na2SO4、KNO3等
下列盐:①Na2CO3 ②NH4HCO3 ③BaSO4 ④NaH2PO3 ⑤Cu(OH)2CO3 ⑥NaHS ⑦Mg(OH)Cl
属于正盐的有 ,
酸式盐的有 ,
碱式盐的有 。
① ③
② ④ ⑥
⑤ ⑦
氧化物
酸性氧化物
碱性氧化物
两性氧化物
CO2、SiO2、SO3、Mn2O7 等
CaO、CuO、K2O 等
Al2O3、ZnO 等
依据组成元素
非金属氧化物
金属氧化物
依据性质
氧化物的分类
CO、NO 等
成盐氧化物
特殊氧化物
NO2、Na2O2、Fe3O4等
不成盐氧化物
Al2O3 + 2NaOH = 2NaAlO2 + H2O
Al2O3 + 6HCl =2 AlCl3 + 3H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
2Na2O2+4HCl=4NaCl+2H2O+O2↑
(偏铝酸钠)
自主完成导纲第2页的思考题。
对议:
互检导纲第2页的思考题。
1.所有的酸性氧化物都能溶于水,与水化合成酸吗?
不能,如:SiO2难溶于水。
不能,如:CuO难溶于水。
2.所有的碱性氧化物都能溶于水,与水化合成碱吗?
3.碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物吗?
4.酸性氧化物一定是非金属氧化物,非金属氧化物一定是酸性氧化物吗?
碱性氧化物
金属氧化物
一定
不一定,如Mn2O7
酸性氧化物
非金属氧化物
不一定,如Mn2O7
不一定,如CO
一定 三 不 定
小 结:
1、同素异形体
2、分类法
3、常见无机化合物的分类
同学们再见!
