1.3.1氧化还原反应ppt(共21张PPT)
文档属性
| 名称 | 1.3.1氧化还原反应ppt(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 507.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-28 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
第三节 氧化还原反应
第一课时
氧化还原反应
你知道为什么食物会腐烂、铁会 生锈吗?
思考与交流
因为都发生了氧化反应。
1.了解氧化还原反应的特征。
2.了解氧化还原反应的实质。(重点)
3.学会电子转移的表示方法----双线桥表示法。
4.了解氧化还原反应与四种基本类型的关系。
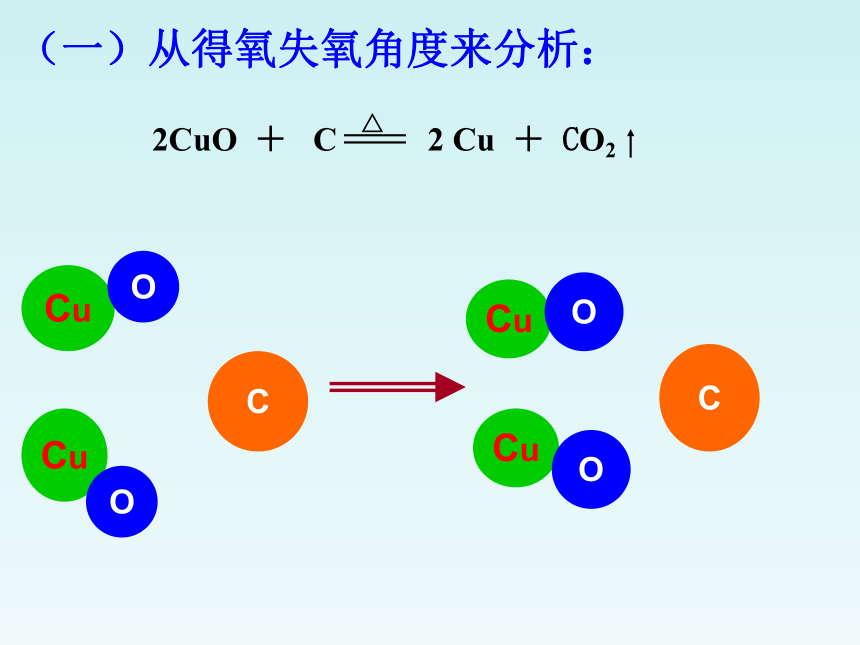
(一)从得氧失氧角度来分析:
2CuO + C 2 Cu + CO2
Cu
C
Cu
O
C
Cu
O
Cu
O
O
△
得到氧,被氧化(氧化反应)
2 CuO + C 2 Cu + CO2
失去氧,被还原(还原反应)
氧化反应:
还原反应:
物质得到氧的反应,如炭得到氧的反应。
物质失去氧的反应,如氧化铜失去氧的反应。
(一)从得氧失氧角度来分析:
△
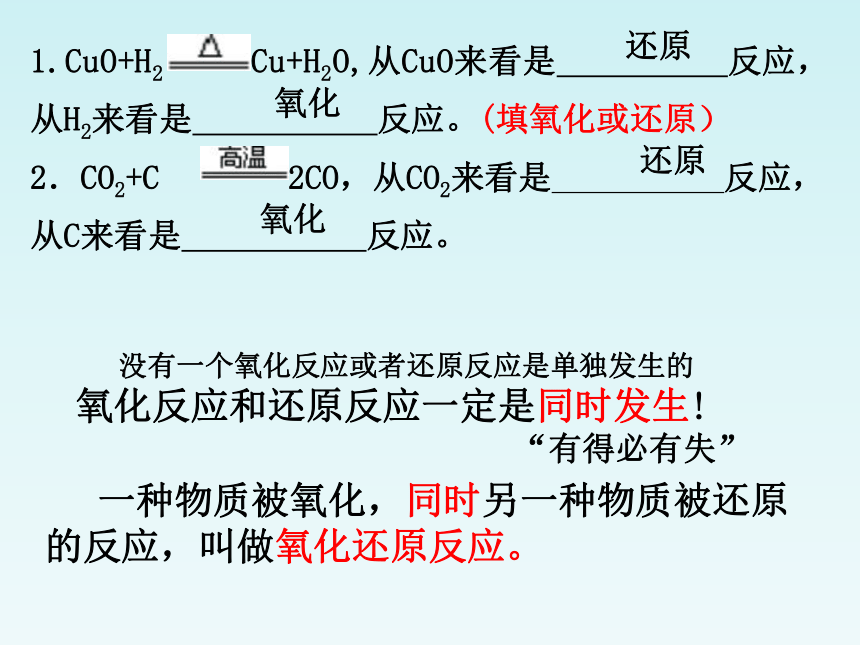
1.CuO+H2 Cu+H2O,从CuO来看是 反应,从H2来看是 反应。(填氧化或还原)
2.CO2+C 2CO,从CO2来看是 反应,从C来看是 反应。
还原
氧化
还原
氧化
没有一个氧化反应或者还原反应是单独发生的
氧化反应和还原反应一定是同时发生!
“有得必有失”
一种物质被氧化,同时另一种物质被还原
的反应,叫做氧化还原反应。
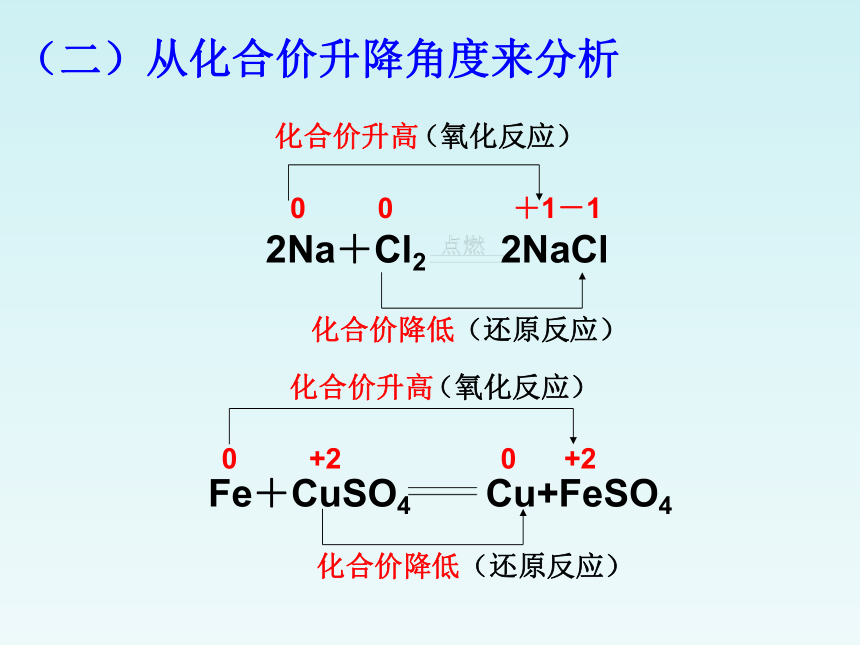
(二)从化合价升降角度来分析
2Na+Cl2 2NaCl
0 0 +1-1
化合价升高
(氧化反应)
化合价降低
(还原反应)
0 +2 0 +2
化合价升高
(氧化反应)
化合价降低
(还原反应)
Fe+CuSO4 Cu+FeSO4
氧化还原反应的特征:反应前后元素化合价发生变化(也是判断依据)。
[定义]有元素化合价升降的化学反应称为氧化还原反应
(二)从化合价升降角度来分析
1、Zn+H2SO4 ZnSO4+H2
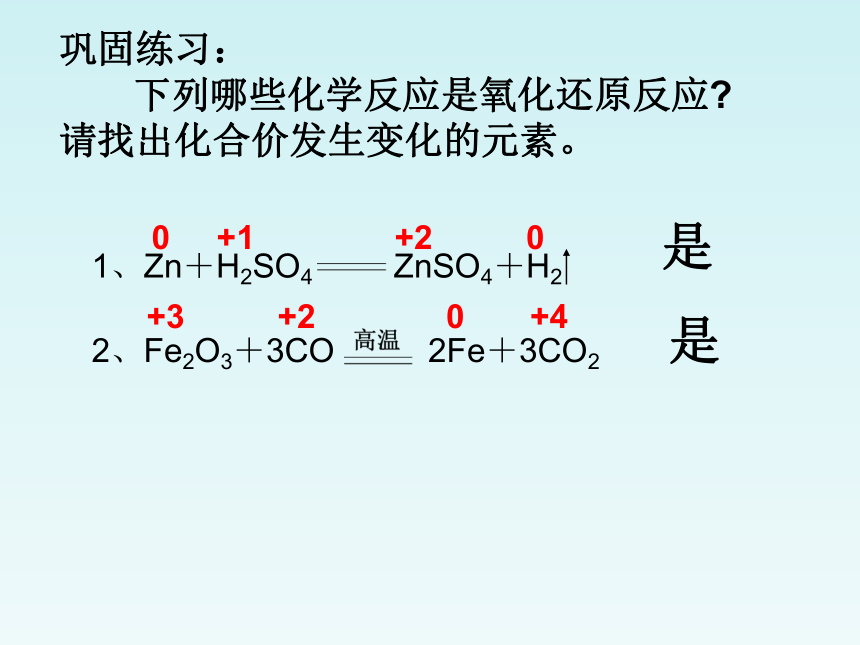
巩固练习:
下列哪些化学反应是氧化还原反应
请找出化合价发生变化的元素。
2、Fe2O3+3CO 2Fe+3CO2
0 +1 +2 0
+3 +2 0 +4
是
是
元素化合价的升降是什么原因引起的?
如何在下面两个反应中表现出来?
例:2Na+Cl2 2NaCl
H2 +Cl2 2HCl
(三)氧化还原反应的实质是什么
思考与交流:
2Na+Cl2 = 2NaCl
Na
Cl
e-
Na+
Cl
-
Na+
Cl-
化合价升降的原因:
电子的得失
点燃
H2+Cl2 = 2HCl
Cl
H
H
Cl
化合价升降的原因:
电子的偏移
氧化还原反应的实质定义:
有电子转移(得失或偏移)的化学反应都是氧化还原反应。
点燃
电子
电子
被氧化
氧化反应
失去电子,化合价升高
被还原
还原反应
得到电子,化合价降低
?
如何形象表示电子转移与化合价的升降情况
【口诀】“升失氧氧,降得还还”
小结 氧化还原反应
◆从得氧失氧角度分析:
一种物质得到氧被氧化,同时另一种物质失去氧被还原的化学反应是氧化还原反应。
说明:仅局限于得氧失氧的反应。
◆从化合价升降角度分析:
有元素化合价升降的化学反应是氧化还原反应。
说明:元素化合价升降是氧化还原反应的表观特征,
可作为氧化还原反应的 判断依据。
◆从电子转移角度分析:
有电子转移(得失或偏移)的化学反应是氧化还原反应。
说明:氧化还原反应的实质是电子转移。
巩固
练习
氧化反应中,转移的电子数目与化合价升降有什么关系?
思考与交流
电子转移的表示方法----“双线桥”法
步骤:
1.标出变价元素的化合价
2.用双箭号表示,箭头从反应物指向生成物的同一种
元素
2Na+ Cl2 = 2NaCl
0
0
+1
-1
2Na+ Cl2 = 2NaCl
0
0
+1
-1
3.标出“失去”、“得到”的电子总数
注意:失电子总数=得电子总数
失去 e-,
得到 e-
2Na+ Cl2 = 2NaCl
0
0
+1
-1
升 失 氧
降 得 还
a×be-
b表示1个原子得失电子数
a表示原子个数
2×
2×
(1)硫在氧气中燃烧。
(2)铁丝在硫酸铜溶液中反应。
写出下列反应的化学反应方程式,是否属于氧化还原反应,若是,请用双线桥法标出电子转移。
S+O2=== SO2
0
0
+4
-2
失去4e-
得到2×2e-
Fe+CuSO4=== FeSO4+Cu
0
0
+2
+2
得到2e-
失去2e-
2Mg+O2===2MgO
点燃
CaO+H2O=Ca(OH)2
2H2O===2H2↑+O2↑
通电
Cu2(OH)2CO3==2CuO+H2O+CO2↑
Fe+H2SO4=FeSO4+H2 ↑
Fe+CuSO4=Cu+FeSO4
HCl+NaOH=NaCl+H2O
BaCl2+K2SO4=BaSO4↓+2KCl
√
√
√
√
置换反应:
分解反应:
化合反应:
复分解反应
例3、判断下列哪些是氧化还原反应?属于哪种基本反应类型?
探究:氧化还原反应与四种基本类型反应有什么联系 ?
置换反应
复分解反应
化合反应
分解反应
氧化还原反应
非氧化还原反应
化 学 反 应
有单质参加的化合反应
有单质生成的分解反应
思考:请同学们讨论以下说法是否正确?
(1)有单质参加的化合反应和有单质生成的分解反应一定是氧化还原反应。
(2)有单质参加或生成的反应一定是氧化还原反应。
同素异形体之间的转化不是氧化还原反应。
√
×
第三节 氧化还原反应
第一课时
氧化还原反应
你知道为什么食物会腐烂、铁会 生锈吗?
思考与交流
因为都发生了氧化反应。
1.了解氧化还原反应的特征。
2.了解氧化还原反应的实质。(重点)
3.学会电子转移的表示方法----双线桥表示法。
4.了解氧化还原反应与四种基本类型的关系。
(一)从得氧失氧角度来分析:
2CuO + C 2 Cu + CO2
Cu
C
Cu
O
C
Cu
O
Cu
O
O
△
得到氧,被氧化(氧化反应)
2 CuO + C 2 Cu + CO2
失去氧,被还原(还原反应)
氧化反应:
还原反应:
物质得到氧的反应,如炭得到氧的反应。
物质失去氧的反应,如氧化铜失去氧的反应。
(一)从得氧失氧角度来分析:
△
1.CuO+H2 Cu+H2O,从CuO来看是 反应,从H2来看是 反应。(填氧化或还原)
2.CO2+C 2CO,从CO2来看是 反应,从C来看是 反应。
还原
氧化
还原
氧化
没有一个氧化反应或者还原反应是单独发生的
氧化反应和还原反应一定是同时发生!
“有得必有失”
一种物质被氧化,同时另一种物质被还原
的反应,叫做氧化还原反应。
(二)从化合价升降角度来分析
2Na+Cl2 2NaCl
0 0 +1-1
化合价升高
(氧化反应)
化合价降低
(还原反应)
0 +2 0 +2
化合价升高
(氧化反应)
化合价降低
(还原反应)
Fe+CuSO4 Cu+FeSO4
氧化还原反应的特征:反应前后元素化合价发生变化(也是判断依据)。
[定义]有元素化合价升降的化学反应称为氧化还原反应
(二)从化合价升降角度来分析
1、Zn+H2SO4 ZnSO4+H2
巩固练习:
下列哪些化学反应是氧化还原反应
请找出化合价发生变化的元素。
2、Fe2O3+3CO 2Fe+3CO2
0 +1 +2 0
+3 +2 0 +4
是
是
元素化合价的升降是什么原因引起的?
如何在下面两个反应中表现出来?
例:2Na+Cl2 2NaCl
H2 +Cl2 2HCl
(三)氧化还原反应的实质是什么
思考与交流:
2Na+Cl2 = 2NaCl
Na
Cl
e-
Na+
Cl
-
Na+
Cl-
化合价升降的原因:
电子的得失
点燃
H2+Cl2 = 2HCl
Cl
H
H
Cl
化合价升降的原因:
电子的偏移
氧化还原反应的实质定义:
有电子转移(得失或偏移)的化学反应都是氧化还原反应。
点燃
电子
电子
被氧化
氧化反应
失去电子,化合价升高
被还原
还原反应
得到电子,化合价降低
?
如何形象表示电子转移与化合价的升降情况
【口诀】“升失氧氧,降得还还”
小结 氧化还原反应
◆从得氧失氧角度分析:
一种物质得到氧被氧化,同时另一种物质失去氧被还原的化学反应是氧化还原反应。
说明:仅局限于得氧失氧的反应。
◆从化合价升降角度分析:
有元素化合价升降的化学反应是氧化还原反应。
说明:元素化合价升降是氧化还原反应的表观特征,
可作为氧化还原反应的 判断依据。
◆从电子转移角度分析:
有电子转移(得失或偏移)的化学反应是氧化还原反应。
说明:氧化还原反应的实质是电子转移。
巩固
练习
氧化反应中,转移的电子数目与化合价升降有什么关系?
思考与交流
电子转移的表示方法----“双线桥”法
步骤:
1.标出变价元素的化合价
2.用双箭号表示,箭头从反应物指向生成物的同一种
元素
2Na+ Cl2 = 2NaCl
0
0
+1
-1
2Na+ Cl2 = 2NaCl
0
0
+1
-1
3.标出“失去”、“得到”的电子总数
注意:失电子总数=得电子总数
失去 e-,
得到 e-
2Na+ Cl2 = 2NaCl
0
0
+1
-1
升 失 氧
降 得 还
a×be-
b表示1个原子得失电子数
a表示原子个数
2×
2×
(1)硫在氧气中燃烧。
(2)铁丝在硫酸铜溶液中反应。
写出下列反应的化学反应方程式,是否属于氧化还原反应,若是,请用双线桥法标出电子转移。
S+O2=== SO2
0
0
+4
-2
失去4e-
得到2×2e-
Fe+CuSO4=== FeSO4+Cu
0
0
+2
+2
得到2e-
失去2e-
2Mg+O2===2MgO
点燃
CaO+H2O=Ca(OH)2
2H2O===2H2↑+O2↑
通电
Cu2(OH)2CO3==2CuO+H2O+CO2↑
Fe+H2SO4=FeSO4+H2 ↑
Fe+CuSO4=Cu+FeSO4
HCl+NaOH=NaCl+H2O
BaCl2+K2SO4=BaSO4↓+2KCl
√
√
√
√
置换反应:
分解反应:
化合反应:
复分解反应
例3、判断下列哪些是氧化还原反应?属于哪种基本反应类型?
探究:氧化还原反应与四种基本类型反应有什么联系 ?
置换反应
复分解反应
化合反应
分解反应
氧化还原反应
非氧化还原反应
化 学 反 应
有单质参加的化合反应
有单质生成的分解反应
思考:请同学们讨论以下说法是否正确?
(1)有单质参加的化合反应和有单质生成的分解反应一定是氧化还原反应。
(2)有单质参加或生成的反应一定是氧化还原反应。
同素异形体之间的转化不是氧化还原反应。
√
×
