人教版九年级化学 第十单元 实验活动6 酸、碱的化学性质课件(共18张PPT)
文档属性
| 名称 | 人教版九年级化学 第十单元 实验活动6 酸、碱的化学性质课件(共18张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 521.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-27 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
实验活动6 酸、碱的化学性质
第十单元 酸和碱
目录
01
课堂检测
【实验目的】
1. 加深对酸和碱的主要性质的认识。2. 通过实验解释生活中的一些现象。
【实验用品】
试管、药匙、蒸发皿、玻璃棒、酒精灯、铁架台(带铁圈)、坩埚钳、胶头滴管、火柴。
稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。
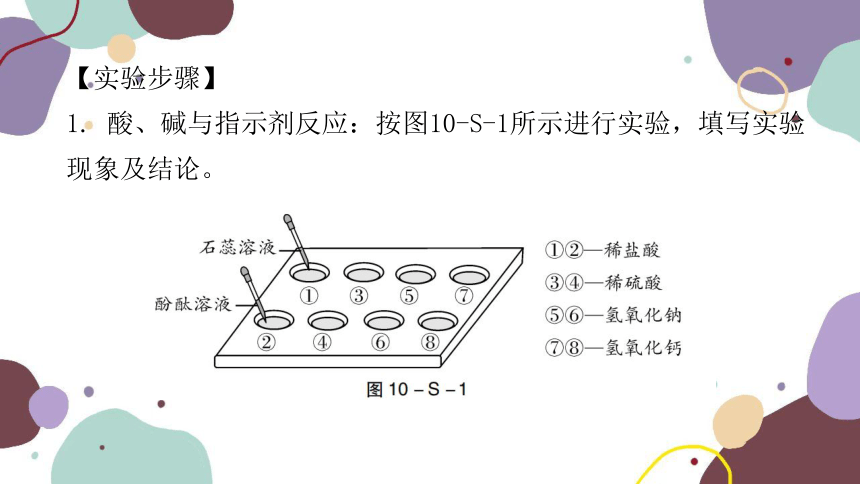
【实验步骤】
1. 酸、碱与指示剂反应:按图10-S-1所示进行实验,填写实验现象及结论。
物质 稀盐酸 稀硫酸 氢氧化钠 氢氧化钙
石蕊溶液 ________色 ________色 ________色 ________色
酚酞溶液 ________色 ________色 ________色 ________色
结论 石蕊溶液遇酸变________色,遇碱变________色;酚酞溶液遇酸________色,遇碱变________色
变红
变红
变蓝
变蓝
不变
不变
变红
变红
红
蓝
不变
红
2. 稀盐酸和生锈的铁钉反应
实验操作 实验现象 验结论及化学方程式
(1)分别取两个生锈的铁钉分别放入两支试管中,然后加入约2 mL稀盐酸,观察现象。当观察到铁钉表面的锈去掉变得光亮时,将其中一支试管的铁钉取出,洗净 铁钉表面的铁锈逐渐消失,溶液由______色变______色 酸能和_____________反应:_______________________
(2)继续观察另一支试管的现象。过一段时间,将铁钉取出,洗净。比较两支铁钉 铁钉表面有____________ 酸能和_____________反应:_______________________
无
黄
金属氧化物
6HCl+Fe2O3 == 2FeCl3+3H2O
气泡冒出
金属
2HCl+Fe == FeCl2+H2↑
实验操作 实验现象 实验结论及化学方程式
(1)往试管中加入约2 mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象 _____________ 碱能和________反应:_________________________________
(2)往(1)中的试管中加入一定量的稀盐酸,观察现象 ______________ 碱能和酸反应:________________________________
3. 硫酸铜溶液与氢氧化钠溶液的反应
生成蓝色沉淀
盐
2NaOH+CuSO4 == Na2SO4+Cu(OH)2↓
蓝色沉淀溶解
Cu(OH)2+2HCl == CuCl2+2H2O
4. 氢氧化钠溶液与稀盐酸的反应
实验操作 实验现象 实验结论及化学方程式
(1)向试管中加入1 mL氢氧化钠溶液,滴入几滴酚酞溶液 溶液变_____色 碱能使酚酞溶液_________
(2)用滴管慢慢滴加稀盐酸,边不断振荡试管,直至溶液颜色恰好变无色为止 溶液由_____色变成_____色 氢氧化钠和盐酸发生反应:_______________________
(3)取上述溶液约1 mL,置于蒸发皿中加热,使液体蒸干,观察现象 出现________ 反应生成了___________
红
变红色
红
无
HCl+NaOH == NaCl+H2O
白色固体
氯化钠
5. 氢氧化钙的性质
实验操作 实验现象 实验结论及化学方程式
(1)向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入1 mL的水,振荡,观察现象;再滴入1~2滴酚酞溶液,观察现象 试管内出现浑浊;液体由________色变成________色 Ca(OH)2________溶于水
(2)继续向其中一支试管中加入约1 mL 的水,振荡;向另一支试管中加入约1 mL的稀盐酸,振荡,观察现象 加水的试管,液体仍然浑浊;加入稀盐酸的试管,溶液变澄清,液体由________色变________色 氢氧化钙和盐酸发生反应:___________________________
无
红
微
红
无
Ca(OH)2+2HCl == CaCl2+2H2O
课堂检测
1. 下列其中一种物质与另三种物质都能发生反应,该物质是( )
A.紫色石蕊溶液
B.单质铁
C.石灰水
D.稀盐酸
D
2.通过实验以及对实验现象的观察、记录和分析,可以发现和验证化学原理。下面是小兰同学在完成酸、碱的性质实验时记录的部分实验现象,其中正确的是( )
A.打开盛有浓盐酸的试剂瓶瓶盖,瓶口有白烟产生
B.向氧化铁中加入足量稀硫酸,红棕色固体溶解,溶液由无色变成浅绿色
C.向氯化铜溶液中加入几滴氢氧化钠溶液,产生蓝色沉淀
D.向氢氧化钙溶液中加入几滴石蕊溶液,溶液由紫色变成红色
C
3. 某同学总结的Ca(OH)2的化学性质如图10-S-2。下列说法错误的是( )
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验
某种温室气体
D.向澄清石灰水中加入石蕊溶液,试液由紫色变为蓝色
A
4. 综合复习时,同学们又来到化学实验室进行实验,加强对酸的化学性质的整体认识。他们将适量的稀盐酸分别滴加到六支试管中进行实验(如图10-S-3所示),请回答下列问题:
(1)上述六支试管中有气泡产生的是_________(填字母),相关反应的化学方程式为_________________________________
________________________________________(只写出一个)。
BD
Mg+2HCl == MgCl2+H2↑(或2HCl+Na2CO3 == 2NaCl+H2O+CO2↑)
(2)能证明“C试管中发生了化学反应”的现象是_______________________________________________。
(3)有一支试管中的物质不与稀盐酸反应,原因是______________________________________________________。
溶液由红色变为无色
在金属活动顺序中铜位于氢后面,所以不与稀盐酸反应
5. 化学兴趣小组的同学在探究碱溶液的化学性质时,进行了图10-S-4所示的实验。
(1)实验A中,推入NaOH溶液后,可观察到的现象是_____________________。
(2)实验B中发生反应的化学方程式为______________________________________________。
(3)实验C说明石灰水呈____________。
瘪气球膨胀
CuSO4+2NaOH == Cu(OH)2↓+Na2SO4
碱性
6. 某化学兴趣小组开展的氢氧化钠性质系列探究活动如图10-S-5所示。据图回答下列问题:
(1)实验甲观察到氢氧化钠表面变________。
(2)实验乙观察到加入紫色石蕊溶液的NaOH溶液变成________色,观察到加入无色酚酞溶液的NaOH溶液变成________色。由此得出:碱溶液能使指示剂变色。
潮湿
蓝
红
(3)实验丙:
①当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有________________________(填化学式)。
②如图10-S-6是氢氧化钠与盐酸反应
的微观模拟示意图:
从微观的角度分析,甲、乙两处应填入
的离子符号分别为________、________。
无
NaCl、HCl
OH-
H+
(4)实验丁观察到的现象是____________________,说明碱溶液能与某些盐反应。该反应的化学方程式为______________________________________________。
(5)实验丙、丁对应的化学反应,属于中和反应的是_______(填“丙”或“丁”)。
(6)实验戊为用软矿泉水瓶所做的对比实验,装___________的软矿泉水瓶变瘪更明显,原因是_________________________
(用化学方程式表示)。
产生蓝色沉淀
CuSO4+2NaOH == Na2SO4+Cu(OH)2↓
丙
NaOH溶液
2NaOH+CO2 == Na2CO3+H2O
实验活动6 酸、碱的化学性质
第十单元 酸和碱
目录
01
课堂检测
【实验目的】
1. 加深对酸和碱的主要性质的认识。2. 通过实验解释生活中的一些现象。
【实验用品】
试管、药匙、蒸发皿、玻璃棒、酒精灯、铁架台(带铁圈)、坩埚钳、胶头滴管、火柴。
稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液、pH试纸、生锈的铁钉。
【实验步骤】
1. 酸、碱与指示剂反应:按图10-S-1所示进行实验,填写实验现象及结论。
物质 稀盐酸 稀硫酸 氢氧化钠 氢氧化钙
石蕊溶液 ________色 ________色 ________色 ________色
酚酞溶液 ________色 ________色 ________色 ________色
结论 石蕊溶液遇酸变________色,遇碱变________色;酚酞溶液遇酸________色,遇碱变________色
变红
变红
变蓝
变蓝
不变
不变
变红
变红
红
蓝
不变
红
2. 稀盐酸和生锈的铁钉反应
实验操作 实验现象 验结论及化学方程式
(1)分别取两个生锈的铁钉分别放入两支试管中,然后加入约2 mL稀盐酸,观察现象。当观察到铁钉表面的锈去掉变得光亮时,将其中一支试管的铁钉取出,洗净 铁钉表面的铁锈逐渐消失,溶液由______色变______色 酸能和_____________反应:_______________________
(2)继续观察另一支试管的现象。过一段时间,将铁钉取出,洗净。比较两支铁钉 铁钉表面有____________ 酸能和_____________反应:_______________________
无
黄
金属氧化物
6HCl+Fe2O3 == 2FeCl3+3H2O
气泡冒出
金属
2HCl+Fe == FeCl2+H2↑
实验操作 实验现象 实验结论及化学方程式
(1)往试管中加入约2 mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象 _____________ 碱能和________反应:_________________________________
(2)往(1)中的试管中加入一定量的稀盐酸,观察现象 ______________ 碱能和酸反应:________________________________
3. 硫酸铜溶液与氢氧化钠溶液的反应
生成蓝色沉淀
盐
2NaOH+CuSO4 == Na2SO4+Cu(OH)2↓
蓝色沉淀溶解
Cu(OH)2+2HCl == CuCl2+2H2O
4. 氢氧化钠溶液与稀盐酸的反应
实验操作 实验现象 实验结论及化学方程式
(1)向试管中加入1 mL氢氧化钠溶液,滴入几滴酚酞溶液 溶液变_____色 碱能使酚酞溶液_________
(2)用滴管慢慢滴加稀盐酸,边不断振荡试管,直至溶液颜色恰好变无色为止 溶液由_____色变成_____色 氢氧化钠和盐酸发生反应:_______________________
(3)取上述溶液约1 mL,置于蒸发皿中加热,使液体蒸干,观察现象 出现________ 反应生成了___________
红
变红色
红
无
HCl+NaOH == NaCl+H2O
白色固体
氯化钠
5. 氢氧化钙的性质
实验操作 实验现象 实验结论及化学方程式
(1)向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入1 mL的水,振荡,观察现象;再滴入1~2滴酚酞溶液,观察现象 试管内出现浑浊;液体由________色变成________色 Ca(OH)2________溶于水
(2)继续向其中一支试管中加入约1 mL 的水,振荡;向另一支试管中加入约1 mL的稀盐酸,振荡,观察现象 加水的试管,液体仍然浑浊;加入稀盐酸的试管,溶液变澄清,液体由________色变________色 氢氧化钙和盐酸发生反应:___________________________
无
红
微
红
无
Ca(OH)2+2HCl == CaCl2+2H2O
课堂检测
1. 下列其中一种物质与另三种物质都能发生反应,该物质是( )
A.紫色石蕊溶液
B.单质铁
C.石灰水
D.稀盐酸
D
2.通过实验以及对实验现象的观察、记录和分析,可以发现和验证化学原理。下面是小兰同学在完成酸、碱的性质实验时记录的部分实验现象,其中正确的是( )
A.打开盛有浓盐酸的试剂瓶瓶盖,瓶口有白烟产生
B.向氧化铁中加入足量稀硫酸,红棕色固体溶解,溶液由无色变成浅绿色
C.向氯化铜溶液中加入几滴氢氧化钠溶液,产生蓝色沉淀
D.向氢氧化钙溶液中加入几滴石蕊溶液,溶液由紫色变成红色
C
3. 某同学总结的Ca(OH)2的化学性质如图10-S-2。下列说法错误的是( )
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验
某种温室气体
D.向澄清石灰水中加入石蕊溶液,试液由紫色变为蓝色
A
4. 综合复习时,同学们又来到化学实验室进行实验,加强对酸的化学性质的整体认识。他们将适量的稀盐酸分别滴加到六支试管中进行实验(如图10-S-3所示),请回答下列问题:
(1)上述六支试管中有气泡产生的是_________(填字母),相关反应的化学方程式为_________________________________
________________________________________(只写出一个)。
BD
Mg+2HCl == MgCl2+H2↑(或2HCl+Na2CO3 == 2NaCl+H2O+CO2↑)
(2)能证明“C试管中发生了化学反应”的现象是_______________________________________________。
(3)有一支试管中的物质不与稀盐酸反应,原因是______________________________________________________。
溶液由红色变为无色
在金属活动顺序中铜位于氢后面,所以不与稀盐酸反应
5. 化学兴趣小组的同学在探究碱溶液的化学性质时,进行了图10-S-4所示的实验。
(1)实验A中,推入NaOH溶液后,可观察到的现象是_____________________。
(2)实验B中发生反应的化学方程式为______________________________________________。
(3)实验C说明石灰水呈____________。
瘪气球膨胀
CuSO4+2NaOH == Cu(OH)2↓+Na2SO4
碱性
6. 某化学兴趣小组开展的氢氧化钠性质系列探究活动如图10-S-5所示。据图回答下列问题:
(1)实验甲观察到氢氧化钠表面变________。
(2)实验乙观察到加入紫色石蕊溶液的NaOH溶液变成________色,观察到加入无色酚酞溶液的NaOH溶液变成________色。由此得出:碱溶液能使指示剂变色。
潮湿
蓝
红
(3)实验丙:
①当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有________________________(填化学式)。
②如图10-S-6是氢氧化钠与盐酸反应
的微观模拟示意图:
从微观的角度分析,甲、乙两处应填入
的离子符号分别为________、________。
无
NaCl、HCl
OH-
H+
(4)实验丁观察到的现象是____________________,说明碱溶液能与某些盐反应。该反应的化学方程式为______________________________________________。
(5)实验丙、丁对应的化学反应,属于中和反应的是_______(填“丙”或“丁”)。
(6)实验戊为用软矿泉水瓶所做的对比实验,装___________的软矿泉水瓶变瘪更明显,原因是_________________________
(用化学方程式表示)。
产生蓝色沉淀
CuSO4+2NaOH == Na2SO4+Cu(OH)2↓
丙
NaOH溶液
2NaOH+CO2 == Na2CO3+H2O
同课章节目录
