课题3 溶液的浓度
图片预览







文档简介
课件31张PPT。复习:
1、溶液由_______和________组成
2、溶液的质量=_____质量 + _____质量
(指“溶解在溶液中的溶质质量”没有溶解的 那部分不算)
3、写出下列溶液的溶质和溶剂的化学式 铁与硫酸铜溶液恰好完全反应得到的溶液
铁与过量的硫酸铜溶液完全反应得到的溶液
过量的铁与硫酸铜溶液完全反应得到的溶液
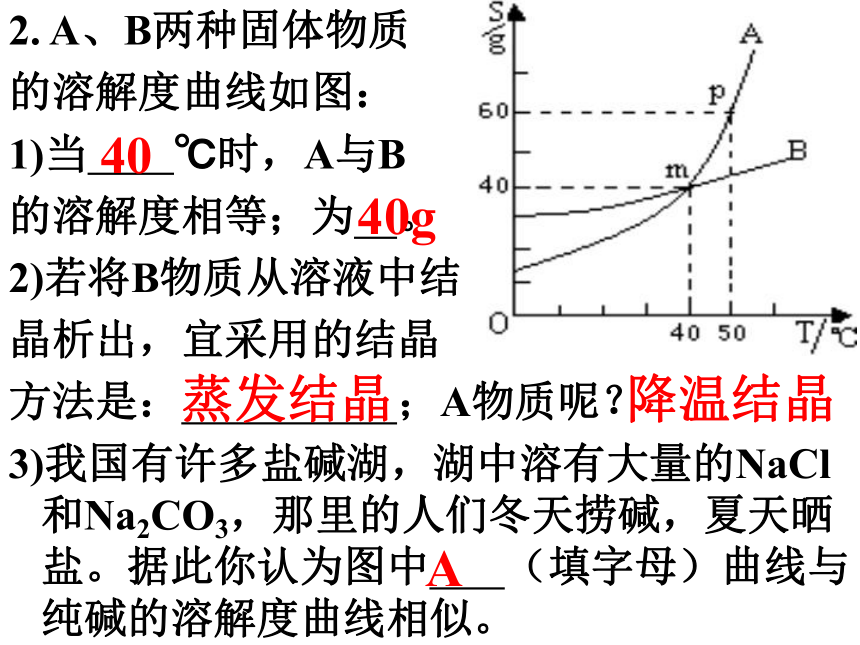
2. A、B两种固体物质
的溶解度曲线如图:
1)当 ℃时,A与B
的溶解度相等;为 。
2)若将B物质从溶液中结
晶析出,宜采用的结晶
方法是: ;A物质呢?
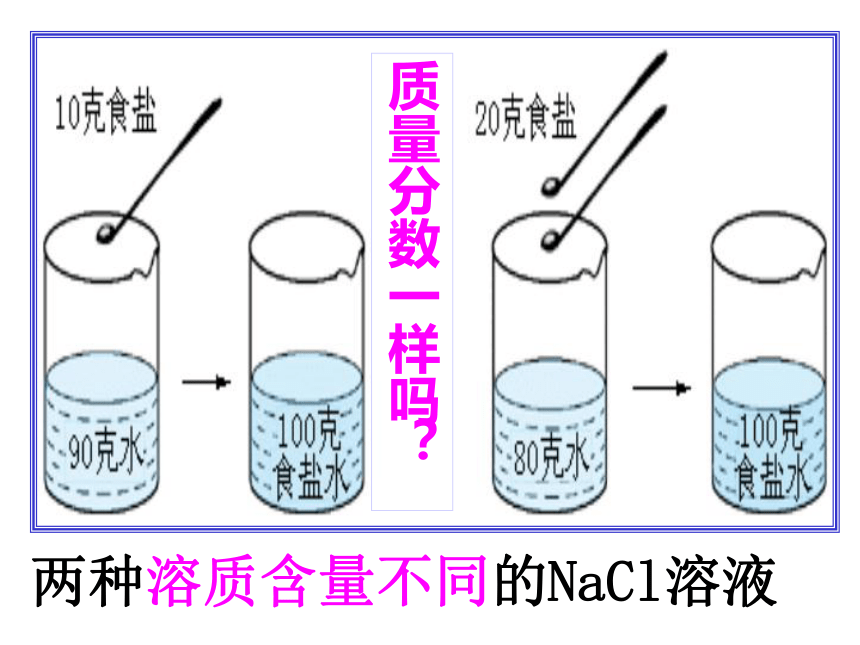
3)我国有许多盐碱湖,湖中溶有大量的NaCl 和Na2CO3,那里的人们冬天捞碱,夏天晒盐。据此你认为图中 (填字母)曲线与纯碱的溶解度曲线相似。4040g蒸发结晶A降温结晶两种溶质含量不同的NaCl溶液质量分数一样吗?
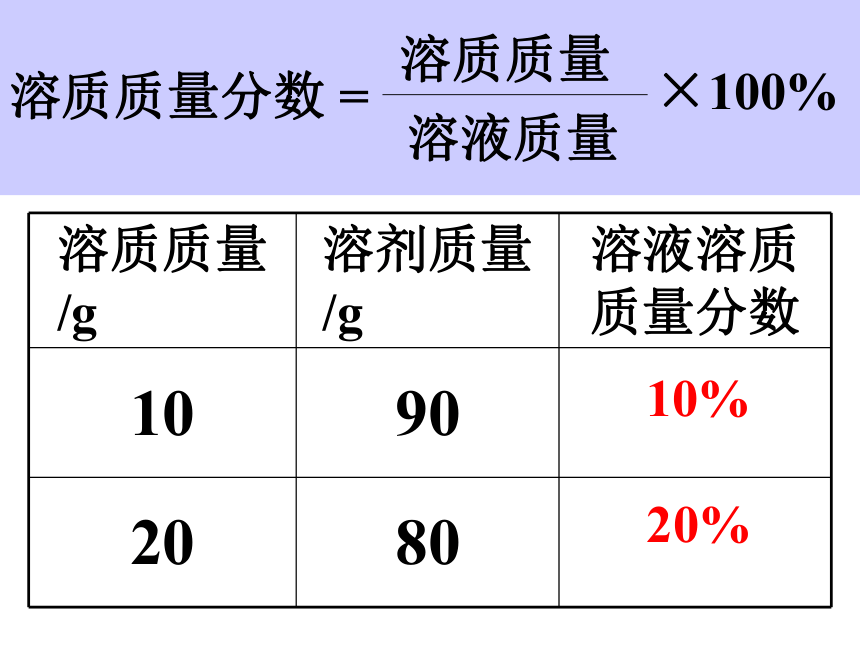
溶质质量分数 =
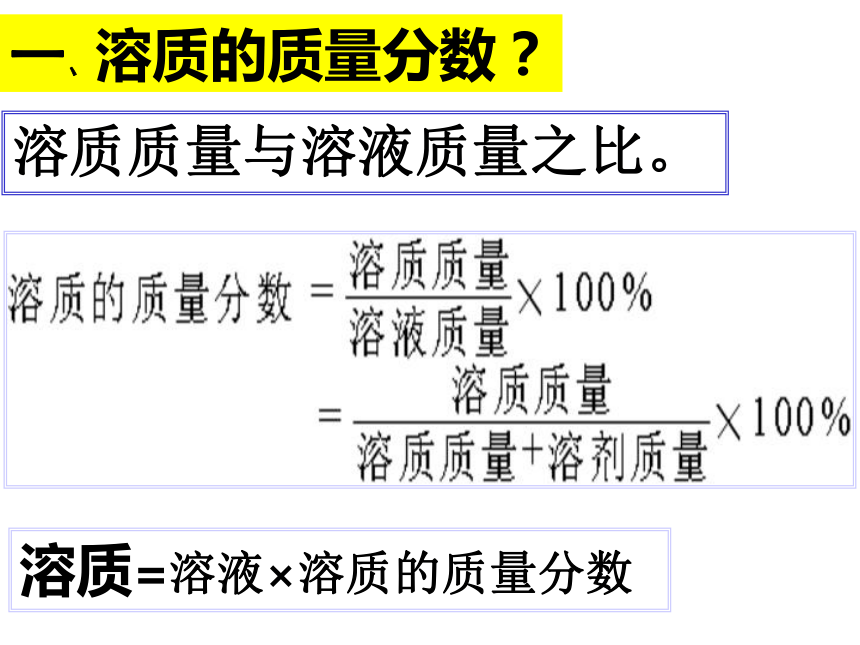
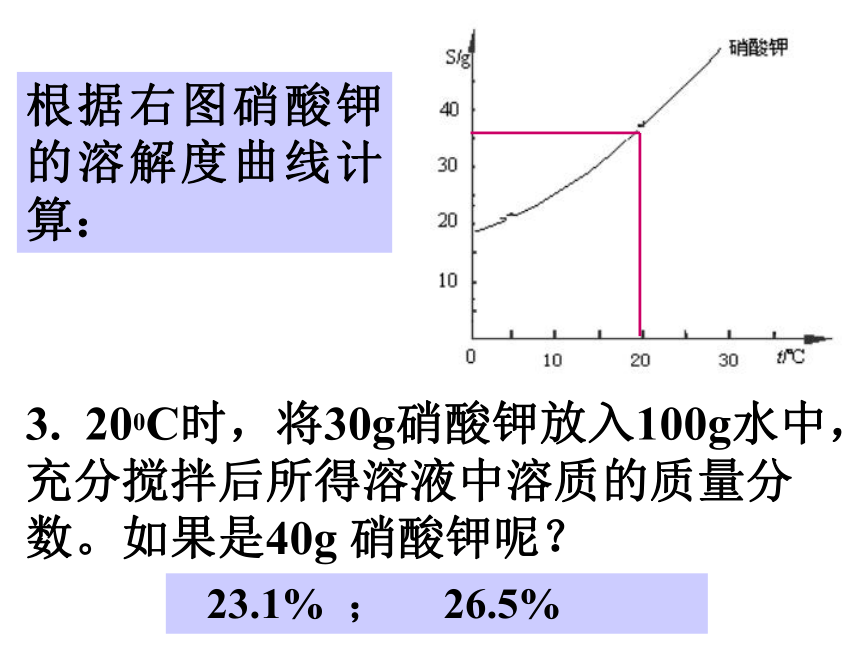
溶质质量与溶液质量之比。一、溶质的质量分数?溶质=溶液×溶质的质量分数1. 将20g硝酸钾加入100g水中,硝酸钾全部溶解,求所得溶液中溶质的质量分数。二、有关溶质质量分数的简单计算 16.7%2. 已知:200C时硝酸钾溶解度为36g,求200C的硝酸钾饱和溶液中溶质的质量分数。 26.5%3. 200C时,将30g硝酸钾放入100g水中,充分搅拌后所得溶液中溶质的质量分数。如果是40g 硝酸钾呢?根据右图硝酸钾的溶解度曲线计算: 23.1% ; 26.5%4.在100克质量分数为10%的食盐溶液中加入5克食盐,全部溶解后得到的溶液中食盐的质量分数为 。三、稀释与浓缩问题:用“变大”、“变小”“不变”填空。
(1) 100克18%的食盐溶液蒸发掉20克水(溶液未饱和),溶质质量______,溶剂质量______,溶液质量______,浓度_______.
(2)往100克18%的食盐溶液中加入20克水,溶质质量_______,溶剂质量______,溶液质量_______,浓度________不变 变小变小变大不变变大变大变小结论:
1.溶液在浓缩和稀释前后, 溶质的质量不变。
2.稀释后溶液的质量=原溶液质量+所加水的质量。
1:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需多少克水? 解:设需要水的质量为x。
50g × 98% = (x+50g) ×20%
x = 195g
答:需要水195kg2.现有100g质量分数为8%的硝酸钾溶液,若要使溶液中溶质的质量分数增大一倍,可采用的方法是
A.加入9.5gKNO3 B.加入8 gKNO3
C.蒸发46g水 D.蒸发42g水 3.某工厂化验室配制5000克20%的盐酸,需要38%的盐酸(密度为1.19g/cm3)多少毫升?溶液的质量 =溶液的体积×溶液的密度 解: 设需要38%的盐酸质量为x
5000g × 20% = x×38%
x = 2631.6g
38%的盐酸的体积= 2631.6g÷1. 19g/cm3
= 2211.4 cm3
= 2211.4mL 要求体积一定先求质量!!!
体积 =质量÷密度 [例1] 配制50克质量分数为6%的氯化钠溶液(水的密度是1g/ml)。计算:需要氯化钠的质量_____克, 水的质量_____克(为_____mL) 称量:用托盘天平称取氯化钠;
用量筒量取水的体积溶解:此过程中,玻璃棒的作用是
____________________________。 四、配制一定质量分数的溶液 3 47 47搅拌,加快溶解速率。四、配制一定质量分数的溶液步骤:计算—称量—溶解—装瓶,贴标签 (写名称,质量分数)仪器:托盘天平、药匙、量筒、 胶头滴管、烧杯、玻璃棒、细口瓶农业常用16%的氯化钠溶液选种。 1) 要配100克该溶液,需氯化钠___克,水___克. 2)所需仪器有______
① 药匙 ②集气瓶 ③烧杯 ④试管 ⑤玻璃棒 ⑥量筒⑦漏斗 ⑧铁架台 ⑨酒精灯 ⑩托盘天平
3)配制顺序是_______
① 向氯化钠固体中加水 ② 称量氯化钠固体 ③ 搅拌加速溶解 ④ 计算氯化钠的质量以及水的体积。1684①③⑤⑥⑩④ ② ①③配制溶液时的误差分析:农业上,常用16%的氯化钠溶液来选种。 如果配制的氯化钠溶液经检测溶质的质量分数小于16%,分析造成此误差的可能原因:溶质取少了:1. 称量后纸片上剩少量溶质溶剂取多了:2. 量取时仰视读数
3. 配制溶液的烧杯内壁有水如果配制的16%氯化钠溶液经检测溶质的质量分数大于16%,造成此误差的可能原因是?溶质多了:1、砝码生锈溶剂少了:2、量取时俯视读数
3、加水溶解时有水倒在烧杯外例1.配制10%的氯化钠溶液时,不会引起溶液中氯化钠的质量分数偏小的是 ( )
A、用量筒量取水时仰视读数 B、配制溶液的烧杯用少量蒸馏润洗 C、氯化钠晶体不纯
D、转移已配好的溶液时,有少量溶液溅出例2.右图是A、B、C三种物质的溶解度曲线。根据图回答问题:
(1)P点表示的意义是________
(2) t1℃时,A、B、C
的溶解度由小到大的
顺序是__________。
(3) t3℃时,A的饱和溶液中溶质的质量分数是___________
(4) t3℃,向50g水中加入50gA,所得溶液中溶质的质量分数是___________t2℃ AC的溶解度相等A74X=1000.1gX = 0.074g石灰水的质量分数=0.074g/100g × 100 % =0.074%答:石灰水的质量分数为0.074%[例题4] 100g稀盐酸溶液恰好与10克碳酸钙完全反应。
(1)反应的化学方程式为
_________________________。
(2)反应后的溶液中,溶质是_____,
溶剂是_________
(3)这种盐酸溶液的质量分数是多少?
(4)生成的二氧化碳多少克?体积是
多少?(ρCO2= 1.997g/L)。
(5)生成溶液溶质的质量分数为多少?CaCl2H2O小结:
1. 2. m溶液=m溶质+m溶剂3. m=ρV4. m稀溶液=m浓溶液+m水5. m浓溶液×ω浓=m稀溶液×ω稀实验结论:1.溶质的质量分数越大,浓度越大,
即溶液越浓。2. “浓”和“稀”由溶质的质量和溶剂的质量共同决定。公 式 变 形溶液质量= ?
溶剂质量= ? 练习1. 实验室现有98%的浓硫酸,但实验需要用稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸,需要水多少克? 2.要配制500mL 20%的硫酸溶液需要98%的硫酸多少mL?(98%的硫酸的密度是1.84g/mL,20%的硫酸的密度是1.22g/mL)实验步骤:计算:计算需要溶质和溶剂的质量
(或体积)称量:用天平称取固体的质量;
用量筒量取液体的体积溶解:在烧杯中溶解溶质装瓶,贴标签:写名称,质量分数2、实验室配制50克5%的硝酸钾溶液。现有①托盘天平② 量筒(10 mL 50 mL 100 mL ) ③药匙,根据要求填空。
1)完成本实验还需要的主要玻璃仪器是:
2)具体操作步骤可概括为:
3)本实验需要硝酸钾 克,需要水 mL 取水应选用 的量筒。量水读数时,眼睛要与
的最低处保持水平,如果俯视读数,则配制的溶液中溶质质量分数(填大于,小于或等于) 5%。*要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是(? )
A.游码没有回到零位就开始称量
B.只在称量食盐的托盘垫上了干净的纸
C.所用烧杯不干燥,有少量水
D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中三、稀释与浓缩问题:用“溶质”、“溶剂” 填空。
(1)往100克18%的食盐溶液中加入20克水,质量发生变化的是________,没有变化的是___________浓度变
(2)100克18%的食盐溶液蒸发掉20克水,质量发生变化的是__________,没有变化的是___________浓度变
溶剂溶质溶剂溶质小大
1、溶液由_______和________组成
2、溶液的质量=_____质量 + _____质量
(指“溶解在溶液中的溶质质量”没有溶解的 那部分不算)
3、写出下列溶液的溶质和溶剂的化学式 铁与硫酸铜溶液恰好完全反应得到的溶液
铁与过量的硫酸铜溶液完全反应得到的溶液
过量的铁与硫酸铜溶液完全反应得到的溶液
2. A、B两种固体物质
的溶解度曲线如图:
1)当 ℃时,A与B
的溶解度相等;为 。
2)若将B物质从溶液中结
晶析出,宜采用的结晶
方法是: ;A物质呢?
3)我国有许多盐碱湖,湖中溶有大量的NaCl 和Na2CO3,那里的人们冬天捞碱,夏天晒盐。据此你认为图中 (填字母)曲线与纯碱的溶解度曲线相似。4040g蒸发结晶A降温结晶两种溶质含量不同的NaCl溶液质量分数一样吗?
溶质质量分数 =
溶质质量与溶液质量之比。一、溶质的质量分数?溶质=溶液×溶质的质量分数1. 将20g硝酸钾加入100g水中,硝酸钾全部溶解,求所得溶液中溶质的质量分数。二、有关溶质质量分数的简单计算 16.7%2. 已知:200C时硝酸钾溶解度为36g,求200C的硝酸钾饱和溶液中溶质的质量分数。 26.5%3. 200C时,将30g硝酸钾放入100g水中,充分搅拌后所得溶液中溶质的质量分数。如果是40g 硝酸钾呢?根据右图硝酸钾的溶解度曲线计算: 23.1% ; 26.5%4.在100克质量分数为10%的食盐溶液中加入5克食盐,全部溶解后得到的溶液中食盐的质量分数为 。三、稀释与浓缩问题:用“变大”、“变小”“不变”填空。
(1) 100克18%的食盐溶液蒸发掉20克水(溶液未饱和),溶质质量______,溶剂质量______,溶液质量______,浓度_______.
(2)往100克18%的食盐溶液中加入20克水,溶质质量_______,溶剂质量______,溶液质量_______,浓度________不变 变小变小变大不变变大变大变小结论:
1.溶液在浓缩和稀释前后, 溶质的质量不变。
2.稀释后溶液的质量=原溶液质量+所加水的质量。
1:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需多少克水? 解:设需要水的质量为x。
50g × 98% = (x+50g) ×20%
x = 195g
答:需要水195kg2.现有100g质量分数为8%的硝酸钾溶液,若要使溶液中溶质的质量分数增大一倍,可采用的方法是
A.加入9.5gKNO3 B.加入8 gKNO3
C.蒸发46g水 D.蒸发42g水 3.某工厂化验室配制5000克20%的盐酸,需要38%的盐酸(密度为1.19g/cm3)多少毫升?溶液的质量 =溶液的体积×溶液的密度 解: 设需要38%的盐酸质量为x
5000g × 20% = x×38%
x = 2631.6g
38%的盐酸的体积= 2631.6g÷1. 19g/cm3
= 2211.4 cm3
= 2211.4mL 要求体积一定先求质量!!!
体积 =质量÷密度 [例1] 配制50克质量分数为6%的氯化钠溶液(水的密度是1g/ml)。计算:需要氯化钠的质量_____克, 水的质量_____克(为_____mL) 称量:用托盘天平称取氯化钠;
用量筒量取水的体积溶解:此过程中,玻璃棒的作用是
____________________________。 四、配制一定质量分数的溶液 3 47 47搅拌,加快溶解速率。四、配制一定质量分数的溶液步骤:计算—称量—溶解—装瓶,贴标签 (写名称,质量分数)仪器:托盘天平、药匙、量筒、 胶头滴管、烧杯、玻璃棒、细口瓶农业常用16%的氯化钠溶液选种。 1) 要配100克该溶液,需氯化钠___克,水___克. 2)所需仪器有______
① 药匙 ②集气瓶 ③烧杯 ④试管 ⑤玻璃棒 ⑥量筒⑦漏斗 ⑧铁架台 ⑨酒精灯 ⑩托盘天平
3)配制顺序是_______
① 向氯化钠固体中加水 ② 称量氯化钠固体 ③ 搅拌加速溶解 ④ 计算氯化钠的质量以及水的体积。1684①③⑤⑥⑩④ ② ①③配制溶液时的误差分析:农业上,常用16%的氯化钠溶液来选种。 如果配制的氯化钠溶液经检测溶质的质量分数小于16%,分析造成此误差的可能原因:溶质取少了:1. 称量后纸片上剩少量溶质溶剂取多了:2. 量取时仰视读数
3. 配制溶液的烧杯内壁有水如果配制的16%氯化钠溶液经检测溶质的质量分数大于16%,造成此误差的可能原因是?溶质多了:1、砝码生锈溶剂少了:2、量取时俯视读数
3、加水溶解时有水倒在烧杯外例1.配制10%的氯化钠溶液时,不会引起溶液中氯化钠的质量分数偏小的是 ( )
A、用量筒量取水时仰视读数 B、配制溶液的烧杯用少量蒸馏润洗 C、氯化钠晶体不纯
D、转移已配好的溶液时,有少量溶液溅出例2.右图是A、B、C三种物质的溶解度曲线。根据图回答问题:
(1)P点表示的意义是________
(2) t1℃时,A、B、C
的溶解度由小到大的
顺序是__________。
(3) t3℃时,A的饱和溶液中溶质的质量分数是___________
(4) t3℃,向50g水中加入50gA,所得溶液中溶质的质量分数是___________t2℃ AC的溶解度相等A
(1)反应的化学方程式为
_________________________。
(2)反应后的溶液中,溶质是_____,
溶剂是_________
(3)这种盐酸溶液的质量分数是多少?
(4)生成的二氧化碳多少克?体积是
多少?(ρCO2= 1.997g/L)。
(5)生成溶液溶质的质量分数为多少?CaCl2H2O小结:
1. 2. m溶液=m溶质+m溶剂3. m=ρV4. m稀溶液=m浓溶液+m水5. m浓溶液×ω浓=m稀溶液×ω稀实验结论:1.溶质的质量分数越大,浓度越大,
即溶液越浓。2. “浓”和“稀”由溶质的质量和溶剂的质量共同决定。公 式 变 形溶液质量= ?
溶剂质量= ? 练习1. 实验室现有98%的浓硫酸,但实验需要用稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸,需要水多少克? 2.要配制500mL 20%的硫酸溶液需要98%的硫酸多少mL?(98%的硫酸的密度是1.84g/mL,20%的硫酸的密度是1.22g/mL)实验步骤:计算:计算需要溶质和溶剂的质量
(或体积)称量:用天平称取固体的质量;
用量筒量取液体的体积溶解:在烧杯中溶解溶质装瓶,贴标签:写名称,质量分数2、实验室配制50克5%的硝酸钾溶液。现有①托盘天平② 量筒(10 mL 50 mL 100 mL ) ③药匙,根据要求填空。
1)完成本实验还需要的主要玻璃仪器是:
2)具体操作步骤可概括为:
3)本实验需要硝酸钾 克,需要水 mL 取水应选用 的量筒。量水读数时,眼睛要与
的最低处保持水平,如果俯视读数,则配制的溶液中溶质质量分数(填大于,小于或等于) 5%。*要配制一定溶质质量分数的食盐溶液,下列操作不影响所配溶液中溶质质量分数的是(? )
A.游码没有回到零位就开始称量
B.只在称量食盐的托盘垫上了干净的纸
C.所用烧杯不干燥,有少量水
D.溶解时先把量筒里的蒸馏水倒入烧杯,后把称好的食盐加入水中三、稀释与浓缩问题:用“溶质”、“溶剂” 填空。
(1)往100克18%的食盐溶液中加入20克水,质量发生变化的是________,没有变化的是___________浓度变
(2)100克18%的食盐溶液蒸发掉20克水,质量发生变化的是__________,没有变化的是___________浓度变
溶剂溶质溶剂溶质小大
同课章节目录
