鲁教版九年级化学下册 9.2 《金属的化学性质》 课件(共40张PPT)
文档属性
| 名称 | 鲁教版九年级化学下册 9.2 《金属的化学性质》 课件(共40张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 498.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-29 00:00:00 | ||
图片预览







文档简介
(共40张PPT)
1、知道铁、铝、铜等金属与氧气的反应
2、认识常见金属与盐酸、硫酸的置换反应,以及与金属化合物溶液的置换反应
3、能用金属活动性顺序对有关的置换反应进行简单的判断
4、能用置换反应和金属活动性顺序解释一些与日常生活有关的化学问题
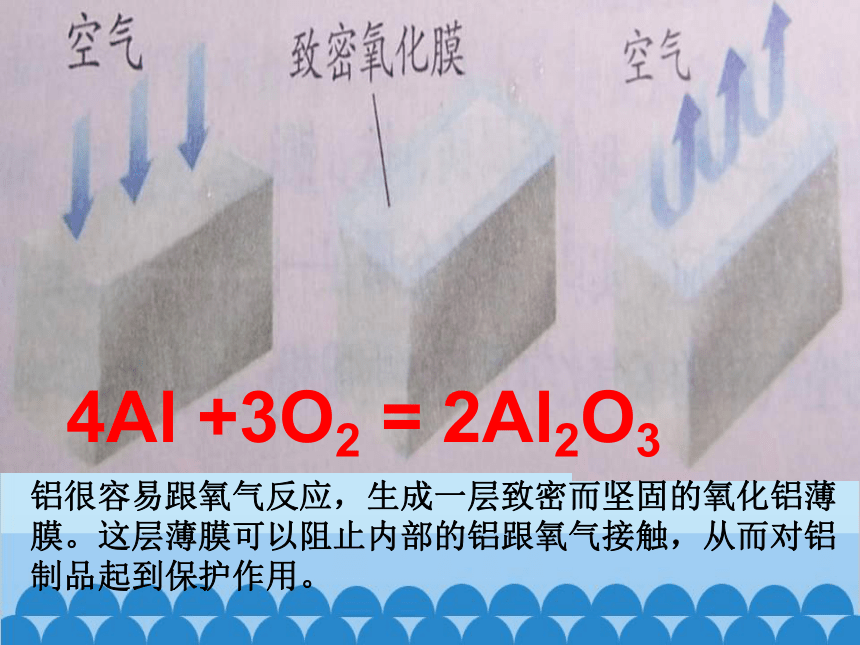
为什么铝制品不易生锈?
铝很容易跟氧气反应,生成一层致密而坚固的氧化铝薄膜。这层薄膜可以阻止内部的铝跟氧气接触,从而对铝制品起到保护作用。
4Al +3O2 = 2Al2O3
实 验 现 象 化学方程式 活泼性比较
铁丝在氧气中燃烧
铝在空气中反应
铜在酒精灯上加热
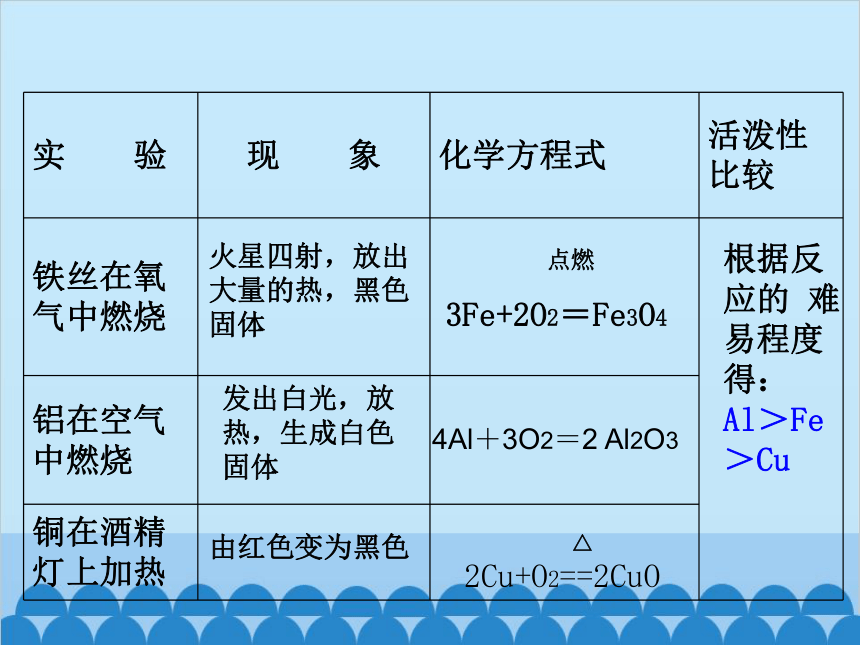
实 验 现 象 化学方程式 活泼性比较
铁丝在氧气中燃烧
铝在空气中燃烧
铜在酒精灯上加热
△
2Cu+O2==2CuO
火星四射,放出大量的热,黑色固体
发出白光,放热,生成白色固体
4Al+3O2=2 Al2O3
由红色变为黑色
点燃
3Fe+2O2=Fe3O4
根据反应的 难易程度得:
Al>Fe>Cu
一、金属与O2的反应
1、大多数金属都能与氧气发生反应
2、判断金属活动性的方法一:
根据金属与氧气反应的难易程度与反应现象的剧烈程度判断
二、金属活动性顺序的探究
探究活动1:
金属与酸的反应
探究活动2
金属与某些化合物的溶液反应
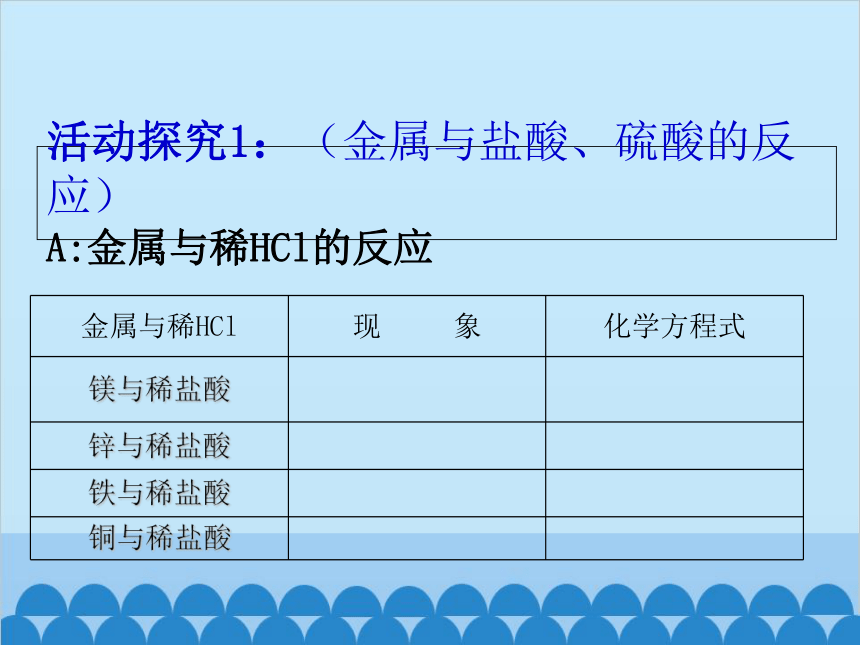
活动探究1:(金属与盐酸、硫酸的反应)
A:金属与稀HCl的反应
金属与稀HCl 现 象 化学方程式
镁与稀盐酸
锌与稀盐酸
铁与稀盐酸
铜与稀盐酸
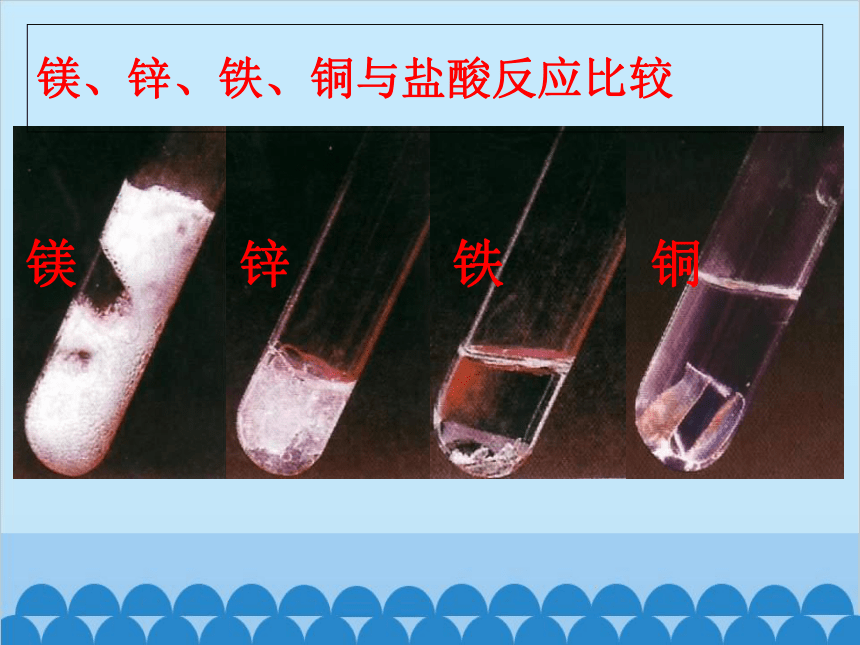
镁 锌 铁 铜
镁、锌、铁、铜与盐酸反应比较
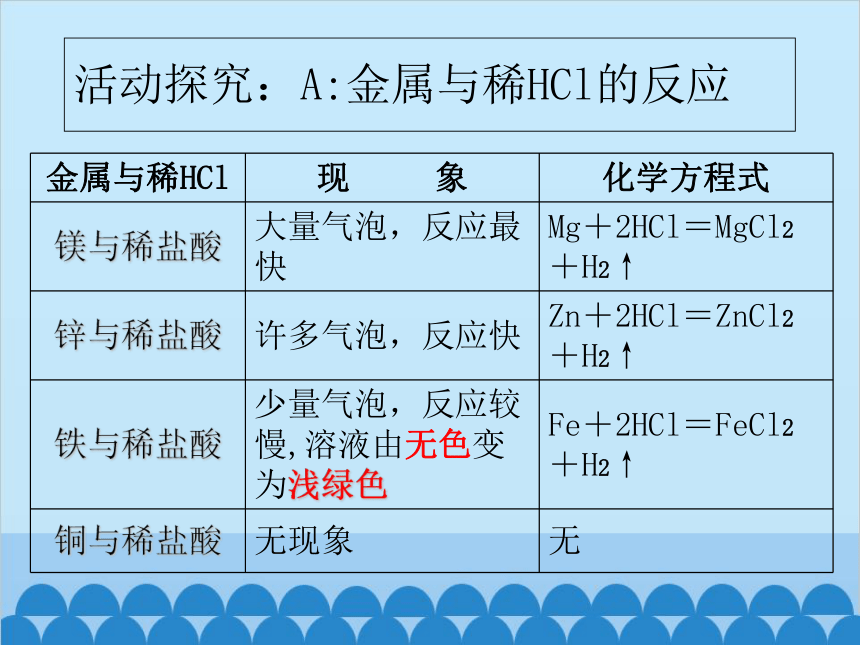
活动探究:A:金属与稀HCl的反应
金属与稀HCl 现 象 化学方程式
镁与稀盐酸 大量气泡,反应最快 Mg+2HCl=MgCl2+H2↑
锌与稀盐酸 许多气泡,反应快 Zn+2HCl=ZnCl2+H2↑
铁与稀盐酸 少量气泡,反应较慢,溶液由无色变为浅绿色 Fe+2HCl=FeCl2+H2↑
铜与稀盐酸 无现象 无
讨论:观察此图,你有何看法?
盐酸
God Save me!!
无所谓, 我无所谓…
为什么受伤的总是我!
我得意的笑,又得意的笑…
金属与盐酸的反应
看图回答问题:
1、哪些金属与盐酸反应?
哪些不与盐酸反应?
2、根据是否与酸反应,可把这四种金属分成几类?
3、与酸反应的剧烈程度如何?谁最活泼?
年代
查找资料
商朝司母戊鼎
春秋时期的铁锄和铁削
现代用电解法冶炼铝
分析资料可知:
金属冶炼的早晚与金属活动性的强弱有关。
活动探究:B:金属与稀H2SO4的反应
金属与稀H2SO4 现 象 化学方程式
镁与稀硫酸
锌与稀硫酸
铁与稀硫酸
铜与稀硫酸
活动探究:B:金属与稀H2SO4的反应
金属与稀H2SO4 现 象 化学方程式
镁与稀硫酸 大量气泡,反应最快 Mg+H2SO4=MgSO4+H2↑
锌与稀硫酸 许多气泡,反应快 Zn+H2SO4=ZnSO4+H2↑
铁与稀硫酸 少量气泡,反应较慢,溶液由无色变为浅绿色 Fe+H2SO4=FeSO4+H2↑
铜与稀硫酸 无现象 无
结论:金属的活动性: Mg > Zn > Fe>Cu
1、金属与酸的反应
(1)判断金属活动性的方法二:可根据金属是否与稀盐酸或稀硫酸反应或反应的剧烈程度判断金属的活动性强弱;
(2)大多数金属能与稀盐酸或稀硫酸反应;
分析与思考:
Fe + 2HCl==FeCl2+H2↑
Zn + 2HCl==ZnCl2+H2 ↑
Mg + H2SO4==MgSO4 + H2↑
单质+化合物 → 单质+化合物
置换反应
铁与硫酸铜溶液的反应:(湿法炼铜!)
Fe + CuSO4 == FeSO4 + Cu
现象:铁表面覆盖一层亮红色的金属,溶液由蓝色变为浅绿色。
回 忆
活动探究二:
提出问题:铝、铜、银三种金属的活动性顺序的强弱
实 验 现象 化学方程式
铝丝浸入CuSO4溶液中
铜丝浸入AgNO3溶液中
铜丝浸入Al2(SO4)3溶液中
活动与探究二:金属与金属化合物溶液的反应
实 验 现 象 化学方程式
铝丝浸入CuSO4溶液中
铜丝浸入AgNO3溶液中
铜丝浸入Al2(SO4)3溶液中
铝丝上有红色物质生成,溶液颜色逐渐变淡
2Al+3CuSO4==
3Cu+Al2(SO4)3
铜丝上有银白色物质生成,溶液由无色逐渐变为淡蓝色
Cu+2AgNO3==
2Ag+Cu(NO3)2
没有明显变化
讨 论
1、以上反应类型都属于( )反应。
2、铝、铜、银三种金属的活动性顺序是( )
置换
Al>Cu>Ag
2、金属能与金属化合物的溶液反应
(1)判断金属活动性的方法三:可根据金属能不能把另一种金属从金属化合物的溶液中置换出来,判断金属活动性的强弱。
(2)部分金属能与金属化合物的溶液(盐的溶液)反应;
金属活动顺序
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2、在金属活动性顺序里,位于氢前面的金属能置换出盐酸,稀硫酸中的氢(元素)
3、在金属活动顺序里,位于前面的金属 能把位于后面的金属从它们化合物的溶液中置换出来。
1、大多数的金属能与氧气发生反应,但反应的难易和剧烈程度是不同的。
2、很多金属都能和氧气、稀盐酸、稀硫酸等反应,但反应的难易和剧烈程度不同。
3、置换反应:单质+化合物===新单质+新化合物
4、金属的活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
课堂小结
1.判断下列物质能否发生反应?若能,
写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
解答:可发生反应的:(2)(4)(6)
化学方程式:
(2)Zn + CuSO4 = Cu + ZnSO4
(4)Al +3AgNO3 = Al(NO3)3 + 3Ag
(6)Mg + FeSO4 = MgSO4 +Fe
2、X、Y、Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性顺序是( )
①Z+YSO4==ZSO4+Y ②X+ YSO4==XSO4+Y
③X+ H2SO4== XSO4+ H2 ↑ ④Z+ H2SO4不反应
A、Z>X>Y B、Z>Y>X
C、X>Y>Z D、X>Z>Y
D
D
3、现有X、Y、Z三种金属,若将Z放入X的盐溶液中,Z表面覆盖有X,将Y和Z分别投入稀盐酸中,Y 溶解而Z不溶,则三种金属的活动顺序正确的是( )
A、Y>X>Z B、Y>Z>X
C、X>Y>Z D、X>Z>Y
4、黄金饰品中的假货常常鱼目混珠,社会上有些不法分子时常以黄铜冒充黄金进行诈骗活动。因为黄铜(铜、锌合金)单纯从颜色、外型上看,与黄金极为相似,所以很难区分,现请你设计一个实验方案用化学方法鉴别真假黄金。
B
5、有X、Y、Z三种金属。X、Y、Z分别放入稀盐酸中,X溶解并放出氢气,Y、Z无变化;将Y放入Z的化合物溶液中无变化;Z放入Y的化合物溶液中有Y析出:则X、Y、Z的活动性顺序如何?
6、实验室制氢气常选择锌与稀盐酸、稀硫酸反应,(1)选用的依据是什么?(2)不选铜的理由?(3)猜想:为什么也不选钾、钙、钠?
7、将铁片放入下列溶液中,铁片的质量会增加 的是( )
A、稀H2SO4 B、FeSO4溶液
C、CuSO4溶液 D、稀HCl
C
8、下列物质不能由金属和酸反应直接生成的是 ( )
A ZnCl2 B CuSO4
C FeCl2 D Al2(SO4)3
B
9、将铁片放入下列溶液中,溶液的质量会减少的是( )
A、HCl B、H2SO4
C、Na2 SO4 D、CuSO4
10、为了测定Ag,Zn,Cu,H的化学活动性强弱,某同学利用Zn粉,Cu片,AgNO3溶液和盐酸4种物质,设计了如下实验方案,其中可行的是( )
A、 Zn+HCl Cu+HCl Zn+AgNO3
B、Zn+HCl Cu+ AgNO3 Zn+AgNO3
C、Cu+HCl Zn+AgNO3 Cu+ AgNO3
D、Zn+HCl Cu+HCl Cu+ AgNO3
11、在CuCl2和NaCl的混合溶液中加入过量的Zn粉,充分反应后过滤,留在滤纸上的固体( )
A、只有Zn B、只有Cu
C、有Cu和Na D、有Cu和Zn
12、把足量锌粉分别加入到含下列各组物质的混合溶液中,充分反应后过滤,滤液中只有一种溶质的是( )(双选)
A、MgSO4 CuSO4 B、CuSO4 H2SO4
C、Cu(NO3)2 AgNO3 D、HCl CuSO4
13.生活中很多人用钢丝球刷铝锅,这种方法妥当吗?为什么?
14.可否用铁桶盛放硫酸铜溶液?
15.下列化学变化属于置换反应的有:
(1)CO+Fe2O3→Fe+CO2
(2)C+Fe2O3 → Fe+CO2
(3)H2O2 → H2O+O2
(4)Fe+AgNO3 → Fe(NO3)2+Ag
16.“药金”又称为“愚人金”,实为铜、锌合金(在合金中各种金属仍然保持各自的化学性质不变)。由于“药金”外观与黄金相似,常被不法商贩用来冒充黄金牟取暴利。请你设计实验,证明“药金”戒指是假黄金戒指。
17、 为了测定某铁粉中杂质的含量,取该铁粉样品20克,放到盛有200克稀盐酸的烧杯中,反应后烧杯中物质总质量变成219.4克.求
1、铁粉中纯铁的质量分数.
2、稀盐酸的质量分数.
3、反应后的溶液中溶质的质量分数.
18.小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器。
(1)根据现有的条件,你认为只能测出_____________合金中铜的质量分数。
(2)为了测定该合金的组成,小华称取10 g该合金粉末,在粉末中连续三次加入稀盐酸反应。每加一次盐酸,小华记录所得气体的质量,实验数据如下:
第一次 第二次 第三次
连续加入盐酸的体积(ml) 10 10 1
生成氢气的质量(g) 0.08 0.08 0.04
(3)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g。
(4)求出该合金中铜的质量分数。
1、知道铁、铝、铜等金属与氧气的反应
2、认识常见金属与盐酸、硫酸的置换反应,以及与金属化合物溶液的置换反应
3、能用金属活动性顺序对有关的置换反应进行简单的判断
4、能用置换反应和金属活动性顺序解释一些与日常生活有关的化学问题
为什么铝制品不易生锈?
铝很容易跟氧气反应,生成一层致密而坚固的氧化铝薄膜。这层薄膜可以阻止内部的铝跟氧气接触,从而对铝制品起到保护作用。
4Al +3O2 = 2Al2O3
实 验 现 象 化学方程式 活泼性比较
铁丝在氧气中燃烧
铝在空气中反应
铜在酒精灯上加热
实 验 现 象 化学方程式 活泼性比较
铁丝在氧气中燃烧
铝在空气中燃烧
铜在酒精灯上加热
△
2Cu+O2==2CuO
火星四射,放出大量的热,黑色固体
发出白光,放热,生成白色固体
4Al+3O2=2 Al2O3
由红色变为黑色
点燃
3Fe+2O2=Fe3O4
根据反应的 难易程度得:
Al>Fe>Cu
一、金属与O2的反应
1、大多数金属都能与氧气发生反应
2、判断金属活动性的方法一:
根据金属与氧气反应的难易程度与反应现象的剧烈程度判断
二、金属活动性顺序的探究
探究活动1:
金属与酸的反应
探究活动2
金属与某些化合物的溶液反应
活动探究1:(金属与盐酸、硫酸的反应)
A:金属与稀HCl的反应
金属与稀HCl 现 象 化学方程式
镁与稀盐酸
锌与稀盐酸
铁与稀盐酸
铜与稀盐酸
镁 锌 铁 铜
镁、锌、铁、铜与盐酸反应比较
活动探究:A:金属与稀HCl的反应
金属与稀HCl 现 象 化学方程式
镁与稀盐酸 大量气泡,反应最快 Mg+2HCl=MgCl2+H2↑
锌与稀盐酸 许多气泡,反应快 Zn+2HCl=ZnCl2+H2↑
铁与稀盐酸 少量气泡,反应较慢,溶液由无色变为浅绿色 Fe+2HCl=FeCl2+H2↑
铜与稀盐酸 无现象 无
讨论:观察此图,你有何看法?
盐酸
God Save me!!
无所谓, 我无所谓…
为什么受伤的总是我!
我得意的笑,又得意的笑…
金属与盐酸的反应
看图回答问题:
1、哪些金属与盐酸反应?
哪些不与盐酸反应?
2、根据是否与酸反应,可把这四种金属分成几类?
3、与酸反应的剧烈程度如何?谁最活泼?
年代
查找资料
商朝司母戊鼎
春秋时期的铁锄和铁削
现代用电解法冶炼铝
分析资料可知:
金属冶炼的早晚与金属活动性的强弱有关。
活动探究:B:金属与稀H2SO4的反应
金属与稀H2SO4 现 象 化学方程式
镁与稀硫酸
锌与稀硫酸
铁与稀硫酸
铜与稀硫酸
活动探究:B:金属与稀H2SO4的反应
金属与稀H2SO4 现 象 化学方程式
镁与稀硫酸 大量气泡,反应最快 Mg+H2SO4=MgSO4+H2↑
锌与稀硫酸 许多气泡,反应快 Zn+H2SO4=ZnSO4+H2↑
铁与稀硫酸 少量气泡,反应较慢,溶液由无色变为浅绿色 Fe+H2SO4=FeSO4+H2↑
铜与稀硫酸 无现象 无
结论:金属的活动性: Mg > Zn > Fe>Cu
1、金属与酸的反应
(1)判断金属活动性的方法二:可根据金属是否与稀盐酸或稀硫酸反应或反应的剧烈程度判断金属的活动性强弱;
(2)大多数金属能与稀盐酸或稀硫酸反应;
分析与思考:
Fe + 2HCl==FeCl2+H2↑
Zn + 2HCl==ZnCl2+H2 ↑
Mg + H2SO4==MgSO4 + H2↑
单质+化合物 → 单质+化合物
置换反应
铁与硫酸铜溶液的反应:(湿法炼铜!)
Fe + CuSO4 == FeSO4 + Cu
现象:铁表面覆盖一层亮红色的金属,溶液由蓝色变为浅绿色。
回 忆
活动探究二:
提出问题:铝、铜、银三种金属的活动性顺序的强弱
实 验 现象 化学方程式
铝丝浸入CuSO4溶液中
铜丝浸入AgNO3溶液中
铜丝浸入Al2(SO4)3溶液中
活动与探究二:金属与金属化合物溶液的反应
实 验 现 象 化学方程式
铝丝浸入CuSO4溶液中
铜丝浸入AgNO3溶液中
铜丝浸入Al2(SO4)3溶液中
铝丝上有红色物质生成,溶液颜色逐渐变淡
2Al+3CuSO4==
3Cu+Al2(SO4)3
铜丝上有银白色物质生成,溶液由无色逐渐变为淡蓝色
Cu+2AgNO3==
2Ag+Cu(NO3)2
没有明显变化
讨 论
1、以上反应类型都属于( )反应。
2、铝、铜、银三种金属的活动性顺序是( )
置换
Al>Cu>Ag
2、金属能与金属化合物的溶液反应
(1)判断金属活动性的方法三:可根据金属能不能把另一种金属从金属化合物的溶液中置换出来,判断金属活动性的强弱。
(2)部分金属能与金属化合物的溶液(盐的溶液)反应;
金属活动顺序
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2、在金属活动性顺序里,位于氢前面的金属能置换出盐酸,稀硫酸中的氢(元素)
3、在金属活动顺序里,位于前面的金属 能把位于后面的金属从它们化合物的溶液中置换出来。
1、大多数的金属能与氧气发生反应,但反应的难易和剧烈程度是不同的。
2、很多金属都能和氧气、稀盐酸、稀硫酸等反应,但反应的难易和剧烈程度不同。
3、置换反应:单质+化合物===新单质+新化合物
4、金属的活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
课堂小结
1.判断下列物质能否发生反应?若能,
写出相关化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(5)银与氯化铜溶液 (6)镁与硫酸亚铁溶液
解答:可发生反应的:(2)(4)(6)
化学方程式:
(2)Zn + CuSO4 = Cu + ZnSO4
(4)Al +3AgNO3 = Al(NO3)3 + 3Ag
(6)Mg + FeSO4 = MgSO4 +Fe
2、X、Y、Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性顺序是( )
①Z+YSO4==ZSO4+Y ②X+ YSO4==XSO4+Y
③X+ H2SO4== XSO4+ H2 ↑ ④Z+ H2SO4不反应
A、Z>X>Y B、Z>Y>X
C、X>Y>Z D、X>Z>Y
D
D
3、现有X、Y、Z三种金属,若将Z放入X的盐溶液中,Z表面覆盖有X,将Y和Z分别投入稀盐酸中,Y 溶解而Z不溶,则三种金属的活动顺序正确的是( )
A、Y>X>Z B、Y>Z>X
C、X>Y>Z D、X>Z>Y
4、黄金饰品中的假货常常鱼目混珠,社会上有些不法分子时常以黄铜冒充黄金进行诈骗活动。因为黄铜(铜、锌合金)单纯从颜色、外型上看,与黄金极为相似,所以很难区分,现请你设计一个实验方案用化学方法鉴别真假黄金。
B
5、有X、Y、Z三种金属。X、Y、Z分别放入稀盐酸中,X溶解并放出氢气,Y、Z无变化;将Y放入Z的化合物溶液中无变化;Z放入Y的化合物溶液中有Y析出:则X、Y、Z的活动性顺序如何?
6、实验室制氢气常选择锌与稀盐酸、稀硫酸反应,(1)选用的依据是什么?(2)不选铜的理由?(3)猜想:为什么也不选钾、钙、钠?
7、将铁片放入下列溶液中,铁片的质量会增加 的是( )
A、稀H2SO4 B、FeSO4溶液
C、CuSO4溶液 D、稀HCl
C
8、下列物质不能由金属和酸反应直接生成的是 ( )
A ZnCl2 B CuSO4
C FeCl2 D Al2(SO4)3
B
9、将铁片放入下列溶液中,溶液的质量会减少的是( )
A、HCl B、H2SO4
C、Na2 SO4 D、CuSO4
10、为了测定Ag,Zn,Cu,H的化学活动性强弱,某同学利用Zn粉,Cu片,AgNO3溶液和盐酸4种物质,设计了如下实验方案,其中可行的是( )
A、 Zn+HCl Cu+HCl Zn+AgNO3
B、Zn+HCl Cu+ AgNO3 Zn+AgNO3
C、Cu+HCl Zn+AgNO3 Cu+ AgNO3
D、Zn+HCl Cu+HCl Cu+ AgNO3
11、在CuCl2和NaCl的混合溶液中加入过量的Zn粉,充分反应后过滤,留在滤纸上的固体( )
A、只有Zn B、只有Cu
C、有Cu和Na D、有Cu和Zn
12、把足量锌粉分别加入到含下列各组物质的混合溶液中,充分反应后过滤,滤液中只有一种溶质的是( )(双选)
A、MgSO4 CuSO4 B、CuSO4 H2SO4
C、Cu(NO3)2 AgNO3 D、HCl CuSO4
13.生活中很多人用钢丝球刷铝锅,这种方法妥当吗?为什么?
14.可否用铁桶盛放硫酸铜溶液?
15.下列化学变化属于置换反应的有:
(1)CO+Fe2O3→Fe+CO2
(2)C+Fe2O3 → Fe+CO2
(3)H2O2 → H2O+O2
(4)Fe+AgNO3 → Fe(NO3)2+Ag
16.“药金”又称为“愚人金”,实为铜、锌合金(在合金中各种金属仍然保持各自的化学性质不变)。由于“药金”外观与黄金相似,常被不法商贩用来冒充黄金牟取暴利。请你设计实验,证明“药金”戒指是假黄金戒指。
17、 为了测定某铁粉中杂质的含量,取该铁粉样品20克,放到盛有200克稀盐酸的烧杯中,反应后烧杯中物质总质量变成219.4克.求
1、铁粉中纯铁的质量分数.
2、稀盐酸的质量分数.
3、反应后的溶液中溶质的质量分数.
18.小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器。
(1)根据现有的条件,你认为只能测出_____________合金中铜的质量分数。
(2)为了测定该合金的组成,小华称取10 g该合金粉末,在粉末中连续三次加入稀盐酸反应。每加一次盐酸,小华记录所得气体的质量,实验数据如下:
第一次 第二次 第三次
连续加入盐酸的体积(ml) 10 10 1
生成氢气的质量(g) 0.08 0.08 0.04
(3)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g。
(4)求出该合金中铜的质量分数。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
