【人教版】2013届中考化学考前热点冲刺《第十二讲 质量守恒定律与化学方程式》(单课考点自主梳理+热点反馈+典例真题分析,21ppt)
文档属性
| 名称 | 【人教版】2013届中考化学考前热点冲刺《第十二讲 质量守恒定律与化学方程式》(单课考点自主梳理+热点反馈+典例真题分析,21ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 497.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-05-01 00:00:00 | ||
图片预览








文档简介
课件21张PPT。第十二讲 质量守恒定律与化学方程式第12讲┃ 质量守恒定律与化学方程式 考点41 质量守恒定律的理解与运用 ┃考点自助梳理与热身反馈 ┃反应各质量生成各化学物理质量不能原子重新组合种类数目质量密闭第12讲┃ 质量守恒定律与化学方程式 1.[2011·娄底]在化学反应A+B===C+D中,若12 g A与一定量的B恰好完全反应,生成28 g C和2 g D,则参加反应的B的质量为( )
A.8 g B.18 g C.28 g D.30 g
2.[2011·桂林]在化学反应中一定没有发生变化的是( )
A.原子的种类 B.分子的种类
C.物质的种类 D.分子的数目BA[解析] 根据质量守恒定律可知,参加反应的B的质量为28g+2g-12g=18g。 第12讲┃ 质量守恒定律与化学方程式 3.[2012·重庆] NH4ClO4(高氯酸铵)可用作火箭推进剂,当它发生分解反应时,不能生成的物质是( )
A.CO2 B.Cl2 C.O2 D.N2
A[解析] 化学反应前后元素种类不变,反应物中没有碳元素,所以生成物中不可能出现CO2。第12讲┃ 质量守恒定律与化学方程式 4.[2012·安顺]我国已经立法规定酒驾入刑。“酒精检测仪”可检查司机是否酒后驾车,其反应原理为C2H5OH+4CrO3+6H2SO4===2Cr2(SO4)3+2CO2↑+9X,反应中红色的CrO3转变为绿色的Cr2(SO2)3,其中X的化学式为( )
A.O2 B.H2O C.SO2 D.COB第12讲┃ 质量守恒定律与化学方程式 5.[2012·青岛]某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铝粉在氧气中燃烧生成固体氧化铝。他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生了变化。请填空:
(1)铝粉燃烧生成氧化铝的质量比参加反应铝粉的质量________(填“大”“小”或“不变”)。
(2)你认为这两个反应是否遵循质量守恒定律?______(填“是”或“否”)。
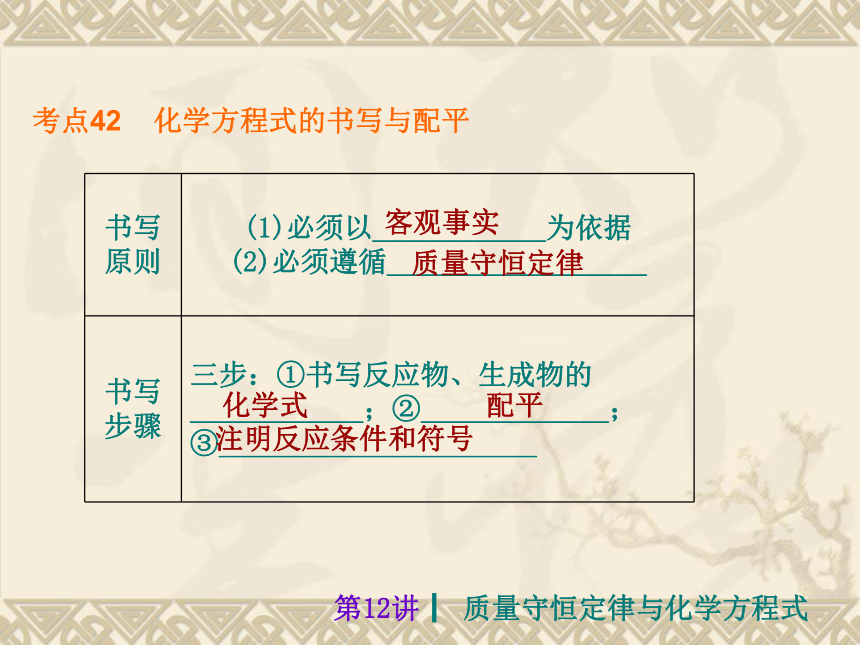
(3)请写出氧化汞受热分解的化学方程式:________________________________。大是第12讲┃ 质量守恒定律与化学方程式 考点42 化学方程式的书写与配平 客观事实 质量守恒定律 化学式配平注明反应条件和符号 第12讲┃ 质量守恒定律与化学方程式 什么物质在什么条件下生成什么物质 多少份质量的什么物质反应生成多少份质量的什么物质第12讲┃ 质量守恒定律与化学方程式 D第12讲┃ 质量守恒定律与化学方程式 2.[2012·桂林]下列化学方程式的表达一定不正确的是( )
A.2Fe+6HCl===2FeCl3+3H2↑
B.BaCl2+CuSO4===BaSO4↓+CuCl2
C.SO3+2NaOH===Na2SO4+H2O
D.Ca(OH)2+Na2CO3===CaCO3↓+2NaOHA[解析] 选项A违背了客观事实,铁与盐酸反应生成氯化亚铁,应改为Fe+2HCl===FeCl2+H2↑。 第12讲┃ 质量守恒定律与化学方程式 3.[2012·天津]写出下列反应的化学方程式。
(1)硫在氧气中燃烧:__________________。
(2)锌片浸入硫酸铜溶液中:____________________________。
(3)过氧化氢溶液中加入少量二氧化锰制取氧气:
______________________。Zn+CuSO4===ZnSO4+Cu 第12讲┃ 质量守恒定律与化学方程式 考点43 根据化学方程式计算 写出并配平反应化学方程式 列出比例式,求解 简明地写出答案 第12讲┃ 质量守恒定律与化学方程式 [注意] 根据化学方程式计算时常见的错误有下列几种:
(1)不认真审题,答非所问;
(2)元素符号或化学式写错;
(3)化学方程式没有配平;
(4)相对分子质量计算有错误;
(5)没有统一单位;
(6)把不纯物质当成纯净物质计算。第12讲┃ 质量守恒定律与化学方程式 12.5 g 第12讲┃ 质量守恒定律与化学方程式 第12讲┃ 质量守恒定律与化学方程式 2.[2012·肇庆]实验室用过量的稀盐酸和大理石制取CO2,取50 g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图12-1所示。
回答下列问题。
(1)从图中看出生成沉淀的最大质
量是______g。
(2)开始加入碳酸钠溶液至10 g时
,还没有沉淀的原因是
__________________________。
(3)计算原滤液中氯化钙的质量。5 图12-1
稀盐酸先与碳酸钠反应 5.55 g 第12讲┃ 质量守恒定律与化学方程式 2.[2012·肇庆]实验室用过量的稀盐酸和大理石制取CO2,取50 g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图12-1所示。
回答下列问题。
(1)从图中看出生成沉淀的最大质
量是______g。
(2)开始加入碳酸钠溶液至10 g时
,还没有沉淀的原因是
__________________________。
(3)计算原滤液中氯化钙的质量。第12讲┃ 质量守恒定律与化学方程式 ┃考点互动探究与方法归纳┃┃典型分析┃ “雷雨发庄稼”是有其科学依据的。打雷(放电)时,空气中的主要成分氮气和氧气直接化合生成一氧化氮气体,一氧化氮很容易与空气中的氧气结合生成二氧化氮气体,二氧化氮溶于水生成硝酸和一氧化氮,生成的硝酸随雨水降落到大地,与土壤中的矿物质作用生成可溶性硝酸盐,为植物提供了氮肥。从氮气变成硝酸的过程中,发生的反应的化学方程式为____________________,____________________,___________________________。第12讲┃ 质量守恒定律与化学方程式 第12讲┃ 质量守恒定律与化学方程式 第12讲┃ 质量守恒定律与化学方程式
A.8 g B.18 g C.28 g D.30 g
2.[2011·桂林]在化学反应中一定没有发生变化的是( )
A.原子的种类 B.分子的种类
C.物质的种类 D.分子的数目BA[解析] 根据质量守恒定律可知,参加反应的B的质量为28g+2g-12g=18g。 第12讲┃ 质量守恒定律与化学方程式 3.[2012·重庆] NH4ClO4(高氯酸铵)可用作火箭推进剂,当它发生分解反应时,不能生成的物质是( )
A.CO2 B.Cl2 C.O2 D.N2
A[解析] 化学反应前后元素种类不变,反应物中没有碳元素,所以生成物中不可能出现CO2。第12讲┃ 质量守恒定律与化学方程式 4.[2012·安顺]我国已经立法规定酒驾入刑。“酒精检测仪”可检查司机是否酒后驾车,其反应原理为C2H5OH+4CrO3+6H2SO4===2Cr2(SO4)3+2CO2↑+9X,反应中红色的CrO3转变为绿色的Cr2(SO2)3,其中X的化学式为( )
A.O2 B.H2O C.SO2 D.COB第12讲┃ 质量守恒定律与化学方程式 5.[2012·青岛]某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铝粉在氧气中燃烧生成固体氧化铝。他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生了变化。请填空:
(1)铝粉燃烧生成氧化铝的质量比参加反应铝粉的质量________(填“大”“小”或“不变”)。
(2)你认为这两个反应是否遵循质量守恒定律?______(填“是”或“否”)。
(3)请写出氧化汞受热分解的化学方程式:________________________________。大是第12讲┃ 质量守恒定律与化学方程式 考点42 化学方程式的书写与配平 客观事实 质量守恒定律 化学式配平注明反应条件和符号 第12讲┃ 质量守恒定律与化学方程式 什么物质在什么条件下生成什么物质 多少份质量的什么物质反应生成多少份质量的什么物质第12讲┃ 质量守恒定律与化学方程式 D第12讲┃ 质量守恒定律与化学方程式 2.[2012·桂林]下列化学方程式的表达一定不正确的是( )
A.2Fe+6HCl===2FeCl3+3H2↑
B.BaCl2+CuSO4===BaSO4↓+CuCl2
C.SO3+2NaOH===Na2SO4+H2O
D.Ca(OH)2+Na2CO3===CaCO3↓+2NaOHA[解析] 选项A违背了客观事实,铁与盐酸反应生成氯化亚铁,应改为Fe+2HCl===FeCl2+H2↑。 第12讲┃ 质量守恒定律与化学方程式 3.[2012·天津]写出下列反应的化学方程式。
(1)硫在氧气中燃烧:__________________。
(2)锌片浸入硫酸铜溶液中:____________________________。
(3)过氧化氢溶液中加入少量二氧化锰制取氧气:
______________________。Zn+CuSO4===ZnSO4+Cu 第12讲┃ 质量守恒定律与化学方程式 考点43 根据化学方程式计算 写出并配平反应化学方程式 列出比例式,求解 简明地写出答案 第12讲┃ 质量守恒定律与化学方程式 [注意] 根据化学方程式计算时常见的错误有下列几种:
(1)不认真审题,答非所问;
(2)元素符号或化学式写错;
(3)化学方程式没有配平;
(4)相对分子质量计算有错误;
(5)没有统一单位;
(6)把不纯物质当成纯净物质计算。第12讲┃ 质量守恒定律与化学方程式 12.5 g 第12讲┃ 质量守恒定律与化学方程式 第12讲┃ 质量守恒定律与化学方程式 2.[2012·肇庆]实验室用过量的稀盐酸和大理石制取CO2,取50 g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图12-1所示。
回答下列问题。
(1)从图中看出生成沉淀的最大质
量是______g。
(2)开始加入碳酸钠溶液至10 g时
,还没有沉淀的原因是
__________________________。
(3)计算原滤液中氯化钙的质量。5 图12-1
稀盐酸先与碳酸钠反应 5.55 g 第12讲┃ 质量守恒定律与化学方程式 2.[2012·肇庆]实验室用过量的稀盐酸和大理石制取CO2,取50 g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图12-1所示。
回答下列问题。
(1)从图中看出生成沉淀的最大质
量是______g。
(2)开始加入碳酸钠溶液至10 g时
,还没有沉淀的原因是
__________________________。
(3)计算原滤液中氯化钙的质量。第12讲┃ 质量守恒定律与化学方程式 ┃考点互动探究与方法归纳┃┃典型分析┃ “雷雨发庄稼”是有其科学依据的。打雷(放电)时,空气中的主要成分氮气和氧气直接化合生成一氧化氮气体,一氧化氮很容易与空气中的氧气结合生成二氧化氮气体,二氧化氮溶于水生成硝酸和一氧化氮,生成的硝酸随雨水降落到大地,与土壤中的矿物质作用生成可溶性硝酸盐,为植物提供了氮肥。从氮气变成硝酸的过程中,发生的反应的化学方程式为____________________,____________________,___________________________。第12讲┃ 质量守恒定律与化学方程式 第12讲┃ 质量守恒定律与化学方程式 第12讲┃ 质量守恒定律与化学方程式
同课章节目录
