人教版九年级化学 第十一单元 课题1 生活中常见的盐 课时2 复分解反应课件(共23张PPT)
文档属性
| 名称 | 人教版九年级化学 第十一单元 课题1 生活中常见的盐 课时2 复分解反应课件(共23张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 294.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-31 00:00:00 | ||
图片预览








文档简介
(共23张PPT)
第十一单元 盐 化肥
课时2 复分解反应
课题1 生活中常见的盐
目录
01
课程要求
02
课前预习
03
知识点精讲
04
课堂检测
课程要求
1. 认识常见的复分解反应;能利用复分解反应解释日常生活中的一些化学现象。
2. 认识初中常见酸碱盐的溶解性规律,熟悉常见的沉淀物质。
课前预习
写出下列复分解反应的化学方程式,归纳出其具有的特征。
反应 化学方程式 特征
①CaCO3+HCl ________________________________ 从物质类别看,反应物和生成物都属于________,且各元素的化合价均_____;
①②生成物中有________;
①②③生成物中有_______;
③④生成物中有________
②NaHCO3+HCl ________________________________
③NaOH+HCl ________________________________
④Ca(OH)2+Na2CO3 ________________________________
⑤CuSO4+Ca(OH)2 ________________________________
CaCO3+2HCl == CaCl2+H2O+CO2↑
CaCO3+2HCl == CaCl2+H2O+CO2↑
NaOH+HCl == NaCl+H2O
Ca(OH)2+Na2CO3 == 2NaOH+CaCO3↓
CuSO4+Ca(OH)2 == CaSO4+Cu(OH)2↓
化合物
不变
气体
水
沉淀
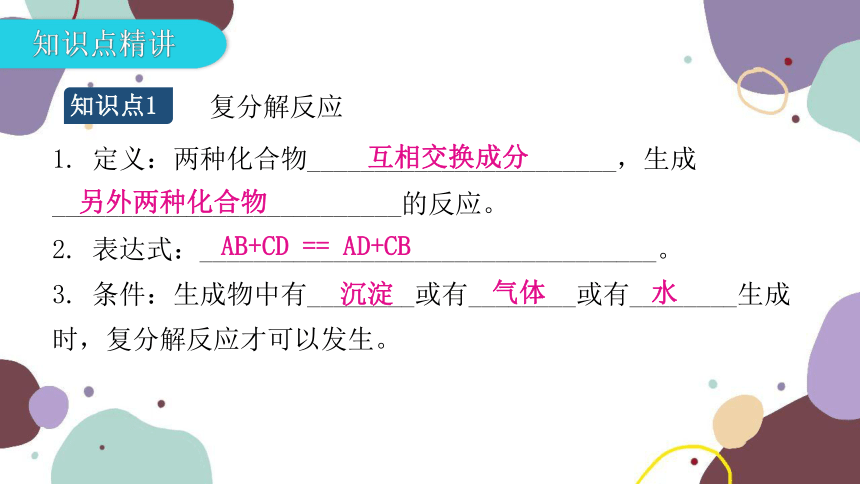
知识点精讲
知识点1
复分解反应
1. 定义:两种化合物_______________________,生成__________________________的反应。
2. 表达式:__________________________________。
3. 条件:生成物中有________或有________或有________生成时,复分解反应才可以发生。
互相交换成分
另外两种化合物
AB+CD == AD+CB
沉淀
气体
水
注意:①反应物中有酸存在时,另一反应物可不溶;若无酸存在时,两种反应物必须可溶。②NaNO3、KNO3、BaSO4、AgCl不发生复分解反应。
4. 实质:两种化合物互相交换成分时,实质是离子间的互换反应。两种离子之间如果能结合成难溶性的碱或盐(沉淀),或不稳定的酸(分解放出气体)或碱,或难电离的水,反应就能发生;反之,反应就不能发生。
课堂练习
1. 下列各组物质中,不能发生复分解反应的是( )
A. HCl和Cu(OH)2
B. Na2CO3和H2SO4
C. Ca(OH)2和Na2CO3
D. KCl和CuSO4
D
2. 下列物质混合,能发生化学反应且现象不明显的是( )
A. 铝与硫酸铜溶液
B. 氢氧化钠溶液与稀盐酸
C. 澄清石灰水与纯碱溶液
D. 硫酸钠溶液与氯化铜溶液
B
思路点拨
(1)一般情况下含有相同离子的两种化合物不发生复分解反应。(2)金属氧化物和酸的反应也属于复分解反应。
(3)非金属氧化物和碱的反应不属于复分解反应。
知识点2
酸、碱、盐的溶解性规律
1. 常见酸碱盐的溶解性口诀:钾钠铵硝盐皆可溶,盐酸盐不溶是银盐,硫酸盐不溶是钡盐,碳酸盐只溶钾钠铵。多数酸溶碱少溶,溶碱只有钾钠铵钡钙。
名称 氢氧 化铜 氢氧 化铁 氢氧 化镁 氢氧 化铝 碳酸钙 碳酸钡 硫酸钡 氯化银
化学式 ______ ______ ______ ______ ______ ______ ______ ______
颜色 ______ ______ ______ ______ ______ ______ ______ ______
2. 常见的八种沉淀(氯化银,硫酸钡不溶于酸)
Cu(OH)2
Fe(OH)3
Mg(OH)2
Al(OH)3
CaCO3
BaCO3
BaSO4
AgCl
蓝色
红褐色
白色
白色
白色
白色
白色
白色
课堂练习
3. 下列物质在水中都不能溶解的一组是( )
A. MgCl2、CaCO3、Mg(OH)2
B. Al(OH)3、Ca(OH)2、Na2CO3
C. AlCl3、Fe(OH)3、BaSO4
D. Cu(OH)2、BaCO3、AgCl
D
4. 在pH=1的无色溶液中,下列离子能大量共存的是 ( )
A. Ba2+、Cu2+、SO42-
B. Ag+、Mg2+、NO3-
C. K+、OH-、CO32-
D. CO32-、Na+、Cl-
B
思路点拨
(1)钾盐、钠盐、铵盐、硝酸盐均溶于水。八大沉淀要记清:Fe(OH)3、Cu(OH)2、Mg(OH)2、Al(OH)3、CaCO3、BaCO3、AgCl、BaSO4。(AgCl、BaSO4既不溶于水也不溶于酸)(2)阴阳离子能共存是因为阴阳离子结合不会生成沉淀或气体或水。
课堂检测
1. 下列反应中不属于复分解反应的是( )
A. CO2+2NaOH == Na2CO3+H2O
B. NaOH+HCl == NaCl+H2O
C. NaCl+AgNO3 == AgCl↓+NaNO3
D. 2HCl+CaO == CaCl2+H2O
A
2. 下列物质间不能发生复分解反应的是( )
A. 碳酸钠溶液和氯化钙溶液
B. 氢氧化钠溶液和氯化钾溶液
C. 碳酸钾溶液和盐酸
D. 硫酸铜溶液和氯化钡溶液
B
3. 下列实验中有化学反应发生,且能观察到明显现象的是( )
A. 向氯化钾溶液中滴入稀硫酸
B. 向硫酸钠溶液中滴入氯化镁溶液
C. 向氧化铜粉末中滴入氢氧化钠溶液
D. 向澄清石灰水中通入二氧化碳
D
4. 现有铁、氢氧化钡溶液、稀硫酸、氯化铜溶液、硫酸镁溶液五种物质,两两之间常温就能发生的反应有( )
A. 4个
B. 5个
C. 6个
D. 7个
B
5. 写出下列常见沉淀的化学式:
红褐色沉淀:________、蓝色沉淀:________、不溶于酸的白色沉淀:________________。
Fe(OH)3
Cu(OH)2
BaSO4、AgCl
6. 判断下列物质间在通常情况下能否发生反应,能发生反应的写出有关反应的化学方程式,不能反应的说明原因。
(1)碳酸钾溶液与氯化钙溶液:__________________________。
(2)碳酸钾溶液与稀盐酸:______________________________。
(3)氯化钠溶液与硫酸钾:______________________________。
(4)氢氧化钡溶液与硫酸:______________________________。
(5)碳酸钠溶液与硝酸钾:______________________________。
K2CO3+CaCl2 == CaCO3↓+2KCl
K2CO3+2HCl == 2KCl+H2O+CO2↑
不反应,没有生成沉淀或气体或水
不反应,没有生成沉淀或气体或水
Ba(OH)2+H2SO4 == BaSO4↓+2H2O
7. 某兴趣小组在实验室中探究复分解反应能否发生,请你参与他们的探究。
【实验过程与分析】
实验序号 实验一 实验二 实验三
实验试剂 NaOH溶液 H2SO4溶液 Na2CO3溶液 H2SO4溶液 BaCl2溶液
H2SO4溶液
实验现象 无明显现象 ______________ ______________
实验结论 氢氧化钠不能与 硫酸发生反应 碳酸钠能与硫酸 发生反应 氯化钡能与硫酸
发生反应
产生气泡
产生白色沉淀
【实验反思与拓展】
(1)某同学认为实验一的结论不正确。经讨论,设计如图11-1-2所示的实验来探究稀硫酸与NaOH溶液能否发生反应。观察到右侧实验试管中的现象是____________________________,说明稀硫酸与NaOH溶液发生了反应,该反应的化学方程式为_____________________________。
溶液由红色变为无色
2NaOH+H2SO4 == Na2SO4+2H2O
(2)对于无明显现象的化学反应,可通过检验有新物质生成或检验_______________________________的方法来证明物质间发生了化学反应。
【实验结论】复分解反应发生的条件:生成物中有______________________________。
某种反应物消失或减少
沉淀或气体或水
第十一单元 盐 化肥
课时2 复分解反应
课题1 生活中常见的盐
目录
01
课程要求
02
课前预习
03
知识点精讲
04
课堂检测
课程要求
1. 认识常见的复分解反应;能利用复分解反应解释日常生活中的一些化学现象。
2. 认识初中常见酸碱盐的溶解性规律,熟悉常见的沉淀物质。
课前预习
写出下列复分解反应的化学方程式,归纳出其具有的特征。
反应 化学方程式 特征
①CaCO3+HCl ________________________________ 从物质类别看,反应物和生成物都属于________,且各元素的化合价均_____;
①②生成物中有________;
①②③生成物中有_______;
③④生成物中有________
②NaHCO3+HCl ________________________________
③NaOH+HCl ________________________________
④Ca(OH)2+Na2CO3 ________________________________
⑤CuSO4+Ca(OH)2 ________________________________
CaCO3+2HCl == CaCl2+H2O+CO2↑
CaCO3+2HCl == CaCl2+H2O+CO2↑
NaOH+HCl == NaCl+H2O
Ca(OH)2+Na2CO3 == 2NaOH+CaCO3↓
CuSO4+Ca(OH)2 == CaSO4+Cu(OH)2↓
化合物
不变
气体
水
沉淀
知识点精讲
知识点1
复分解反应
1. 定义:两种化合物_______________________,生成__________________________的反应。
2. 表达式:__________________________________。
3. 条件:生成物中有________或有________或有________生成时,复分解反应才可以发生。
互相交换成分
另外两种化合物
AB+CD == AD+CB
沉淀
气体
水
注意:①反应物中有酸存在时,另一反应物可不溶;若无酸存在时,两种反应物必须可溶。②NaNO3、KNO3、BaSO4、AgCl不发生复分解反应。
4. 实质:两种化合物互相交换成分时,实质是离子间的互换反应。两种离子之间如果能结合成难溶性的碱或盐(沉淀),或不稳定的酸(分解放出气体)或碱,或难电离的水,反应就能发生;反之,反应就不能发生。
课堂练习
1. 下列各组物质中,不能发生复分解反应的是( )
A. HCl和Cu(OH)2
B. Na2CO3和H2SO4
C. Ca(OH)2和Na2CO3
D. KCl和CuSO4
D
2. 下列物质混合,能发生化学反应且现象不明显的是( )
A. 铝与硫酸铜溶液
B. 氢氧化钠溶液与稀盐酸
C. 澄清石灰水与纯碱溶液
D. 硫酸钠溶液与氯化铜溶液
B
思路点拨
(1)一般情况下含有相同离子的两种化合物不发生复分解反应。(2)金属氧化物和酸的反应也属于复分解反应。
(3)非金属氧化物和碱的反应不属于复分解反应。
知识点2
酸、碱、盐的溶解性规律
1. 常见酸碱盐的溶解性口诀:钾钠铵硝盐皆可溶,盐酸盐不溶是银盐,硫酸盐不溶是钡盐,碳酸盐只溶钾钠铵。多数酸溶碱少溶,溶碱只有钾钠铵钡钙。
名称 氢氧 化铜 氢氧 化铁 氢氧 化镁 氢氧 化铝 碳酸钙 碳酸钡 硫酸钡 氯化银
化学式 ______ ______ ______ ______ ______ ______ ______ ______
颜色 ______ ______ ______ ______ ______ ______ ______ ______
2. 常见的八种沉淀(氯化银,硫酸钡不溶于酸)
Cu(OH)2
Fe(OH)3
Mg(OH)2
Al(OH)3
CaCO3
BaCO3
BaSO4
AgCl
蓝色
红褐色
白色
白色
白色
白色
白色
白色
课堂练习
3. 下列物质在水中都不能溶解的一组是( )
A. MgCl2、CaCO3、Mg(OH)2
B. Al(OH)3、Ca(OH)2、Na2CO3
C. AlCl3、Fe(OH)3、BaSO4
D. Cu(OH)2、BaCO3、AgCl
D
4. 在pH=1的无色溶液中,下列离子能大量共存的是 ( )
A. Ba2+、Cu2+、SO42-
B. Ag+、Mg2+、NO3-
C. K+、OH-、CO32-
D. CO32-、Na+、Cl-
B
思路点拨
(1)钾盐、钠盐、铵盐、硝酸盐均溶于水。八大沉淀要记清:Fe(OH)3、Cu(OH)2、Mg(OH)2、Al(OH)3、CaCO3、BaCO3、AgCl、BaSO4。(AgCl、BaSO4既不溶于水也不溶于酸)(2)阴阳离子能共存是因为阴阳离子结合不会生成沉淀或气体或水。
课堂检测
1. 下列反应中不属于复分解反应的是( )
A. CO2+2NaOH == Na2CO3+H2O
B. NaOH+HCl == NaCl+H2O
C. NaCl+AgNO3 == AgCl↓+NaNO3
D. 2HCl+CaO == CaCl2+H2O
A
2. 下列物质间不能发生复分解反应的是( )
A. 碳酸钠溶液和氯化钙溶液
B. 氢氧化钠溶液和氯化钾溶液
C. 碳酸钾溶液和盐酸
D. 硫酸铜溶液和氯化钡溶液
B
3. 下列实验中有化学反应发生,且能观察到明显现象的是( )
A. 向氯化钾溶液中滴入稀硫酸
B. 向硫酸钠溶液中滴入氯化镁溶液
C. 向氧化铜粉末中滴入氢氧化钠溶液
D. 向澄清石灰水中通入二氧化碳
D
4. 现有铁、氢氧化钡溶液、稀硫酸、氯化铜溶液、硫酸镁溶液五种物质,两两之间常温就能发生的反应有( )
A. 4个
B. 5个
C. 6个
D. 7个
B
5. 写出下列常见沉淀的化学式:
红褐色沉淀:________、蓝色沉淀:________、不溶于酸的白色沉淀:________________。
Fe(OH)3
Cu(OH)2
BaSO4、AgCl
6. 判断下列物质间在通常情况下能否发生反应,能发生反应的写出有关反应的化学方程式,不能反应的说明原因。
(1)碳酸钾溶液与氯化钙溶液:__________________________。
(2)碳酸钾溶液与稀盐酸:______________________________。
(3)氯化钠溶液与硫酸钾:______________________________。
(4)氢氧化钡溶液与硫酸:______________________________。
(5)碳酸钠溶液与硝酸钾:______________________________。
K2CO3+CaCl2 == CaCO3↓+2KCl
K2CO3+2HCl == 2KCl+H2O+CO2↑
不反应,没有生成沉淀或气体或水
不反应,没有生成沉淀或气体或水
Ba(OH)2+H2SO4 == BaSO4↓+2H2O
7. 某兴趣小组在实验室中探究复分解反应能否发生,请你参与他们的探究。
【实验过程与分析】
实验序号 实验一 实验二 实验三
实验试剂 NaOH溶液 H2SO4溶液 Na2CO3溶液 H2SO4溶液 BaCl2溶液
H2SO4溶液
实验现象 无明显现象 ______________ ______________
实验结论 氢氧化钠不能与 硫酸发生反应 碳酸钠能与硫酸 发生反应 氯化钡能与硫酸
发生反应
产生气泡
产生白色沉淀
【实验反思与拓展】
(1)某同学认为实验一的结论不正确。经讨论,设计如图11-1-2所示的实验来探究稀硫酸与NaOH溶液能否发生反应。观察到右侧实验试管中的现象是____________________________,说明稀硫酸与NaOH溶液发生了反应,该反应的化学方程式为_____________________________。
溶液由红色变为无色
2NaOH+H2SO4 == Na2SO4+2H2O
(2)对于无明显现象的化学反应,可通过检验有新物质生成或检验_______________________________的方法来证明物质间发生了化学反应。
【实验结论】复分解反应发生的条件:生成物中有______________________________。
某种反应物消失或减少
沉淀或气体或水
同课章节目录
