2021-2022学年九年级化学人教版上册3.2原子的结构1课时(课件20页)
文档属性
| 名称 | 2021-2022学年九年级化学人教版上册3.2原子的结构1课时(课件20页) |
|
|
| 格式 | pptx | ||
| 文件大小 | 849.9KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-01 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
课题2 原子的结构
(1课时)
Na
Cl
H
C
什么是分子
什么是原子
分子和原子的根本区别是什么
分子是保持物质化学性质的最小粒子。
原子是化学变化中的最小粒子。
在化学变化中分子可分,而原子不可分。
【思考】
原子究竟是什么样子呢?
今天,我们一起揭开原子结构“神秘的面纱”
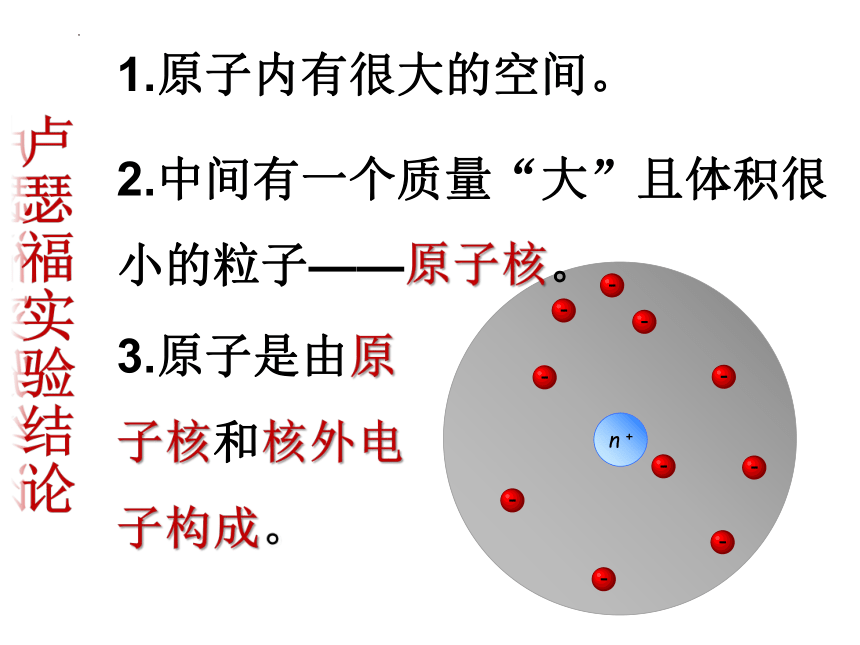
卢瑟福实验结果
n +
1.大多数的α粒子能按原来方向穿过金箔,说明:
A. 原子是实心球体
2.极少数α粒子(带正电)被反弹回来,必定是碰到了坚硬的微粒,这种微粒与α粒子电荷(不同, )、质量(小, )。
3 . 由于被反弹回来α粒子极少,所以原子中这个带正电的微粒的体积相对原子来说很(大, )
交流讨论
B. 原子不是实心球体
相同
大
小
1.原子内有很大的空间。
n +
-
-
-
-
-
-
-
-
-
-
卢瑟福实验结论
2.中间有一个质量“大”且体积很小的粒子——原子核。
3.原子是由原子核和核外电子构成。
原子
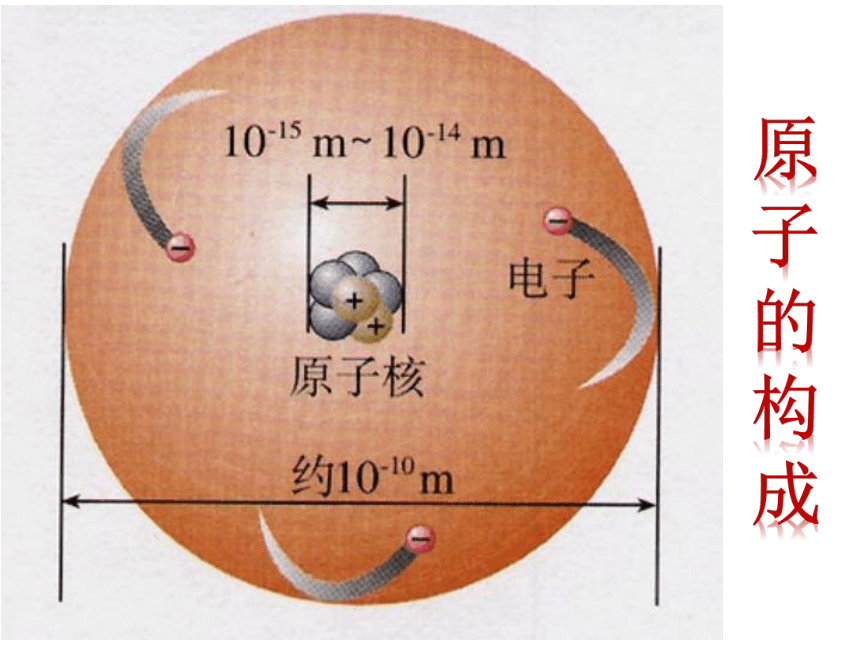
原子核比原子小得多
原子核
原子核有多小?
原子的构成
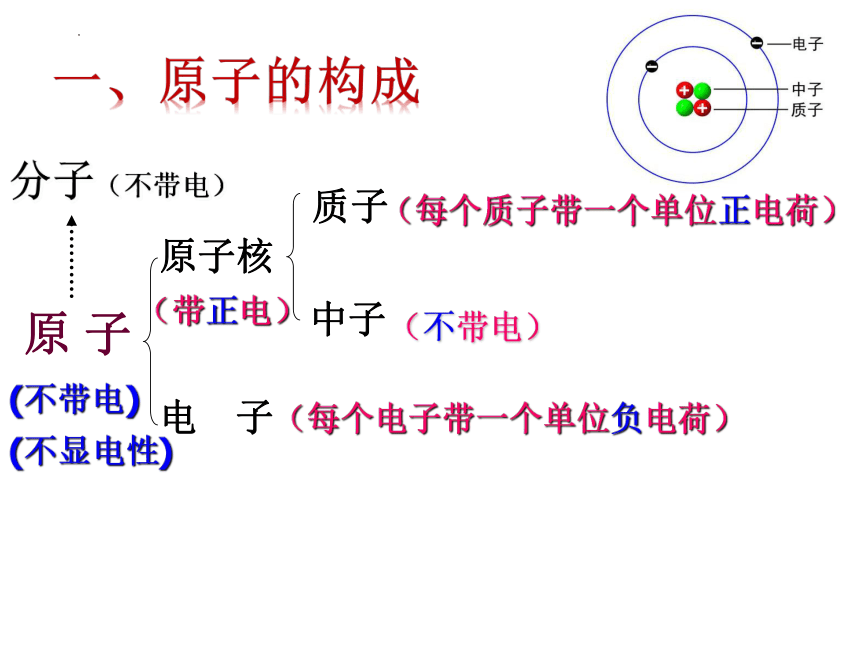
一、原子的构成
原 子
电 子
原子核
质子
中子
(每个质子带一个单位正电荷)
(不带电)
(每个电子带一个单位负电荷)
(带正电)
(不带电)
(不显电性)
分子(不带电)
原子为什么不显电性?
一个质子带一个单位正电荷
一个电子带一个单位负电荷
中子不带电
质子数=核外电子数
原子不显电性
正负电荷总数相等
讨论
阅读P53表3-1
你能得出什么结论呢?
讨论
原子种类 质子数 中子数 核外电子数 核电荷数 原子序数
氢 1 0 1 1 1
碳 6 6 6 6 6
氧 8 8 8 8 8
钠 11 12 11 11 11
氯 17 18 17 17 17
观察表格(表3-1),思考下列问题
1.不同原子之间有哪些区别?
2.所有原子都是由质子、中子、电子构成的吗?
不是所有的原子都有中子。如氢原子
不同种类的原子,核内质子数、核外电子数不同
原子种类 质子数 中子数 核外电子数 核电荷数 原子序数
氢 1 0 1 1 1
碳 6 6 6 6 6
氧 8 8 8 8 8
钠 11 12 11 11 11
氯 17 18 17 17 17
观察表格(表3-1),思考下列问题
3. 质子数、中子数在数量上有什么关系?
4.质子数、电子数、核电荷数、原子序数有什么联系?
质子数不一定等于中子数
核电荷数=质子数=核外电子数=原子序数
以碳原子为例,说明构成原子的粒子有哪几种?它们是怎样构成原子的?
质子数 中子数 核外电子数
碳原子 6 6 6
拓展:1、分子由原子构成,因此分子也不显电性。
2 、带正电的粒子: 原子核、质子
带负电的粒子: 电子
不带电的粒子:中子、原子、分子
由于原子核(即核内质子)所带电量和核外电子的电量相等,但电性相反,所以整个原子不显电性。
质子数 中子数 核外电子数
氧原子 8 8 8
碳原子是否显电性?为什么?
质子数 中子数 核外电子数
碳原子 6 6 6
1.原子是由居于原子中心、带______的原子核和核外带______ 的电子构成,由于它们所带的电荷_______ ,电性_____,所以整个原子______(填显或不显)电性。原子核 是由 _______和______构成。
2、保持物质的化学性质的最小粒子是_____;化学变化中的最小粒子是______;原子中带正电荷的粒子是 ;不显电性的粒子是 。
3、据报道,1994年12月科学家发现了一种新元素,它的原子核内有质子111个,中子161个,则该元素核外电子数是_____
正电
负电
质子
中子
相等
相反
不显
分子
原子
质子和原子核
中子
111
小 结
1、原子的构成:构成原子的粒子一般是质子、中子、电子(氢原子例外)。
2.在原子中,
核电荷数=质子数=核外电子数=原子序数
3.质子数和中子数不一定相等。
4.原子的种类不同,其质子数也不相同。
1、下列关于原子的说法中,不正确的是( )。
A.原子是化学变化中的最小粒子,但原子可以再分
B.核外电子在原子核外的空间里作高速运动
C.原子核是由质子和电子构成的,呈电中性
D.原子可以构成分子,也可以构成物质
C
2、已知原子的核电荷数,可以确定它的 ( )。
A 原子质量 B 质子数
C 中子数 D 电子数
B D
3、在分子、原子、原子核、质子、中子、电子等粒子中找出符合下列条件的粒子填空:
(1)能保持物质化学性质的粒子是( )
(2)化学变化中最小的粒子( )
(3)带正电荷的粒子( )
(4)不显电性的粒子( )
(5)质量最小的粒子( )
(6)决定原子质量的粒子( )
(7)同一原子中数目相等的粒子( )
分子、原子
原子
原子核、质子
中子、分子、原子
电子
质子、电子
原子核或质子和中子
练习
不同种类的原子:质子数、核外电子数都不同。
同一原子中质子数等于核外电子数,但不一定等于中子数
氢原子的中子数为零,因此不是所有原子中都存在中 子,但一定存在质子和核外电子。
1、不同种类的原子之间有哪些区别?
3、所有原子都是由质子、中子和电子构成的吗?
2、同一原子的质子、中子、电子在数量上有什么关系?
原子中:质子数= 核外电子数= 核电荷数
课题2 原子的结构
(1课时)
Na
Cl
H
C
什么是分子
什么是原子
分子和原子的根本区别是什么
分子是保持物质化学性质的最小粒子。
原子是化学变化中的最小粒子。
在化学变化中分子可分,而原子不可分。
【思考】
原子究竟是什么样子呢?
今天,我们一起揭开原子结构“神秘的面纱”
卢瑟福实验结果
n +
1.大多数的α粒子能按原来方向穿过金箔,说明:
A. 原子是实心球体
2.极少数α粒子(带正电)被反弹回来,必定是碰到了坚硬的微粒,这种微粒与α粒子电荷(不同, )、质量(小, )。
3 . 由于被反弹回来α粒子极少,所以原子中这个带正电的微粒的体积相对原子来说很(大, )
交流讨论
B. 原子不是实心球体
相同
大
小
1.原子内有很大的空间。
n +
-
-
-
-
-
-
-
-
-
-
卢瑟福实验结论
2.中间有一个质量“大”且体积很小的粒子——原子核。
3.原子是由原子核和核外电子构成。
原子
原子核比原子小得多
原子核
原子核有多小?
原子的构成
一、原子的构成
原 子
电 子
原子核
质子
中子
(每个质子带一个单位正电荷)
(不带电)
(每个电子带一个单位负电荷)
(带正电)
(不带电)
(不显电性)
分子(不带电)
原子为什么不显电性?
一个质子带一个单位正电荷
一个电子带一个单位负电荷
中子不带电
质子数=核外电子数
原子不显电性
正负电荷总数相等
讨论
阅读P53表3-1
你能得出什么结论呢?
讨论
原子种类 质子数 中子数 核外电子数 核电荷数 原子序数
氢 1 0 1 1 1
碳 6 6 6 6 6
氧 8 8 8 8 8
钠 11 12 11 11 11
氯 17 18 17 17 17
观察表格(表3-1),思考下列问题
1.不同原子之间有哪些区别?
2.所有原子都是由质子、中子、电子构成的吗?
不是所有的原子都有中子。如氢原子
不同种类的原子,核内质子数、核外电子数不同
原子种类 质子数 中子数 核外电子数 核电荷数 原子序数
氢 1 0 1 1 1
碳 6 6 6 6 6
氧 8 8 8 8 8
钠 11 12 11 11 11
氯 17 18 17 17 17
观察表格(表3-1),思考下列问题
3. 质子数、中子数在数量上有什么关系?
4.质子数、电子数、核电荷数、原子序数有什么联系?
质子数不一定等于中子数
核电荷数=质子数=核外电子数=原子序数
以碳原子为例,说明构成原子的粒子有哪几种?它们是怎样构成原子的?
质子数 中子数 核外电子数
碳原子 6 6 6
拓展:1、分子由原子构成,因此分子也不显电性。
2 、带正电的粒子: 原子核、质子
带负电的粒子: 电子
不带电的粒子:中子、原子、分子
由于原子核(即核内质子)所带电量和核外电子的电量相等,但电性相反,所以整个原子不显电性。
质子数 中子数 核外电子数
氧原子 8 8 8
碳原子是否显电性?为什么?
质子数 中子数 核外电子数
碳原子 6 6 6
1.原子是由居于原子中心、带______的原子核和核外带______ 的电子构成,由于它们所带的电荷_______ ,电性_____,所以整个原子______(填显或不显)电性。原子核 是由 _______和______构成。
2、保持物质的化学性质的最小粒子是_____;化学变化中的最小粒子是______;原子中带正电荷的粒子是 ;不显电性的粒子是 。
3、据报道,1994年12月科学家发现了一种新元素,它的原子核内有质子111个,中子161个,则该元素核外电子数是_____
正电
负电
质子
中子
相等
相反
不显
分子
原子
质子和原子核
中子
111
小 结
1、原子的构成:构成原子的粒子一般是质子、中子、电子(氢原子例外)。
2.在原子中,
核电荷数=质子数=核外电子数=原子序数
3.质子数和中子数不一定相等。
4.原子的种类不同,其质子数也不相同。
1、下列关于原子的说法中,不正确的是( )。
A.原子是化学变化中的最小粒子,但原子可以再分
B.核外电子在原子核外的空间里作高速运动
C.原子核是由质子和电子构成的,呈电中性
D.原子可以构成分子,也可以构成物质
C
2、已知原子的核电荷数,可以确定它的 ( )。
A 原子质量 B 质子数
C 中子数 D 电子数
B D
3、在分子、原子、原子核、质子、中子、电子等粒子中找出符合下列条件的粒子填空:
(1)能保持物质化学性质的粒子是( )
(2)化学变化中最小的粒子( )
(3)带正电荷的粒子( )
(4)不显电性的粒子( )
(5)质量最小的粒子( )
(6)决定原子质量的粒子( )
(7)同一原子中数目相等的粒子( )
分子、原子
原子
原子核、质子
中子、分子、原子
电子
质子、电子
原子核或质子和中子
练习
不同种类的原子:质子数、核外电子数都不同。
同一原子中质子数等于核外电子数,但不一定等于中子数
氢原子的中子数为零,因此不是所有原子中都存在中 子,但一定存在质子和核外电子。
1、不同种类的原子之间有哪些区别?
3、所有原子都是由质子、中子和电子构成的吗?
2、同一原子的质子、中子、电子在数量上有什么关系?
原子中:质子数= 核外电子数= 核电荷数
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
