2021-2022学年九年级化学人教版下册第10单元实验活动6:酸、碱的化学性质(课件18页)
文档属性
| 名称 | 2021-2022学年九年级化学人教版下册第10单元实验活动6:酸、碱的化学性质(课件18页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-01 00:00:00 | ||
图片预览




文档简介
(共18张PPT)
第10单元 酸和碱
化学课件
编辑时间:2020-12-08
2020年度新制作的课件
实验活动 6 酸、碱的化学性质
【51】
知识提纲
一 酸碱与指示剂的反应
二 金属氧化物与酸的反应
三 酸碱盐溶液之间的反应
实验活动 6
酸、碱的化学性质
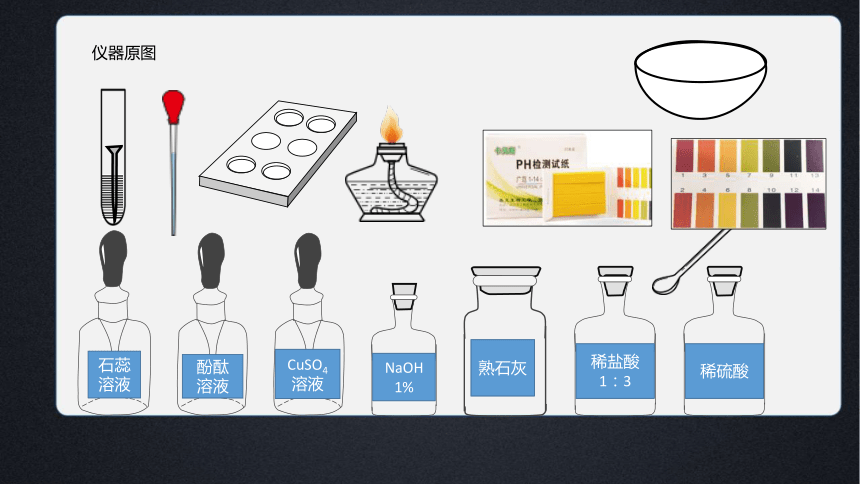
仪器原图
石蕊
溶液
酚酞
溶液
CuSO4溶液
NaOH
1%
熟石灰
稀盐酸
1:3
稀硫酸
【实验目的】
1. 加深对酸和碱的主要性质的认识。
2. 通过实验解释生活中的一些现象。
【实验用品】
实验 仪器
实验 药品
实验 物品
【实验用品】
试管、药匙、蒸发皿、玻璃棒、点滴板、酒精灯、铁架台(带铁圈)、坩埚钳、胶头滴管。
pH试纸、生锈的铁钉、火柴
稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液
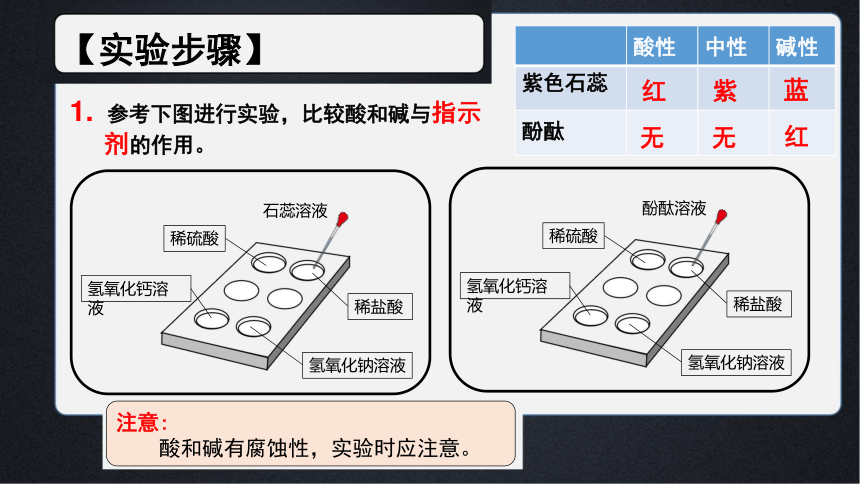
【实验步骤】
1. 参考下图进行实验,比较酸和碱与指示
剂的作用。
注意:
酸和碱有腐蚀性,实验时应注意。
稀盐酸
氢氧化钠溶液
稀硫酸
氢氧化钙溶液
石蕊溶液
稀盐酸
氢氧化钠溶液
稀硫酸
氢氧化钙溶液
酚酞溶液
酸性 中性 碱性
紫色石蕊
酚酞
红
紫
蓝
无
无
红
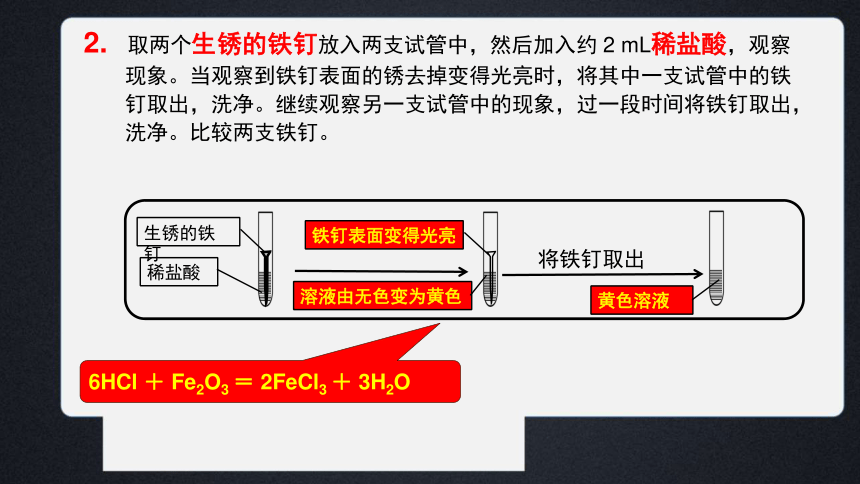
2. 取两个生锈的铁钉放入两支试管中,然后加入约 2 mL稀盐酸,观察
现象。当观察到铁钉表面的锈去掉变得光亮时,将其中一支试管中的铁
钉取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,
洗净。比较两支铁钉。
稀盐酸
生锈的铁钉
铁钉表面变得光亮
将铁钉取出
溶液由无色变为黄色
6HCl + Fe2O3 = 2FeCl3 + 3H2O
黄色溶液
2. 取两个生锈的铁钉放入两支试管中,然后加入约 2 mL稀盐酸,观察
现象。当观察到铁钉表面的锈去掉变得光亮时,将其中一支试管中的铁
钉取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,
洗净。比较两支铁钉。
生锈的铁钉
稀盐酸
铁钉表面变得光亮
继续反应
溶液由无色变为黄色
铁钉表面有气泡产生
Fe+ 2HCl=FeCl2+ H2↑
6HCl + Fe2O3 = 2FeCl3 + 3H2O
3. 在试管中加入约2 mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。
然后再向试管中加入稀盐酸,观察现象。
NaOH溶液
CuSO4溶液
蓝色
Cu(OH)2
蓝色沉淀
CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4`````````````````+8*6+
6
4. 在试管中加入约1 mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢
慢滴入稀盐酸,边不断振荡试管,至溶液颜色恰好变成无色为止。取该无
色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
酚酞溶液
稀盐酸
白色固体
HCl + NaOH = NaCl + H2O
5. 向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),
然后各加入1mL水,振荡;再各滴入1~2滴酚酞溶液,观察现象。继续向
其中一支试管中加入约1 mL水,振荡;向另一支试管加入约1 mL稀盐酸,
振荡; 比较两支试管中的现象。
1mL水
1mL水
酚酞
溶液变红
酚酞
溶液变红
1mL水
1mL
稀盐酸
溶液
仍为红色
溶液
变为无色
Ca(OH)2 + 2HCl= 2CaCl2 + 2H2O
【问题与交流】通过实验步骤 5,可以验证氢氧化钙的哪些性质
想一想:
将铁钉放入试管时 应 如何操作
1. Ca(OH)2 溶液呈碱性
2. Ca(OH)2 能与稀盐酸发生反应
一、常见酸(HCl、H2SO4)的化学性质(“酸五条”)
1. 请写出下列物质的化学式:A. _______;B. ________。
Na2CO3
NaOH
2. 请写出图中涉及的化学方程式①_________________________________、___________________________________、 _________________________________、___________________________________;②_________________________________、___________________________________、 __________________________________、___________________________________;
Fe+H2SO4=== FeSO4+H2↑
Zn+2HCl=== ZnCl2+H2↑
Fe+2HCl=== FeCl2+H2↑
Zn+H2SO4=== ZnSO4+H2↑
Ca(OH)2+H2SO4=== CaSO4+2H2O
2NaOH+H2SO4=== Na2SO4+2H2O
Ca(OH)2+2HCl=== CaCl2+2H2O
NaOH+HCl=== NaCl+H2O
2. 请写出图中涉及的化学方程式③_______________________________________、_______________________________________;④_______________________________________、_______________________________________、 _______________________________________、_______________________________________;⑤______________________________________;⑥_____________________________________。
Na2CO3+H2SO4=== Na2SO4+H2O+CO2↑
Na2CO3+2HCl=== 2NaCl+H2O+CO2↑
Fe2O3+6HCl=== 2FeCl3+3H2O
CuO+2HCl=== CuCl2+H2O
Fe2O3+3H2SO4=== Fe2(SO4)3+3H2O
CuO+H2SO4=== CuSO4+H2O
BaCl2+H2SO4=== BaSO4↓+2HCl
AgNO3+HCl=== AgCl↓+HNO3
二、常见碱[NaOH、Ca(OH)2]的化学性质(“碱四条”)
1. 请写出下列物质的化学式:A. _______;B. _________。
2. 请写出图中涉及的化学方程式①______________________________________、_______________________________________、 ______________________________________、_______________________________________;
Na2CO3
CO2
HCl+NaOH=== NaCl+H2O
H2SO4+2NaOH=== Na2SO4+2H2O
2HCl+Ca(OH)2=== CaCl2+2H2O
H2SO4+Ca(OH)2=== CaSO4+2H2O
2. 请写出图中涉及的化学方程式②_________________________________________、_________________________________________、 _________________________________________、_________________________________________;
MgCl2+2NaOH=== Mg(OH)2↓+2NaCl
CuSO4+2NaOH=== Cu(OH)2↓+Na2SO4
MgCl2+Ca(OH)2=== Mg(OH)2↓+CaCl2
CuSO4+Ca(OH)2=== Cu(OH)2↓+CaSO4
2. 请写出图中涉及的化学方程式③_________________________________________、_________________________________________、 _________________________________________、_________________________________________;④_________________________________________(工业制烧碱的原理)。
CO2+2NaOH=== Na2CO3+H2O
SO2+2NaOH=== Na2SO3+H2O
CO2+Ca(OH)2=== CaCO3↓+H2O
SO2+Ca(OH)2=== CaSO3↓+H2O
Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH
第10单元 酸和碱
化学课件
编辑时间:2020-12-08
2020年度新制作的课件
实验活动 6 酸、碱的化学性质
【51】
知识提纲
一 酸碱与指示剂的反应
二 金属氧化物与酸的反应
三 酸碱盐溶液之间的反应
实验活动 6
酸、碱的化学性质
仪器原图
石蕊
溶液
酚酞
溶液
CuSO4溶液
NaOH
1%
熟石灰
稀盐酸
1:3
稀硫酸
【实验目的】
1. 加深对酸和碱的主要性质的认识。
2. 通过实验解释生活中的一些现象。
【实验用品】
实验 仪器
实验 药品
实验 物品
【实验用品】
试管、药匙、蒸发皿、玻璃棒、点滴板、酒精灯、铁架台(带铁圈)、坩埚钳、胶头滴管。
pH试纸、生锈的铁钉、火柴
稀盐酸、稀硫酸、稀氢氧化钠溶液、氢氧化钙溶液、硫酸铜溶液、氢氧化钙粉末、石蕊溶液、酚酞溶液
【实验步骤】
1. 参考下图进行实验,比较酸和碱与指示
剂的作用。
注意:
酸和碱有腐蚀性,实验时应注意。
稀盐酸
氢氧化钠溶液
稀硫酸
氢氧化钙溶液
石蕊溶液
稀盐酸
氢氧化钠溶液
稀硫酸
氢氧化钙溶液
酚酞溶液
酸性 中性 碱性
紫色石蕊
酚酞
红
紫
蓝
无
无
红
2. 取两个生锈的铁钉放入两支试管中,然后加入约 2 mL稀盐酸,观察
现象。当观察到铁钉表面的锈去掉变得光亮时,将其中一支试管中的铁
钉取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,
洗净。比较两支铁钉。
稀盐酸
生锈的铁钉
铁钉表面变得光亮
将铁钉取出
溶液由无色变为黄色
6HCl + Fe2O3 = 2FeCl3 + 3H2O
黄色溶液
2. 取两个生锈的铁钉放入两支试管中,然后加入约 2 mL稀盐酸,观察
现象。当观察到铁钉表面的锈去掉变得光亮时,将其中一支试管中的铁
钉取出,洗净。继续观察另一支试管中的现象,过一段时间将铁钉取出,
洗净。比较两支铁钉。
生锈的铁钉
稀盐酸
铁钉表面变得光亮
继续反应
溶液由无色变为黄色
铁钉表面有气泡产生
Fe+ 2HCl=FeCl2+ H2↑
6HCl + Fe2O3 = 2FeCl3 + 3H2O
3. 在试管中加入约2 mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察现象。
然后再向试管中加入稀盐酸,观察现象。
NaOH溶液
CuSO4溶液
蓝色
Cu(OH)2
蓝色沉淀
CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4`````````````````+8*6+
6
4. 在试管中加入约1 mL氢氧化钠溶液,滴入几滴酚酞溶液。然后边用滴管慢
慢滴入稀盐酸,边不断振荡试管,至溶液颜色恰好变成无色为止。取该无
色溶液约1mL,置于蒸发皿中加热,使液体蒸干,观察现象。
酚酞溶液
稀盐酸
白色固体
HCl + NaOH = NaCl + H2O
5. 向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),
然后各加入1mL水,振荡;再各滴入1~2滴酚酞溶液,观察现象。继续向
其中一支试管中加入约1 mL水,振荡;向另一支试管加入约1 mL稀盐酸,
振荡; 比较两支试管中的现象。
1mL水
1mL水
酚酞
溶液变红
酚酞
溶液变红
1mL水
1mL
稀盐酸
溶液
仍为红色
溶液
变为无色
Ca(OH)2 + 2HCl= 2CaCl2 + 2H2O
【问题与交流】通过实验步骤 5,可以验证氢氧化钙的哪些性质
想一想:
将铁钉放入试管时 应 如何操作
1. Ca(OH)2 溶液呈碱性
2. Ca(OH)2 能与稀盐酸发生反应
一、常见酸(HCl、H2SO4)的化学性质(“酸五条”)
1. 请写出下列物质的化学式:A. _______;B. ________。
Na2CO3
NaOH
2. 请写出图中涉及的化学方程式①_________________________________、___________________________________、 _________________________________、___________________________________;②_________________________________、___________________________________、 __________________________________、___________________________________;
Fe+H2SO4=== FeSO4+H2↑
Zn+2HCl=== ZnCl2+H2↑
Fe+2HCl=== FeCl2+H2↑
Zn+H2SO4=== ZnSO4+H2↑
Ca(OH)2+H2SO4=== CaSO4+2H2O
2NaOH+H2SO4=== Na2SO4+2H2O
Ca(OH)2+2HCl=== CaCl2+2H2O
NaOH+HCl=== NaCl+H2O
2. 请写出图中涉及的化学方程式③_______________________________________、_______________________________________;④_______________________________________、_______________________________________、 _______________________________________、_______________________________________;⑤______________________________________;⑥_____________________________________。
Na2CO3+H2SO4=== Na2SO4+H2O+CO2↑
Na2CO3+2HCl=== 2NaCl+H2O+CO2↑
Fe2O3+6HCl=== 2FeCl3+3H2O
CuO+2HCl=== CuCl2+H2O
Fe2O3+3H2SO4=== Fe2(SO4)3+3H2O
CuO+H2SO4=== CuSO4+H2O
BaCl2+H2SO4=== BaSO4↓+2HCl
AgNO3+HCl=== AgCl↓+HNO3
二、常见碱[NaOH、Ca(OH)2]的化学性质(“碱四条”)
1. 请写出下列物质的化学式:A. _______;B. _________。
2. 请写出图中涉及的化学方程式①______________________________________、_______________________________________、 ______________________________________、_______________________________________;
Na2CO3
CO2
HCl+NaOH=== NaCl+H2O
H2SO4+2NaOH=== Na2SO4+2H2O
2HCl+Ca(OH)2=== CaCl2+2H2O
H2SO4+Ca(OH)2=== CaSO4+2H2O
2. 请写出图中涉及的化学方程式②_________________________________________、_________________________________________、 _________________________________________、_________________________________________;
MgCl2+2NaOH=== Mg(OH)2↓+2NaCl
CuSO4+2NaOH=== Cu(OH)2↓+Na2SO4
MgCl2+Ca(OH)2=== Mg(OH)2↓+CaCl2
CuSO4+Ca(OH)2=== Cu(OH)2↓+CaSO4
2. 请写出图中涉及的化学方程式③_________________________________________、_________________________________________、 _________________________________________、_________________________________________;④_________________________________________(工业制烧碱的原理)。
CO2+2NaOH=== Na2CO3+H2O
SO2+2NaOH=== Na2SO3+H2O
CO2+Ca(OH)2=== CaCO3↓+H2O
SO2+Ca(OH)2=== CaSO3↓+H2O
Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH
同课章节目录
