2021年中考化学考点精讲基础知识(课件36页)
文档属性
| 名称 | 2021年中考化学考点精讲基础知识(课件36页) |
|
|
| 格式 | pptx | ||
| 文件大小 | 6.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-02 00:00:00 | ||
图片预览


文档简介
(共36张PPT)
考点精讲:基础知识
化学课件
编辑时间:2021-01-01
2020年度新制作的课件
【60】
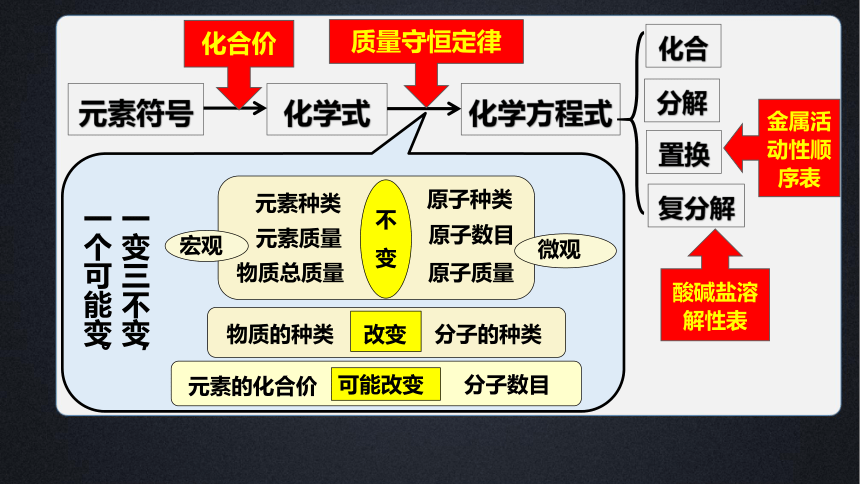
元素符号
化学式
化学方程式
化合价
质量守恒定律
化合
分解
置换
复分解
金属活动性顺序表
酸碱盐溶解性表
原子数目
原子质量
原子种类
微观
元素质量
元素种类
不
变
物质的种类
分子的种类
改变
可能改变
分子数目
元素的化合价
宏观
物质总质量
一变三不变,
一个可能变。
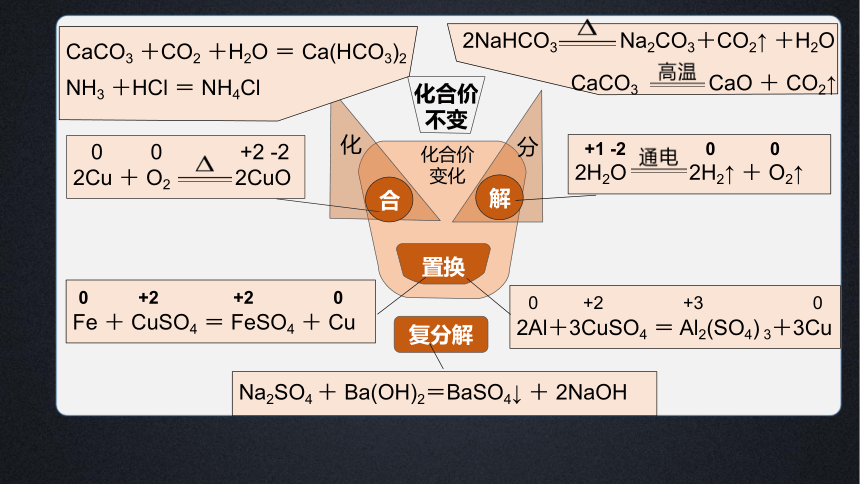
化合价
不变
置换
化合价
变化
复分解
合
化
解
分
CaCO3 +CO2 +H2O = Ca(HCO3)2
NH3 +HCl = NH4Cl
CaCO3 CaO + CO2↑
2NaHCO3 Na2CO3+CO2↑ +H2O
0 0 +2 -2
2Cu + O2 2CuO
+1 -2 0 0
2H2O 2H2↑ + O2↑
0 +2 +2 0
Fe + CuSO4 = FeSO4 + Cu
0 +2 +3 0
2Al+3CuSO4 = Al2(SO4) 3+3Cu
Na2SO4 + Ba(OH)2=BaSO4↓ + 2NaOH
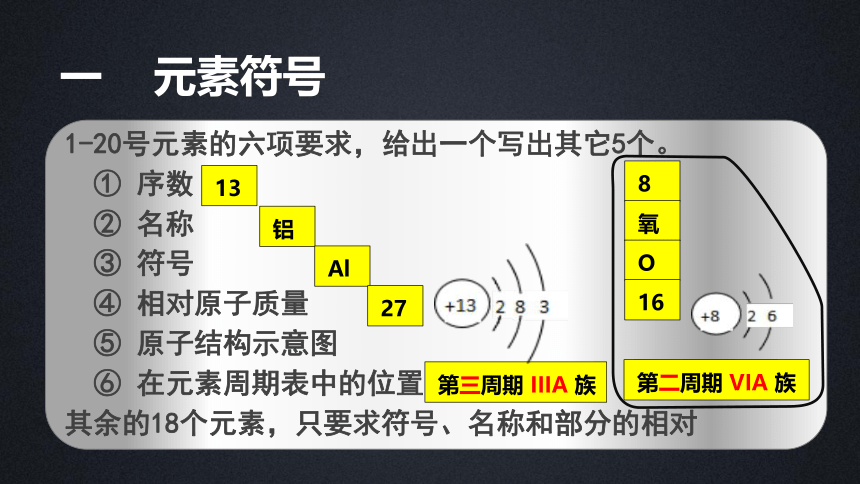
1-20号元素的六项要求,给出一个写出其它5个。
① 序数
② 名称
③ 符号
④ 相对原子质量
⑤ 原子结构示意图
⑥ 在元素周期表中的位置
其余的18个元素,只要求符号、名称和部分的相对
一 元素符号
13
铝
Al
27
第三周期 IIIA 族
第二周期 VIA 族
8
氧
O
16
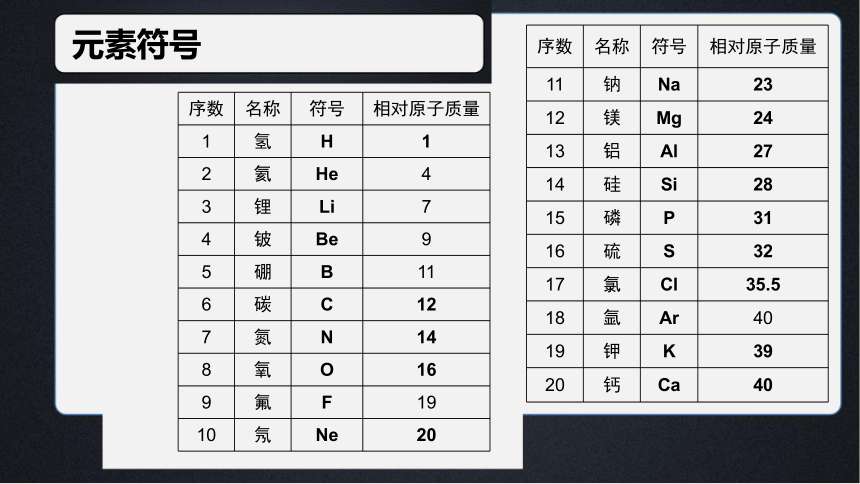
元素符号
序数 名称 符号 相对原子质量
1 氢 H 1
2 氦 He 4
3 锂 Li 7
4 铍 Be 9
5 硼 B 11
6 碳 C 12
7 氮 N 14
8 氧 O 16
9 氟 F 19
10 氖 Ne 20
序数 名称 符号 相对原子质量
11 钠 Na 23
12 镁 Mg 24
13 铝 Al 27
14 硅 Si 28
15 磷 P 31
16 硫 S 32
17 氯 Cl 35.5
18 氩 Ar 40
19 钾 K 39
20 钙 Ca 40
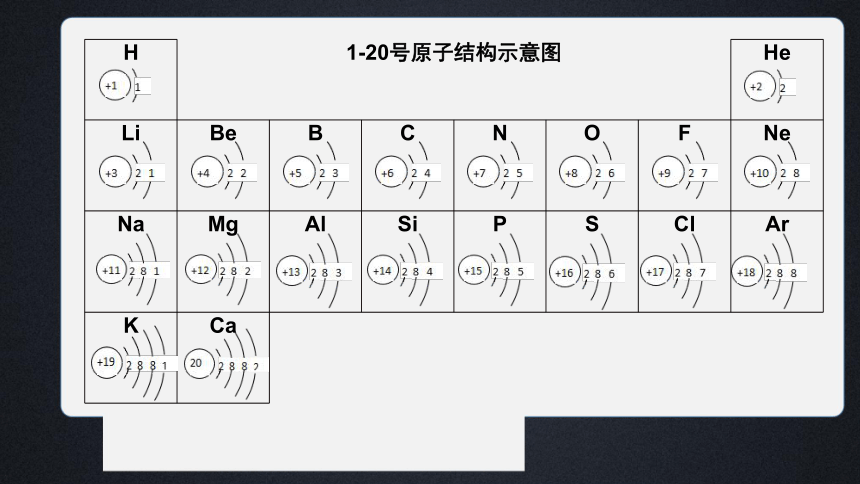
H 1-20号原子结构示意图 He
Li Be B C N O F Ne
Na Mg Al Si P S Cl Ar
K Ca
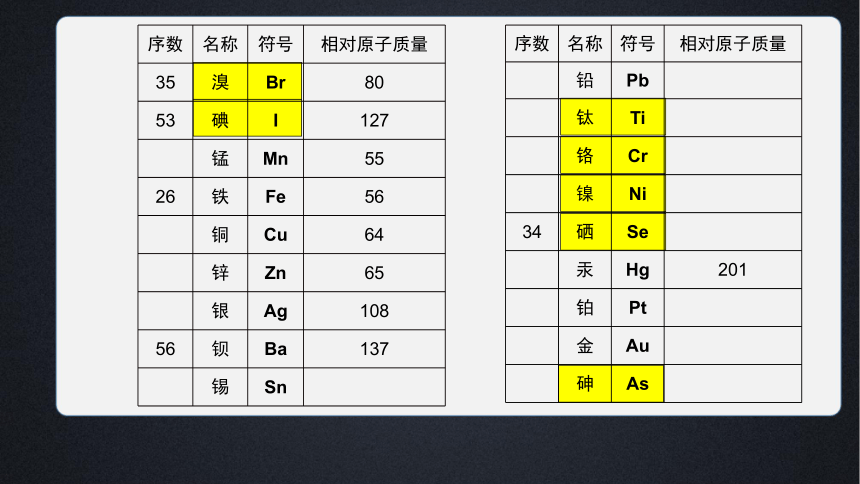
序数 名称 符号 相对原子质量
35 溴 Br 80
53 碘 I 127
锰 Mn 55
26 铁 Fe 56
铜 Cu 64
锌 Zn 65
银 Ag 108
56 钡 Ba 137
锡 Sn
序数 名称 符号 相对原子质量
铅 Pb
钛 Ti
铬 Cr
镍 Ni
34 硒 Se
汞 Hg 201
铂 Pt
金 Au
砷 As
1. 化合物中各元素化合价代数和为0,单质化合价为0。
2. 根据化合价代数和为0,可以求出元素的化合价。
3. 能根据给出的化合价,写出化合物的化学式。
4. 知道金属的化合价只有正价和0价,没有负价。
5. 常见变价元素如:Mn、Cl、S、C、N等
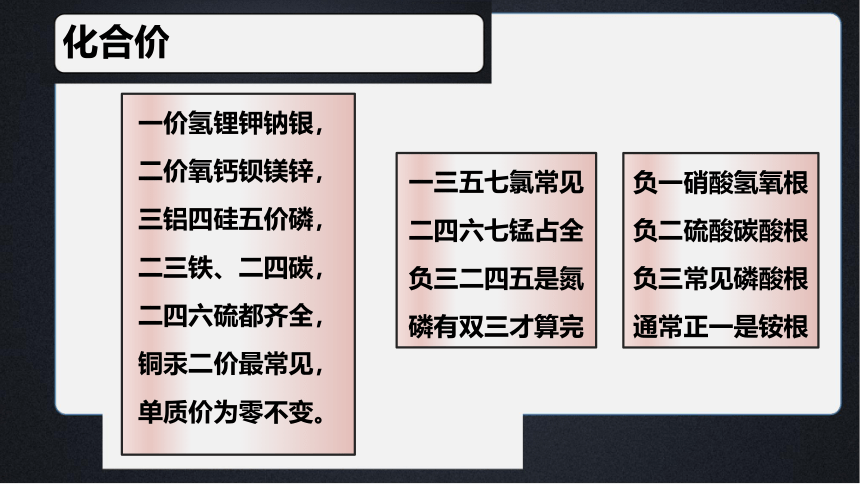
二 化合价
化合价
一三五七氯常见
二四六七锰占全
负三二四五是氮
磷有双三才算完
负一硝酸氢氧根
负二硫酸碳酸根
负三常见磷酸根
通常正一是铵根
一价氢锂钾钠银,
二价氧钙钡镁锌,
三铝四硅五价磷,
二三铁、二四碳,
二四六硫都齐全,
铜汞二价最常见,
单质价为零不变。
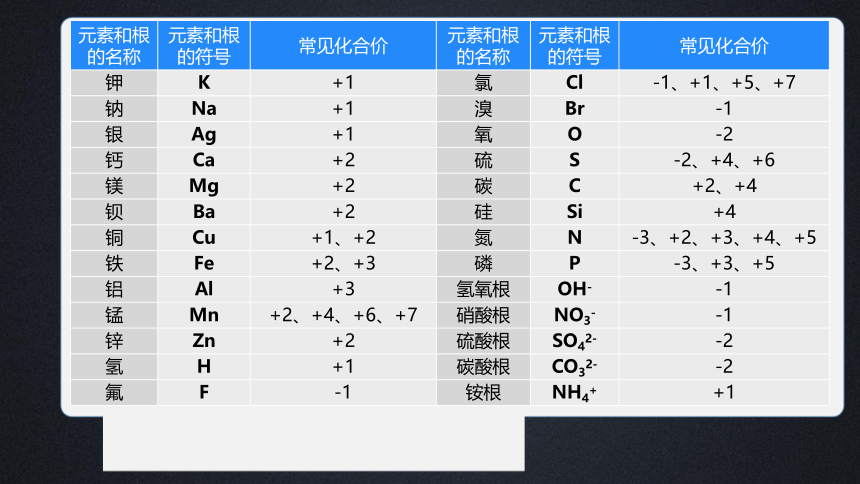
元素和根的名称 元素和根的符号 常见化合价 元素和根的名称 元素和根的符号 常见化合价
钾 K +1 氯 Cl -1、+1、+5、+7
钠 Na +1 溴 Br -1
银 Ag +1 氧 O -2
钙 Ca +2 硫 S -2、+4、+6
镁 Mg +2 碳 C +2、+4
钡 Ba +2 硅 Si +4
铜 Cu +1、+2 氮 N -3、+2、+3、+4、+5
铁 Fe +2、+3 磷 P -3、+3、+5
铝 Al +3 氢氧根 OH- -1
锰 Mn +2、+4、+6、+7 硝酸根 NO3- -1
锌 Zn +2 硫酸根 SO42- -2
氢 H +1 碳酸根 CO32- -2
氟 F -1 铵根 NH4+ +1
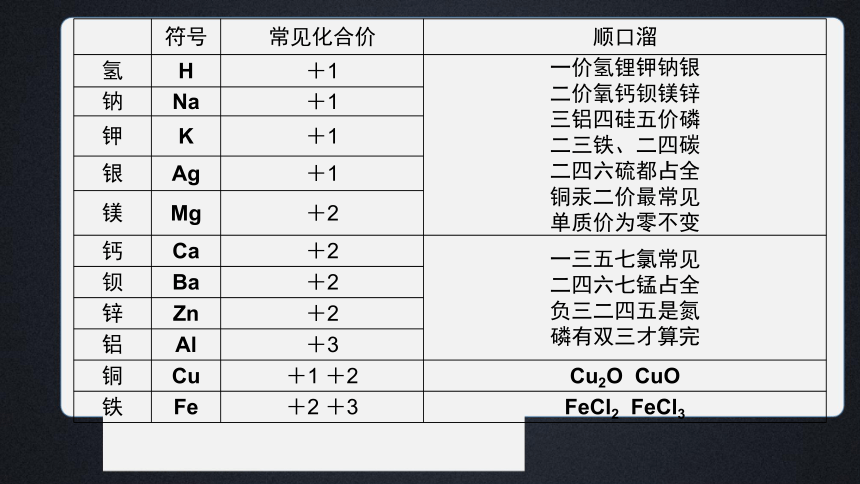
符号 常见化合价 顺口溜
氢 H +1 一价氢锂钾钠银
二价氧钙钡镁锌
三铝四硅五价磷
二三铁、二四碳
二四六硫都占全
铜汞二价最常见
单质价为零不变
钠 Na +1
钾 K +1
银 Ag +1
镁 Mg +2
钙 Ca +2 一三五七氯常见
二四六七锰占全
负三二四五是氮
磷有双三才算完
钡 Ba +2
锌 Zn +2
铝 Al +3
铜 Cu +1 +2 Cu2O CuO
铁 Fe +2 +3 FeCl2 FeCl3
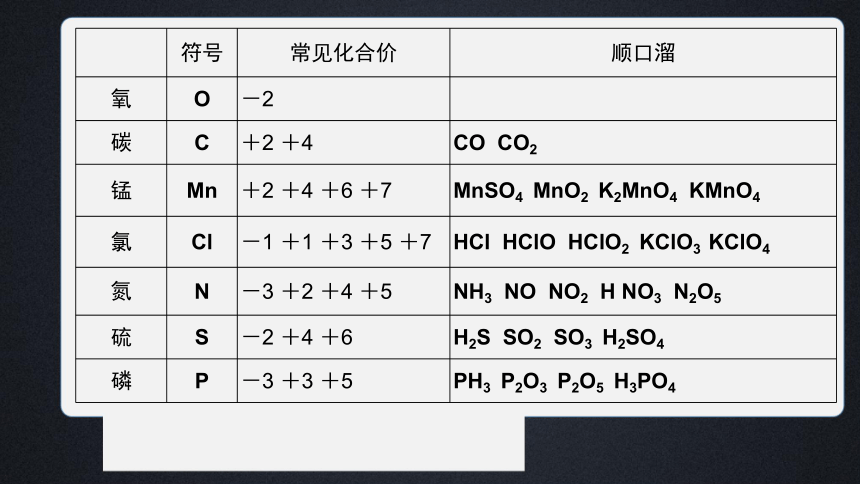
符号 常见化合价 顺口溜
氧 O -2
碳 C +2 +4 CO CO2
锰 Mn +2 +4 +6 +7 MnSO4 MnO2 K2MnO4 KMnO4
氯 Cl -1 +1 +3 +5 +7 HCl HClO HClO2 KClO3 KClO4
氮 N -3 +2 +4 +5 NH3 NO NO2 H NO3 N2O5
硫 S -2 +4 +6 H2S SO2 SO3 H2SO4
磷 P -3 +3 +5 PH3 P2O3 P2O5 H3PO4
符号 常见化合价 顺口溜
铵根 NH4+ +1 负一硝酸氢氧根
负二硫酸碳酸根
负三常见磷酸根
通常正一是铵根
硝酸根 NO3- -1
氢氧根 OH- -1
硫酸根 SO42- -2
碳酸根 CO32- -2
磷酸根 PO43- -3
1. 判断金属能否与酸反应生成H2。
2. 判断一种金属能否把另一种金属从其溶液中置换出来。
三 金属活动性顺序表
拼音 jiǎ gaì nà měi lǚ xīn tiě xī qiān qīng tóng gǒng yín bó jīn
名称 钾 钙 钠 镁 铝 锌 铁 锡 铅 氢 铜 汞 银 铂 金
符号 K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
顺口溜
金属活动性顺序表
嫁给那美女
新铁你嫌轻
统共一百斤
名称 钾钙钠镁铝 锌铁锡铅氢 铜汞银铂金
化合价 +2 +3 +2 +2 +1 +2 +2 +1
符号 K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
置换反应:
一种单质与一种化合物反应,生成另外一种单质和另一外种化合物的反应叫置换反应。
配平窍门:金属单质的化合价升高与盐溶液中金属离子化合价降低的总价数相等。
① 2-2 Mg + CuSO4 = Cu + MgSO4
② 1-2 Fe + 2AgNO3 = 2Ag + Fe(NO3) 2
③ 1-3 Al + 3AgNO3 = 3Ag + Al(NO3) 3
④ 2-3 2Al + 3CuSO4 = 3Cu + Al2(SO4) 3
活泼金属与稀酸的反应:活泼金属 + 稀酸 → 盐 + 氢气
001 镁与稀硫酸的反应 2-1 Mg + H2SO4 =MgSO4 + H2↑
002 铝与稀硫酸的反应 3-1 2Al + 3H2SO4 = Al2(SO4) 3+ 3H2↑
003 锌与稀硫酸的反应 2-1 Zn + H2SO4 = ZnSO4 + H2↑
004 铁与稀硫酸的反应 2-1 Fe + H2SO4 = FeSO4 + H2↑
(硫酸亚铁 Fe为+2价)
005 镁与稀盐酸的反应 2-1 Mg + 2HCl = MgCl2 + H2↑
006 铝与稀盐酸的反应 3-1 2Al + 6HCl = 2 AlCl3+ 3H2↑
007 锌与稀盐酸的反应 2-1 Zn + 2HCl = ZnCl2 + H2↑
008 铁与稀盐酸的反应 2-1 Fe + 2HCl = FeCl2 + H2↑
(氯化亚铁 Fe显+2价)
活泼金属与盐溶液的反应:活泼金属 + 盐 → 金属 + 另一种盐
009 铁丝放入硫酸铜溶液 2-2 Fe + CuSO4 = FeSO4 + Cu
010 镁条放入硫酸亚铁溶液 2-2 Mg + FeSO4 = MgSO4 + Fe
011 镁条放入硫酸铝溶液 2-3 3Mg + Al2(SO4) 3=3MgSO4+2Al
012 铝片放入硫酸铜溶液 3-2 2Al + 3CuSO4 = Al2(SO4) 3 + 3Cu
013 铜片放入硝酸银溶液 2-1 Cu + 2AgNO3 =Cu(NO3)2 + 2Ag
014 铝片放入硝酸银溶液 3-1 Al + 3AgNO3 = Al (NO3)3 + 3Ag
1. 判断酸碱盐中任意两种溶液能否发生反应。
2. 判断一种金属能否把另一种金属从其溶液中置换出来。
四 酸碱盐溶解性表
酸、碱、盐之间并不是都能发生复分解反应。只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
复分解反应发生的条件:生成物中有沉淀或气体或有水生成
H+ + OH- = H2O
2H+ + CO32- = H2O + CO2↑
Ba2+ + SO42- = BaSO4↓
离子的种类减少
复分解反应的本质:
碱
盐
四 酸碱盐溶解性表
OH- NO3- Cl- SO42- CO32-
H+ H2O HNO3 HCl H2SO4 H2CO3
NH4+ NH3 H2O
K+ KOH
… …
Ag+ Ba(OH)2
酸
水
CaSO4 MgCO3
Ca(OH)2 Ag2SO4
AgOH Al2(CO3)3
CuCO3 Fe2(CO3)3
硫酸钙、碳酸镁,
氢氧化钙硫酸银,
四个微溶要记会
红褐色Fe(OH)3
蓝色Cu(OH)2
钾钠铵盐硝酸盐,
易溶于水不沉淀。
盐酸盐不溶银亚汞,
硫酸盐不溶钡和铅。
部分酸碱盐的溶解性表记忆顺口溜
溶碱有五位,
钾钠铵钙钡。
其余多不溶,
红褐铁蓝铜。
氢氧化银碳酸铝,
碳酸铜和碳酸铁,
水溶液中不能存。
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
钾钠铵盐硝酸盐,
易溶于水不沉淀。
酸碱盐中只要含有
K+Na+NH4+NO3- 就一定是易溶于水的
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
盐酸盐不溶银亚汞,
硫酸盐不溶钡和铅。
除了AgCl↓ BaSO4↓
这两种既不溶于水也不溶于稀硝酸的白色沉淀,
其余的氯化物和硫酸盐都溶于水
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
硫酸钙、碳酸镁,
氢氧化钙硫酸银,
四个微溶要记会。
CaSO4
MgCO3
Ca(OH)2
Ag2SO4
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
氢氧化银碳酸铝,
碳酸铜和碳酸铁,
水溶液中不能存。
AgOH
Al2(CO3)3
CuCO3
Fe2(CO3)3
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
溶碱有五位,
钾钠铵钙钡。
其余多不溶,
红褐铁蓝铜。
红褐色Fe(OH)3
蓝色Cu(OH)2
OH- NO3- Cl- SO42- CO32-
H+ H2O HNO3 HCl H2SO4 H2CO3
NH4+ NH3 H2O NH4NO3 NH4Cl (NH4)2SO4 (NH4)2CO3
K+ KOH KNO3 KCl K2SO4 K2CO3
Na+ NaOH NaNO3 NaCl Na2SO4 Na2CO3
Ba2+ Ba(OH)2 Ba(NO3)2 BaCl2 BaSO4↓ BaCO3↓
Ca2+ Ca(OH)2微 Ca(NO3)2 CaCl2 CaSO4微 CaCO3↓
Mg2+ Mg(OH)2↓ Mg(NO3)2 MgCl2 MgSO4 MgCO3微
OH- NO3- Cl- SO42- CO32-
Al3+ Al(OH)3↓ Al(NO3)3 AlCl3 Al2(SO4)3 不存在
Mn2+ Mn(OH)2↓ Mn(NO3)2 MnCl2 MnSO4 MnCO3↓
Zn2+ Zn(OH)2↓ Zn(NO3)2 ZnCl2 ZnSO4 ZnCO3↓
Fe2+ Fe(OH)2↓ Fe(NO3)2 FeCl2 FeSO4 FeCO3↓
Fe3+ Fe(OH)3↓ Fe(NO3)3 FeCl3 Fe2(SO4)3 不存在
Cu2+ Cu(OH)2↓ Cu(NO3)2 CuCl2 CuSO4 不存在
Ag+ 不存在 AgNO3 AgCl↓ Ag2SO4微 Ag2CO3↓
Mg(OH)2↓
BaSO4↓
BaCO3↓
CaCO3↓
Al(OH)3↓
Fe(OH)3↓
Cu(OH)2↓
AgCl↓
常考的八大沉淀
治疗胃
酸过多
有颜色
的沉淀
既不溶于水,也不溶于酸。
不溶于水,可以溶于酸。
(一) 金属氧化物和酸反应:金属氧化物 + 酸 → 盐 + 水001 盐酸除锈 6HCl + Fe2O3 = 2FeCl3 + 3H2O002 硫酸除锈 3H2SO4 + Fe2O3=Fe2(SO4)3 + 3H2O003 氧化镁与盐酸 2HCl + MgO = MgCl2 + H2O004 氧化铝与硫酸 3H2SO4 + Al2O3 = Al2(SO4)3+ 3H2O005 氧化铜与硫酸 H2SO4 + CuO = CuSO4 + H2O006 氧化钙与硫酸 H2SO4 + CaO = CaSO4 + H2O
(二) 酸和碱反应:酸 + 碱→ 盐 + 水007 氢氧化钠溶液和稀盐酸反应 NaOH + HCl = NaCl +H2O008 氢氧化钠溶液和稀硫酸反应 2NaOH + H2SO4=Na2SO4 + 2H2O009 氢氧化钡溶液和稀硫酸反应 Ba(OH) 2+ H2SO4=BaSO4↓ + 2H2O010 氢氧化镁固体和稀硫酸反应 Mg(OH) 2+ H2SO4=MgSO4 + 2H2O011 氢氧化铜固体和稀盐酸反应 Cu(OH) 2+ 2HCl=CuCl2 + 2H2O012 氢氧化铁固体和稀盐酸反应 Fe(OH) 3+ 3HCl=Fe Cl3 + 3H2O013 氢氧化铝固体和稀硫酸反应 2Al(OH) 3+ 3H2SO4=Al2(SO4)3 +6H2O014 氢氧化铁固体和稀硫酸反应 2Fe(OH) 3+ 3H2SO4=Fe2(SO4)3 +6H2O
(三) 酸和盐反应:酸 + 盐→ 新酸 + 新盐015 盐酸和碳酸钙反应 2HCl + CaCO3=CaCl2 + CO2↑ +H2O016 盐酸和碳酸钠反应 2HCl + Na2CO3=2NaCl +CO2↑ +H2O017 盐酸和碳酸氢钠反应 HCl + NaHCO3= NaCl + CO2↑ +H2O018 硫酸和碳酸钠反应 H2SO4+Na2CO3=Na2SO4+CO2↑+H2O019 硫酸和碳酸氢钠反应 H2SO4+2NaHCO3=Na2SO4+2CO2↑+2H2O020 硝酸银和盐酸反应 HCl + AgNO3 = AgCl ↓ + HNO3021 硝酸钡和硫酸反应 Ba(NO3) 2+ H2SO4=BaSO4↓ + 2HNO3
(四) 碱和盐反应:碱 + 盐→ 新碱 + 新盐022 硫酸铜与氢氧化钠反应 CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4 023 氯化铁与氢氧化钠反应 FeCl3 +3NaOH = 3NaCl+Fe (OH)3↓024 硫酸钠与氢氧化钡反应 Na2SO4 + Ba(OH)2=BaSO4↓ + 2NaOH025 氢氧化钡和硫酸铁反应 Fe2(SO4)3+3Ba(OH)2=3BaSO4↓+2Fe(OH) 3↓026 碳酸钠与石灰水反应 Na2CO3+ Ca(OH)2 =CaCO3↓+ 2NaOH027 硫酸铵与熟石灰反应 (NH4)2SO4+Ca(OH)2 CaSO4+2NH3↑+2H2O028 氯化铵与熟石灰反应 2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O029 氯化镁与氢氧化钠反应 MgCl2 + 2NaOH = Mg (OH)2↓+ 2NaCl030 制波尔多液 CuSO4 +Ca(OH)2 = Ca SO4 + Cu(OH)2↓
(五)盐和盐反应:盐 + 盐→ 新盐1 + 新盐2031 氯化钠溶液与硝酸银溶液反应 NaCl+ AgNO3 = AgCl ↓+NaNO3032 硫酸铜溶液和氯化钡溶液反应 CuSO4 +BaCl2=BaSO4↓+CuCl2033 氯化钙溶液与碳酸钠溶液反应 CaCl2 +Na2CO3=CaCO3↓+2NaCl034 氯化钡溶液与硫酸钠溶液反应 BaCl2 +Na2SO4=BaSO4↓+2NaCl
考点精讲:基础知识
化学课件
编辑时间:2021-01-01
2020年度新制作的课件
【60】
元素符号
化学式
化学方程式
化合价
质量守恒定律
化合
分解
置换
复分解
金属活动性顺序表
酸碱盐溶解性表
原子数目
原子质量
原子种类
微观
元素质量
元素种类
不
变
物质的种类
分子的种类
改变
可能改变
分子数目
元素的化合价
宏观
物质总质量
一变三不变,
一个可能变。
化合价
不变
置换
化合价
变化
复分解
合
化
解
分
CaCO3 +CO2 +H2O = Ca(HCO3)2
NH3 +HCl = NH4Cl
CaCO3 CaO + CO2↑
2NaHCO3 Na2CO3+CO2↑ +H2O
0 0 +2 -2
2Cu + O2 2CuO
+1 -2 0 0
2H2O 2H2↑ + O2↑
0 +2 +2 0
Fe + CuSO4 = FeSO4 + Cu
0 +2 +3 0
2Al+3CuSO4 = Al2(SO4) 3+3Cu
Na2SO4 + Ba(OH)2=BaSO4↓ + 2NaOH
1-20号元素的六项要求,给出一个写出其它5个。
① 序数
② 名称
③ 符号
④ 相对原子质量
⑤ 原子结构示意图
⑥ 在元素周期表中的位置
其余的18个元素,只要求符号、名称和部分的相对
一 元素符号
13
铝
Al
27
第三周期 IIIA 族
第二周期 VIA 族
8
氧
O
16
元素符号
序数 名称 符号 相对原子质量
1 氢 H 1
2 氦 He 4
3 锂 Li 7
4 铍 Be 9
5 硼 B 11
6 碳 C 12
7 氮 N 14
8 氧 O 16
9 氟 F 19
10 氖 Ne 20
序数 名称 符号 相对原子质量
11 钠 Na 23
12 镁 Mg 24
13 铝 Al 27
14 硅 Si 28
15 磷 P 31
16 硫 S 32
17 氯 Cl 35.5
18 氩 Ar 40
19 钾 K 39
20 钙 Ca 40
H 1-20号原子结构示意图 He
Li Be B C N O F Ne
Na Mg Al Si P S Cl Ar
K Ca
序数 名称 符号 相对原子质量
35 溴 Br 80
53 碘 I 127
锰 Mn 55
26 铁 Fe 56
铜 Cu 64
锌 Zn 65
银 Ag 108
56 钡 Ba 137
锡 Sn
序数 名称 符号 相对原子质量
铅 Pb
钛 Ti
铬 Cr
镍 Ni
34 硒 Se
汞 Hg 201
铂 Pt
金 Au
砷 As
1. 化合物中各元素化合价代数和为0,单质化合价为0。
2. 根据化合价代数和为0,可以求出元素的化合价。
3. 能根据给出的化合价,写出化合物的化学式。
4. 知道金属的化合价只有正价和0价,没有负价。
5. 常见变价元素如:Mn、Cl、S、C、N等
二 化合价
化合价
一三五七氯常见
二四六七锰占全
负三二四五是氮
磷有双三才算完
负一硝酸氢氧根
负二硫酸碳酸根
负三常见磷酸根
通常正一是铵根
一价氢锂钾钠银,
二价氧钙钡镁锌,
三铝四硅五价磷,
二三铁、二四碳,
二四六硫都齐全,
铜汞二价最常见,
单质价为零不变。
元素和根的名称 元素和根的符号 常见化合价 元素和根的名称 元素和根的符号 常见化合价
钾 K +1 氯 Cl -1、+1、+5、+7
钠 Na +1 溴 Br -1
银 Ag +1 氧 O -2
钙 Ca +2 硫 S -2、+4、+6
镁 Mg +2 碳 C +2、+4
钡 Ba +2 硅 Si +4
铜 Cu +1、+2 氮 N -3、+2、+3、+4、+5
铁 Fe +2、+3 磷 P -3、+3、+5
铝 Al +3 氢氧根 OH- -1
锰 Mn +2、+4、+6、+7 硝酸根 NO3- -1
锌 Zn +2 硫酸根 SO42- -2
氢 H +1 碳酸根 CO32- -2
氟 F -1 铵根 NH4+ +1
符号 常见化合价 顺口溜
氢 H +1 一价氢锂钾钠银
二价氧钙钡镁锌
三铝四硅五价磷
二三铁、二四碳
二四六硫都占全
铜汞二价最常见
单质价为零不变
钠 Na +1
钾 K +1
银 Ag +1
镁 Mg +2
钙 Ca +2 一三五七氯常见
二四六七锰占全
负三二四五是氮
磷有双三才算完
钡 Ba +2
锌 Zn +2
铝 Al +3
铜 Cu +1 +2 Cu2O CuO
铁 Fe +2 +3 FeCl2 FeCl3
符号 常见化合价 顺口溜
氧 O -2
碳 C +2 +4 CO CO2
锰 Mn +2 +4 +6 +7 MnSO4 MnO2 K2MnO4 KMnO4
氯 Cl -1 +1 +3 +5 +7 HCl HClO HClO2 KClO3 KClO4
氮 N -3 +2 +4 +5 NH3 NO NO2 H NO3 N2O5
硫 S -2 +4 +6 H2S SO2 SO3 H2SO4
磷 P -3 +3 +5 PH3 P2O3 P2O5 H3PO4
符号 常见化合价 顺口溜
铵根 NH4+ +1 负一硝酸氢氧根
负二硫酸碳酸根
负三常见磷酸根
通常正一是铵根
硝酸根 NO3- -1
氢氧根 OH- -1
硫酸根 SO42- -2
碳酸根 CO32- -2
磷酸根 PO43- -3
1. 判断金属能否与酸反应生成H2。
2. 判断一种金属能否把另一种金属从其溶液中置换出来。
三 金属活动性顺序表
拼音 jiǎ gaì nà měi lǚ xīn tiě xī qiān qīng tóng gǒng yín bó jīn
名称 钾 钙 钠 镁 铝 锌 铁 锡 铅 氢 铜 汞 银 铂 金
符号 K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
顺口溜
金属活动性顺序表
嫁给那美女
新铁你嫌轻
统共一百斤
名称 钾钙钠镁铝 锌铁锡铅氢 铜汞银铂金
化合价 +2 +3 +2 +2 +1 +2 +2 +1
符号 K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au
置换反应:
一种单质与一种化合物反应,生成另外一种单质和另一外种化合物的反应叫置换反应。
配平窍门:金属单质的化合价升高与盐溶液中金属离子化合价降低的总价数相等。
① 2-2 Mg + CuSO4 = Cu + MgSO4
② 1-2 Fe + 2AgNO3 = 2Ag + Fe(NO3) 2
③ 1-3 Al + 3AgNO3 = 3Ag + Al(NO3) 3
④ 2-3 2Al + 3CuSO4 = 3Cu + Al2(SO4) 3
活泼金属与稀酸的反应:活泼金属 + 稀酸 → 盐 + 氢气
001 镁与稀硫酸的反应 2-1 Mg + H2SO4 =MgSO4 + H2↑
002 铝与稀硫酸的反应 3-1 2Al + 3H2SO4 = Al2(SO4) 3+ 3H2↑
003 锌与稀硫酸的反应 2-1 Zn + H2SO4 = ZnSO4 + H2↑
004 铁与稀硫酸的反应 2-1 Fe + H2SO4 = FeSO4 + H2↑
(硫酸亚铁 Fe为+2价)
005 镁与稀盐酸的反应 2-1 Mg + 2HCl = MgCl2 + H2↑
006 铝与稀盐酸的反应 3-1 2Al + 6HCl = 2 AlCl3+ 3H2↑
007 锌与稀盐酸的反应 2-1 Zn + 2HCl = ZnCl2 + H2↑
008 铁与稀盐酸的反应 2-1 Fe + 2HCl = FeCl2 + H2↑
(氯化亚铁 Fe显+2价)
活泼金属与盐溶液的反应:活泼金属 + 盐 → 金属 + 另一种盐
009 铁丝放入硫酸铜溶液 2-2 Fe + CuSO4 = FeSO4 + Cu
010 镁条放入硫酸亚铁溶液 2-2 Mg + FeSO4 = MgSO4 + Fe
011 镁条放入硫酸铝溶液 2-3 3Mg + Al2(SO4) 3=3MgSO4+2Al
012 铝片放入硫酸铜溶液 3-2 2Al + 3CuSO4 = Al2(SO4) 3 + 3Cu
013 铜片放入硝酸银溶液 2-1 Cu + 2AgNO3 =Cu(NO3)2 + 2Ag
014 铝片放入硝酸银溶液 3-1 Al + 3AgNO3 = Al (NO3)3 + 3Ag
1. 判断酸碱盐中任意两种溶液能否发生反应。
2. 判断一种金属能否把另一种金属从其溶液中置换出来。
四 酸碱盐溶解性表
酸、碱、盐之间并不是都能发生复分解反应。只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
复分解反应发生的条件:生成物中有沉淀或气体或有水生成
H+ + OH- = H2O
2H+ + CO32- = H2O + CO2↑
Ba2+ + SO42- = BaSO4↓
离子的种类减少
复分解反应的本质:
碱
盐
四 酸碱盐溶解性表
OH- NO3- Cl- SO42- CO32-
H+ H2O HNO3 HCl H2SO4 H2CO3
NH4+ NH3 H2O
K+ KOH
… …
Ag+ Ba(OH)2
酸
水
CaSO4 MgCO3
Ca(OH)2 Ag2SO4
AgOH Al2(CO3)3
CuCO3 Fe2(CO3)3
硫酸钙、碳酸镁,
氢氧化钙硫酸银,
四个微溶要记会
红褐色Fe(OH)3
蓝色Cu(OH)2
钾钠铵盐硝酸盐,
易溶于水不沉淀。
盐酸盐不溶银亚汞,
硫酸盐不溶钡和铅。
部分酸碱盐的溶解性表记忆顺口溜
溶碱有五位,
钾钠铵钙钡。
其余多不溶,
红褐铁蓝铜。
氢氧化银碳酸铝,
碳酸铜和碳酸铁,
水溶液中不能存。
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
钾钠铵盐硝酸盐,
易溶于水不沉淀。
酸碱盐中只要含有
K+Na+NH4+NO3- 就一定是易溶于水的
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
盐酸盐不溶银亚汞,
硫酸盐不溶钡和铅。
除了AgCl↓ BaSO4↓
这两种既不溶于水也不溶于稀硝酸的白色沉淀,
其余的氯化物和硫酸盐都溶于水
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
硫酸钙、碳酸镁,
氢氧化钙硫酸银,
四个微溶要记会。
CaSO4
MgCO3
Ca(OH)2
Ag2SO4
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
氢氧化银碳酸铝,
碳酸铜和碳酸铁,
水溶液中不能存。
AgOH
Al2(CO3)3
CuCO3
Fe2(CO3)3
OH- NO3- Cl- SO42- CO32-
H+ H2O 溶挥 溶挥 溶 溶挥
NH4+ 溶 溶 溶 溶 溶
K+ 溶 溶 溶 溶 溶
Na+ 溶 溶 溶 溶 溶
Ba2+ 溶 溶 溶 BaSO4↓ 白↓
Ca2+ 微溶 溶 溶 微溶 白↓
Mg2+ 白↓ 溶 溶 溶 微溶
OH- NO3- Cl- SO42- CO32-
Al3+ 白↓ 溶 溶 溶 不存在
Mn2+ ↓ 溶 溶 溶 ↓
Zn2+ 白↓ 溶 溶 溶 ↓
Fe2+ 白↓ 溶浅绿 溶浅绿 溶浅绿 ↓
Fe3+ 红褐↓ 溶、黄 溶、黄 溶、黄 不存在
Cu2+ 蓝色↓ 溶、蓝 溶、蓝 溶、蓝 不存在
Ag+ 不存在 溶 AgCl↓ 微溶 ↓
溶碱有五位,
钾钠铵钙钡。
其余多不溶,
红褐铁蓝铜。
红褐色Fe(OH)3
蓝色Cu(OH)2
OH- NO3- Cl- SO42- CO32-
H+ H2O HNO3 HCl H2SO4 H2CO3
NH4+ NH3 H2O NH4NO3 NH4Cl (NH4)2SO4 (NH4)2CO3
K+ KOH KNO3 KCl K2SO4 K2CO3
Na+ NaOH NaNO3 NaCl Na2SO4 Na2CO3
Ba2+ Ba(OH)2 Ba(NO3)2 BaCl2 BaSO4↓ BaCO3↓
Ca2+ Ca(OH)2微 Ca(NO3)2 CaCl2 CaSO4微 CaCO3↓
Mg2+ Mg(OH)2↓ Mg(NO3)2 MgCl2 MgSO4 MgCO3微
OH- NO3- Cl- SO42- CO32-
Al3+ Al(OH)3↓ Al(NO3)3 AlCl3 Al2(SO4)3 不存在
Mn2+ Mn(OH)2↓ Mn(NO3)2 MnCl2 MnSO4 MnCO3↓
Zn2+ Zn(OH)2↓ Zn(NO3)2 ZnCl2 ZnSO4 ZnCO3↓
Fe2+ Fe(OH)2↓ Fe(NO3)2 FeCl2 FeSO4 FeCO3↓
Fe3+ Fe(OH)3↓ Fe(NO3)3 FeCl3 Fe2(SO4)3 不存在
Cu2+ Cu(OH)2↓ Cu(NO3)2 CuCl2 CuSO4 不存在
Ag+ 不存在 AgNO3 AgCl↓ Ag2SO4微 Ag2CO3↓
Mg(OH)2↓
BaSO4↓
BaCO3↓
CaCO3↓
Al(OH)3↓
Fe(OH)3↓
Cu(OH)2↓
AgCl↓
常考的八大沉淀
治疗胃
酸过多
有颜色
的沉淀
既不溶于水,也不溶于酸。
不溶于水,可以溶于酸。
(一) 金属氧化物和酸反应:金属氧化物 + 酸 → 盐 + 水001 盐酸除锈 6HCl + Fe2O3 = 2FeCl3 + 3H2O002 硫酸除锈 3H2SO4 + Fe2O3=Fe2(SO4)3 + 3H2O003 氧化镁与盐酸 2HCl + MgO = MgCl2 + H2O004 氧化铝与硫酸 3H2SO4 + Al2O3 = Al2(SO4)3+ 3H2O005 氧化铜与硫酸 H2SO4 + CuO = CuSO4 + H2O006 氧化钙与硫酸 H2SO4 + CaO = CaSO4 + H2O
(二) 酸和碱反应:酸 + 碱→ 盐 + 水007 氢氧化钠溶液和稀盐酸反应 NaOH + HCl = NaCl +H2O008 氢氧化钠溶液和稀硫酸反应 2NaOH + H2SO4=Na2SO4 + 2H2O009 氢氧化钡溶液和稀硫酸反应 Ba(OH) 2+ H2SO4=BaSO4↓ + 2H2O010 氢氧化镁固体和稀硫酸反应 Mg(OH) 2+ H2SO4=MgSO4 + 2H2O011 氢氧化铜固体和稀盐酸反应 Cu(OH) 2+ 2HCl=CuCl2 + 2H2O012 氢氧化铁固体和稀盐酸反应 Fe(OH) 3+ 3HCl=Fe Cl3 + 3H2O013 氢氧化铝固体和稀硫酸反应 2Al(OH) 3+ 3H2SO4=Al2(SO4)3 +6H2O014 氢氧化铁固体和稀硫酸反应 2Fe(OH) 3+ 3H2SO4=Fe2(SO4)3 +6H2O
(三) 酸和盐反应:酸 + 盐→ 新酸 + 新盐015 盐酸和碳酸钙反应 2HCl + CaCO3=CaCl2 + CO2↑ +H2O016 盐酸和碳酸钠反应 2HCl + Na2CO3=2NaCl +CO2↑ +H2O017 盐酸和碳酸氢钠反应 HCl + NaHCO3= NaCl + CO2↑ +H2O018 硫酸和碳酸钠反应 H2SO4+Na2CO3=Na2SO4+CO2↑+H2O019 硫酸和碳酸氢钠反应 H2SO4+2NaHCO3=Na2SO4+2CO2↑+2H2O020 硝酸银和盐酸反应 HCl + AgNO3 = AgCl ↓ + HNO3021 硝酸钡和硫酸反应 Ba(NO3) 2+ H2SO4=BaSO4↓ + 2HNO3
(四) 碱和盐反应:碱 + 盐→ 新碱 + 新盐022 硫酸铜与氢氧化钠反应 CuSO4 + 2NaOH = Cu(OH)2↓+ Na2SO4 023 氯化铁与氢氧化钠反应 FeCl3 +3NaOH = 3NaCl+Fe (OH)3↓024 硫酸钠与氢氧化钡反应 Na2SO4 + Ba(OH)2=BaSO4↓ + 2NaOH025 氢氧化钡和硫酸铁反应 Fe2(SO4)3+3Ba(OH)2=3BaSO4↓+2Fe(OH) 3↓026 碳酸钠与石灰水反应 Na2CO3+ Ca(OH)2 =CaCO3↓+ 2NaOH027 硫酸铵与熟石灰反应 (NH4)2SO4+Ca(OH)2 CaSO4+2NH3↑+2H2O028 氯化铵与熟石灰反应 2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O029 氯化镁与氢氧化钠反应 MgCl2 + 2NaOH = Mg (OH)2↓+ 2NaCl030 制波尔多液 CuSO4 +Ca(OH)2 = Ca SO4 + Cu(OH)2↓
(五)盐和盐反应:盐 + 盐→ 新盐1 + 新盐2031 氯化钠溶液与硝酸银溶液反应 NaCl+ AgNO3 = AgCl ↓+NaNO3032 硫酸铜溶液和氯化钡溶液反应 CuSO4 +BaCl2=BaSO4↓+CuCl2033 氯化钙溶液与碳酸钠溶液反应 CaCl2 +Na2CO3=CaCO3↓+2NaCl034 氯化钡溶液与硫酸钠溶液反应 BaCl2 +Na2SO4=BaSO4↓+2NaCl
同课章节目录
