2013届中考化学考前热点聚焦《第6课时 构成物质的基本微粒》(单课考点聚焦+热考精讲+知识点归类)课件 沪教版
文档属性
| 名称 | 2013届中考化学考前热点聚焦《第6课时 构成物质的基本微粒》(单课考点聚焦+热考精讲+知识点归类)课件 沪教版 |

|
|
| 格式 | zip | ||
| 文件大小 | 499.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-05-03 00:00:00 | ||
图片预览







文档简介
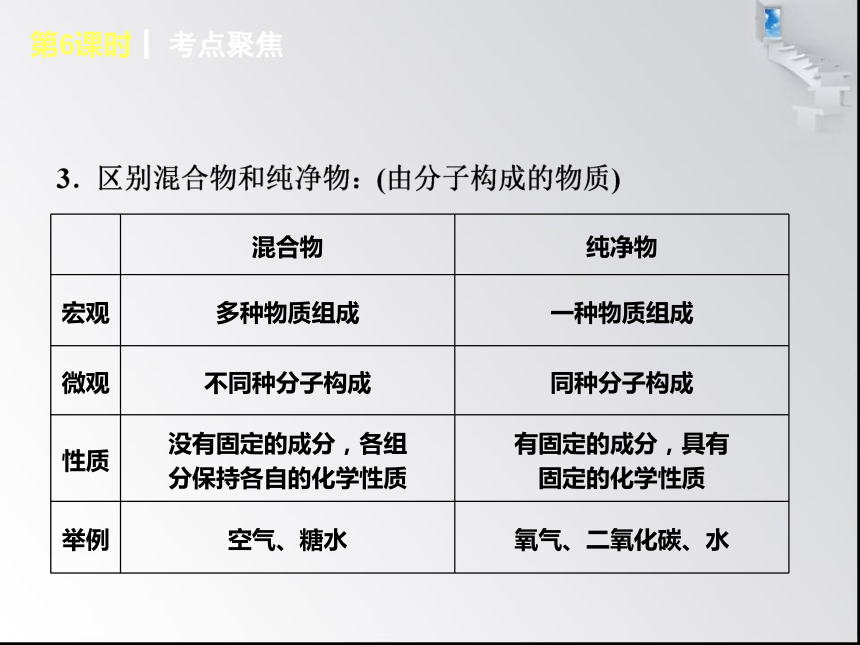
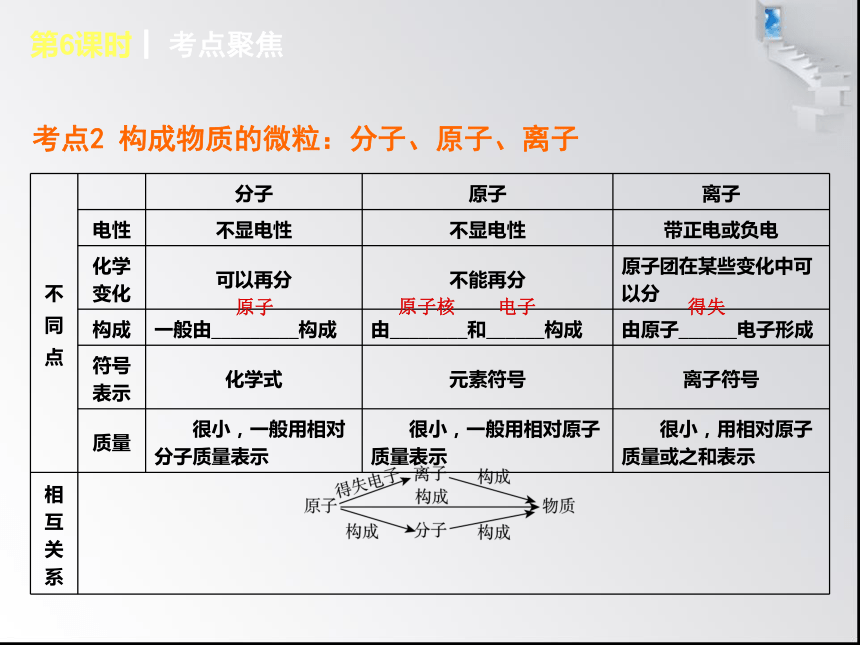
课件25张PPT。第3章 物质构成的奥秘第6课时┃ 构成物质的基本微粒第6课时 构成物质的基本微粒第6课时┃ 考点聚焦考点1 微粒的性质及应用第6课时┃ 考点聚焦第6课时┃ 考点聚焦第6课时┃ 考点聚焦考点2 构成物质的微粒:分子、原子、离子原子原子核电子得失第6课时┃ 考点聚焦第6课时┃ 考点聚焦考点3 原子的结构及相对原子质量原子核质子 正电荷 中子 电子 负电荷质子数电子数第6课时┃ 考点聚焦碳原子这一基准的比第6课时┃ 考点聚焦图6-1 第6课时┃ 考点聚焦考点4 核外电子的分层排布 分层排布失去 阳离子 得到 阴离子 相对稳定结构第6课时┃ 归类示例? 类型一 微粒的性质命题角度:用微粒的知识解释生活中的现象。 D第6课时┃ 归类示例 [解析] 题中能闻到梅花香味很显然与分子的性质有关,而解释相关现象用得较多的就是:分子之间有间隔和分子在不断地运动。因此,不难得出本题反映了分子在不停地运动这一性质。 [方法点拨]借助于古诗词或信息类知识来进行考查,其中给材料的考题一般我们称之为信息题,往往会通过一些科技前沿或实际生活内容的信息来进行考查。这些都是中考试题中考查分子性质(主要以分子不停地运动、分子间有间隔这两点性质为主)的常用载体,只要把握好试题的考查点,理解分子的性质,不难解答。这类试题的特点是起点高,落点低,解答时应“依据教材、合理联系”,因为最终解答时仍然需要用教材的知识点来完成。 变式题 下列对一些事实的微观解释错误的是 ( )第6课时┃ 归类示例A第6课时┃ 归类示例 [解析] 分子、原子都是①很小(质量小、体积小);②不断运动,温度越高运动越快;③有间隔的粒子。人们能闻到花香是由于分子不断运动的结果;自行车胎容易爆裂是在高温下分子运动加剧,分子间间隔变大的结果;化学变化都能说明分子的可分性,水的分解是化学变化;热胀冷缩现象产生的原因是构成物质的粒子间间隔变化的结果,架在高处的电线夏季变得比冬季长就是热胀冷缩现象,电线是金属材料,由金属原子直接构成的。第6课时┃ 归类示例? 类型二 构成物质的微粒 例2 分子、原子、离子都是构成物质的微粒。下列由原子直接构成的是 ( )
A.铜 B.氧气
C.氯化钠 D.二氧化碳命题角度:考查构成物质的微粒。 [解析] 铜由原子构成,氧气、二氧化碳由分子构成,氯化钠由离子构成。 A第6课时┃ 归类示例 [方法点拨]物质可以由分子、原子、离子构成,由原子直接构成的如铜、铁、钙、金刚石、硅、稀有气体等;由分子构成的如氧气、二氧化碳、酒精等;由离子构成的如食盐、氢氧化钠等。其中,如果是由分子或原子构成的,则构成物质的粒子肯定是同一种,而由离子构成的,至少有一种阳离子和一种阴离子,以氯化钠为例,不能错误地描述为“氯化钠由氯化钠离子构成”,而应该是由氯离子和钠离子
构成。第6课时┃ 归类示例 变式题 [2010·上海] (1)构成物质的微粒有分子、原子、离子。水由______构成,铁由______构成,氯化钠由______构成(填“分子”“原子”或“离子”)。
(2)金刚石和石墨都是由碳原子构成的,但它们的物理性质不同,是由于__________________不同。
(3)糖是甜的,辣椒是辣的,说明____________________
_________________________________。分子原子离子碳原子的排列方式分子的种类不同,物质的性质不同第6课时┃ 归类示例? 类型三 原子的结构 命题角度:熟悉原子的内部结构,同时认识一些特殊的原子结构。 D第6课时┃ 归类示例 [方法点拨]原子由原子核和核外电子构成,一般情况下,原子核由质子和中子构成。但也有特例,如氢原子的原子核只有质子而没有中子。第6课时┃ 归类示例 变式题 科学家设想宇宙中可能存在完全由反粒子构成的物质——反物质。物质与反物质相遇会释放出巨大的能量,在能源研究领域中前景可观,正电子、负质子等都是反粒子,它们与通常所说的电子、质子相比较,质量相等但电性相反。请你推测,反氢原子的结构可能是 ( )
A.由1个带正电荷的质子和1个带负电荷的电子构成
B.由1个带负电荷的质子和1个带正电荷的电子构成
C.由1个带正电荷的质子和1个带正电荷的电子构成
D.由1个带负电荷的质子和1个带负电荷的电子构成B第6课时┃ 归类示例? 类型四 核外电子的分层排布 命题角度:考查原子结构示意图、原子与离子的识别。D第6课时┃ 归类示例 [解析]选项A、B、C的原子结构示意图的最外层电子数都大于4个,因此它们均不属于金属元素。 [方法点拨]了解原子结构中最外层电子数与元素类别的关系:一般金属元素原子最外层电子数小于4个,非金属元素原子最外层电子数大于4个,稀有气体元素原子的最外层电子数为2个或8个。第6课时┃ 归类示例D [解析] 在原子结构示意图中,一般最外层电子数小于4的为金属元素,最外层电子数大于4的为非金属元素,最外层电子数等于2或8的为稀有气体元素,若不是原子结构示意图时要将其转化为原子结构示意图之后再去加以判断。谢谢合作 再见
A.铜 B.氧气
C.氯化钠 D.二氧化碳命题角度:考查构成物质的微粒。 [解析] 铜由原子构成,氧气、二氧化碳由分子构成,氯化钠由离子构成。 A第6课时┃ 归类示例 [方法点拨]物质可以由分子、原子、离子构成,由原子直接构成的如铜、铁、钙、金刚石、硅、稀有气体等;由分子构成的如氧气、二氧化碳、酒精等;由离子构成的如食盐、氢氧化钠等。其中,如果是由分子或原子构成的,则构成物质的粒子肯定是同一种,而由离子构成的,至少有一种阳离子和一种阴离子,以氯化钠为例,不能错误地描述为“氯化钠由氯化钠离子构成”,而应该是由氯离子和钠离子
构成。第6课时┃ 归类示例 变式题 [2010·上海] (1)构成物质的微粒有分子、原子、离子。水由______构成,铁由______构成,氯化钠由______构成(填“分子”“原子”或“离子”)。
(2)金刚石和石墨都是由碳原子构成的,但它们的物理性质不同,是由于__________________不同。
(3)糖是甜的,辣椒是辣的,说明____________________
_________________________________。分子原子离子碳原子的排列方式分子的种类不同,物质的性质不同第6课时┃ 归类示例? 类型三 原子的结构 命题角度:熟悉原子的内部结构,同时认识一些特殊的原子结构。 D第6课时┃ 归类示例 [方法点拨]原子由原子核和核外电子构成,一般情况下,原子核由质子和中子构成。但也有特例,如氢原子的原子核只有质子而没有中子。第6课时┃ 归类示例 变式题 科学家设想宇宙中可能存在完全由反粒子构成的物质——反物质。物质与反物质相遇会释放出巨大的能量,在能源研究领域中前景可观,正电子、负质子等都是反粒子,它们与通常所说的电子、质子相比较,质量相等但电性相反。请你推测,反氢原子的结构可能是 ( )
A.由1个带正电荷的质子和1个带负电荷的电子构成
B.由1个带负电荷的质子和1个带正电荷的电子构成
C.由1个带正电荷的质子和1个带正电荷的电子构成
D.由1个带负电荷的质子和1个带负电荷的电子构成B第6课时┃ 归类示例? 类型四 核外电子的分层排布 命题角度:考查原子结构示意图、原子与离子的识别。D第6课时┃ 归类示例 [解析]选项A、B、C的原子结构示意图的最外层电子数都大于4个,因此它们均不属于金属元素。 [方法点拨]了解原子结构中最外层电子数与元素类别的关系:一般金属元素原子最外层电子数小于4个,非金属元素原子最外层电子数大于4个,稀有气体元素原子的最外层电子数为2个或8个。第6课时┃ 归类示例D [解析] 在原子结构示意图中,一般最外层电子数小于4的为金属元素,最外层电子数大于4的为非金属元素,最外层电子数等于2或8的为稀有气体元素,若不是原子结构示意图时要将其转化为原子结构示意图之后再去加以判断。谢谢合作 再见
同课章节目录
