2022年人教版化学九年级(下)第11单元 盐 化肥课后习题(word版 含答案)
文档属性
| 名称 | 2022年人教版化学九年级(下)第11单元 盐 化肥课后习题(word版 含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 339.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-03 21:42:30 | ||
图片预览


文档简介
2022春人教化学九(下)第11单元 盐 化肥课后习题含答案
一、选择题。
1、下列各组物质能在pH=1的无色溶液中大量共存的是( )
A. K2SO4 Ba(OH)2 KCl B. Cu( NO3)2 NaCl KNO3
C. Na2CO3KNO3NH4Cl D. MgSO4 NaNO3KCl
2、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
3、我国某地曾发生过把外形和食盐相似,有咸味的工业用盐误作食盐,食用后发生中毒事件,这种工业用盐可能含有的有毒物质是 ( )
A. K2MnO4 B. Na2CO3 C. NaNO2 D. CuSO4
4、某同学在实验室测定了几种液体的pH,其结果如下表。该同学由此得出的结论正确的是 ( )
液体 盐酸 CuCl2溶液 Na2SO4溶液 H2O Na2CO3溶液 NaOH溶液
pH <7 <7 =7 =7 >7 >7
A.盐溶液可能显酸性、碱性或中性 B.pH>7,一定是碱溶液
C.pH=7,一定是盐溶液 D.pH<7,一定是酸溶液
5、在“粗盐的初步提纯”实验中,下列操作正确的是( )
A B C D
6、(双选)下列常见化肥属于复合肥料的是( )
A.K2SO4 B.KNO3 C.NH4NO3 D.NH4H2PO4
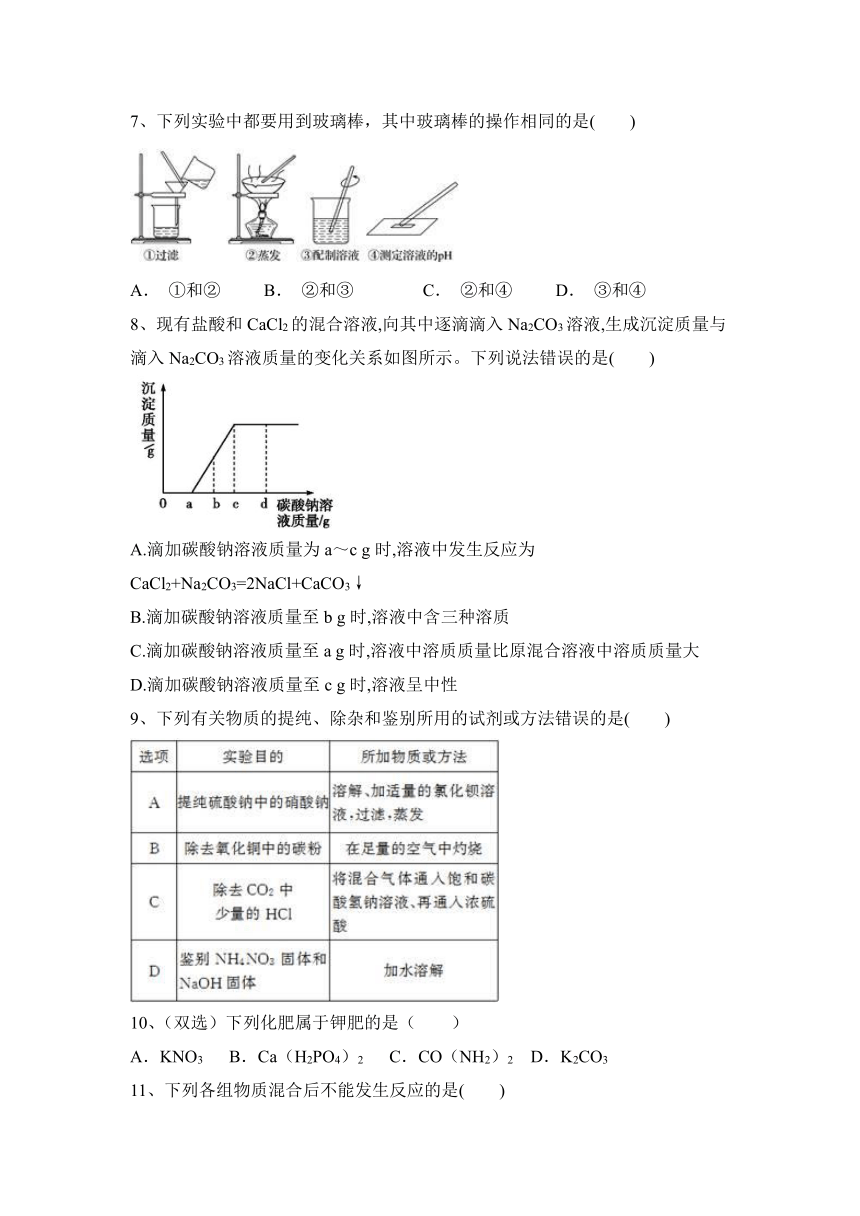
7、下列实验中都要用到玻璃棒,其中玻璃棒的操作相同的是( )
A. ①和② B. ②和③ C. ②和④ D. ③和④
8、现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。下列说法错误的是( )
A.滴加碳酸钠溶液质量为a~c g时,溶液中发生反应为CaCl2+Na2CO3=2NaCl+CaCO3↓
B.滴加碳酸钠溶液质量至b g时,溶液中含三种溶质
C.滴加碳酸钠溶液质量至a g时,溶液中溶质质量比原混合溶液中溶质质量大
D.滴加碳酸钠溶液质量至c g时,溶液呈中性
9、下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是( )
10、(双选)下列化肥属于钾肥的是( )
A.KNO3 B.Ca(H2PO4)2 C.CO(NH2)2 D.K2CO3
11、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
12、在粗盐难溶性杂质去除实验中,操作错误的是( )
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
二、填空题。
13、如图所示,弹簧秤下悬挂着一重物(不与溶液反应),若向硫酸铜溶液中逐渐滴加氢氧化钡溶液刚好完全反应后,弹簧秤的示数将________(填“变大”“变小”或“不变”);发生反应的化学方程式是___________________________。
14、现有:①维生素C、②蛋白质、③生石灰、④尿素、⑤硝酸钾、⑥铁粉,六种物质中,可用来作食品“双吸剂”(即能出去水蒸气和氧气)的是________(填序号,下同),属于复合肥料的是________,蔬菜、水果富含的营养素是________,用来修补受损组织的物质是________.
15、镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的。主要步骤如下:
(1)上述步骤中试剂①应过量,理由是_________________________________。
(2)请写出Mg(OH)2沉淀与试剂②发生中和反应的化学方程式
_____________________________________________。
(3)无水MgCl2在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为A________,B________。
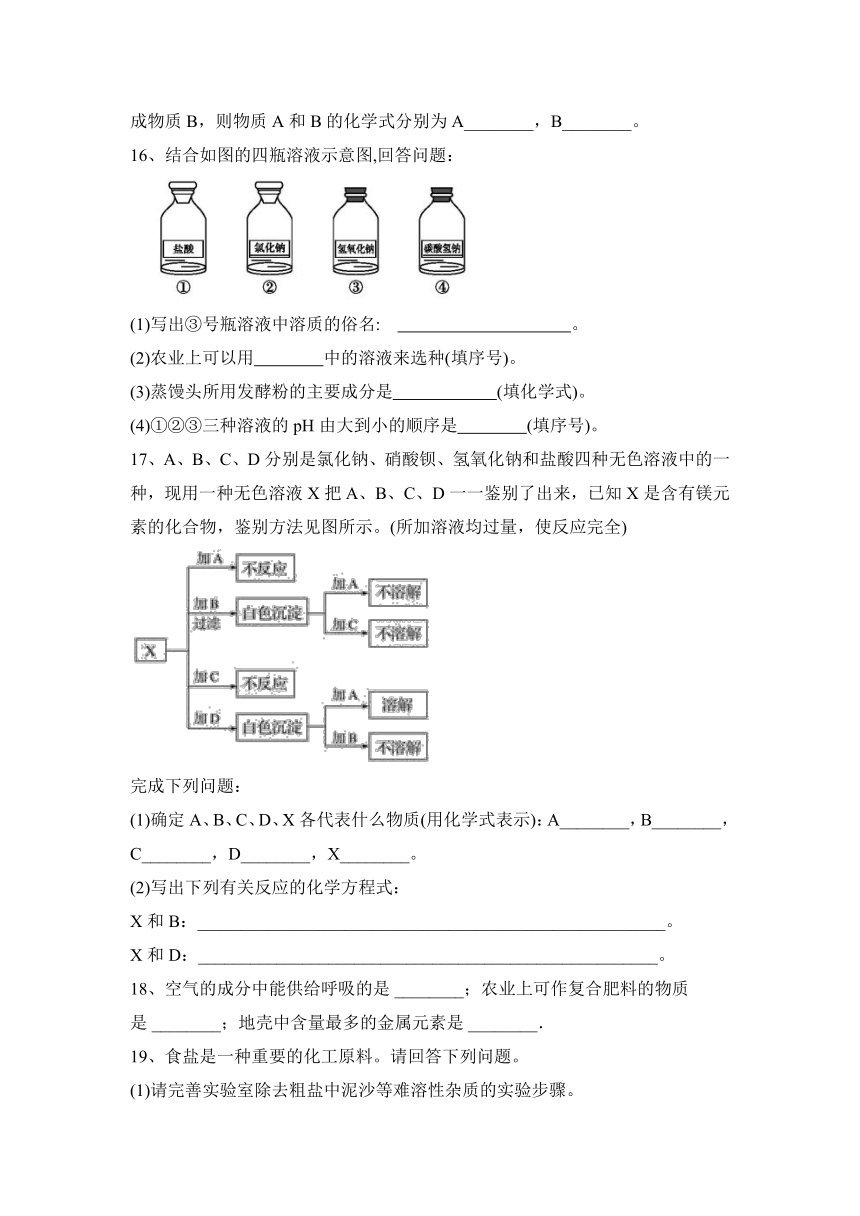
16、结合如图的四瓶溶液示意图,回答问题:
(1)写出③号瓶溶液中溶质的俗名: 。
(2)农业上可以用 中的溶液来选种(填序号)。
(3)蒸馒头所用发酵粉的主要成分是 (填化学式)。
(4)①②③三种溶液的pH由大到小的顺序是 (填序号)。
17、A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠和盐酸四种无色溶液中的一种,现用一种无色溶液X把A、B、C、D一一鉴别了出来,已知X是含有镁元素的化合物,鉴别方法见图所示。(所加溶液均过量,使反应完全)
完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):A________,B________,C________,D________,X________。
(2)写出下列有关反应的化学方程式:
X和B:______________________________________________________。
X和D:_____________________________________________________。
18、空气的成分中能供给呼吸的是 ________;农业上可作复合肥料的物质是 ________;地壳中含量最多的金属元素是 ________.
19、食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和________。
②在蒸发过程中,待______________时,停止加热,利用余热将滤液蒸干。
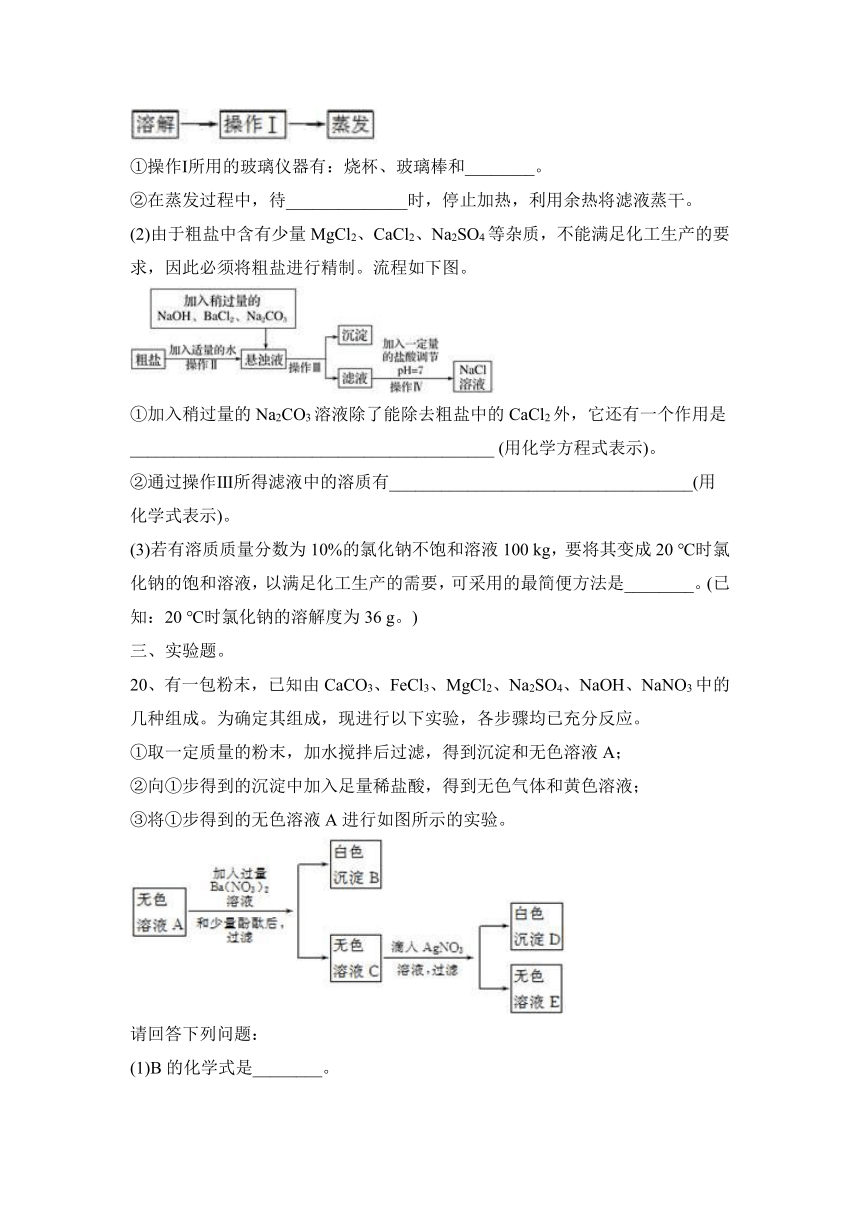
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是
__________________________________________ (用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有___________________________________(用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是________。(已知:20 ℃时氯化钠的溶解度为36 g。)
三、实验题。
20、有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如图所示的实验。
请回答下列问题:
(1)B的化学式是________。
(2)A中一定存在的溶质的化学式是________。
(3)生成白色沉淀D的化学方程式是_______________________________。
(4)这包粉末中可能含有物质的化学式是________。
21、我市有江苏最长的海岸线、最大的沿海滩涂、最大的海域面积…“沿海兴,则盐城兴”.某校学生以此为主题展开相关研究。
(1)盐城在古代以盛产“盐”而得名.通过晾晒海水或煮盐井水等,可以得到粗盐。
①海水“晒盐”得到的粗盐中含有少量的泥沙等不溶性杂质,可通过下列步骤除去:
溶解→过滤→________ (填写操作步骤).如果两次过滤后滤液仍浑浊,原因可能是: ________ (写出一种即可)。
②粗盐提纯实验中,先称取5.0g粗盐,量取10mL水只溶解4.0g粗盐,最终得到3.6g精盐,则精盐的产率是________ 。
(2)许多反应都有盐类物质生成,请写出两种制取氯化铜的方法:(用化学方程式表示)
①________ ; ②________ 。
四、计算题。
22、厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少 (计算结果精确至0.1%)
2022春人教化学九(下)第11单元 盐 化肥课后习题含答案
一、选择题。
1、下列各组物质能在pH=1的无色溶液中大量共存的是( )
A. K2SO4 Ba(OH)2 KCl B. Cu( NO3)2 NaCl KNO3
C. Na2CO3KNO3NH4Cl D. MgSO4 NaNO3KCl
【答案】D
2、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
【答案】C
3、我国某地曾发生过把外形和食盐相似,有咸味的工业用盐误作食盐,食用后发生中毒事件,这种工业用盐可能含有的有毒物质是 ( )
A. K2MnO4 B. Na2CO3 C. NaNO2 D. CuSO4
【答案】C
4、某同学在实验室测定了几种液体的pH,其结果如下表。该同学由此得出的结论正确的是 ( )
液体 盐酸 CuCl2溶液 Na2SO4溶液 H2O Na2CO3溶液 NaOH溶液
pH <7 <7 =7 =7 >7 >7
A.盐溶液可能显酸性、碱性或中性 B.pH>7,一定是碱溶液
C.pH=7,一定是盐溶液 D.pH<7,一定是酸溶液
【答案】A
5、在“粗盐的初步提纯”实验中,下列操作正确的是( )
A B C D
【答案】C
6、(双选)下列常见化肥属于复合肥料的是( )
A.K2SO4 B.KNO3 C.NH4NO3 D.NH4H2PO4
【答案】BD。
7、下列实验中都要用到玻璃棒,其中玻璃棒的操作相同的是( )
A. ①和② B. ②和③ C. ②和④ D. ③和④
【答案】B
8、现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。下列说法错误的是( )
A.滴加碳酸钠溶液质量为a~c g时,溶液中发生反应为CaCl2+Na2CO3=2NaCl+CaCO3↓
B.滴加碳酸钠溶液质量至b g时,溶液中含三种溶质
C.滴加碳酸钠溶液质量至a g时,溶液中溶质质量比原混合溶液中溶质质量大
D.滴加碳酸钠溶液质量至c g时,溶液呈中性
【答案】B
9、下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是( )
【答案】A
10、(双选)下列化肥属于钾肥的是( )
A.KNO3 B.Ca(H2PO4)2 C.CO(NH2)2 D.K2CO3
【答案】AD。
11、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
【答案】A
12、在粗盐难溶性杂质去除实验中,操作错误的是( )
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
【答案】C
二、填空题。
13、如图所示,弹簧秤下悬挂着一重物(不与溶液反应),若向硫酸铜溶液中逐渐滴加氢氧化钡溶液刚好完全反应后,弹簧秤的示数将________(填“变大”“变小”或“不变”);发生反应的化学方程式是___________________________。
【答案】变大 Ba(OH)2+CuSO4===Cu(OH)2↓+BaSO4↓
14、现有:①维生素C、②蛋白质、③生石灰、④尿素、⑤硝酸钾、⑥铁粉,六种物质中,可用来作食品“双吸剂”(即能出去水蒸气和氧气)的是________(填序号,下同),属于复合肥料的是________,蔬菜、水果富含的营养素是________,用来修补受损组织的物质是________.
【答案】⑥;⑤;①;②
15、镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的。主要步骤如下:
(1)上述步骤中试剂①应过量,理由是_________________________________。
(2)请写出Mg(OH)2沉淀与试剂②发生中和反应的化学方程式
_____________________________________________________________。
(3)无水MgCl2在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为A________,B________。
【答案】(1)使MgCl2完全转化为沉淀
(2)Mg(OH)2+2HCl===MgCl2+2H2O (3)Cl2 HCl
16、结合如图的四瓶溶液示意图,回答问题:
(1)写出③号瓶溶液中溶质的俗名: 。
(2)农业上可以用 中的溶液来选种(填序号)。
(3)蒸馒头所用发酵粉的主要成分是 (填化学式)。
(4)①②③三种溶液的pH由大到小的顺序是 (填序号)。
【答案】(1)烧碱 (2)② (3)NaHCO3 (4)③②①
17、A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠和盐酸四种无色溶液中的一种,现用一种无色溶液X把A、B、C、D一一鉴别了出来,已知X是含有镁元素的化合物,鉴别方法见图所示。(所加溶液均过量,使反应完全)
完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):A________,B________,C________,D________,X________。
(2)写出下列有关反应的化学方程式:
X和B:______________________________________________________。
X和D:_____________________________________________________。
【答案】(1)HCl Ba(NO3)2 NaCl NaOH MgSO4
(2)MgSO4+Ba(NO3)2===Mg(NO3)2+BaSO4↓
MgSO4+2NaOH===Na2SO4+Mg(OH)2↓
18、空气的成分中能供给呼吸的是 ________;农业上可作复合肥料的物质是 ________;地壳中含量最多的金属元素是 ________.
【答案】氧气;硝酸钾;铝
19、食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和________。
②在蒸发过程中,待______________时,停止加热,利用余热将滤液蒸干。
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是
__________________________________________ (用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有___________________________________(用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是________。(已知:20 ℃时氯化钠的溶解度为36 g。)
【答案】(1)①漏斗 ②少量液体剩余(较多晶体析出)
(2)① Na2CO3+BaCl2===BaCO3↓+2NaCl
② Na2CO3、NaOH、NaCl
(3)加入22.4 kg的氯化钠固体
三、实验题。
20、有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如图所示的实验。
请回答下列问题:
(1)B的化学式是________。
(2)A中一定存在的溶质的化学式是________。
(3)生成白色沉淀D的化学方程式是_______________________________。
(4)这包粉末中可能含有物质的化学式是________。
【答案】 (1)BaSO4 (2)Na2SO4、NaCl
(3)NaCl+AgNO3===AgCl↓+NaNO3 (4)MgCl2、NaNO3
【解析】①根据碳酸钙难溶于水、氯化铁溶液显黄色、氯化铁和氢氧化钠会生成氯化钠和红褐色的氢氧化铁沉淀、氯化镁和氢氧化钠会生成氯化钠和白色的氢氧化镁沉淀可知,原粉末中可能含有CaCO3、FeCl3、MgCl2、NaOH;②根据碳酸钙与稀盐酸反应生成无色气体二氧化碳,氢氧化铁与稀盐酸反应会生成氯化铁的黄色溶液可知,原粉末中一定含有CaCO3、FeCl3、NaOH;
③根据硫酸钠和硝酸钡反应生成硝酸钠和硫酸钡沉淀,①步得到的无色溶液A中含有的氯化钠和硝酸银反应生成硝酸钠和氯化银沉淀等知识进行分析。
21、我市有江苏最长的海岸线、最大的沿海滩涂、最大的海域面积…“沿海兴,则盐城兴”.某校学生以此为主题展开相关研究。
(1)盐城在古代以盛产“盐”而得名.通过晾晒海水或煮盐井水等,可以得到粗盐。
①海水“晒盐”得到的粗盐中含有少量的泥沙等不溶性杂质,可通过下列步骤除去:
溶解→过滤→________ (填写操作步骤).如果两次过滤后滤液仍浑浊,原因可能是: ________ (写出一种即可)。
②粗盐提纯实验中,先称取5.0g粗盐,量取10mL水只溶解4.0g粗盐,最终得到3.6g精盐,则精盐的产率是________ 。
(2)许多反应都有盐类物质生成,请写出两种制取氯化铜的方法:(用化学方程式表示)
①________ ; ②________ 。
【答案】(1)①蒸发(结晶);滤纸破损或滤液高于滤纸边缘;②90%;
(2)CuO+2HCl=CuCl2+H2O; Cu(OH)2+2HCl=CuCl2+2H2O
四、计算题。
22、厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少 (计算结果精确至0.1%)
【答案】88.3%
一、选择题。
1、下列各组物质能在pH=1的无色溶液中大量共存的是( )
A. K2SO4 Ba(OH)2 KCl B. Cu( NO3)2 NaCl KNO3
C. Na2CO3KNO3NH4Cl D. MgSO4 NaNO3KCl
2、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
3、我国某地曾发生过把外形和食盐相似,有咸味的工业用盐误作食盐,食用后发生中毒事件,这种工业用盐可能含有的有毒物质是 ( )
A. K2MnO4 B. Na2CO3 C. NaNO2 D. CuSO4
4、某同学在实验室测定了几种液体的pH,其结果如下表。该同学由此得出的结论正确的是 ( )
液体 盐酸 CuCl2溶液 Na2SO4溶液 H2O Na2CO3溶液 NaOH溶液
pH <7 <7 =7 =7 >7 >7
A.盐溶液可能显酸性、碱性或中性 B.pH>7,一定是碱溶液
C.pH=7,一定是盐溶液 D.pH<7,一定是酸溶液
5、在“粗盐的初步提纯”实验中,下列操作正确的是( )
A B C D
6、(双选)下列常见化肥属于复合肥料的是( )
A.K2SO4 B.KNO3 C.NH4NO3 D.NH4H2PO4
7、下列实验中都要用到玻璃棒,其中玻璃棒的操作相同的是( )
A. ①和② B. ②和③ C. ②和④ D. ③和④
8、现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。下列说法错误的是( )
A.滴加碳酸钠溶液质量为a~c g时,溶液中发生反应为CaCl2+Na2CO3=2NaCl+CaCO3↓
B.滴加碳酸钠溶液质量至b g时,溶液中含三种溶质
C.滴加碳酸钠溶液质量至a g时,溶液中溶质质量比原混合溶液中溶质质量大
D.滴加碳酸钠溶液质量至c g时,溶液呈中性
9、下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是( )
10、(双选)下列化肥属于钾肥的是( )
A.KNO3 B.Ca(H2PO4)2 C.CO(NH2)2 D.K2CO3
11、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
12、在粗盐难溶性杂质去除实验中,操作错误的是( )
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
二、填空题。
13、如图所示,弹簧秤下悬挂着一重物(不与溶液反应),若向硫酸铜溶液中逐渐滴加氢氧化钡溶液刚好完全反应后,弹簧秤的示数将________(填“变大”“变小”或“不变”);发生反应的化学方程式是___________________________。
14、现有:①维生素C、②蛋白质、③生石灰、④尿素、⑤硝酸钾、⑥铁粉,六种物质中,可用来作食品“双吸剂”(即能出去水蒸气和氧气)的是________(填序号,下同),属于复合肥料的是________,蔬菜、水果富含的营养素是________,用来修补受损组织的物质是________.
15、镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的。主要步骤如下:
(1)上述步骤中试剂①应过量,理由是_________________________________。
(2)请写出Mg(OH)2沉淀与试剂②发生中和反应的化学方程式
_____________________________________________。
(3)无水MgCl2在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为A________,B________。
16、结合如图的四瓶溶液示意图,回答问题:
(1)写出③号瓶溶液中溶质的俗名: 。
(2)农业上可以用 中的溶液来选种(填序号)。
(3)蒸馒头所用发酵粉的主要成分是 (填化学式)。
(4)①②③三种溶液的pH由大到小的顺序是 (填序号)。
17、A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠和盐酸四种无色溶液中的一种,现用一种无色溶液X把A、B、C、D一一鉴别了出来,已知X是含有镁元素的化合物,鉴别方法见图所示。(所加溶液均过量,使反应完全)
完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):A________,B________,C________,D________,X________。
(2)写出下列有关反应的化学方程式:
X和B:______________________________________________________。
X和D:_____________________________________________________。
18、空气的成分中能供给呼吸的是 ________;农业上可作复合肥料的物质是 ________;地壳中含量最多的金属元素是 ________.
19、食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和________。
②在蒸发过程中,待______________时,停止加热,利用余热将滤液蒸干。
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是
__________________________________________ (用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有___________________________________(用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是________。(已知:20 ℃时氯化钠的溶解度为36 g。)
三、实验题。
20、有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如图所示的实验。
请回答下列问题:
(1)B的化学式是________。
(2)A中一定存在的溶质的化学式是________。
(3)生成白色沉淀D的化学方程式是_______________________________。
(4)这包粉末中可能含有物质的化学式是________。
21、我市有江苏最长的海岸线、最大的沿海滩涂、最大的海域面积…“沿海兴,则盐城兴”.某校学生以此为主题展开相关研究。
(1)盐城在古代以盛产“盐”而得名.通过晾晒海水或煮盐井水等,可以得到粗盐。
①海水“晒盐”得到的粗盐中含有少量的泥沙等不溶性杂质,可通过下列步骤除去:
溶解→过滤→________ (填写操作步骤).如果两次过滤后滤液仍浑浊,原因可能是: ________ (写出一种即可)。
②粗盐提纯实验中,先称取5.0g粗盐,量取10mL水只溶解4.0g粗盐,最终得到3.6g精盐,则精盐的产率是________ 。
(2)许多反应都有盐类物质生成,请写出两种制取氯化铜的方法:(用化学方程式表示)
①________ ; ②________ 。
四、计算题。
22、厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少 (计算结果精确至0.1%)
2022春人教化学九(下)第11单元 盐 化肥课后习题含答案
一、选择题。
1、下列各组物质能在pH=1的无色溶液中大量共存的是( )
A. K2SO4 Ba(OH)2 KCl B. Cu( NO3)2 NaCl KNO3
C. Na2CO3KNO3NH4Cl D. MgSO4 NaNO3KCl
【答案】D
2、已知粉末X样品是下列四种物质中的一种,取三等份该粉末,分别加入足量的氢氧化钙溶液、氯化钡溶液、稀盐酸中并振荡,产生的现象如下表。则该固体粉末X是( )
加入物质 氢氧化钙溶液 氯化钡溶液 稀盐酸
现象 产生白色沉淀 产生白色沉淀 固体溶解,产生无色气体
A.CuSO4 B.Na2SO4 C.K2CO3 D.Mg
【答案】C
3、我国某地曾发生过把外形和食盐相似,有咸味的工业用盐误作食盐,食用后发生中毒事件,这种工业用盐可能含有的有毒物质是 ( )
A. K2MnO4 B. Na2CO3 C. NaNO2 D. CuSO4
【答案】C
4、某同学在实验室测定了几种液体的pH,其结果如下表。该同学由此得出的结论正确的是 ( )
液体 盐酸 CuCl2溶液 Na2SO4溶液 H2O Na2CO3溶液 NaOH溶液
pH <7 <7 =7 =7 >7 >7
A.盐溶液可能显酸性、碱性或中性 B.pH>7,一定是碱溶液
C.pH=7,一定是盐溶液 D.pH<7,一定是酸溶液
【答案】A
5、在“粗盐的初步提纯”实验中,下列操作正确的是( )
A B C D
【答案】C
6、(双选)下列常见化肥属于复合肥料的是( )
A.K2SO4 B.KNO3 C.NH4NO3 D.NH4H2PO4
【答案】BD。
7、下列实验中都要用到玻璃棒,其中玻璃棒的操作相同的是( )
A. ①和② B. ②和③ C. ②和④ D. ③和④
【答案】B
8、现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。下列说法错误的是( )
A.滴加碳酸钠溶液质量为a~c g时,溶液中发生反应为CaCl2+Na2CO3=2NaCl+CaCO3↓
B.滴加碳酸钠溶液质量至b g时,溶液中含三种溶质
C.滴加碳酸钠溶液质量至a g时,溶液中溶质质量比原混合溶液中溶质质量大
D.滴加碳酸钠溶液质量至c g时,溶液呈中性
【答案】B
9、下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是( )
【答案】A
10、(双选)下列化肥属于钾肥的是( )
A.KNO3 B.Ca(H2PO4)2 C.CO(NH2)2 D.K2CO3
【答案】AD。
11、下列各组物质混合后不能发生反应的是( )
A. 银和稀盐酸 B. 氢氧化钡溶液和硝酸
C. 铝和稀硫酸 D. 氯化钡溶液和硫酸钠溶液
【答案】A
12、在粗盐难溶性杂质去除实验中,操作错误的是( )
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
【答案】C
二、填空题。
13、如图所示,弹簧秤下悬挂着一重物(不与溶液反应),若向硫酸铜溶液中逐渐滴加氢氧化钡溶液刚好完全反应后,弹簧秤的示数将________(填“变大”“变小”或“不变”);发生反应的化学方程式是___________________________。
【答案】变大 Ba(OH)2+CuSO4===Cu(OH)2↓+BaSO4↓
14、现有:①维生素C、②蛋白质、③生石灰、④尿素、⑤硝酸钾、⑥铁粉,六种物质中,可用来作食品“双吸剂”(即能出去水蒸气和氧气)的是________(填序号,下同),属于复合肥料的是________,蔬菜、水果富含的营养素是________,用来修补受损组织的物质是________.
【答案】⑥;⑤;①;②
15、镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的。主要步骤如下:
(1)上述步骤中试剂①应过量,理由是_________________________________。
(2)请写出Mg(OH)2沉淀与试剂②发生中和反应的化学方程式
_____________________________________________________________。
(3)无水MgCl2在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为A________,B________。
【答案】(1)使MgCl2完全转化为沉淀
(2)Mg(OH)2+2HCl===MgCl2+2H2O (3)Cl2 HCl
16、结合如图的四瓶溶液示意图,回答问题:
(1)写出③号瓶溶液中溶质的俗名: 。
(2)农业上可以用 中的溶液来选种(填序号)。
(3)蒸馒头所用发酵粉的主要成分是 (填化学式)。
(4)①②③三种溶液的pH由大到小的顺序是 (填序号)。
【答案】(1)烧碱 (2)② (3)NaHCO3 (4)③②①
17、A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠和盐酸四种无色溶液中的一种,现用一种无色溶液X把A、B、C、D一一鉴别了出来,已知X是含有镁元素的化合物,鉴别方法见图所示。(所加溶液均过量,使反应完全)
完成下列问题:
(1)确定A、B、C、D、X各代表什么物质(用化学式表示):A________,B________,C________,D________,X________。
(2)写出下列有关反应的化学方程式:
X和B:______________________________________________________。
X和D:_____________________________________________________。
【答案】(1)HCl Ba(NO3)2 NaCl NaOH MgSO4
(2)MgSO4+Ba(NO3)2===Mg(NO3)2+BaSO4↓
MgSO4+2NaOH===Na2SO4+Mg(OH)2↓
18、空气的成分中能供给呼吸的是 ________;农业上可作复合肥料的物质是 ________;地壳中含量最多的金属元素是 ________.
【答案】氧气;硝酸钾;铝
19、食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和________。
②在蒸发过程中,待______________时,停止加热,利用余热将滤液蒸干。
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是
__________________________________________ (用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有___________________________________(用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是________。(已知:20 ℃时氯化钠的溶解度为36 g。)
【答案】(1)①漏斗 ②少量液体剩余(较多晶体析出)
(2)① Na2CO3+BaCl2===BaCO3↓+2NaCl
② Na2CO3、NaOH、NaCl
(3)加入22.4 kg的氯化钠固体
三、实验题。
20、有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①步得到的无色溶液A进行如图所示的实验。
请回答下列问题:
(1)B的化学式是________。
(2)A中一定存在的溶质的化学式是________。
(3)生成白色沉淀D的化学方程式是_______________________________。
(4)这包粉末中可能含有物质的化学式是________。
【答案】 (1)BaSO4 (2)Na2SO4、NaCl
(3)NaCl+AgNO3===AgCl↓+NaNO3 (4)MgCl2、NaNO3
【解析】①根据碳酸钙难溶于水、氯化铁溶液显黄色、氯化铁和氢氧化钠会生成氯化钠和红褐色的氢氧化铁沉淀、氯化镁和氢氧化钠会生成氯化钠和白色的氢氧化镁沉淀可知,原粉末中可能含有CaCO3、FeCl3、MgCl2、NaOH;②根据碳酸钙与稀盐酸反应生成无色气体二氧化碳,氢氧化铁与稀盐酸反应会生成氯化铁的黄色溶液可知,原粉末中一定含有CaCO3、FeCl3、NaOH;
③根据硫酸钠和硝酸钡反应生成硝酸钠和硫酸钡沉淀,①步得到的无色溶液A中含有的氯化钠和硝酸银反应生成硝酸钠和氯化银沉淀等知识进行分析。
21、我市有江苏最长的海岸线、最大的沿海滩涂、最大的海域面积…“沿海兴,则盐城兴”.某校学生以此为主题展开相关研究。
(1)盐城在古代以盛产“盐”而得名.通过晾晒海水或煮盐井水等,可以得到粗盐。
①海水“晒盐”得到的粗盐中含有少量的泥沙等不溶性杂质,可通过下列步骤除去:
溶解→过滤→________ (填写操作步骤).如果两次过滤后滤液仍浑浊,原因可能是: ________ (写出一种即可)。
②粗盐提纯实验中,先称取5.0g粗盐,量取10mL水只溶解4.0g粗盐,最终得到3.6g精盐,则精盐的产率是________ 。
(2)许多反应都有盐类物质生成,请写出两种制取氯化铜的方法:(用化学方程式表示)
①________ ; ②________ 。
【答案】(1)①蒸发(结晶);滤纸破损或滤液高于滤纸边缘;②90%;
(2)CuO+2HCl=CuCl2+H2O; Cu(OH)2+2HCl=CuCl2+2H2O
四、计算题。
22、厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少 (计算结果精确至0.1%)
【答案】88.3%
同课章节目录
