5.1质量守恒定律课件(共25张PPT)--八年级化学人教版(五四学制)全一册
文档属性
| 名称 | 5.1质量守恒定律课件(共25张PPT)--八年级化学人教版(五四学制)全一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-03 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
质量守恒定律
人教版初中化学上册第五单元课题1 质量守恒定律
XX市XX中学 XXX
1、通过实验探究认识质量守恒定律。
学习目标
4、初步学会用实验的方法来定量研究问题和分析问题
2、通过电解水反应的演示,从微观角度解释质量守恒定律。
3、能应用质量守恒定律解释化学反应中的“不守恒”现象。
情景引入
镁条的燃烧
镁条燃烧后与燃烧前相比,质量如何改变?
活动1
演示实验,初次探究
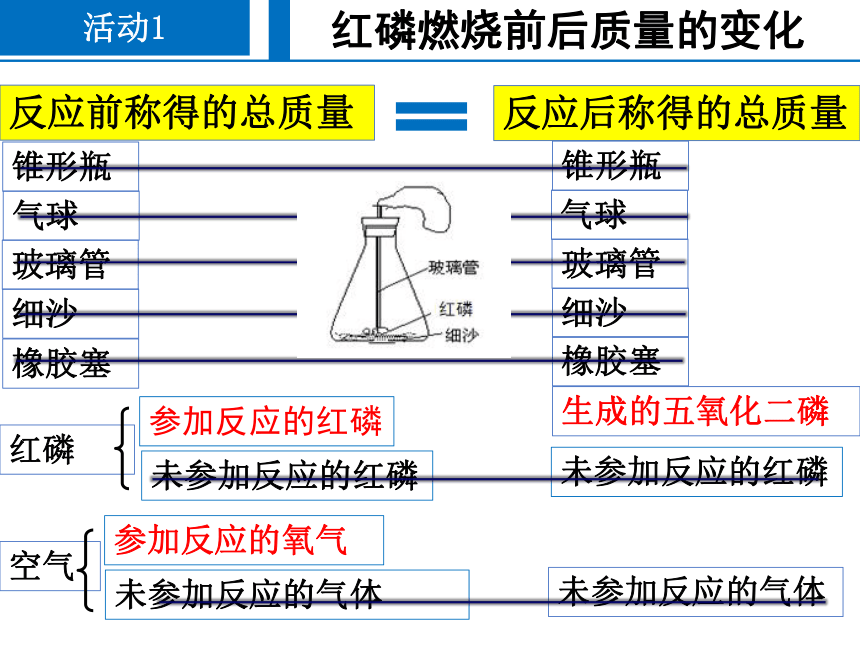
活动1
现象
红磷燃烧产生大量白烟,放热;
红磷燃烧前后质量的测定
思考
1
2
3
气球——
玻璃管——
铺细沙——
防止瓶底炸裂
引燃红磷
平衡压强
气球先变大后变小;
反应前后所有物质的质量总和相等
锥形瓶
气球
玻璃管
细沙
橡胶塞
红磷
空气
反应前称得的总质量
反应后称得的总质量
生成的五氧化二磷
未参加反应的气体
锥形瓶
气球
玻璃管
细沙
橡胶塞
参加反应的红磷
未参加反应的红磷
参加反应的氧气
未参加反应的气体
未参加反应的红磷
活动1
红磷燃烧前后质量的变化
活动1
现象
分析结果
表达式
红磷燃烧产生大量白烟,放热;气球先胀大后变瘪;反应前后所有物质的质量总和相等
参加反应的红磷和氧气的质量总和等于生成五氧化二磷的质量
红磷+氧气 五氧化二磷
点燃
红磷燃烧前后质量的变化
实验1: 铁与硫酸铜反应
实验2:碳酸钠与稀盐酸反应
活动2
学生分组,再次探究
步骤:
1、称量反应前铁丝、硫酸铜溶液、装置的总质量
2、将硫酸铜溶液与铁丝进行混合
3、称量反应后铁丝、硫酸铜溶液、装置的总质量
步骤:
1、称量反应前碳酸钠、稀盐酸、装置的总质量
2、将碳酸钠与稀盐酸进行混合
3、称量反应后碳酸钠、稀盐酸、装置的总质量
实验1
铁与硫酸铜反应的质量关系
敞口装置A:(1、3组)
密闭装置B:(2、4组)
实验2
碳酸钠与稀盐酸反应的质量关系
敞口装置A:(5、7组)
密闭装置B:(6、8组)
实验1: 铁 + 硫酸铜 → 铜 + 硫酸亚铁
实验2:碳酸钠+稀盐酸→氯化钠+水+二氧化碳
活动2
学生分组,再次探究
步骤:
1、称量反应前铁丝、硫酸铜溶液、装置的总质量
2、将硫酸铜溶液与铁丝进行混合,观察现象
3、称量反应后铁丝、硫酸铜溶液、装置的总质量
步骤:
1、称量反应前碳酸钠、稀盐酸、装置的总质量
2、将碳酸钠与稀盐酸进行混合,观察现象
3、称量反应后碳酸钠、稀盐酸、装置的总质量
实验1
铁与硫酸铜反应的质量关系
敞口装置A(1、3组)
密闭装置B(2、4组)
称量结果
现象
铁表面有红色物质出现,溶液由蓝色变为浅绿色
反应前后各物质的总质量不变
反应原理
铁 + 硫酸铜 → 铜 + 硫酸亚铁
实验2
敞口装置A
(5、7组)
密闭装置B
(6、8组)
称量结果
现象
改变
碳酸钠与稀盐酸反应的质量关系
有气泡产生,碳酸钠粉末逐渐溶解
不变
有气泡产生,碳酸钠粉末逐渐溶解,气球变大
反应原理
碳酸钠+稀盐酸→氯化钠+水+二氧化碳
活动2
质量守恒定律
反应原理
对于有气体参与或生成的反应,作定量研究时,需要用密闭装置
经验总结:
敞口装置A:
密闭装置B:
1、铁 + 硫酸铜 → 铜 + 硫酸亚铁
2、碳酸钠+稀盐酸→氯化钠+水+二氧化碳
参加化学反应的各物质的质量总和,等于
反应后生成的各物质的质量总和。
1、10g的水受热蒸发变成10g的水蒸气,这一变化是否符合质量守恒定律呢?
2、Ag的木炭与Bg的氧气反应,一定生成
(A+B)g的二氧化碳吗?为什么?
质量守恒定律
思考
参加化学反应的各物质的质量总和,等于
反应后生成的各物质的质量总和。
2、对象:质量总和
1、适用范围:一切化学变化
3、参加反应(未参加的不能计算在内)
4、各物质(别忘记考虑空气中是否有物质参加反应)
质量守恒定律
注意
情景回顾
镁条的燃烧
现象
发出耀眼白光,生成白色固体
表达式
镁条+氧气 氧化镁
点燃
镁条燃烧后与燃烧前相比,质量如何改变?
情景回顾
镁条的燃烧
燃烧前
燃烧后
情景回顾
燃烧前
燃烧后
镁条燃烧后生成的氧化镁的质量大于镁条的质量。
根据质量守恒定律,参加反应的镁条和氧气的质量总和等于生成的氧化镁的质量。所以生成氧化镁的质量大于镁条的质量。
若用该实验来验证质量守恒定律,应该怎么做?
请从质量守恒的角度进行解释。
想一想
想一想
为什么化学反应前后,各物质的总质量相等呢?
各物质质量
总和不变
种类
不变
个数
不变
质量
不变
质量
不变
种类
不变
原子
元素
物质
微观
宏观
微观角度解释
质量守恒定律
1、不能应用质量守恒定律解释的是( )
A.木炭燃烧后质量变少了
B.铁生锈质量增加了
C.打开酒精灯的瓶盖,一段时间后酒精灯质量变小了。
D.蜡烛燃烧变短了
C
当堂检测
2、加热2.45g氯酸钾和0.8g二氧化锰的混合物,完全反应得氯化钾1.49g,同时生成氧气的质量为______g。
0.96
3.在化学变化中,一定不变的是_____________。①原子的数目 ②分子的数目 ③元素的种类
④物质的种类 ⑤原子的种类 ⑥原子的质量
⑦元素的质量 ⑧分子的种类 ⑨物质的总质量
①③⑤⑥⑦⑨
当堂检测
4、蔗糖受热分解生成碳和水,由此可知蔗糖中含有哪几种元素?
C、H、O
5.康康发现:铁丝完全燃烧后得到的黑色固体的质量比铁丝的质量大,认为这个反应不遵循质量守恒定律。你同意康康的观点吗?为什么?
不同意。根据质量守恒定律,参加反应的铁丝和氧气的质量总和等于生成的四氧化三铁的质量。所以生成四氧化三铁的质量大于铁丝的质量。
当堂检测
学习了本课之后你的收获有哪些?
1.从知识技能方面…
2.从学习方法方面…
3.从情感态度价值观方面…
质量守恒定律
人教版初中化学上册第五单元课题1 质量守恒定律
XX市XX中学 XXX
1、通过实验探究认识质量守恒定律。
学习目标
4、初步学会用实验的方法来定量研究问题和分析问题
2、通过电解水反应的演示,从微观角度解释质量守恒定律。
3、能应用质量守恒定律解释化学反应中的“不守恒”现象。
情景引入
镁条的燃烧
镁条燃烧后与燃烧前相比,质量如何改变?
活动1
演示实验,初次探究
活动1
现象
红磷燃烧产生大量白烟,放热;
红磷燃烧前后质量的测定
思考
1
2
3
气球——
玻璃管——
铺细沙——
防止瓶底炸裂
引燃红磷
平衡压强
气球先变大后变小;
反应前后所有物质的质量总和相等
锥形瓶
气球
玻璃管
细沙
橡胶塞
红磷
空气
反应前称得的总质量
反应后称得的总质量
生成的五氧化二磷
未参加反应的气体
锥形瓶
气球
玻璃管
细沙
橡胶塞
参加反应的红磷
未参加反应的红磷
参加反应的氧气
未参加反应的气体
未参加反应的红磷
活动1
红磷燃烧前后质量的变化
活动1
现象
分析结果
表达式
红磷燃烧产生大量白烟,放热;气球先胀大后变瘪;反应前后所有物质的质量总和相等
参加反应的红磷和氧气的质量总和等于生成五氧化二磷的质量
红磷+氧气 五氧化二磷
点燃
红磷燃烧前后质量的变化
实验1: 铁与硫酸铜反应
实验2:碳酸钠与稀盐酸反应
活动2
学生分组,再次探究
步骤:
1、称量反应前铁丝、硫酸铜溶液、装置的总质量
2、将硫酸铜溶液与铁丝进行混合
3、称量反应后铁丝、硫酸铜溶液、装置的总质量
步骤:
1、称量反应前碳酸钠、稀盐酸、装置的总质量
2、将碳酸钠与稀盐酸进行混合
3、称量反应后碳酸钠、稀盐酸、装置的总质量
实验1
铁与硫酸铜反应的质量关系
敞口装置A:(1、3组)
密闭装置B:(2、4组)
实验2
碳酸钠与稀盐酸反应的质量关系
敞口装置A:(5、7组)
密闭装置B:(6、8组)
实验1: 铁 + 硫酸铜 → 铜 + 硫酸亚铁
实验2:碳酸钠+稀盐酸→氯化钠+水+二氧化碳
活动2
学生分组,再次探究
步骤:
1、称量反应前铁丝、硫酸铜溶液、装置的总质量
2、将硫酸铜溶液与铁丝进行混合,观察现象
3、称量反应后铁丝、硫酸铜溶液、装置的总质量
步骤:
1、称量反应前碳酸钠、稀盐酸、装置的总质量
2、将碳酸钠与稀盐酸进行混合,观察现象
3、称量反应后碳酸钠、稀盐酸、装置的总质量
实验1
铁与硫酸铜反应的质量关系
敞口装置A(1、3组)
密闭装置B(2、4组)
称量结果
现象
铁表面有红色物质出现,溶液由蓝色变为浅绿色
反应前后各物质的总质量不变
反应原理
铁 + 硫酸铜 → 铜 + 硫酸亚铁
实验2
敞口装置A
(5、7组)
密闭装置B
(6、8组)
称量结果
现象
改变
碳酸钠与稀盐酸反应的质量关系
有气泡产生,碳酸钠粉末逐渐溶解
不变
有气泡产生,碳酸钠粉末逐渐溶解,气球变大
反应原理
碳酸钠+稀盐酸→氯化钠+水+二氧化碳
活动2
质量守恒定律
反应原理
对于有气体参与或生成的反应,作定量研究时,需要用密闭装置
经验总结:
敞口装置A:
密闭装置B:
1、铁 + 硫酸铜 → 铜 + 硫酸亚铁
2、碳酸钠+稀盐酸→氯化钠+水+二氧化碳
参加化学反应的各物质的质量总和,等于
反应后生成的各物质的质量总和。
1、10g的水受热蒸发变成10g的水蒸气,这一变化是否符合质量守恒定律呢?
2、Ag的木炭与Bg的氧气反应,一定生成
(A+B)g的二氧化碳吗?为什么?
质量守恒定律
思考
参加化学反应的各物质的质量总和,等于
反应后生成的各物质的质量总和。
2、对象:质量总和
1、适用范围:一切化学变化
3、参加反应(未参加的不能计算在内)
4、各物质(别忘记考虑空气中是否有物质参加反应)
质量守恒定律
注意
情景回顾
镁条的燃烧
现象
发出耀眼白光,生成白色固体
表达式
镁条+氧气 氧化镁
点燃
镁条燃烧后与燃烧前相比,质量如何改变?
情景回顾
镁条的燃烧
燃烧前
燃烧后
情景回顾
燃烧前
燃烧后
镁条燃烧后生成的氧化镁的质量大于镁条的质量。
根据质量守恒定律,参加反应的镁条和氧气的质量总和等于生成的氧化镁的质量。所以生成氧化镁的质量大于镁条的质量。
若用该实验来验证质量守恒定律,应该怎么做?
请从质量守恒的角度进行解释。
想一想
想一想
为什么化学反应前后,各物质的总质量相等呢?
各物质质量
总和不变
种类
不变
个数
不变
质量
不变
质量
不变
种类
不变
原子
元素
物质
微观
宏观
微观角度解释
质量守恒定律
1、不能应用质量守恒定律解释的是( )
A.木炭燃烧后质量变少了
B.铁生锈质量增加了
C.打开酒精灯的瓶盖,一段时间后酒精灯质量变小了。
D.蜡烛燃烧变短了
C
当堂检测
2、加热2.45g氯酸钾和0.8g二氧化锰的混合物,完全反应得氯化钾1.49g,同时生成氧气的质量为______g。
0.96
3.在化学变化中,一定不变的是_____________。①原子的数目 ②分子的数目 ③元素的种类
④物质的种类 ⑤原子的种类 ⑥原子的质量
⑦元素的质量 ⑧分子的种类 ⑨物质的总质量
①③⑤⑥⑦⑨
当堂检测
4、蔗糖受热分解生成碳和水,由此可知蔗糖中含有哪几种元素?
C、H、O
5.康康发现:铁丝完全燃烧后得到的黑色固体的质量比铁丝的质量大,认为这个反应不遵循质量守恒定律。你同意康康的观点吗?为什么?
不同意。根据质量守恒定律,参加反应的铁丝和氧气的质量总和等于生成的四氧化三铁的质量。所以生成四氧化三铁的质量大于铁丝的质量。
当堂检测
学习了本课之后你的收获有哪些?
1.从知识技能方面…
2.从学习方法方面…
3.从情感态度价值观方面…
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
