粤教版九年级化学下册6.2 金属的化学性质(第二课时)学案
文档属性
| 名称 | 粤教版九年级化学下册6.2 金属的化学性质(第二课时)学案 |
|
|
| 格式 | docx | ||
| 文件大小 | 33.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-07 00:00:00 | ||
图片预览

文档简介
6.2 金属的化学性质(第二课时)
第2课时 金属活动性顺序的应用
探究点一 金属活动性顺序及其应用
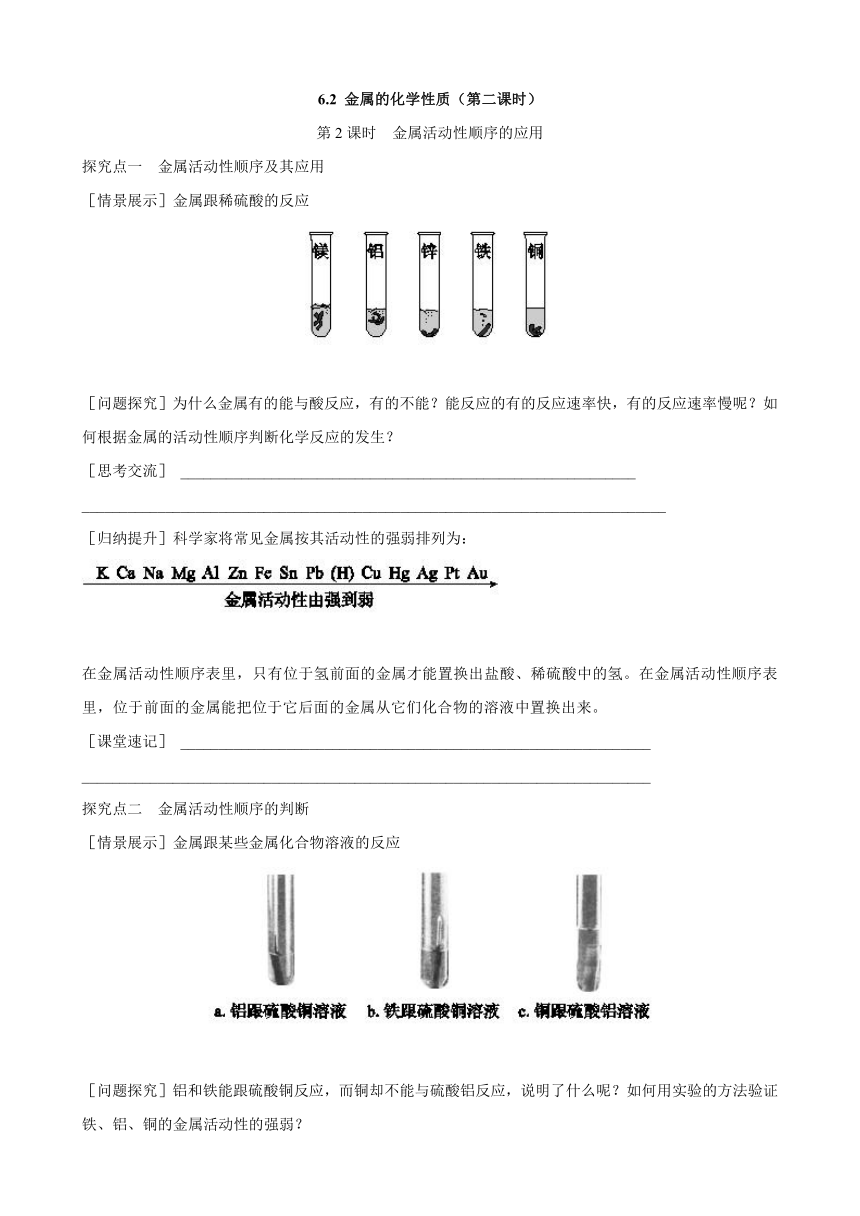
[情景展示]金属跟稀硫酸的反应
[问题探究]为什么金属有的能与酸反应,有的不能?能反应的有的反应速率快,有的反应速率慢呢?如何根据金属的活动性顺序判断化学反应的发生?
[思考交流] ____________________________________________________________
_____________________________________________________________________________
[归纳提升]科学家将常见金属按其活动性的强弱排列为:
在金属活动性顺序表里,只有位于氢前面的金属才能置换出盐酸、稀硫酸中的氢。在金属活动性顺序表里,位于前面的金属能把位于它后面的金属从它们化合物的溶液中置换出来。
[课堂速记] ______________________________________________________________
___________________________________________________________________________
探究点二 金属活动性顺序的判断
[情景展示]金属跟某些金属化合物溶液的反应
[问题探究]铝和铁能跟硫酸铜反应,而铜却不能与硫酸铝反应,说明了什么呢?如何用实验的方法验证铁、铝、铜的金属活动性的强弱?
[思考交流]______________________________________________________________
______________________________________________________________________________
[归纳提升]不同金属的活动性顺序常依据化学反应的现象来判断,从实验现象上可知,从溶液中被置换出来的金属是活动性弱的金属,能与酸反应放出氢气的金属是排在氢前面的金属。
设计实验方案判断金属的活动性顺序可以首先将金属按其活动性顺序进行排列,其次选取中间的金属单质,两端的金属组成的可溶性金属化合物溶液;或选取两端的金属单质,中间的金属组成的可溶性金属化合物的溶液。
[课堂速记] ______________________________________________________________
_______________________________________________________________________________
第2课时 金属活动性顺序的应用
探究点一 金属活动性顺序及其应用
[情景展示]金属跟稀硫酸的反应
[问题探究]为什么金属有的能与酸反应,有的不能?能反应的有的反应速率快,有的反应速率慢呢?如何根据金属的活动性顺序判断化学反应的发生?
[思考交流] ____________________________________________________________
_____________________________________________________________________________
[归纳提升]科学家将常见金属按其活动性的强弱排列为:
在金属活动性顺序表里,只有位于氢前面的金属才能置换出盐酸、稀硫酸中的氢。在金属活动性顺序表里,位于前面的金属能把位于它后面的金属从它们化合物的溶液中置换出来。
[课堂速记] ______________________________________________________________
___________________________________________________________________________
探究点二 金属活动性顺序的判断
[情景展示]金属跟某些金属化合物溶液的反应
[问题探究]铝和铁能跟硫酸铜反应,而铜却不能与硫酸铝反应,说明了什么呢?如何用实验的方法验证铁、铝、铜的金属活动性的强弱?
[思考交流]______________________________________________________________
______________________________________________________________________________
[归纳提升]不同金属的活动性顺序常依据化学反应的现象来判断,从实验现象上可知,从溶液中被置换出来的金属是活动性弱的金属,能与酸反应放出氢气的金属是排在氢前面的金属。
设计实验方案判断金属的活动性顺序可以首先将金属按其活动性顺序进行排列,其次选取中间的金属单质,两端的金属组成的可溶性金属化合物溶液;或选取两端的金属单质,中间的金属组成的可溶性金属化合物的溶液。
[课堂速记] ______________________________________________________________
_______________________________________________________________________________
