第六单元课题3二氧化碳和一氧化碳课件—2021-2022学年九年级化学人教版上册(共43张PPT)
文档属性
| 名称 | 第六单元课题3二氧化碳和一氧化碳课件—2021-2022学年九年级化学人教版上册(共43张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 139.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-08 00:00:00 | ||
图片预览






文档简介
(共43张PPT)
第6单元 碳和碳的氧化物
公开课
编辑时间:2021-10-23
课题 3 二氧化碳和一氧化碳
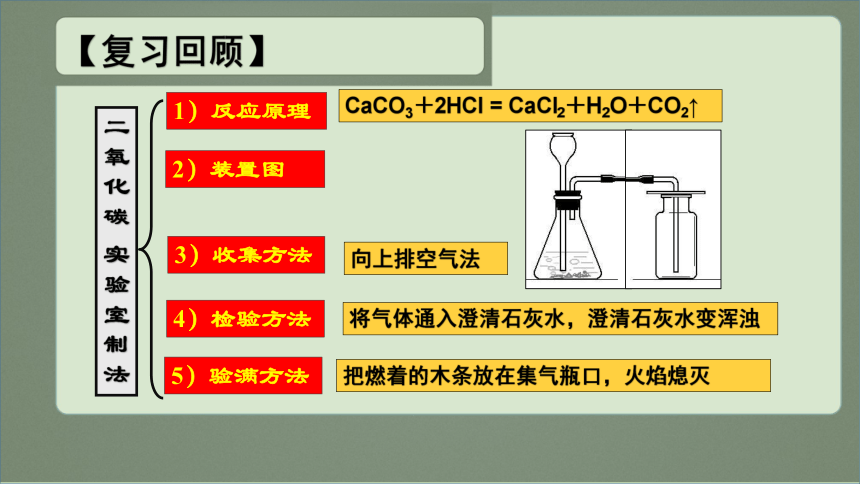
【复习回顾】
1)反应原理
2)装置图
3)收集方法
4)检验方法
二氧化碳
实验室制法
向上排空气法
将气体通入澄清石灰水,澄清石灰水变浑浊
5)验满方法
把燃着的木条放在集气瓶口,火焰熄灭
CaCO3+2HCl = CaCl2+H2O+CO2↑
【 引 入 】
在意大利某地有个奇怪的山洞,人过这个洞安然无恙,而狗走进山洞就一命呜呼了。因此,当地居民称它为“狗死洞”。这是为什么呢?
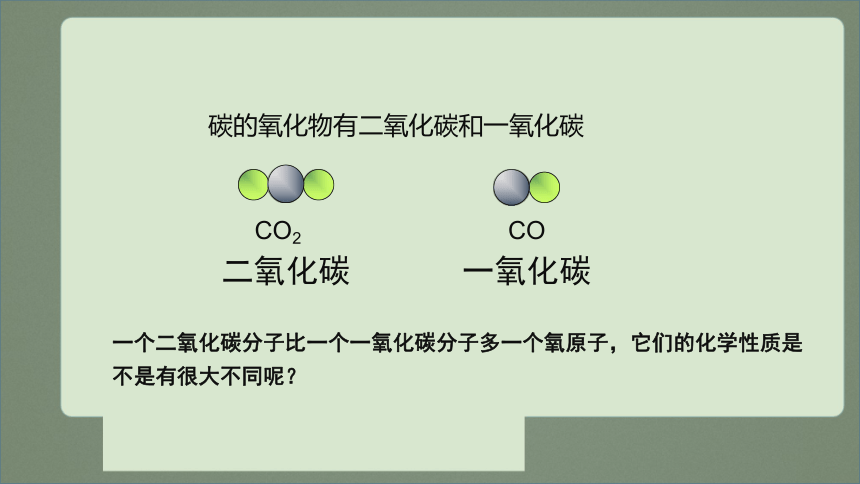
碳的氧化物有二氧化碳和一氧化碳
二氧化碳
一氧化碳
CO2
CO
一个二氧化碳分子比一个一氧化碳分子多一个氧原子,它们的化学性质是不是有很大不同呢?
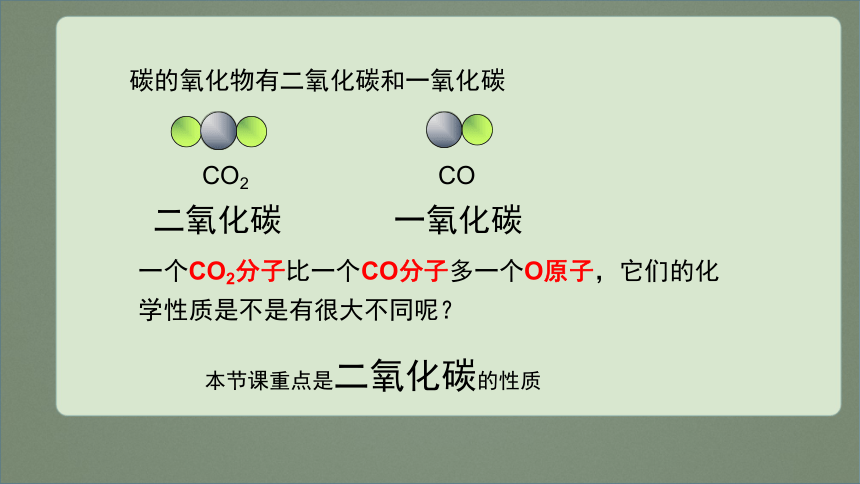
碳的氧化物有二氧化碳和一氧化碳
二氧化碳
一氧化碳
CO2
CO
一个CO2分子比一个CO分子多一个O原子,它们的化学性质是不是有很大不同呢?
本节课重点是二氧化碳的性质
一 成功学习
1 成功目标(学习要高效,目标不可少)
(1) 掌握二氧化碳的物理性质和化学性质
(2) 了解二氧化碳的用途了解温室效应及对环境的影响
2 成功自学 (目标已明确,高效来自学)
(自学课本117-120完成下列题)
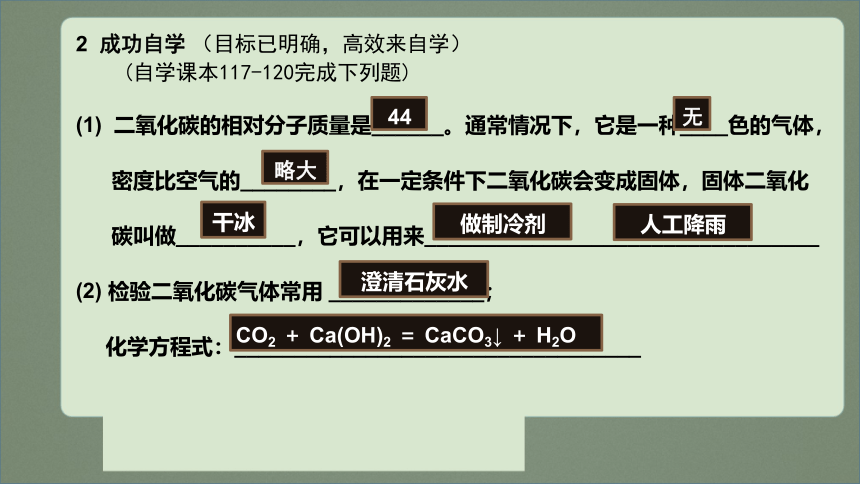
(1) 二氧化碳的相对分子质量是______。通常情况下,它是一种____色的气体,
密度比空气的________,在一定条件下二氧化碳会变成固体,固体二氧化
碳叫做__________,它可以用来_________________________________
(2) 检验二氧化碳气体常用 _____________;
化学方程式:__________________________________
44
CO2 + Ca(OH)2 = CaCO3↓ + H2O
干冰
无
略大
做制冷剂
澄清石灰水
人工降雨
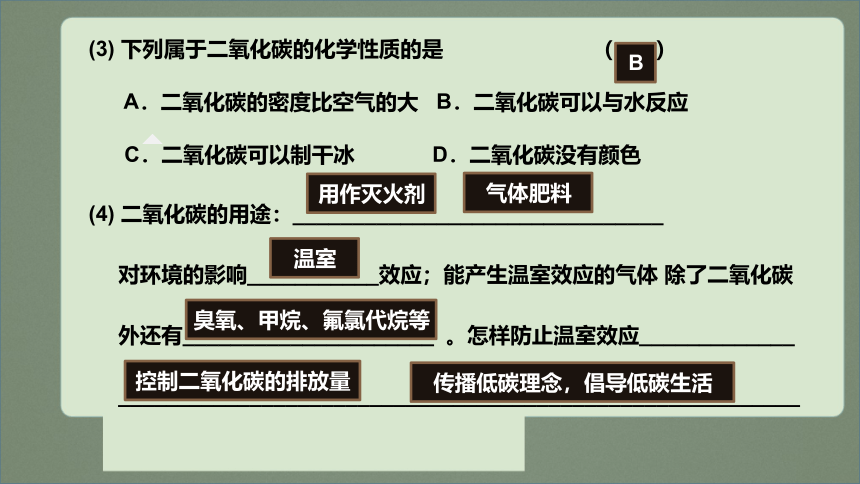
(3) 下列属于二氧化碳的化学性质的是 ( )
A.二氧化碳的密度比空气的大 B.二氧化碳可以与水反应
C.二氧化碳可以制干冰 D.二氧化碳没有颜色
(4) 二氧化碳的用途:_______________________________
对环境的影响___________效应;能产生温室效应的气体 除了二氧化碳
外还有_____________________ 。怎样防止温室效应_____________
_________________________________________________________
B
用作灭火剂
气体肥料
温室
臭氧、甲烷、氟氯代烷等
控制二氧化碳的排放量
传播低碳理念,倡导低碳生活
3.成功合作(小组面对面,交流更方便)
(1) 设计实验2、3的目的是什么?
(提示:第2、3朵都没变红)由此能得到什么结论?
(2) 实验4能得到什么结论?在该反应在发生了哪些化学反应?
(提示:花先变红,烘干后又变成紫色)
二 成功示学
(各组请同学展示讨论结果,组间互助,补充答案。根据表现选出最活跃
小组及最活跃个人。)
(1) 我来说成功自学的答案
(2) 我来说本节课学习到的内容
(展示大舞台,有我更精彩)
【课标要求】
1.通过实验探究,认识二氧化碳的性质。
2.认识二氧化碳的用途。
3.知道温室效应的危害及预防。
【重、难点】
认识二氧化碳的物理和化学性质。 (重点、难点)
探究二氧化碳的性质
第1部分
一 探究二氧化碳的性质
探究目的:
倾倒二氧化碳
二氧化碳的溶解性实验
1. 氧化碳的密度是否比空气大。
2. 探究二氧化碳是否支持燃烧。
3. 探究二氧化碳是否溶于水。
1. CO2的密度的判定
实验视频:CO2熄灭蜡烛实验
1.装置如左图,向右边倾倒入CO2
2.观察自制造天平向哪边倾斜。
常温下,CO2是无色无味的气体,密度比空气大(即ρCO2>ρ空气)
【实验6-3】 如图6-14所示,将二氧化碳气体慢慢
倒入烧杯中,观察现象并分析。
实验 现象
结论
分析
下层的蜡烛先熄灭,上层的蜡烛后熄灭
1. CO2不能燃烧,也不支持燃烧。
2. CO2密度比空气大
CO2不能燃烧,也不支持燃烧,且密度比空气大,倾倒时会在烧杯底部先聚集较多的CO2,使下层的蜡烛先接触到CO2而熄灭,上层的蜡烛后接触到CO2而熄灭。
“狗死洞”是怎么一回事儿呢?现在你懂了吗?
山洞中有大量石笋,经反应生成二氧化碳,二氧化碳的密度比氧气和空气的密度大,因此二氧化碳沉积在人类腰间以下,狗的身高不足人膝,狗的呼吸也需要氧气,因为氧气的含量不足所以狗因缺氧而死。
二氧化碳不能供给呼吸
2. CO2的溶解性
实验视频:CO2的溶解性
【实验6-4】如图6-15所示,向一个收集满二氧化碳气体的质地较
软的望料瓶中加入约I/3体积的水,立即旋紧瓶盖,
振荡。观察现象并分析。
实验现象
结论
分析
塑料瓶变瘪了
二氧化碳能溶于水
部分CO2溶于水使瓶内气体减少,气压变小,大气压强使瓶子变瘪
颜色 状态 气味 密度(与空气比较) 溶解性 是否燃烧 是否支持燃烧
二氧化碳
性质类型 无色
气态
无味
密度比空气大
能溶
于水
不能燃烧
二氧化碳的性质
物 理 性 质
化学性质
不支持
3. CO2 与水的反应
提出问题:由上面的实验探究我们得知CO2能溶于水,那么它溶于水时究竟有没有发生化学变化呢?
操作 取变瘪的矿泉水瓶中的液体少许于试管中,加入少量紫色石蕊溶液,观察现象,然后再加热试管,再观察现象
现象
结论
紫色石蕊溶液变红,加热后又变为紫色。
塑料瓶中的溶液里有酸性物质
石蕊是一种色素,遇酸变成红色。
思考:出现以上现象原因是什么呢?
归纳: ① 水能使紫色石蕊试液变红?
② 二氧化碳能使紫色石蕊试液变红?
③ 水和二氧化碳反应生成的新物质使紫色石蕊试液变红?
提问: 是什么物质使紫色石蕊试液变红呢?
归纳出以下三种猜想与假设:
设问:如何验证这些假设呢?
CO2与水的反应
实验视频:CO2与水的反应
【实验6-5】 取四朵用石蕊①溶液染成紫色的干燥的纸花。
第一朵纸花喷上稀醋酸,
第二朵纸花喷上水,
第三朵纸花直接放入盛满CO2的集气瓶中,
第四朵纸花喷上水后,再放入盛满CO2的集气瓶中,
观察四朵纸花的颜色变化。
然后将第四朵纸花取出,小心地用吹风机烘干,
观察现象。
组别 Ⅰ(醋酸) Ⅱ(水) Ⅳ(CO2) Ⅳ(水和CO2 ) 烘干第4朵花
现象
分析
变红
不变色
不变色
变红
醋酸
显酸性
CO2不显
酸性
CO2的水溶液
显酸性
水不显
酸性
红色变回紫色
酸性物质
受热分解
步 骤 现 象 分 析
Ⅰ 喷上 稀醋酸
Ⅱ 喷水
Ⅲ 直接放 CO2中
Ⅳ 喷水后放入CO2中
Ⅴ 将Ⅳ中的小花取出,加热
紫色小花变红
紫色小花变红
紫色小花不变色
紫色小花
不变色
稀醋酸使紫色石蕊变红,说明石蕊是一种指示剂,遇酸变红色
水不能使紫色石蕊变红
二氧化碳不能使紫色石蕊变红
二氧化碳与水反应的生成物使紫色石蕊变红
红色又
变成紫色
碳酸不稳定,受热分解,所以红花又变成紫色
CO2 + H2O = H2CO3
H2CO3 H2O CO2↑
4. CO2与澄清石灰水的反应
提出问题:
以前我们经常说,检验二氧化碳气体选用什么样的试剂?
它的原理是什么呢?
实验方案
实验现象
分析
方程式
澄清石灰水变浑浊
CO2与石灰水反应生成白色沉淀
CO2 + Ca(OH)2 = CaCO3↓ + H2O
向澄清石灰水中通入二氧化碳。
实验视频:CO2与澄清石灰水的反应
CO2与澄清石灰水的反应
实验视频:CO2与澄清石灰水的反应
鸡蛋保鲜小窍门—石灰水法
新鲜鸡蛋
石灰水法
1)二氧化碳与水反应
现象:将喷水后的小花放入二氧化碳中,紫色石蕊溶液变红。
碳酸很不稳定,容易分解
当加热时,碳酸分解,CO2从溶液中逸出,所以红色石蕊溶液又变成紫色。
CO2 + H2O H2CO3
H2CO3 H2O + CO2↑
思考:为了使用石灰浆[Ca(OH)2]抹的墙壁快点干燥,为什么常常需在
室内生炭火盆?为什么开始放炭火盆时,墙壁反而潮湿?
现象:澄清的石灰水变浑浊。
CO2 + Ca(OH)2 CaCO3 ↓+ H2O
2)二氧化碳与石灰水反应
H2CO3 H2O CO2↑
5. 干冰
在一定条件下,二氧化碳气体会变成液体或固体。固态二氧化碳叫作“干冰”。干冰升华时吸收大量的热量,因此可作制冷剂。
③ 舞台烟幕
升华时产生大量的烟雾
① 人工降雨
升华时吸收大量的热量
② 保存食物
升华时使周围温度降低
干冰的作用
二氧化碳对环境和生活的影响
第2部分
二 CO2的对生活和环境的影响
空气中CO2的体积分数/% 对人体健康的影响
1 使人感到气闷、头昏、心悸
4~5 使人感到气喘、头痛、眩晕
10 使人神志不清、呼吸停止,以致死亡
1. CO2对人体健康的影响
CO2本身没有毒,但二氧化碳不能供给呼吸。
当CO2含量较高时,人会缺氧。
2. CO2的用途
① 光合作用的原料。
② 气体肥料。
③ 灭火
④ 干冰升华时吸收大量热,可用它做
致冷剂或用于人工降雨。
⑤ 化工原料:工业制纯碱和尿素等。
⑥ 因为易溶于水,所以可制汽水等碳酸饮料。
CO2不支持燃烧,不能燃烧,
且比空气重,可用它来灭火。
CO2
灭火
尿素
纯碱
汽水
工业原料
光合作用
致冷剂
3. CO2对生活和生产的影响
人工降雨
4. CO2的对环境的影响
(1) 大气中的二氧化碳气体能像温室的玻璃或塑料薄膜
那样,使地面吸收的太阳光的能量不易散失,从而
使全球变暖,这种现象叫“温室效应”。
能产生温室效应的气体:二氧化碳
臭氧
甲烷
氟氯代烷等。
自然界中二氧化碳的循环
(2)温室效应的危害:
(1)导致两极的冰川融化,海平面升高,淹没许多城市,
(2)土地沙漠化,农业减产,
(3)引起暴雨、洪水的灾害。
冰川融化
城市淹没
土地沙化
暴雨洪涝
(3)减缓温室效应的措施:
(1)减少使用煤、石油、天然气等化石燃料;
(2)更多地利用太阳能、风能、地热;
(3)大力植树造林,严禁乱砍滥伐森林。
提倡“低碳”生活
【课堂小结】
无色、无味、气体
密度:比空气大
溶解性:能溶于水
二氧化碳
性质
物理性质
化学性质
用途
不能供给呼吸
不燃烧、也不支持燃烧
能与水的反应
能与石灰水的反应 (CO2的检验方法)
灭 火
光合作用
气体肥料
化工原料
人工降雨、人造舞台、制冷剂等
体现
决定
CO2 + H2O H2CO3
CO2 + Ca(OH)2 CaCO3↓+ H2O
课堂练习之成功测学
第3部分
三 成功测学
1 基础题
(1) 现有两瓶气体:CO2和O2,将他们鉴别出来的方法中不正确的是 ( )
A.分别观察颜色 B.分别滴入紫色石蕊溶液
C.分别用燃烧的小木条深入瓶内 D.分别滴加澄清石灰水
(2) 二氧化碳能用于灭火是因为 ( )
A.二氧化碳是气体
B.二氧化碳能溶于水生成碳酸
C.二氧化碳可以变成干冰
D.二氧化碳密度比空气大,且一般不支持燃烧
A
D
2 拓展题
(3) 把二氧化碳气体通入紫色石蕊溶液中,现象是:________________,
原因是(用化学方程式表示)______________________________;
把上述溶液放在酒精灯上加热,现象是:______________________
原因是(用化学方程式表示)_______________________________
(4) 二氧化碳只能用向上排空气法收集的原因是 ( )
A.密度比空气大 B.密度比空气小
C.难溶于水 D.能溶于水且密度比空气大
(5)长期放置的澄清石灰水的试剂瓶壁上会有一层白膜,要洗净该试剂瓶宜采用
的方法是____________________________,该反应的化学方程式为:
_________________________________
溶液变为红色
CO2 + H2O =H2CO3
红色溶液又变为紫色
H2CO3 H2O + CO2↑
D
用稀盐酸清洗
CaCO3+2HCl=CaCl2+H2O+CO2↑
3 中考链接
【2019-25 (3)】 D装置的作用是_____________________________________;
E装置中可能发生的有关反应的化学方程式为
_____________________________________。
吸收CO2中混有的HCl气体
CO2+Ca(OH)2= CaCO3↓+H2O
第6单元 碳和碳的氧化物
公开课
编辑时间:2021-10-23
课题 3 二氧化碳和一氧化碳
【复习回顾】
1)反应原理
2)装置图
3)收集方法
4)检验方法
二氧化碳
实验室制法
向上排空气法
将气体通入澄清石灰水,澄清石灰水变浑浊
5)验满方法
把燃着的木条放在集气瓶口,火焰熄灭
CaCO3+2HCl = CaCl2+H2O+CO2↑
【 引 入 】
在意大利某地有个奇怪的山洞,人过这个洞安然无恙,而狗走进山洞就一命呜呼了。因此,当地居民称它为“狗死洞”。这是为什么呢?
碳的氧化物有二氧化碳和一氧化碳
二氧化碳
一氧化碳
CO2
CO
一个二氧化碳分子比一个一氧化碳分子多一个氧原子,它们的化学性质是不是有很大不同呢?
碳的氧化物有二氧化碳和一氧化碳
二氧化碳
一氧化碳
CO2
CO
一个CO2分子比一个CO分子多一个O原子,它们的化学性质是不是有很大不同呢?
本节课重点是二氧化碳的性质
一 成功学习
1 成功目标(学习要高效,目标不可少)
(1) 掌握二氧化碳的物理性质和化学性质
(2) 了解二氧化碳的用途了解温室效应及对环境的影响
2 成功自学 (目标已明确,高效来自学)
(自学课本117-120完成下列题)
(1) 二氧化碳的相对分子质量是______。通常情况下,它是一种____色的气体,
密度比空气的________,在一定条件下二氧化碳会变成固体,固体二氧化
碳叫做__________,它可以用来_________________________________
(2) 检验二氧化碳气体常用 _____________;
化学方程式:__________________________________
44
CO2 + Ca(OH)2 = CaCO3↓ + H2O
干冰
无
略大
做制冷剂
澄清石灰水
人工降雨
(3) 下列属于二氧化碳的化学性质的是 ( )
A.二氧化碳的密度比空气的大 B.二氧化碳可以与水反应
C.二氧化碳可以制干冰 D.二氧化碳没有颜色
(4) 二氧化碳的用途:_______________________________
对环境的影响___________效应;能产生温室效应的气体 除了二氧化碳
外还有_____________________ 。怎样防止温室效应_____________
_________________________________________________________
B
用作灭火剂
气体肥料
温室
臭氧、甲烷、氟氯代烷等
控制二氧化碳的排放量
传播低碳理念,倡导低碳生活
3.成功合作(小组面对面,交流更方便)
(1) 设计实验2、3的目的是什么?
(提示:第2、3朵都没变红)由此能得到什么结论?
(2) 实验4能得到什么结论?在该反应在发生了哪些化学反应?
(提示:花先变红,烘干后又变成紫色)
二 成功示学
(各组请同学展示讨论结果,组间互助,补充答案。根据表现选出最活跃
小组及最活跃个人。)
(1) 我来说成功自学的答案
(2) 我来说本节课学习到的内容
(展示大舞台,有我更精彩)
【课标要求】
1.通过实验探究,认识二氧化碳的性质。
2.认识二氧化碳的用途。
3.知道温室效应的危害及预防。
【重、难点】
认识二氧化碳的物理和化学性质。 (重点、难点)
探究二氧化碳的性质
第1部分
一 探究二氧化碳的性质
探究目的:
倾倒二氧化碳
二氧化碳的溶解性实验
1. 氧化碳的密度是否比空气大。
2. 探究二氧化碳是否支持燃烧。
3. 探究二氧化碳是否溶于水。
1. CO2的密度的判定
实验视频:CO2熄灭蜡烛实验
1.装置如左图,向右边倾倒入CO2
2.观察自制造天平向哪边倾斜。
常温下,CO2是无色无味的气体,密度比空气大(即ρCO2>ρ空气)
【实验6-3】 如图6-14所示,将二氧化碳气体慢慢
倒入烧杯中,观察现象并分析。
实验 现象
结论
分析
下层的蜡烛先熄灭,上层的蜡烛后熄灭
1. CO2不能燃烧,也不支持燃烧。
2. CO2密度比空气大
CO2不能燃烧,也不支持燃烧,且密度比空气大,倾倒时会在烧杯底部先聚集较多的CO2,使下层的蜡烛先接触到CO2而熄灭,上层的蜡烛后接触到CO2而熄灭。
“狗死洞”是怎么一回事儿呢?现在你懂了吗?
山洞中有大量石笋,经反应生成二氧化碳,二氧化碳的密度比氧气和空气的密度大,因此二氧化碳沉积在人类腰间以下,狗的身高不足人膝,狗的呼吸也需要氧气,因为氧气的含量不足所以狗因缺氧而死。
二氧化碳不能供给呼吸
2. CO2的溶解性
实验视频:CO2的溶解性
【实验6-4】如图6-15所示,向一个收集满二氧化碳气体的质地较
软的望料瓶中加入约I/3体积的水,立即旋紧瓶盖,
振荡。观察现象并分析。
实验现象
结论
分析
塑料瓶变瘪了
二氧化碳能溶于水
部分CO2溶于水使瓶内气体减少,气压变小,大气压强使瓶子变瘪
颜色 状态 气味 密度(与空气比较) 溶解性 是否燃烧 是否支持燃烧
二氧化碳
性质类型 无色
气态
无味
密度比空气大
能溶
于水
不能燃烧
二氧化碳的性质
物 理 性 质
化学性质
不支持
3. CO2 与水的反应
提出问题:由上面的实验探究我们得知CO2能溶于水,那么它溶于水时究竟有没有发生化学变化呢?
操作 取变瘪的矿泉水瓶中的液体少许于试管中,加入少量紫色石蕊溶液,观察现象,然后再加热试管,再观察现象
现象
结论
紫色石蕊溶液变红,加热后又变为紫色。
塑料瓶中的溶液里有酸性物质
石蕊是一种色素,遇酸变成红色。
思考:出现以上现象原因是什么呢?
归纳: ① 水能使紫色石蕊试液变红?
② 二氧化碳能使紫色石蕊试液变红?
③ 水和二氧化碳反应生成的新物质使紫色石蕊试液变红?
提问: 是什么物质使紫色石蕊试液变红呢?
归纳出以下三种猜想与假设:
设问:如何验证这些假设呢?
CO2与水的反应
实验视频:CO2与水的反应
【实验6-5】 取四朵用石蕊①溶液染成紫色的干燥的纸花。
第一朵纸花喷上稀醋酸,
第二朵纸花喷上水,
第三朵纸花直接放入盛满CO2的集气瓶中,
第四朵纸花喷上水后,再放入盛满CO2的集气瓶中,
观察四朵纸花的颜色变化。
然后将第四朵纸花取出,小心地用吹风机烘干,
观察现象。
组别 Ⅰ(醋酸) Ⅱ(水) Ⅳ(CO2) Ⅳ(水和CO2 ) 烘干第4朵花
现象
分析
变红
不变色
不变色
变红
醋酸
显酸性
CO2不显
酸性
CO2的水溶液
显酸性
水不显
酸性
红色变回紫色
酸性物质
受热分解
步 骤 现 象 分 析
Ⅰ 喷上 稀醋酸
Ⅱ 喷水
Ⅲ 直接放 CO2中
Ⅳ 喷水后放入CO2中
Ⅴ 将Ⅳ中的小花取出,加热
紫色小花变红
紫色小花变红
紫色小花不变色
紫色小花
不变色
稀醋酸使紫色石蕊变红,说明石蕊是一种指示剂,遇酸变红色
水不能使紫色石蕊变红
二氧化碳不能使紫色石蕊变红
二氧化碳与水反应的生成物使紫色石蕊变红
红色又
变成紫色
碳酸不稳定,受热分解,所以红花又变成紫色
CO2 + H2O = H2CO3
H2CO3 H2O CO2↑
4. CO2与澄清石灰水的反应
提出问题:
以前我们经常说,检验二氧化碳气体选用什么样的试剂?
它的原理是什么呢?
实验方案
实验现象
分析
方程式
澄清石灰水变浑浊
CO2与石灰水反应生成白色沉淀
CO2 + Ca(OH)2 = CaCO3↓ + H2O
向澄清石灰水中通入二氧化碳。
实验视频:CO2与澄清石灰水的反应
CO2与澄清石灰水的反应
实验视频:CO2与澄清石灰水的反应
鸡蛋保鲜小窍门—石灰水法
新鲜鸡蛋
石灰水法
1)二氧化碳与水反应
现象:将喷水后的小花放入二氧化碳中,紫色石蕊溶液变红。
碳酸很不稳定,容易分解
当加热时,碳酸分解,CO2从溶液中逸出,所以红色石蕊溶液又变成紫色。
CO2 + H2O H2CO3
H2CO3 H2O + CO2↑
思考:为了使用石灰浆[Ca(OH)2]抹的墙壁快点干燥,为什么常常需在
室内生炭火盆?为什么开始放炭火盆时,墙壁反而潮湿?
现象:澄清的石灰水变浑浊。
CO2 + Ca(OH)2 CaCO3 ↓+ H2O
2)二氧化碳与石灰水反应
H2CO3 H2O CO2↑
5. 干冰
在一定条件下,二氧化碳气体会变成液体或固体。固态二氧化碳叫作“干冰”。干冰升华时吸收大量的热量,因此可作制冷剂。
③ 舞台烟幕
升华时产生大量的烟雾
① 人工降雨
升华时吸收大量的热量
② 保存食物
升华时使周围温度降低
干冰的作用
二氧化碳对环境和生活的影响
第2部分
二 CO2的对生活和环境的影响
空气中CO2的体积分数/% 对人体健康的影响
1 使人感到气闷、头昏、心悸
4~5 使人感到气喘、头痛、眩晕
10 使人神志不清、呼吸停止,以致死亡
1. CO2对人体健康的影响
CO2本身没有毒,但二氧化碳不能供给呼吸。
当CO2含量较高时,人会缺氧。
2. CO2的用途
① 光合作用的原料。
② 气体肥料。
③ 灭火
④ 干冰升华时吸收大量热,可用它做
致冷剂或用于人工降雨。
⑤ 化工原料:工业制纯碱和尿素等。
⑥ 因为易溶于水,所以可制汽水等碳酸饮料。
CO2不支持燃烧,不能燃烧,
且比空气重,可用它来灭火。
CO2
灭火
尿素
纯碱
汽水
工业原料
光合作用
致冷剂
3. CO2对生活和生产的影响
人工降雨
4. CO2的对环境的影响
(1) 大气中的二氧化碳气体能像温室的玻璃或塑料薄膜
那样,使地面吸收的太阳光的能量不易散失,从而
使全球变暖,这种现象叫“温室效应”。
能产生温室效应的气体:二氧化碳
臭氧
甲烷
氟氯代烷等。
自然界中二氧化碳的循环
(2)温室效应的危害:
(1)导致两极的冰川融化,海平面升高,淹没许多城市,
(2)土地沙漠化,农业减产,
(3)引起暴雨、洪水的灾害。
冰川融化
城市淹没
土地沙化
暴雨洪涝
(3)减缓温室效应的措施:
(1)减少使用煤、石油、天然气等化石燃料;
(2)更多地利用太阳能、风能、地热;
(3)大力植树造林,严禁乱砍滥伐森林。
提倡“低碳”生活
【课堂小结】
无色、无味、气体
密度:比空气大
溶解性:能溶于水
二氧化碳
性质
物理性质
化学性质
用途
不能供给呼吸
不燃烧、也不支持燃烧
能与水的反应
能与石灰水的反应 (CO2的检验方法)
灭 火
光合作用
气体肥料
化工原料
人工降雨、人造舞台、制冷剂等
体现
决定
CO2 + H2O H2CO3
CO2 + Ca(OH)2 CaCO3↓+ H2O
课堂练习之成功测学
第3部分
三 成功测学
1 基础题
(1) 现有两瓶气体:CO2和O2,将他们鉴别出来的方法中不正确的是 ( )
A.分别观察颜色 B.分别滴入紫色石蕊溶液
C.分别用燃烧的小木条深入瓶内 D.分别滴加澄清石灰水
(2) 二氧化碳能用于灭火是因为 ( )
A.二氧化碳是气体
B.二氧化碳能溶于水生成碳酸
C.二氧化碳可以变成干冰
D.二氧化碳密度比空气大,且一般不支持燃烧
A
D
2 拓展题
(3) 把二氧化碳气体通入紫色石蕊溶液中,现象是:________________,
原因是(用化学方程式表示)______________________________;
把上述溶液放在酒精灯上加热,现象是:______________________
原因是(用化学方程式表示)_______________________________
(4) 二氧化碳只能用向上排空气法收集的原因是 ( )
A.密度比空气大 B.密度比空气小
C.难溶于水 D.能溶于水且密度比空气大
(5)长期放置的澄清石灰水的试剂瓶壁上会有一层白膜,要洗净该试剂瓶宜采用
的方法是____________________________,该反应的化学方程式为:
_________________________________
溶液变为红色
CO2 + H2O =H2CO3
红色溶液又变为紫色
H2CO3 H2O + CO2↑
D
用稀盐酸清洗
CaCO3+2HCl=CaCl2+H2O+CO2↑
3 中考链接
【2019-25 (3)】 D装置的作用是_____________________________________;
E装置中可能发生的有关反应的化学方程式为
_____________________________________。
吸收CO2中混有的HCl气体
CO2+Ca(OH)2= CaCO3↓+H2O
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
