人教版化学九年级下册 10.2 pH与中和反应 学案
文档属性
| 名称 | 人教版化学九年级下册 10.2 pH与中和反应 学案 |
|
|
| 格式 | doc | ||
| 文件大小 | 134.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-08 00:00:00 | ||
图片预览

文档简介
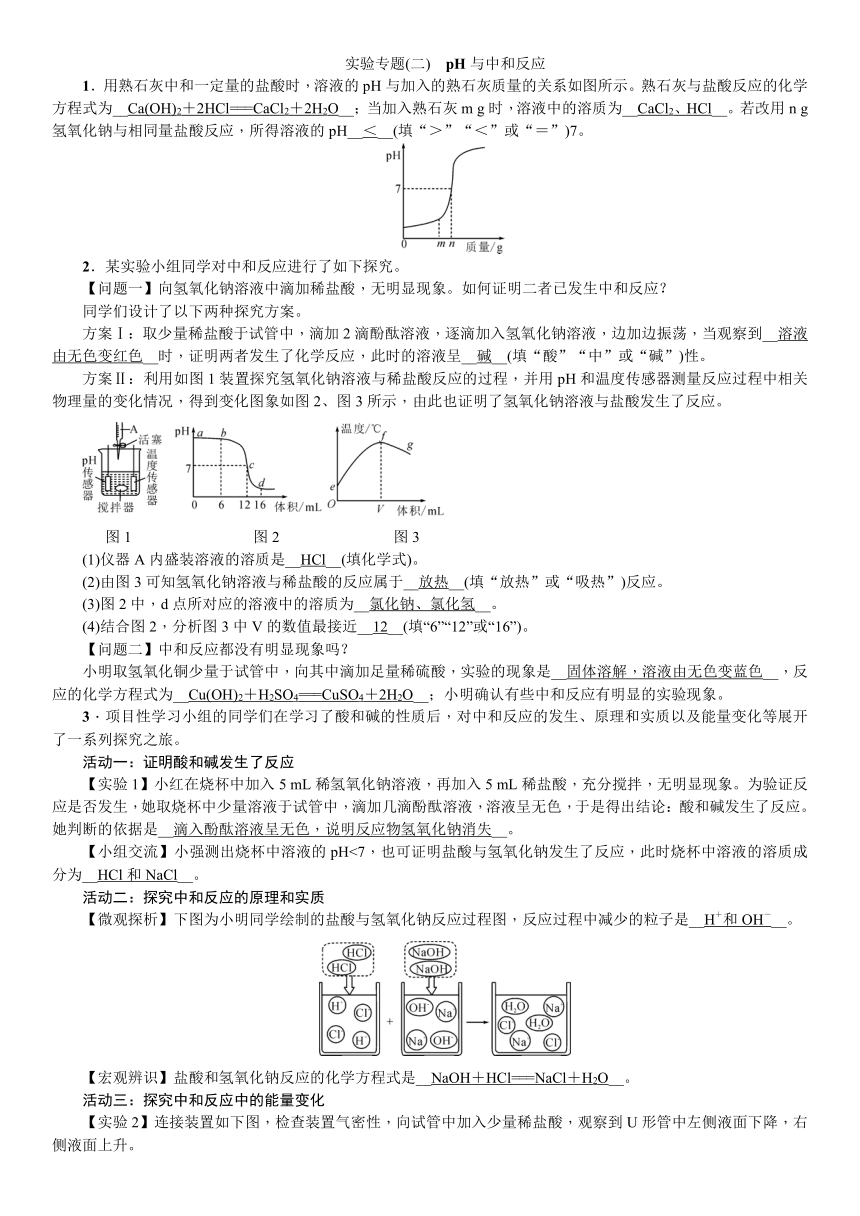
实验专题(二) pH与中和反应
1.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示。熟石灰与盐酸反应的化学方程式为__Ca(OH)2+2HCl===CaCl2+2H2O__;当加入熟石灰m g时,溶液中的溶质为__CaCl2、HCl__。若改用n g氢氧化钠与相同量盐酸反应,所得溶液的pH__<__(填“>”“<”或“=”)7。
2.某实验小组同学对中和反应进行了如下探究。
【问题一】向氢氧化钠溶液中滴加稀盐酸,无明显现象。如何证明二者已发生中和反应?
同学们设计了以下两种探究方案。
方案Ⅰ:取少量稀盐酸于试管中,滴加2滴酚酞溶液,逐滴加入氢氧化钠溶液,边加边振荡,当观察到__溶液由无色变红色__时,证明两者发生了化学反应,此时的溶液呈__碱__(填“酸”“中”或“碱”)性。
方案Ⅱ:利用如图1装置探究氢氧化钠溶液与稀盐酸反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到变化图象如图2、图3所示,由此也证明了氢氧化钠溶液与盐酸发生了反应。
图1 图2 图3
(1)仪器A内盛装溶液的溶质是__HCl__(填化学式)。
(2)由图3可知氢氧化钠溶液与稀盐酸的反应属于__放热__(填“放热”或“吸热”)反应。
(3)图2中,d点所对应的溶液中的溶质为__氯化钠、氯化氢__。
(4)结合图2,分析图3中V的数值最接近__12__(填“6”“12”或“16”)。
【问题二】中和反应都没有明显现象吗?
小明取氢氧化铜少量于试管中,向其中滴加足量稀硫酸,实验的现象是__固体溶解,溶液由无色变蓝色__,反应的化学方程式为__Cu(OH)2+H2SO4===CuSO4+2H2O__;小明确认有些中和反应有明显的实验现象。
3.项目性学习小组的同学们在学习了酸和碱的性质后,对中和反应的发生、原理和实质以及能量变化等展开了一系列探究之旅。
活动一:证明酸和碱发生了反应
【实验1】小红在烧杯中加入5 mL稀氢氧化钠溶液,再加入5 mL稀盐酸,充分搅拌,无明显现象。为验证反应是否发生,她取烧杯中少量溶液于试管中,滴加几滴酚酞溶液,溶液呈无色,于是得出结论:酸和碱发生了反应。她判断的依据是__滴入酚酞溶液呈无色,说明反应物氢氧化钠消失__。
【小组交流】小强测出烧杯中溶液的pH<7,也可证明盐酸与氢氧化钠发生了反应,此时烧杯中溶液的溶质成分为__HCl和NaCl__。
活动二:探究中和反应的原理和实质
【微观探析】下图为小明同学绘制的盐酸与氢氧化钠反应过程图,反应过程中减少的粒子是__H+和OH-__。
【宏观辨识】盐酸和氢氧化钠反应的化学方程式是__NaOH+HCl===NaCl+H2O__。
活动三:探究中和反应中的能量变化
【实验2】连接装置如下图,检查装置气密性,向试管中加入少量稀盐酸,观察到U形管中左侧液面下降,右侧液面上升。
【实验结论】__酸和碱的中和反应放热__。
【交流研讨】左侧液面下降,右侧液面上升的原因是__锥形瓶内温度升高,压强变大(合理即可)__。
【总结提升】
(1)要使上述中和反应所得溶液呈中性,实验操作步骤为:在烧杯中加入5 mL稀氢氧化钠溶液,__滴入几滴酚酞溶液,再用滴管慢慢滴入稀盐酸,并不断搅拌,至溶液恰好变为无色为止__。
(2)写出中和反应在生活或工农业生产中的一点应用:__用熟石灰改良酸性土壤(或用稀硫酸中和碱性废水或用碱性物质治疗胃酸过多症或蚊虫叮咬涂碱性物质减轻痛痒等,合理即可)__。
4.中和反应在工农业生产和生活中有广泛的应用。某化学实验小组的同学对酸碱中和反应进行了如下探究。小组同学设计如图所示的实验,验证稀H2SO4与NaOH溶液混合后,发生了化学反应。
(1)用胶头滴管滴入稀硫酸,能证明乙中发生反应的现象是__溶液由红色变为无色__,发生反应的化学方程式为__2NaOH+H2SO4===Na2SO4+2H2O__。
(2)有同学提出也可以使用石蕊溶液代替酚酞溶液进行(1)的实验。你认为__酚酞溶液__(填“酚酞溶液”或“石蕊溶液”)更适合用于验证稀硫酸与氢氧化钠溶液发生中和反应,你的理由是__石蕊溶液在碱性溶液中呈蓝色,在中性溶液中呈紫色,颜色变化不明显__。
(3)实验后小明对烧杯内的溶液中的稀硫酸是否过量进行如下探究。
实验步骤 实验现象 实验结论
取乙中反应后的溶液于试管中,向其中加入__锌粒(或碳酸钠等)__ __产生大量气泡__ 稀硫酸过量
【实验拓展】室温下,某同学利用图丙装置研究将氢氧化钠溶液慢慢滴加到盛有稀硫酸的烧杯中,并用温度传感器测量反应过程中溶液温度随时间的变化曲线如图丁所示:
(4)该曲线B点后溶液温度逐渐下降的原因是__过量的氢氧化钠溶液起到冷却的作用__。
(5)B到A点的过程中溶液的pH逐渐__增大__(填“增大”“减小”或“无变化”)。
5.小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究目的】探究所得溶液的酸碱性
(1)【提出猜想】所得溶液可能呈碱性,也可能呈__酸__性,还可能呈__中__性。
(2)【实验验证】
实验操作 实验现象 结论
用试管取该溶液1~2 mL,滴入1~2滴无色酚酞溶液,振荡 无色酚酞溶液变__红__ 溶液呈碱性
无色酚酞溶液不变色 溶液不呈__碱性__
(3)【分析与思考】
①若溶液呈碱性,则溶液中使其呈碱性的离子是__OH-__(填微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入__氯化铜(合理即可)__溶液,直到不再产生沉淀为止。然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为__CuCl2+2NaOH===Cu(OH)2↓+2NaCl__。
②若无色酚酞溶液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钙粉末,若观察到__有气泡产生__,则所取溶液呈酸性;若无明显现象,则呈中性。
方案二:取样,加入金属锌,若有气泡产生,则所取溶液呈酸性,该反应的化学方程式为__Zn+2HCl===ZnCl2+H2↑__;若无明显现象,则呈中性。
方案三:取样,加入紫色石蕊溶液,若观察到__溶液变红色__,则所取溶液呈酸性;若不变色,则呈中性。
1.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示。熟石灰与盐酸反应的化学方程式为__Ca(OH)2+2HCl===CaCl2+2H2O__;当加入熟石灰m g时,溶液中的溶质为__CaCl2、HCl__。若改用n g氢氧化钠与相同量盐酸反应,所得溶液的pH__<__(填“>”“<”或“=”)7。
2.某实验小组同学对中和反应进行了如下探究。
【问题一】向氢氧化钠溶液中滴加稀盐酸,无明显现象。如何证明二者已发生中和反应?
同学们设计了以下两种探究方案。
方案Ⅰ:取少量稀盐酸于试管中,滴加2滴酚酞溶液,逐滴加入氢氧化钠溶液,边加边振荡,当观察到__溶液由无色变红色__时,证明两者发生了化学反应,此时的溶液呈__碱__(填“酸”“中”或“碱”)性。
方案Ⅱ:利用如图1装置探究氢氧化钠溶液与稀盐酸反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到变化图象如图2、图3所示,由此也证明了氢氧化钠溶液与盐酸发生了反应。
图1 图2 图3
(1)仪器A内盛装溶液的溶质是__HCl__(填化学式)。
(2)由图3可知氢氧化钠溶液与稀盐酸的反应属于__放热__(填“放热”或“吸热”)反应。
(3)图2中,d点所对应的溶液中的溶质为__氯化钠、氯化氢__。
(4)结合图2,分析图3中V的数值最接近__12__(填“6”“12”或“16”)。
【问题二】中和反应都没有明显现象吗?
小明取氢氧化铜少量于试管中,向其中滴加足量稀硫酸,实验的现象是__固体溶解,溶液由无色变蓝色__,反应的化学方程式为__Cu(OH)2+H2SO4===CuSO4+2H2O__;小明确认有些中和反应有明显的实验现象。
3.项目性学习小组的同学们在学习了酸和碱的性质后,对中和反应的发生、原理和实质以及能量变化等展开了一系列探究之旅。
活动一:证明酸和碱发生了反应
【实验1】小红在烧杯中加入5 mL稀氢氧化钠溶液,再加入5 mL稀盐酸,充分搅拌,无明显现象。为验证反应是否发生,她取烧杯中少量溶液于试管中,滴加几滴酚酞溶液,溶液呈无色,于是得出结论:酸和碱发生了反应。她判断的依据是__滴入酚酞溶液呈无色,说明反应物氢氧化钠消失__。
【小组交流】小强测出烧杯中溶液的pH<7,也可证明盐酸与氢氧化钠发生了反应,此时烧杯中溶液的溶质成分为__HCl和NaCl__。
活动二:探究中和反应的原理和实质
【微观探析】下图为小明同学绘制的盐酸与氢氧化钠反应过程图,反应过程中减少的粒子是__H+和OH-__。
【宏观辨识】盐酸和氢氧化钠反应的化学方程式是__NaOH+HCl===NaCl+H2O__。
活动三:探究中和反应中的能量变化
【实验2】连接装置如下图,检查装置气密性,向试管中加入少量稀盐酸,观察到U形管中左侧液面下降,右侧液面上升。
【实验结论】__酸和碱的中和反应放热__。
【交流研讨】左侧液面下降,右侧液面上升的原因是__锥形瓶内温度升高,压强变大(合理即可)__。
【总结提升】
(1)要使上述中和反应所得溶液呈中性,实验操作步骤为:在烧杯中加入5 mL稀氢氧化钠溶液,__滴入几滴酚酞溶液,再用滴管慢慢滴入稀盐酸,并不断搅拌,至溶液恰好变为无色为止__。
(2)写出中和反应在生活或工农业生产中的一点应用:__用熟石灰改良酸性土壤(或用稀硫酸中和碱性废水或用碱性物质治疗胃酸过多症或蚊虫叮咬涂碱性物质减轻痛痒等,合理即可)__。
4.中和反应在工农业生产和生活中有广泛的应用。某化学实验小组的同学对酸碱中和反应进行了如下探究。小组同学设计如图所示的实验,验证稀H2SO4与NaOH溶液混合后,发生了化学反应。
(1)用胶头滴管滴入稀硫酸,能证明乙中发生反应的现象是__溶液由红色变为无色__,发生反应的化学方程式为__2NaOH+H2SO4===Na2SO4+2H2O__。
(2)有同学提出也可以使用石蕊溶液代替酚酞溶液进行(1)的实验。你认为__酚酞溶液__(填“酚酞溶液”或“石蕊溶液”)更适合用于验证稀硫酸与氢氧化钠溶液发生中和反应,你的理由是__石蕊溶液在碱性溶液中呈蓝色,在中性溶液中呈紫色,颜色变化不明显__。
(3)实验后小明对烧杯内的溶液中的稀硫酸是否过量进行如下探究。
实验步骤 实验现象 实验结论
取乙中反应后的溶液于试管中,向其中加入__锌粒(或碳酸钠等)__ __产生大量气泡__ 稀硫酸过量
【实验拓展】室温下,某同学利用图丙装置研究将氢氧化钠溶液慢慢滴加到盛有稀硫酸的烧杯中,并用温度传感器测量反应过程中溶液温度随时间的变化曲线如图丁所示:
(4)该曲线B点后溶液温度逐渐下降的原因是__过量的氢氧化钠溶液起到冷却的作用__。
(5)B到A点的过程中溶液的pH逐渐__增大__(填“增大”“减小”或“无变化”)。
5.小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究目的】探究所得溶液的酸碱性
(1)【提出猜想】所得溶液可能呈碱性,也可能呈__酸__性,还可能呈__中__性。
(2)【实验验证】
实验操作 实验现象 结论
用试管取该溶液1~2 mL,滴入1~2滴无色酚酞溶液,振荡 无色酚酞溶液变__红__ 溶液呈碱性
无色酚酞溶液不变色 溶液不呈__碱性__
(3)【分析与思考】
①若溶液呈碱性,则溶液中使其呈碱性的离子是__OH-__(填微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入__氯化铜(合理即可)__溶液,直到不再产生沉淀为止。然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为__CuCl2+2NaOH===Cu(OH)2↓+2NaCl__。
②若无色酚酞溶液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钙粉末,若观察到__有气泡产生__,则所取溶液呈酸性;若无明显现象,则呈中性。
方案二:取样,加入金属锌,若有气泡产生,则所取溶液呈酸性,该反应的化学方程式为__Zn+2HCl===ZnCl2+H2↑__;若无明显现象,则呈中性。
方案三:取样,加入紫色石蕊溶液,若观察到__溶液变红色__,则所取溶液呈酸性;若不变色,则呈中性。
同课章节目录
