2.2氧气-2022-2023学年九年级化学人教版上册(共17张PPT)
文档属性
| 名称 | 2.2氧气-2022-2023学年九年级化学人教版上册(共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 397.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-10 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
2.2氧气
思考
集气瓶里搜集的是一种常见的气体,你知道它是空气,氧气,还是氮气?如果想验证它是氧气,就必须知道氧气的性质
氧气?
OR
空气?
氮气?
OR
一、氧气的性质
1.氧气的物理性质
【观察】观察集气瓶中的氧气,你能得出氧气有哪些物理性质?
O2
①无色、无味的气体
②密度比空气大(密度:1.429g/L)
③不易溶于水(微溶)
改变条件:
氧气 液氧 固态氧(无色) (淡蓝色) (淡蓝色)
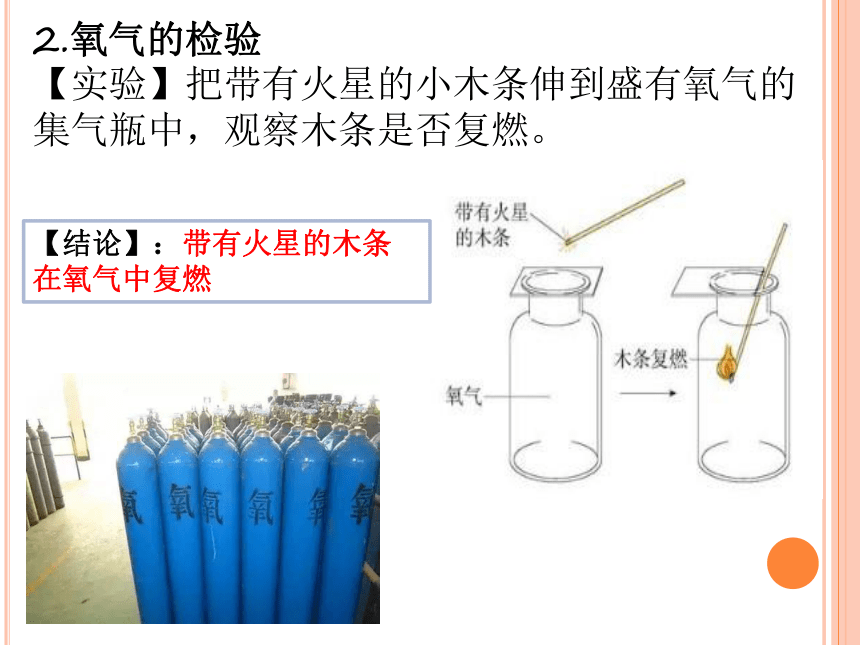
2.氧气的检验
【实验】把带有火星的小木条伸到盛有氧气的集气瓶中,观察木条是否复燃。
【结论】:带有火星的木条在氧气中复燃
【讨论】现在桌上有四瓶无色气体,分别是氧气、空气、氮气、二氧化碳,你如何区别?
【方法】
1、在四个集气瓶中同时加入带火星的木条,
①木条在集气瓶中复燃的则为氧气;
②木条在集气瓶中没有变化的则是空气;
③木条在剩余两瓶中均熄灭,则其中一瓶是氮气一瓶是二氧化碳
2、在其余两个集气瓶中,分别加入少量的澄清石灰水然后观察:
②石灰水变浑浊的则为二氧化碳
石灰水没有变化的则为氮气
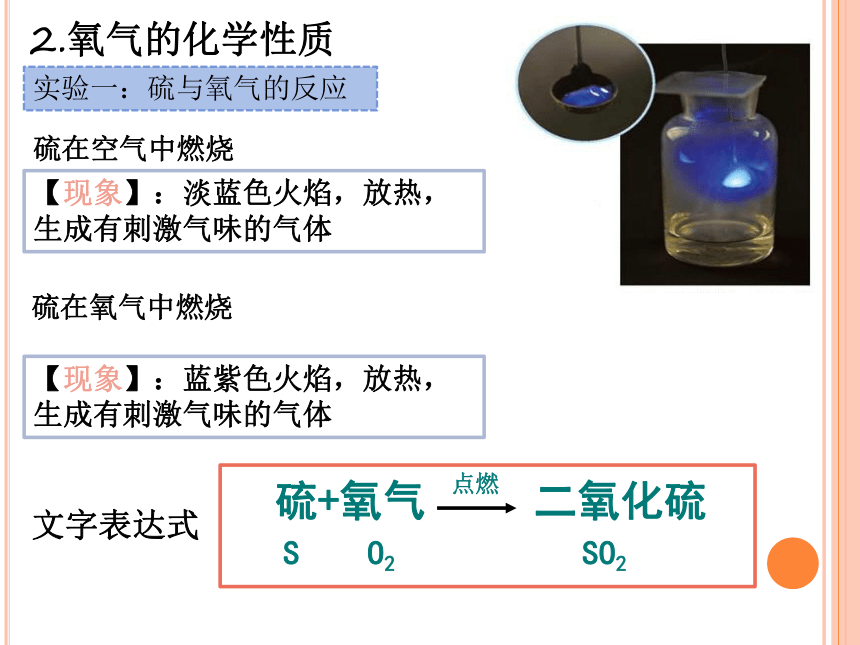
实验一:硫与氧气的反应
2.氧气的化学性质
硫在空气中燃烧
硫在氧气中燃烧
【现象】:淡蓝色火焰,放热,生成有刺激气味的气体
【现象】:蓝紫色火焰,放热,生成有刺激气味的气体
硫+氧气 二氧化硫
点燃
S O2 SO2
文字表达式
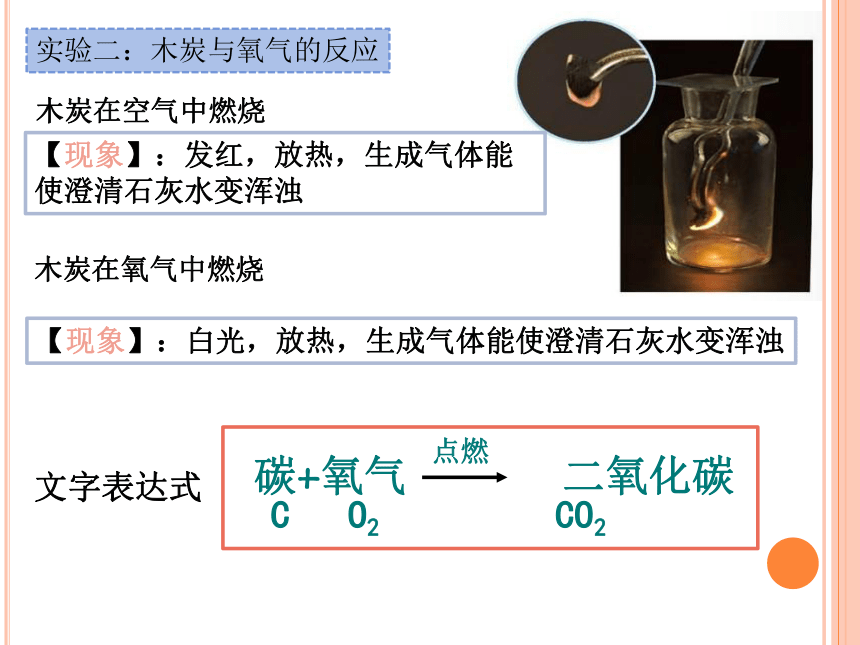
实验二:木炭与氧气的反应
木炭在空气中燃烧
木炭在氧气中燃烧
【现象】:发红,放热,生成气体能使澄清石灰水变浑浊
【现象】:白光,放热,生成气体能使澄清石灰水变浑浊
文字表达式
碳+氧气 二氧化碳
点燃
C O2 CO2
实验三:铁与氧气的反应
铁在氧气中燃烧
【现象】:1.剧烈燃烧,火星四溅
2.放出大量的热,生成黑色固体
文字表达式
铁+氧气 四氧化三铁
点燃
Fe O2 Fe3O4
【思考】:实验前为什么在集气瓶底部放一些水或者细沙呢?
为了防止燃烧过程中生成物溅落在瓶底,使集气瓶炸裂
【讨论】:物质在空气中燃烧和在氧气中燃烧现象一样吗?这说明了什么?
答:物质在空气中燃烧主要是与空气中的氧气燃烧,反应剧烈程度取决于氧气含量,氧气含量越高燃烧越剧烈
实验编号 反应的文字表达式
实验一
实验二
实验三
硫+氧气 二氧化硫
点燃
碳+氧气 二氧化碳
点燃
铁+氧气 四氧化三铁
点燃
【思考】:上述三个反应有什么共同特征?
1、反应前都是两种物质
2、都生出了一种新物质
3、反应条件都是点燃
4、反应前都有氧气
3.化合反应和氧化反应
化合反应:由两种或两种以上的物质生成另一种物质的反应(多变一)
氧化反应:物质与氧发生的反应叫做氧化反应
缓慢氧化:进行得很慢,甚至不易察觉的氧化反应叫缓慢氧化。如:呼吸作用,食物腐烂、酒和醋的酿造等。
4.化合反应和氧化反应区别和联系
(1)区别:
反应物 生成物
化合反应
氧化反应
多种物质
(不一定是O2)
一种物质
一般有氧气参与
一种或多种
(2)联系:
氧化反应
化合反应
既是氧化反应又是化合反应
判断下列哪些反应既是是化合反应,又是是氧化反应
锌 + 盐酸 氯化锌+氢气
石蜡 + 氧气 二氧化碳+水
点燃
镁 + 氧气 氧化镁
点燃
√
√
硫 + 氧气 二氧化硫
点燃
×
×
1、下列物质在纯氧中燃烧会出现火星四射,并生成黑色固体的是( )
A 木炭 B 铁丝 C 硫磺 D 蜡烛
2、通过燃烧除去密闭容器中的氧气,若不产生其它气体,可选的物质是( )
A 红磷 B 蜡烛 C 木炭 D 硫磺
3、判断下列哪些反应是化合反应( )
A,碳+氧气→二氧化碳
B,氧化钙+水→氢氧化钙
C,乙炔+氧气→二氧化碳+水
D,镁+氧气→氧化镁
E,碱式碳酸铜→氧化铜+水+二氧化碳
G,镁+盐酸→氢气+氯化镁
课后练习
课后练习
4、下列反应中,属于化合反应的是( )
A、碳酸钙 氧化钙 + 二氧化碳
C、甲烷+氧气 二氧化碳 + 水
D、水 氢气 + 氧气
B、氢气 + 氧气 水
高温
点燃
点燃
通电
B
A. H2 + CuO Cu + H2O
B. H2CO3 CO2 + H2O
C. S+O2 SO2
D.CO2+NaOH Na2CO3+H2O
C
5.下列反应属于化合反应的是( )
6、下列化学变化:①呼吸作用;②食物腐烂变质;③农家肥堆积腐烂;④铁制品生锈;⑤用黄豆等材料通过发酵制腐乳;⑥酿酒和酿醋;⑦纸张燃烧;其中属于缓慢氧化的是( )
A.①②③⑤④⑥⑦ C.②③⑤④⑥
B.①②③⑤④⑥ D.①⑥
B
课后练习
谢谢聆听!!
2.2氧气
思考
集气瓶里搜集的是一种常见的气体,你知道它是空气,氧气,还是氮气?如果想验证它是氧气,就必须知道氧气的性质
氧气?
OR
空气?
氮气?
OR
一、氧气的性质
1.氧气的物理性质
【观察】观察集气瓶中的氧气,你能得出氧气有哪些物理性质?
O2
①无色、无味的气体
②密度比空气大(密度:1.429g/L)
③不易溶于水(微溶)
改变条件:
氧气 液氧 固态氧(无色) (淡蓝色) (淡蓝色)
2.氧气的检验
【实验】把带有火星的小木条伸到盛有氧气的集气瓶中,观察木条是否复燃。
【结论】:带有火星的木条在氧气中复燃
【讨论】现在桌上有四瓶无色气体,分别是氧气、空气、氮气、二氧化碳,你如何区别?
【方法】
1、在四个集气瓶中同时加入带火星的木条,
①木条在集气瓶中复燃的则为氧气;
②木条在集气瓶中没有变化的则是空气;
③木条在剩余两瓶中均熄灭,则其中一瓶是氮气一瓶是二氧化碳
2、在其余两个集气瓶中,分别加入少量的澄清石灰水然后观察:
②石灰水变浑浊的则为二氧化碳
石灰水没有变化的则为氮气
实验一:硫与氧气的反应
2.氧气的化学性质
硫在空气中燃烧
硫在氧气中燃烧
【现象】:淡蓝色火焰,放热,生成有刺激气味的气体
【现象】:蓝紫色火焰,放热,生成有刺激气味的气体
硫+氧气 二氧化硫
点燃
S O2 SO2
文字表达式
实验二:木炭与氧气的反应
木炭在空气中燃烧
木炭在氧气中燃烧
【现象】:发红,放热,生成气体能使澄清石灰水变浑浊
【现象】:白光,放热,生成气体能使澄清石灰水变浑浊
文字表达式
碳+氧气 二氧化碳
点燃
C O2 CO2
实验三:铁与氧气的反应
铁在氧气中燃烧
【现象】:1.剧烈燃烧,火星四溅
2.放出大量的热,生成黑色固体
文字表达式
铁+氧气 四氧化三铁
点燃
Fe O2 Fe3O4
【思考】:实验前为什么在集气瓶底部放一些水或者细沙呢?
为了防止燃烧过程中生成物溅落在瓶底,使集气瓶炸裂
【讨论】:物质在空气中燃烧和在氧气中燃烧现象一样吗?这说明了什么?
答:物质在空气中燃烧主要是与空气中的氧气燃烧,反应剧烈程度取决于氧气含量,氧气含量越高燃烧越剧烈
实验编号 反应的文字表达式
实验一
实验二
实验三
硫+氧气 二氧化硫
点燃
碳+氧气 二氧化碳
点燃
铁+氧气 四氧化三铁
点燃
【思考】:上述三个反应有什么共同特征?
1、反应前都是两种物质
2、都生出了一种新物质
3、反应条件都是点燃
4、反应前都有氧气
3.化合反应和氧化反应
化合反应:由两种或两种以上的物质生成另一种物质的反应(多变一)
氧化反应:物质与氧发生的反应叫做氧化反应
缓慢氧化:进行得很慢,甚至不易察觉的氧化反应叫缓慢氧化。如:呼吸作用,食物腐烂、酒和醋的酿造等。
4.化合反应和氧化反应区别和联系
(1)区别:
反应物 生成物
化合反应
氧化反应
多种物质
(不一定是O2)
一种物质
一般有氧气参与
一种或多种
(2)联系:
氧化反应
化合反应
既是氧化反应又是化合反应
判断下列哪些反应既是是化合反应,又是是氧化反应
锌 + 盐酸 氯化锌+氢气
石蜡 + 氧气 二氧化碳+水
点燃
镁 + 氧气 氧化镁
点燃
√
√
硫 + 氧气 二氧化硫
点燃
×
×
1、下列物质在纯氧中燃烧会出现火星四射,并生成黑色固体的是( )
A 木炭 B 铁丝 C 硫磺 D 蜡烛
2、通过燃烧除去密闭容器中的氧气,若不产生其它气体,可选的物质是( )
A 红磷 B 蜡烛 C 木炭 D 硫磺
3、判断下列哪些反应是化合反应( )
A,碳+氧气→二氧化碳
B,氧化钙+水→氢氧化钙
C,乙炔+氧气→二氧化碳+水
D,镁+氧气→氧化镁
E,碱式碳酸铜→氧化铜+水+二氧化碳
G,镁+盐酸→氢气+氯化镁
课后练习
课后练习
4、下列反应中,属于化合反应的是( )
A、碳酸钙 氧化钙 + 二氧化碳
C、甲烷+氧气 二氧化碳 + 水
D、水 氢气 + 氧气
B、氢气 + 氧气 水
高温
点燃
点燃
通电
B
A. H2 + CuO Cu + H2O
B. H2CO3 CO2 + H2O
C. S+O2 SO2
D.CO2+NaOH Na2CO3+H2O
C
5.下列反应属于化合反应的是( )
6、下列化学变化:①呼吸作用;②食物腐烂变质;③农家肥堆积腐烂;④铁制品生锈;⑤用黄豆等材料通过发酵制腐乳;⑥酿酒和酿醋;⑦纸张燃烧;其中属于缓慢氧化的是( )
A.①②③⑤④⑥⑦ C.②③⑤④⑥
B.①②③⑤④⑥ D.①⑥
B
课后练习
谢谢聆听!!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
