第3章物质的性质与转化微项目论证重污染天气“汽车限行”的合理性课件2022-2023学年高一上学期化学鲁科版(2019)必修第一册(48张ppt)
文档属性
| 名称 | 第3章物质的性质与转化微项目论证重污染天气“汽车限行”的合理性课件2022-2023学年高一上学期化学鲁科版(2019)必修第一册(48张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-14 00:00:00 | ||
图片预览










文档简介
(共48张PPT)
微项目 论证重污染天气 “汽车限行”的合理性
——探讨社会性科学议题
第3章 物质的性质与转化
素养目标
1.能够综合应用氮及其化合物的性质及其转化关系,探讨相关的社会性科学议题。
2.在寻求证据支持观点的过程中,能够综合运用信息查找、问卷调查、访谈等多种方法获得必要资料;能够对资料进行加工分析,依据观点、证据和结论之间的逻辑关系进行有条理的阐述,逐步培养科学态度与社会责任的能力。
3.能够从科学、环境、经济、社会等多个方面,权衡不同观点的利与弊,有依据地作出决策。
基础落实 必备知识全过关
自主梳理
1.氮及其化合物的转化关系
①N2+3H2 2NH3
②4NH3+5O2 4NO+6H2O
N2+O2 2NO
④2NO+O2==2NO2
3NO2+H2O==2HNO3+NO
HNO3+NH3==NH4NO3
⑦3Cu+8HNO3(稀) ==3Cu(NO3)2+2NO↑+4H2O
⑧Cu+4HNO3(浓) ==Cu(NO3)2+2NO2↑+2H2O
2.氮氧化物催化转化法
在汽车排气管上安装催化转化器,使汽车尾气中的NOx(NO或NO2)与CO反应转化成无毒的物质,反应原理为2NO+2CO N2+2CO2,
2NO2+4CO N2+4CO2。
【微思考】如何治理汽车尾气
提示 NOx尾气处理方法
①碱液吸收法:
2NO2+2NaOH==NaNO3+NaNO2+H2O
NO2+NO+2NaOH==2NaNO2+H2O
NO2、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO2)≥n(NO)。一般适合工业尾气中NOx的处理。
②催化转化法:
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体N2;NOx与CO在一定温度下催化转化为无毒气体N2和CO2(一般适用于汽车尾气的处理)。
重难探究 能力素养全提升
探究1
科学认识社会性科学议题,寻找利与弊
问题探究
汽车尾气有什么危害
提示 汽车尾气中的NOx在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生了一种有毒的烟雾——光化学烟雾,光化学烟雾中含甲醛、乙醛等刺激性有毒物质,会刺激人的呼吸道。
归纳拓展
车辆限行,顾名思义,就是为了缓解交通压力或防治大气污染,而采取限制某些车辆通行的措施。车辆限行有很多种,有的是某个路段限行,有的是某个时段限行,有的是某种车型限行,还有最常见的是尾号限行。其中,尾号限行制度是为了缓解城市交通压力而催生的一种交通制度。如2008年的北京奥运测试赛期间,北京开始单双号限行。单号日子时候,只能车号的末尾数字是单号的私家车可以上路,双号日子的时候,只能车号末尾数字是双号的私家车可以上路。
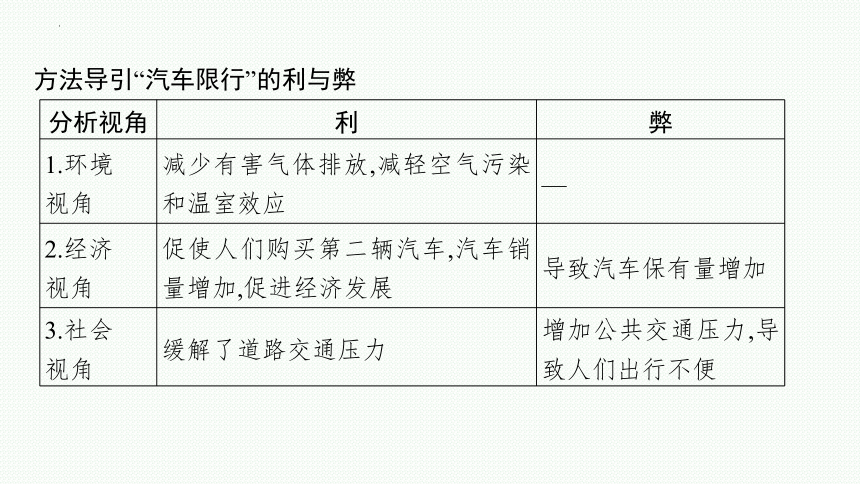
方法导引“汽车限行”的利与弊
分析视角 利 弊
1.环境 视角 减少有害气体排放,减轻空气污染和温室效应 —
2.经济 视角 促使人们购买第二辆汽车,汽车销量增加,促进经济发展 导致汽车保有量增加
3.社会 视角 缓解了道路交通压力 增加公共交通压力,导致人们出行不便
应用体验
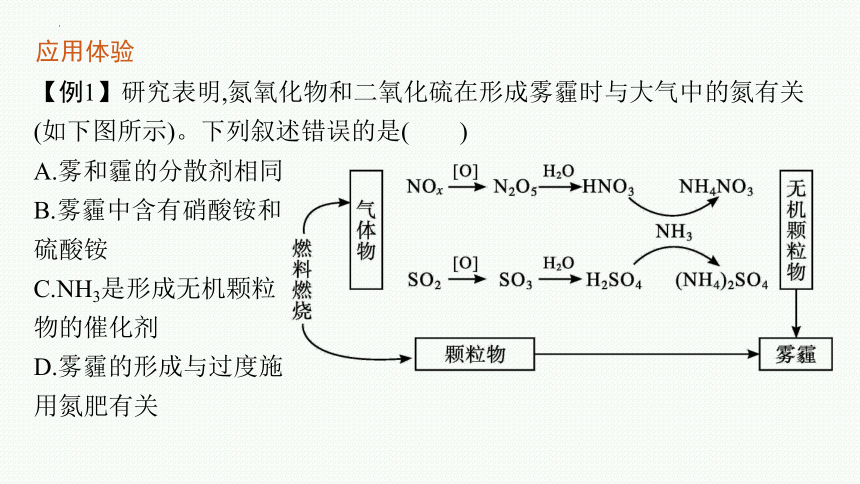
【例1】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氮有关(如下图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH3是形成无机颗粒物的催化剂
D.雾霾的形成与过度施用氮肥有关
答案 C
解析 雾和霾的分散剂均为空气,A项正确;根据题目信息,硝酸铵和硫酸铵均为无机颗粒物,是形成雾霾的因素之一,B项正确;氨气分别和硝酸、硫酸生成硝酸铵和硫酸铵,是形成无机颗粒物的反应物,C项错误;过度施用化肥会导致空气中氨气含量增加,促进了无机颗粒物中硝酸铵、硫酸铵含量的增加,D项正确。
变式训练1如图表示汽车尾气净化器处理汽车尾气的过程。有关叙述不正确的是( )
A.CO氧化为CO2所需氧来源于NOx
B.汽车安装这种净化器后,能避免铅污染
C.Pt-Rh催化剂化学反应前后质量不变
D.使用该净化器能减少酸雨的发生
答案 B
解析 由题目的信息可知,CO氧化为CO2所需的氧来源于氮的氧化物,A项正确;汽车安装这种净化器后,能避免一氧化碳、氮的氧化物造成的空气污染,但不能避免铅污染,B项错误;Pt-Rh催化剂在化学反应前后质量和化学性质都不变,C项正确;氮的氧化物也会造成酸雨,因此使用该净化器能减少酸雨的发生,D项正确。
探究2
学习科学论证,论证利与弊
问题探究
汽车尾号限行对治理空气污染有用吗
提示 通过一定的实际测定和对比,得出结论:汽车尾号限行的举措对于减轻空气污染是有一定效果的。
机动车尾气排放成为一个备受指责的因素,特别是柴油车和某些重型小轿车。这些汽车尾气中的化学元凶包括悬浮微粒(PM)和氮氧化物(NOx)。悬浮微粒是一种烟尘,能够侵入肺部并引起心血管疾病,氮氧化物则会加剧呼吸困难。
归纳拓展
方法导引科学论证的水平
水平 示例
水平1:有笼统的观点,缺少必要的资料 观点:采取“汽车限行”措施能够减轻空气污染
水平2:有观点和资料,缺少从资料到观点的推理过程或者推理过程不合理,或者资料不充分 观点:采取“汽车限行”措施能够减轻空气污染
资料:汽车行驶过程中会产生氮氧化物
水平 示例
水平3:有观点、资料以及从资料到观点的推理过程;资料充分,推理过程合理 观点:采取“汽车限行”措施能够减轻空气污染
资料:汽车行驶过程中会产生氮氧化物;大量汽车行驶会产生较多的氮氧化物;氮氧化物进入大气,会导致光化学烟雾,还会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题,污染大气
推理过程:汽车行驶过程中会产生氮氧化物→汽车尾气中有氮氧化物→氮氧化物进入大气(超过排放标准)→大气中的氮氧化物会导致光化学烟雾,也会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题
水平 示例
水平4:有观点、资料以及从资料到观点的推理过程;资料充分,推理过程合理;考虑了可能的反驳及其证据 观点:采取“汽车限行”措施能够减轻空气污染
资料:汽车行驶过程中会产生氮氧化物;大量汽车行驶会产生较多的氮氧化物;氮氧化物进入大气,会导致光化学烟雾,还会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题,污染大气推理过程:汽车行驶过程中会产生氮氧化物→汽车尾气中有氮氧化物→氮氧化物进入大气(超过排放标准)→大气中的氮氧化物导致光化学烟雾,也会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题
反驳及其证据:汽车中装有净化装置,会将氮氧化物转化成氮气后再排放
进一步推理:虽然有净化装置,但装置中的催化剂很容易中毒;一旦催化剂中毒,就不能有效吸收氮氧化物了。我国的汽车更换净化装置的比率很低
【例2】汽车排放的尾气中含有NO2,NO2是城市大气污染的主要污染物之一。在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为①2NO2→2NO+2O,②2NO+O2→2NO2,③O+O2→O3。下列对该反应过程及生成物叙述正确的是( )
A.NO2只起催化剂作用
B.NO起催化剂作用
C.NO2只起氧化剂作用
D.O3与O2互为同素异形体
应用体验
答案 D
解析 由反应过程①+②得O2 ―→ 2O,反应③为O+O2 ―→ O3,则NO2起催化剂作用,反应过程中NO2还做还原剂,A、B、C项错误;O3与O2互为同素异形体,D项正确。
变式训练2下列现象的产生,与氮循环无关的是( )
A.光化学烟雾 B.白色污染
C.水体富营养化 D.酸雨
答案 B
解析 光化学污染是氮的氧化物和有机烃类在光作用下的一系列复杂变化,与氮循环有关;白色污染是指难降解的塑料垃圾(多指塑料袋)对环境的污染;水体富营养化是指水中的氮、磷等元素浓度过大造成的水污染,会导致藻类疯长,从而引起水中缺氧,导致水生生物大量死亡,与氮循环有关;酸雨是二氧化硫和氮氧化物与雨水作用的结果,与氮循环有关。
探究3
权衡利弊,作出决策
问题探究
根据汽车限行的利弊,如何作出决策
提示 经过充分的论证分析后,分清主次,权衡利弊,作出决策。
归纳拓展
方法导引评价要素及评价等级
评价 要素 评价等级
A B C D
知识的 应用 不仅能充分、科学、合理地应用有关元素及其化合物的知识进行阐述分析,还能应用相关的新知识 能充分、科学、合理地应用有关元素及其化合物的知识进行阐述分析 能比较充分、科学地应用有关元素及其化合物的知识进行阐述分析 应用有关元素及其化合物的知识进行阐述分析时不够全面或出现错误
评价 要素 评价等级
A B C D
科学 论证 有针对议题的明确观点,资料充分,从资料到观点的推理过程合理,考虑了反驳及其证据 有针对议题的明确观点,资料充分,从资料到观点的推理过程合理 有针对议题的明确观点,资料比较充分,从资料到观点的推理过程有瑕疵但基本合理 有针对议题的明确观点,资料基本充分,但缺少从资料到观点的推理过程
评价 要素 评价等级
A B C D
科学态 度与社 会责任 素养 能根据实际情况,自主依据绿色化学思想和可持续发展观念对社会性科学议题进行综合分析 能根据实际情况,从科学、环境、经济、社会等方面对社会性科学议题进行具体分析 能分析社会性科学议题可能给环境、社会发展、人类健康等带来的双重影响,但不够充分、具体 仅关注对个体的影响,缺乏对环境、社会发展、人类健康等社会性影响的关注
应用体验
【例3】硫的氧化物、氮的氧化物是常见的大气污染物。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年氮氧化物的排放量约为5×107 kg。NO2溶于水生成 (写名称)和NO。
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中的氮的氧化物用 吸收,写出NO2与之反应的离子方程式: 。
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。
①若原料气从左向右流,上述装置连接的顺序是:
原料气→ → → → → (填字母)。
②装置②中发生反应的离子方程式为 ;当装置②中出现 现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中含碘的淀粉溶液的是
(填字母)。
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
解析 (1)①NO2溶于水生成硝酸和NO;②氮的氧化物能够与氢氧化钠溶液反应生成盐,达到吸收的目的;氢氧化钠与NO2反应生成硝酸钠和亚硝酸钠两种盐,离子方程式为
(2)①由于氮气、氧气都不溶于水,可以通过排水法测量其体积,因此正确的顺序为cdbae;②碘单质具有氧化性,把二氧化硫氧化为硫酸,本身还原为碘离子;由于淀粉遇碘显蓝色,当碘单质反应完全后,蓝色溶液恰好变为无色,立即停止通气;③酸性KMnO4溶液和溴水都具有氧化性,且溶液都有颜色,所以能够代替,NaOH溶液和氨水都能与二氧化硫反应,但是没现象,A、C正确。
变式训练3回答下列有关环境的问题:
(1)造成水体富营养化的元素是 和 ,水体富营养化的后果是导致水生藻类“疯长”,并迅速覆盖在水面上,在海水中形成 现象,而这种现象在淡水中称为 。
(2)大气中的下列氧化物的存在既不能形成酸雨,也不能形成光化学污染的是 。
A.二氧化硫 B.二氧化碳
C.二氧化氮 D.一氧化氮
(3)目前,大城市内的光化学污染是大气主要污染形式之一,该污染的现象是形成烟雾,故又叫光化学烟雾,形成光化学烟雾的过程属于
(填“化学变化”或“物理变化”)。
(4)汽车尾气中氮的氧化物来源除因为燃油中含有氮元素(燃烧时,氮转化为氮的氧化物)外,还有一个原因。请你用化学方程式表示这个原因: 。
答案 (1)氮 磷 赤潮 水华
(2)B (3)化学变化
(4)N2+O2 2NO
解析 (1)水体中过量的氮、磷造成了水体的富营养化,温度适宜则会导致近海水域的赤潮现象,在江河湖泊等淡水中爆发性生长藻类则叫水华。
(2)酸雨是指pH小于5.6的雨、雪、霜或其他形式的大气降水。二氧化碳溶解于水,尽管也可以使水显酸性,但大气中的二氧化碳在水中溶解后pH不可能小于5.6,故二氧化碳不是酸雨形成的原因。
(3)光化学烟雾的形成是一个复杂的氧化还原反应过程。
(4)机动车在工作时,其气缸内的温度和压力非常高,故吸入其中的空气(氮气与氧气)会相互反应,生成氮的氧化物。
学以致用 随堂检测全达标
1.世界大学生夏季运动会是规模仅次于夏季奥运会的世界级综合性运动会。2021年第31届世界大学生运动会在成都举办。“绿色”是成都的城市发展理念,也是这次运动会的组织理念。下面有关说法不正确的是( )
A.成都市目前使用的清洁燃料压缩天然气(CNG)和液化石油气(LPG)的主要成分均是烃类
B.兴建运动会场馆所用到的金属材料中可能含有非金属元素
C.“绿色化学”的核心是应用化学原理对环境污染进行治理
D.新能源汽车的使用有助于减少氮氧化物的排放
答案 C
解析 A项,压缩天然气(CNG)的主要成分是甲烷,液化石油气(LPG)的成分是丙烷、丁烷等,所以这两类燃料的主要成分都是烃类,故A正确;B项,合金可能含有非金属元素,故B正确;C项,“绿色化学”的核心是从源头上控制污染,而不是治理污染,故C错误;D项,新能源汽车的使用可减少化石燃料的使用,可减少常规汽车的使用,能减少氮氧化物的排放,故D正确。
2.当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中
的氮氧化物,其原理如下:
下列关于该“消除”过程的叙述不正确的是( )
A.部分光能转变为化学能 B.消除总变化为NOx+O2+H2O→HNO3
C.消除反应能全天候发生 D.使用纳米TiO2的消除效率更高
答案 C
解析 在TiO2的催化作用下紫外线提供能量,部分光能转变为化学能,故A项正确,不符合题意;题中示意图表明,在TiO2的催化作用下紫外线提供能量,发生反应:NOx+O2+H2O→HNO3,故B项正确,不符合题意;没有紫外线时上述反应不能发生,故C项错误,符合题意;纳米与紫外线接触面积更大,将产生更多的光生电子和光生空穴,从而消除更多的NOx,故D项正确,不符合题意。
3.SO2废气的回收利用方案如图所示。下列说法错误的是( )
B.Y中含有NH4HSO3
C.气体a既有氧化性又有还原性
D.(NH4)2S2O8是一种纯净物
答案 B
所以A项正确;(NH4)2SO3与过量H2SO4反应生成(NH4)2SO4、SO2和H2O,Y为(NH4)2SO4和过量的H2SO4,不含NH4HSO3,所以B项错误;气体a为SO2,SO2中S元素的化合价为+4价,既有氧化性又有还原性,所以C项正确;(NH4)2S2O8是一种化合物,属于纯净物,D项正确。
4.下图所示是酸雨的形成示意图。根据图示回答下列问题。
(1)下列气体容易形成酸雨的是 。
A.CO2 B.SO2 C.N2 D.NO2
(2)现有雨水样品1份,每隔一段时间测定该
雨水样品的pH,所得数据如下:
测试时间/h 0 1 2 3 4
雨水的pH 4.73 4.63 4.56 4.55 4.55
分析数据,回答下列问题:
①雨水样品的pH变化的原因是 (用化学方程式表示)。
②如果将刚取样的上述雨水和自来水相混合,雨水pH将变 。
(3)下列措施中,可减少酸雨产生的是 (填字母)。
①少用煤作燃料 ②把工厂烟囱造高
③燃料脱硫 ④在已酸化的土壤中加石灰
⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
答案 (1)BD (2)①SO2+H2O H2SO3、2H2SO3+O2 === 2H2SO4 ②小 (3)C
解析 (1)SO2、NO2的大量排放易形成酸雨。
(2)①雨水放置过程中pH变小,其原因是SO2与H2O反应生成的H2SO3被空气中氧气氧化所致:SO2+H2O H2SO3、2H2SO3+O2 === 2H2SO4。②雨水和自来水混合,应考虑SO2(或H2SO3)与Cl2(或HClO)的反应,反应后生成强酸,因此雨水与自来水混合后,其pH将变小。
5.(2020山东潍坊高一期末)我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有 (写化学式)。
(2)图中物质溶于水溶液呈碱性的是 。
(3)写出SO2转化为SO3的化学方程式: 。
(4)工业上利用氨气制备一氧化氮,反应的化学方程式为
。
(5)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为
(用化学方程式表示)。
(6)氨气与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为 。
解析 (1)酸性氧化物是能与碱反应得到盐和水的氧化物,符合要求的有SO2、SO3和N2O5。
(2)图中物质溶于水呈碱性的只有NH3。
(3)二氧化硫在催化剂存在时可以转化为三氧化硫:2SO2+O2 2SO3。
(4)氨气经催化氧化可以形成一氧化氮:4NH3+5O2 4NO+6H2O。
(5)浓硝酸见光或受热时易发生分解反应4HNO3 4NO2↑+O2↑+2H2O,因此要保存在棕色试剂瓶中。
(6)氨气中的氮为-3价,一氧化氮中的氮为+2价,因此二者可以在一定条件下发生归中反应得到氮气:6NO+4NH3 5N2+6H2O。
好好学习 继续努力
微项目 论证重污染天气 “汽车限行”的合理性
——探讨社会性科学议题
第3章 物质的性质与转化
素养目标
1.能够综合应用氮及其化合物的性质及其转化关系,探讨相关的社会性科学议题。
2.在寻求证据支持观点的过程中,能够综合运用信息查找、问卷调查、访谈等多种方法获得必要资料;能够对资料进行加工分析,依据观点、证据和结论之间的逻辑关系进行有条理的阐述,逐步培养科学态度与社会责任的能力。
3.能够从科学、环境、经济、社会等多个方面,权衡不同观点的利与弊,有依据地作出决策。
基础落实 必备知识全过关
自主梳理
1.氮及其化合物的转化关系
①N2+3H2 2NH3
②4NH3+5O2 4NO+6H2O
N2+O2 2NO
④2NO+O2==2NO2
3NO2+H2O==2HNO3+NO
HNO3+NH3==NH4NO3
⑦3Cu+8HNO3(稀) ==3Cu(NO3)2+2NO↑+4H2O
⑧Cu+4HNO3(浓) ==Cu(NO3)2+2NO2↑+2H2O
2.氮氧化物催化转化法
在汽车排气管上安装催化转化器,使汽车尾气中的NOx(NO或NO2)与CO反应转化成无毒的物质,反应原理为2NO+2CO N2+2CO2,
2NO2+4CO N2+4CO2。
【微思考】如何治理汽车尾气
提示 NOx尾气处理方法
①碱液吸收法:
2NO2+2NaOH==NaNO3+NaNO2+H2O
NO2+NO+2NaOH==2NaNO2+H2O
NO2、NO的混合气体能被足量烧碱溶液完全吸收的条件是n(NO2)≥n(NO)。一般适合工业尾气中NOx的处理。
②催化转化法:
在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体N2;NOx与CO在一定温度下催化转化为无毒气体N2和CO2(一般适用于汽车尾气的处理)。
重难探究 能力素养全提升
探究1
科学认识社会性科学议题,寻找利与弊
问题探究
汽车尾气有什么危害
提示 汽车尾气中的NOx在紫外线作用下,与碳氢化合物发生一系列光化学反应,产生了一种有毒的烟雾——光化学烟雾,光化学烟雾中含甲醛、乙醛等刺激性有毒物质,会刺激人的呼吸道。
归纳拓展
车辆限行,顾名思义,就是为了缓解交通压力或防治大气污染,而采取限制某些车辆通行的措施。车辆限行有很多种,有的是某个路段限行,有的是某个时段限行,有的是某种车型限行,还有最常见的是尾号限行。其中,尾号限行制度是为了缓解城市交通压力而催生的一种交通制度。如2008年的北京奥运测试赛期间,北京开始单双号限行。单号日子时候,只能车号的末尾数字是单号的私家车可以上路,双号日子的时候,只能车号末尾数字是双号的私家车可以上路。
方法导引“汽车限行”的利与弊
分析视角 利 弊
1.环境 视角 减少有害气体排放,减轻空气污染和温室效应 —
2.经济 视角 促使人们购买第二辆汽车,汽车销量增加,促进经济发展 导致汽车保有量增加
3.社会 视角 缓解了道路交通压力 增加公共交通压力,导致人们出行不便
应用体验
【例1】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氮有关(如下图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH3是形成无机颗粒物的催化剂
D.雾霾的形成与过度施用氮肥有关
答案 C
解析 雾和霾的分散剂均为空气,A项正确;根据题目信息,硝酸铵和硫酸铵均为无机颗粒物,是形成雾霾的因素之一,B项正确;氨气分别和硝酸、硫酸生成硝酸铵和硫酸铵,是形成无机颗粒物的反应物,C项错误;过度施用化肥会导致空气中氨气含量增加,促进了无机颗粒物中硝酸铵、硫酸铵含量的增加,D项正确。
变式训练1如图表示汽车尾气净化器处理汽车尾气的过程。有关叙述不正确的是( )
A.CO氧化为CO2所需氧来源于NOx
B.汽车安装这种净化器后,能避免铅污染
C.Pt-Rh催化剂化学反应前后质量不变
D.使用该净化器能减少酸雨的发生
答案 B
解析 由题目的信息可知,CO氧化为CO2所需的氧来源于氮的氧化物,A项正确;汽车安装这种净化器后,能避免一氧化碳、氮的氧化物造成的空气污染,但不能避免铅污染,B项错误;Pt-Rh催化剂在化学反应前后质量和化学性质都不变,C项正确;氮的氧化物也会造成酸雨,因此使用该净化器能减少酸雨的发生,D项正确。
探究2
学习科学论证,论证利与弊
问题探究
汽车尾号限行对治理空气污染有用吗
提示 通过一定的实际测定和对比,得出结论:汽车尾号限行的举措对于减轻空气污染是有一定效果的。
机动车尾气排放成为一个备受指责的因素,特别是柴油车和某些重型小轿车。这些汽车尾气中的化学元凶包括悬浮微粒(PM)和氮氧化物(NOx)。悬浮微粒是一种烟尘,能够侵入肺部并引起心血管疾病,氮氧化物则会加剧呼吸困难。
归纳拓展
方法导引科学论证的水平
水平 示例
水平1:有笼统的观点,缺少必要的资料 观点:采取“汽车限行”措施能够减轻空气污染
水平2:有观点和资料,缺少从资料到观点的推理过程或者推理过程不合理,或者资料不充分 观点:采取“汽车限行”措施能够减轻空气污染
资料:汽车行驶过程中会产生氮氧化物
水平 示例
水平3:有观点、资料以及从资料到观点的推理过程;资料充分,推理过程合理 观点:采取“汽车限行”措施能够减轻空气污染
资料:汽车行驶过程中会产生氮氧化物;大量汽车行驶会产生较多的氮氧化物;氮氧化物进入大气,会导致光化学烟雾,还会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题,污染大气
推理过程:汽车行驶过程中会产生氮氧化物→汽车尾气中有氮氧化物→氮氧化物进入大气(超过排放标准)→大气中的氮氧化物会导致光化学烟雾,也会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题
水平 示例
水平4:有观点、资料以及从资料到观点的推理过程;资料充分,推理过程合理;考虑了可能的反驳及其证据 观点:采取“汽车限行”措施能够减轻空气污染
资料:汽车行驶过程中会产生氮氧化物;大量汽车行驶会产生较多的氮氧化物;氮氧化物进入大气,会导致光化学烟雾,还会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题,污染大气推理过程:汽车行驶过程中会产生氮氧化物→汽车尾气中有氮氧化物→氮氧化物进入大气(超过排放标准)→大气中的氮氧化物导致光化学烟雾,也会转化为硝酸及其盐类物质导致酸雨、雾霾等环境问题
反驳及其证据:汽车中装有净化装置,会将氮氧化物转化成氮气后再排放
进一步推理:虽然有净化装置,但装置中的催化剂很容易中毒;一旦催化剂中毒,就不能有效吸收氮氧化物了。我国的汽车更换净化装置的比率很低
【例2】汽车排放的尾气中含有NO2,NO2是城市大气污染的主要污染物之一。在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为①2NO2→2NO+2O,②2NO+O2→2NO2,③O+O2→O3。下列对该反应过程及生成物叙述正确的是( )
A.NO2只起催化剂作用
B.NO起催化剂作用
C.NO2只起氧化剂作用
D.O3与O2互为同素异形体
应用体验
答案 D
解析 由反应过程①+②得O2 ―→ 2O,反应③为O+O2 ―→ O3,则NO2起催化剂作用,反应过程中NO2还做还原剂,A、B、C项错误;O3与O2互为同素异形体,D项正确。
变式训练2下列现象的产生,与氮循环无关的是( )
A.光化学烟雾 B.白色污染
C.水体富营养化 D.酸雨
答案 B
解析 光化学污染是氮的氧化物和有机烃类在光作用下的一系列复杂变化,与氮循环有关;白色污染是指难降解的塑料垃圾(多指塑料袋)对环境的污染;水体富营养化是指水中的氮、磷等元素浓度过大造成的水污染,会导致藻类疯长,从而引起水中缺氧,导致水生生物大量死亡,与氮循环有关;酸雨是二氧化硫和氮氧化物与雨水作用的结果,与氮循环有关。
探究3
权衡利弊,作出决策
问题探究
根据汽车限行的利弊,如何作出决策
提示 经过充分的论证分析后,分清主次,权衡利弊,作出决策。
归纳拓展
方法导引评价要素及评价等级
评价 要素 评价等级
A B C D
知识的 应用 不仅能充分、科学、合理地应用有关元素及其化合物的知识进行阐述分析,还能应用相关的新知识 能充分、科学、合理地应用有关元素及其化合物的知识进行阐述分析 能比较充分、科学地应用有关元素及其化合物的知识进行阐述分析 应用有关元素及其化合物的知识进行阐述分析时不够全面或出现错误
评价 要素 评价等级
A B C D
科学 论证 有针对议题的明确观点,资料充分,从资料到观点的推理过程合理,考虑了反驳及其证据 有针对议题的明确观点,资料充分,从资料到观点的推理过程合理 有针对议题的明确观点,资料比较充分,从资料到观点的推理过程有瑕疵但基本合理 有针对议题的明确观点,资料基本充分,但缺少从资料到观点的推理过程
评价 要素 评价等级
A B C D
科学态 度与社 会责任 素养 能根据实际情况,自主依据绿色化学思想和可持续发展观念对社会性科学议题进行综合分析 能根据实际情况,从科学、环境、经济、社会等方面对社会性科学议题进行具体分析 能分析社会性科学议题可能给环境、社会发展、人类健康等带来的双重影响,但不够充分、具体 仅关注对个体的影响,缺乏对环境、社会发展、人类健康等社会性影响的关注
应用体验
【例3】硫的氧化物、氮的氧化物是常见的大气污染物。
(1)酸雨是降水呈酸性(pH小于5.6)的统称,个别地方甚至低于2.1。引起酸雨的罪魁祸首是大气中的硫的氧化物和氮的氧化物,它们的主要来源是煤和石油的燃烧。
①汽车排放的尾气、硝酸厂和化肥厂的废气中都含有氮的氧化物,全世界每年氮氧化物的排放量约为5×107 kg。NO2溶于水生成 (写名称)和NO。
②为了减少酸雨的形成,必须减少SO2的排放量,对燃料中的硫元素进行固化处理,对废气中的氮的氧化物用 吸收,写出NO2与之反应的离子方程式: 。
(2)某化学兴趣小组选用下图实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。
①若原料气从左向右流,上述装置连接的顺序是:
原料气→ → → → → (填字母)。
②装置②中发生反应的离子方程式为 ;当装置②中出现 现象时,立即停止通气。
③你认为下列试剂中,可以用来代替试管中含碘的淀粉溶液的是
(填字母)。
A.酸性KMnO4溶液 B.NaOH溶液
C.溴水 D.氨水
解析 (1)①NO2溶于水生成硝酸和NO;②氮的氧化物能够与氢氧化钠溶液反应生成盐,达到吸收的目的;氢氧化钠与NO2反应生成硝酸钠和亚硝酸钠两种盐,离子方程式为
(2)①由于氮气、氧气都不溶于水,可以通过排水法测量其体积,因此正确的顺序为cdbae;②碘单质具有氧化性,把二氧化硫氧化为硫酸,本身还原为碘离子;由于淀粉遇碘显蓝色,当碘单质反应完全后,蓝色溶液恰好变为无色,立即停止通气;③酸性KMnO4溶液和溴水都具有氧化性,且溶液都有颜色,所以能够代替,NaOH溶液和氨水都能与二氧化硫反应,但是没现象,A、C正确。
变式训练3回答下列有关环境的问题:
(1)造成水体富营养化的元素是 和 ,水体富营养化的后果是导致水生藻类“疯长”,并迅速覆盖在水面上,在海水中形成 现象,而这种现象在淡水中称为 。
(2)大气中的下列氧化物的存在既不能形成酸雨,也不能形成光化学污染的是 。
A.二氧化硫 B.二氧化碳
C.二氧化氮 D.一氧化氮
(3)目前,大城市内的光化学污染是大气主要污染形式之一,该污染的现象是形成烟雾,故又叫光化学烟雾,形成光化学烟雾的过程属于
(填“化学变化”或“物理变化”)。
(4)汽车尾气中氮的氧化物来源除因为燃油中含有氮元素(燃烧时,氮转化为氮的氧化物)外,还有一个原因。请你用化学方程式表示这个原因: 。
答案 (1)氮 磷 赤潮 水华
(2)B (3)化学变化
(4)N2+O2 2NO
解析 (1)水体中过量的氮、磷造成了水体的富营养化,温度适宜则会导致近海水域的赤潮现象,在江河湖泊等淡水中爆发性生长藻类则叫水华。
(2)酸雨是指pH小于5.6的雨、雪、霜或其他形式的大气降水。二氧化碳溶解于水,尽管也可以使水显酸性,但大气中的二氧化碳在水中溶解后pH不可能小于5.6,故二氧化碳不是酸雨形成的原因。
(3)光化学烟雾的形成是一个复杂的氧化还原反应过程。
(4)机动车在工作时,其气缸内的温度和压力非常高,故吸入其中的空气(氮气与氧气)会相互反应,生成氮的氧化物。
学以致用 随堂检测全达标
1.世界大学生夏季运动会是规模仅次于夏季奥运会的世界级综合性运动会。2021年第31届世界大学生运动会在成都举办。“绿色”是成都的城市发展理念,也是这次运动会的组织理念。下面有关说法不正确的是( )
A.成都市目前使用的清洁燃料压缩天然气(CNG)和液化石油气(LPG)的主要成分均是烃类
B.兴建运动会场馆所用到的金属材料中可能含有非金属元素
C.“绿色化学”的核心是应用化学原理对环境污染进行治理
D.新能源汽车的使用有助于减少氮氧化物的排放
答案 C
解析 A项,压缩天然气(CNG)的主要成分是甲烷,液化石油气(LPG)的成分是丙烷、丁烷等,所以这两类燃料的主要成分都是烃类,故A正确;B项,合金可能含有非金属元素,故B正确;C项,“绿色化学”的核心是从源头上控制污染,而不是治理污染,故C错误;D项,新能源汽车的使用可减少化石燃料的使用,可减少常规汽车的使用,能减少氮氧化物的排放,故D正确。
2.当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中
的氮氧化物,其原理如下:
下列关于该“消除”过程的叙述不正确的是( )
A.部分光能转变为化学能 B.消除总变化为NOx+O2+H2O→HNO3
C.消除反应能全天候发生 D.使用纳米TiO2的消除效率更高
答案 C
解析 在TiO2的催化作用下紫外线提供能量,部分光能转变为化学能,故A项正确,不符合题意;题中示意图表明,在TiO2的催化作用下紫外线提供能量,发生反应:NOx+O2+H2O→HNO3,故B项正确,不符合题意;没有紫外线时上述反应不能发生,故C项错误,符合题意;纳米与紫外线接触面积更大,将产生更多的光生电子和光生空穴,从而消除更多的NOx,故D项正确,不符合题意。
3.SO2废气的回收利用方案如图所示。下列说法错误的是( )
B.Y中含有NH4HSO3
C.气体a既有氧化性又有还原性
D.(NH4)2S2O8是一种纯净物
答案 B
所以A项正确;(NH4)2SO3与过量H2SO4反应生成(NH4)2SO4、SO2和H2O,Y为(NH4)2SO4和过量的H2SO4,不含NH4HSO3,所以B项错误;气体a为SO2,SO2中S元素的化合价为+4价,既有氧化性又有还原性,所以C项正确;(NH4)2S2O8是一种化合物,属于纯净物,D项正确。
4.下图所示是酸雨的形成示意图。根据图示回答下列问题。
(1)下列气体容易形成酸雨的是 。
A.CO2 B.SO2 C.N2 D.NO2
(2)现有雨水样品1份,每隔一段时间测定该
雨水样品的pH,所得数据如下:
测试时间/h 0 1 2 3 4
雨水的pH 4.73 4.63 4.56 4.55 4.55
分析数据,回答下列问题:
①雨水样品的pH变化的原因是 (用化学方程式表示)。
②如果将刚取样的上述雨水和自来水相混合,雨水pH将变 。
(3)下列措施中,可减少酸雨产生的是 (填字母)。
①少用煤作燃料 ②把工厂烟囱造高
③燃料脱硫 ④在已酸化的土壤中加石灰
⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
答案 (1)BD (2)①SO2+H2O H2SO3、2H2SO3+O2 === 2H2SO4 ②小 (3)C
解析 (1)SO2、NO2的大量排放易形成酸雨。
(2)①雨水放置过程中pH变小,其原因是SO2与H2O反应生成的H2SO3被空气中氧气氧化所致:SO2+H2O H2SO3、2H2SO3+O2 === 2H2SO4。②雨水和自来水混合,应考虑SO2(或H2SO3)与Cl2(或HClO)的反应,反应后生成强酸,因此雨水与自来水混合后,其pH将变小。
5.(2020山东潍坊高一期末)我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有 (写化学式)。
(2)图中物质溶于水溶液呈碱性的是 。
(3)写出SO2转化为SO3的化学方程式: 。
(4)工业上利用氨气制备一氧化氮,反应的化学方程式为
。
(5)实验室长期保存浓硝酸,需使用棕色试剂瓶,并放置在阴凉处,其原因为
(用化学方程式表示)。
(6)氨气与一氧化氮(NO)在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为 。
解析 (1)酸性氧化物是能与碱反应得到盐和水的氧化物,符合要求的有SO2、SO3和N2O5。
(2)图中物质溶于水呈碱性的只有NH3。
(3)二氧化硫在催化剂存在时可以转化为三氧化硫:2SO2+O2 2SO3。
(4)氨气经催化氧化可以形成一氧化氮:4NH3+5O2 4NO+6H2O。
(5)浓硝酸见光或受热时易发生分解反应4HNO3 4NO2↑+O2↑+2H2O,因此要保存在棕色试剂瓶中。
(6)氨气中的氮为-3价,一氧化氮中的氮为+2价,因此二者可以在一定条件下发生归中反应得到氮气:6NO+4NH3 5N2+6H2O。
好好学习 继续努力
