高二化学复习:氯及其化合物 课件(共15张PPT)
文档属性
| 名称 | 高二化学复习:氯及其化合物 课件(共15张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-14 00:00:00 | ||
图片预览



文档简介
(共15张PPT)
高二化学复习
氯及其化合物
1. 氯元素单质及其重要化合物的制备方法,掌握其主要性质及应用;
2. 氯水的性质及其成分探究;
3. 常见的含氯消毒剂及其合理使用;
复习目标
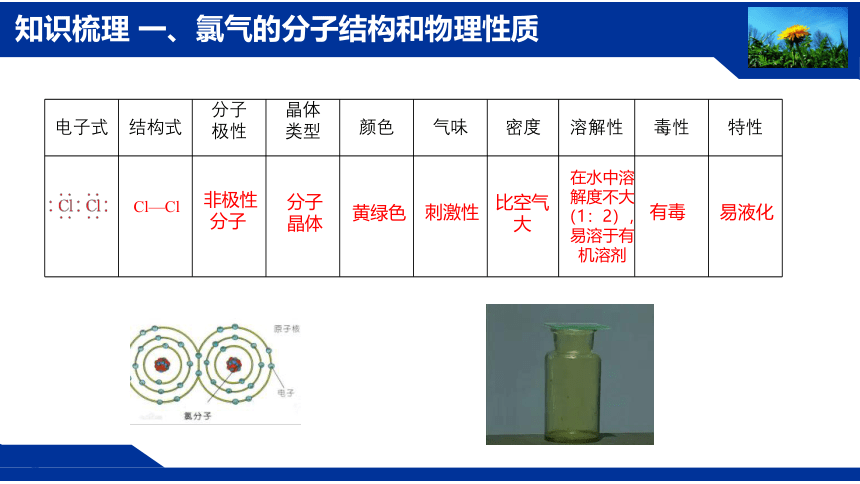
知识梳理 一、氯气的分子结构和物理性质
电子式 结构式 分子 极性 晶体 类型 颜色 气味 密度 溶解性 毒性 特性
Cl—Cl
非极性
分子
分子
晶体
黄绿色
刺激性
比空气大
在水中溶解度不大
(1:2),易溶于有机溶剂
有毒
易液化
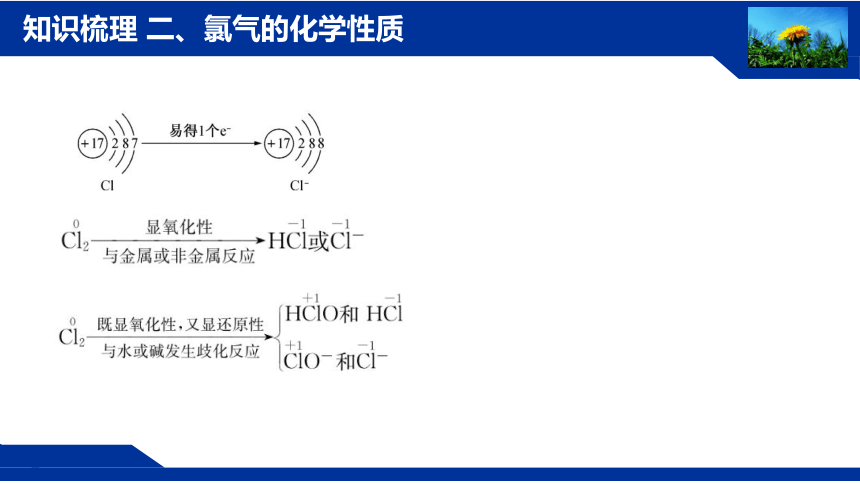
知识梳理 二、氯气的化学性质
体现氧化性 与金属 与Fe:
与Cu:
与非金属 与H2:
能将P、Si氧化为:
与还原性化合物 与KI溶液:
与FeCl2溶液:
与SO2水溶液:
与NH3反应:
既先氧化性又显还原性 与H2O
与碱 与NaOH溶液:
与Ca(OH)2溶液:
Cu+Cl2 CuCl2
点燃
==
知识梳理 二、氯气的化学性质
2Fe+3Cl2 2FeCl3
点燃
==
(棕褐色烟)
(棕黄色烟)
H2+ Cl2 2HCl
点燃:安静燃烧,有苍白色火焰,有白雾
光照:剧烈反应,发生爆炸,有白雾
PCl3、PCl5、SiCl4
Cl2+2KI == I2+2KCl
Cl2 + 2FeCl2 == 2FeCl3
Cl2 + SO2 + 2H2O == H2SO4 + 2HCl
Cl2+H2O HCl+HClO
离子:
Cl2+H2O H++Cl-+HClO
Cl2 + 2NaOH == NaCl + NaClO + H2O
2Cl2 + 2Ca(OH)2 == CaCl2 + Ca(ClO)2 + 2H2O
(吸收氯气尾气或制消毒液)
(工业制漂白粉)
3Cl2 +8NH3 == N2+ 6NH4Cl
(检验氯气:湿润的淀粉碘化钾试纸变蓝)
(检验氯气是否泄露)
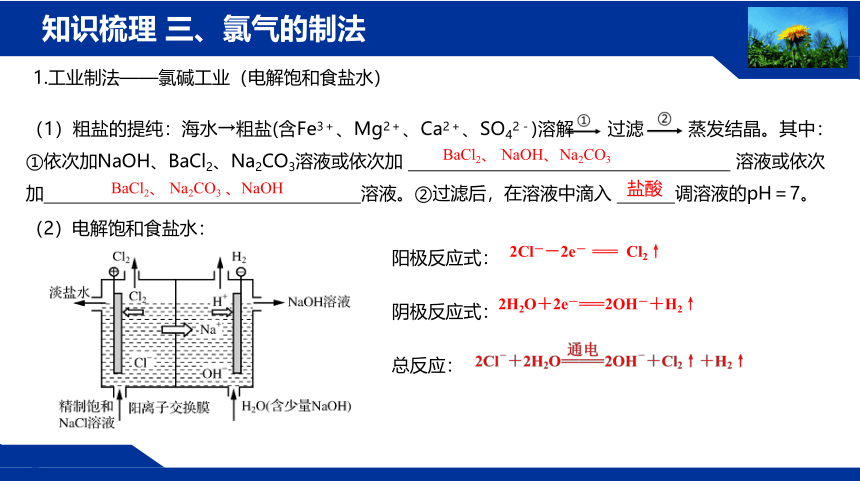
知识梳理 三、氯气的制法
1.工业制法——氯碱工业(电解饱和食盐水)
(1)粗盐的提纯:海水→粗盐(含Fe3+、Mg2+、Ca2+、SO42-)溶解 过滤 蒸发结晶。其中:①依次加NaOH、BaCl2、Na2CO3溶液或依次加 溶液或依次
加 溶液。②过滤后,在溶液中滴入 调溶液的pH=7。
(2)电解饱和食盐水:
阳极反应式:
阴极反应式:
总反应:
BaCl2、 NaOH、Na2CO3
BaCl2、 Na2CO3 、NaOH
盐酸
2Cl--2e- === Cl2↑
2H2O+2e-===2OH-+H2↑
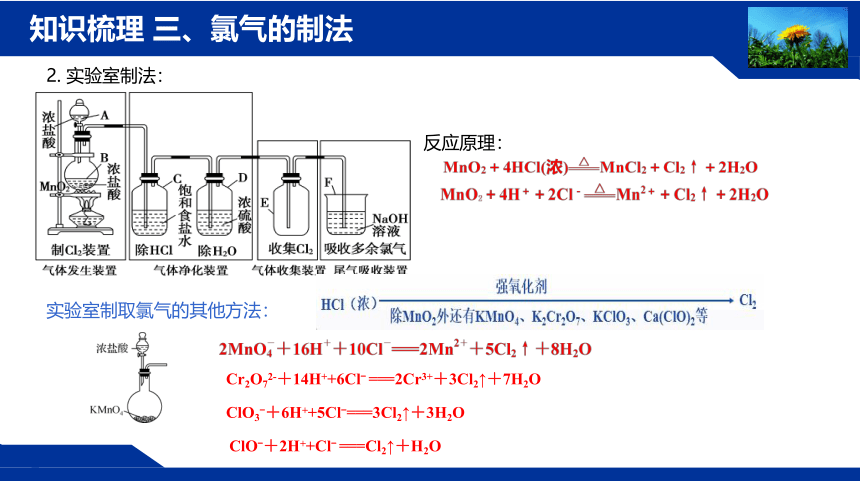
知识梳理 三、氯气的制法
2. 实验室制法:
反应原理:
实验室制取氯气的其他方法:
Cr2O72-+14H++6Cl- ===2Cr3++3Cl2↑+7H2O
ClO3-+6H++5Cl-===3Cl2↑+3H2O
ClO-+2H++Cl- ===Cl2↑+H2O
知识梳理 四、含氯化合物
1. 次氯酸(HClO)
(1) HClO是弱酸:酸性比碳酸 。
(2) HClO不稳定性: 。
(3) HClO具有较强的氧化性:作杀菌消毒剂、漂白剂。
2. 漂白粉
(1) 工业上制取漂白粉是用氯气与石灰乳反应制得,不是用氯气与石灰水反应制得。
漂白粉是混合物[CaCl2、Ca(ClO)2],其中有效成分是________________。
(2) 漂白粉的漂白原理:
化学方程式:_____________________________________。
弱
Ca(ClO)2
知识梳理 四、含氯化合物
3. NaClO
NaClO具有强的氧化性,能杀菌消毒,可以漂白棉、麻、纸张。
“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)混合立即会产生氯气,其离子方程式: 。
4. ClO2
二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是自来水消毒和果蔬保鲜等方面应用广泛且高效、低毒的消毒剂。二氧化氯(ClO2)具有很强的杀菌消毒能力是因为其具有 性。
ClO-+2H++Cl- ===Cl2↑+H2O
强氧化
能力提升 一、从平衡的角度理解氯水的成分和性质
氯气能溶于水(1∶2),氯气的水溶液称为氯水,溶于水的氯气只有少量与水反应。
三种平衡关系:
H2O H++OH-
HClO H++ClO-
Cl2+H2O H++Cl-+HClO
能力提升 二、卤素的歧化反应与归中反应
1. 歧化反应
2. 归中反应
Cl2+2OH- == Cl- + ClO- + H2O
Δ
3Cl2+6OH- == 5Cl- + ClO3- + 3H2O
Cl- + ClO- +2H+ == Cl2 ↑+ H2O
5Cl- + ClO3- +6H+ == 3Cl2 ↑+ 3H2O
实战演练
1. 某同学用下列装置制备并检验Cl2的性质下列说法正确的是
A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B.Ⅱ图中:量筒中发生了加成反应
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中至溶液显酸性,结果有Cl2生成
D
实战演练
2. 氯及其化合物在生产、生活中有广泛应用。下列物质的性质与用途具有对应关系的是
Cl2 能溶于水,可用于工业制盐酸
ClO2有强氧化性,可用于自来水消毒
C. HClO不稳定,可用作棉、麻的漂白剂
D. FeCl3溶液呈酸性,可用于蚀刻印刷电路板
B
实战演练
3. 以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2 分解为CaCl2和O2。
①生成Ca(ClO)2的化学方程式为 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有 。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为:
6 Ca(OH)2+6 Cl2=Ca(ClO3)2+5 CaCl2+6H2O 氯化完成后过滤。
①滤渣的主要成分为 (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] ∶n[CaCl2] 1∶5
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100g L-1,从该溶液中尽可能多地析出KClO3固体的方法是 。
2Cl2+ 2Ca(OH)2== Ca(ClO)2+ CaCl2+ 2H2O
AB
CaCO3、Ca(OH)2
蒸发浓缩、冷却结晶
<
谢 谢
高二化学复习
高二化学复习
氯及其化合物
1. 氯元素单质及其重要化合物的制备方法,掌握其主要性质及应用;
2. 氯水的性质及其成分探究;
3. 常见的含氯消毒剂及其合理使用;
复习目标
知识梳理 一、氯气的分子结构和物理性质
电子式 结构式 分子 极性 晶体 类型 颜色 气味 密度 溶解性 毒性 特性
Cl—Cl
非极性
分子
分子
晶体
黄绿色
刺激性
比空气大
在水中溶解度不大
(1:2),易溶于有机溶剂
有毒
易液化
知识梳理 二、氯气的化学性质
体现氧化性 与金属 与Fe:
与Cu:
与非金属 与H2:
能将P、Si氧化为:
与还原性化合物 与KI溶液:
与FeCl2溶液:
与SO2水溶液:
与NH3反应:
既先氧化性又显还原性 与H2O
与碱 与NaOH溶液:
与Ca(OH)2溶液:
Cu+Cl2 CuCl2
点燃
==
知识梳理 二、氯气的化学性质
2Fe+3Cl2 2FeCl3
点燃
==
(棕褐色烟)
(棕黄色烟)
H2+ Cl2 2HCl
点燃:安静燃烧,有苍白色火焰,有白雾
光照:剧烈反应,发生爆炸,有白雾
PCl3、PCl5、SiCl4
Cl2+2KI == I2+2KCl
Cl2 + 2FeCl2 == 2FeCl3
Cl2 + SO2 + 2H2O == H2SO4 + 2HCl
Cl2+H2O HCl+HClO
离子:
Cl2+H2O H++Cl-+HClO
Cl2 + 2NaOH == NaCl + NaClO + H2O
2Cl2 + 2Ca(OH)2 == CaCl2 + Ca(ClO)2 + 2H2O
(吸收氯气尾气或制消毒液)
(工业制漂白粉)
3Cl2 +8NH3 == N2+ 6NH4Cl
(检验氯气:湿润的淀粉碘化钾试纸变蓝)
(检验氯气是否泄露)
知识梳理 三、氯气的制法
1.工业制法——氯碱工业(电解饱和食盐水)
(1)粗盐的提纯:海水→粗盐(含Fe3+、Mg2+、Ca2+、SO42-)溶解 过滤 蒸发结晶。其中:①依次加NaOH、BaCl2、Na2CO3溶液或依次加 溶液或依次
加 溶液。②过滤后,在溶液中滴入 调溶液的pH=7。
(2)电解饱和食盐水:
阳极反应式:
阴极反应式:
总反应:
BaCl2、 NaOH、Na2CO3
BaCl2、 Na2CO3 、NaOH
盐酸
2Cl--2e- === Cl2↑
2H2O+2e-===2OH-+H2↑
知识梳理 三、氯气的制法
2. 实验室制法:
反应原理:
实验室制取氯气的其他方法:
Cr2O72-+14H++6Cl- ===2Cr3++3Cl2↑+7H2O
ClO3-+6H++5Cl-===3Cl2↑+3H2O
ClO-+2H++Cl- ===Cl2↑+H2O
知识梳理 四、含氯化合物
1. 次氯酸(HClO)
(1) HClO是弱酸:酸性比碳酸 。
(2) HClO不稳定性: 。
(3) HClO具有较强的氧化性:作杀菌消毒剂、漂白剂。
2. 漂白粉
(1) 工业上制取漂白粉是用氯气与石灰乳反应制得,不是用氯气与石灰水反应制得。
漂白粉是混合物[CaCl2、Ca(ClO)2],其中有效成分是________________。
(2) 漂白粉的漂白原理:
化学方程式:_____________________________________。
弱
Ca(ClO)2
知识梳理 四、含氯化合物
3. NaClO
NaClO具有强的氧化性,能杀菌消毒,可以漂白棉、麻、纸张。
“84”消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)混合立即会产生氯气,其离子方程式: 。
4. ClO2
二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,是自来水消毒和果蔬保鲜等方面应用广泛且高效、低毒的消毒剂。二氧化氯(ClO2)具有很强的杀菌消毒能力是因为其具有 性。
ClO-+2H++Cl- ===Cl2↑+H2O
强氧化
能力提升 一、从平衡的角度理解氯水的成分和性质
氯气能溶于水(1∶2),氯气的水溶液称为氯水,溶于水的氯气只有少量与水反应。
三种平衡关系:
H2O H++OH-
HClO H++ClO-
Cl2+H2O H++Cl-+HClO
能力提升 二、卤素的歧化反应与归中反应
1. 歧化反应
2. 归中反应
Cl2+2OH- == Cl- + ClO- + H2O
Δ
3Cl2+6OH- == 5Cl- + ClO3- + 3H2O
Cl- + ClO- +2H+ == Cl2 ↑+ H2O
5Cl- + ClO3- +6H+ == 3Cl2 ↑+ 3H2O
实战演练
1. 某同学用下列装置制备并检验Cl2的性质下列说法正确的是
A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B.Ⅱ图中:量筒中发生了加成反应
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中至溶液显酸性,结果有Cl2生成
D
实战演练
2. 氯及其化合物在生产、生活中有广泛应用。下列物质的性质与用途具有对应关系的是
Cl2 能溶于水,可用于工业制盐酸
ClO2有强氧化性,可用于自来水消毒
C. HClO不稳定,可用作棉、麻的漂白剂
D. FeCl3溶液呈酸性,可用于蚀刻印刷电路板
B
实战演练
3. 以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2 分解为CaCl2和O2。
①生成Ca(ClO)2的化学方程式为 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有 。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为:
6 Ca(OH)2+6 Cl2=Ca(ClO3)2+5 CaCl2+6H2O 氯化完成后过滤。
①滤渣的主要成分为 (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] ∶n[CaCl2] 1∶5
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100g L-1,从该溶液中尽可能多地析出KClO3固体的方法是 。
2Cl2+ 2Ca(OH)2== Ca(ClO)2+ CaCl2+ 2H2O
AB
CaCO3、Ca(OH)2
蒸发浓缩、冷却结晶
<
谢 谢
高二化学复习
同课章节目录
