高二化学复习:卤族元素 课件(共17张PPT)
文档属性
| 名称 | 高二化学复习:卤族元素 课件(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-14 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
高二化学复习
卤族元素
1. 掌握氯、溴、碘单质及其化合物的递变规律和重要用途;
2. 了解卤素离子的检验方法;
3. 了解溴、碘的提取工艺。
复习目标
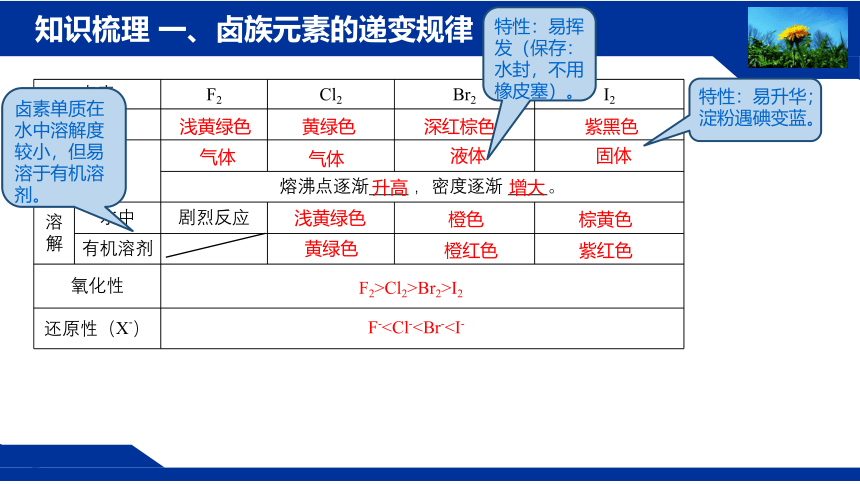
卤素 F2 Cl2 Br2 I2
颜色
状态
熔沸点逐渐 ,密度逐渐 。 溶解 水中 剧烈反应
有机溶剂
氧化性 还原性(X-) 浅黄绿色
黄绿色
深红棕色
紫黑色
气体
气体
液体
固体
升高
增大
浅黄绿色
紫红色
橙红色
黄绿色
橙色
棕黄色
卤素单质在水中溶解度较小,但易溶于有机溶剂。
F2>Cl2>Br2>I2
F-特性:易挥发(保存:水封,不用橡皮塞)。
特性:易升华;淀粉遇碘变蓝。
知识梳理 一、卤族元素的递变规律
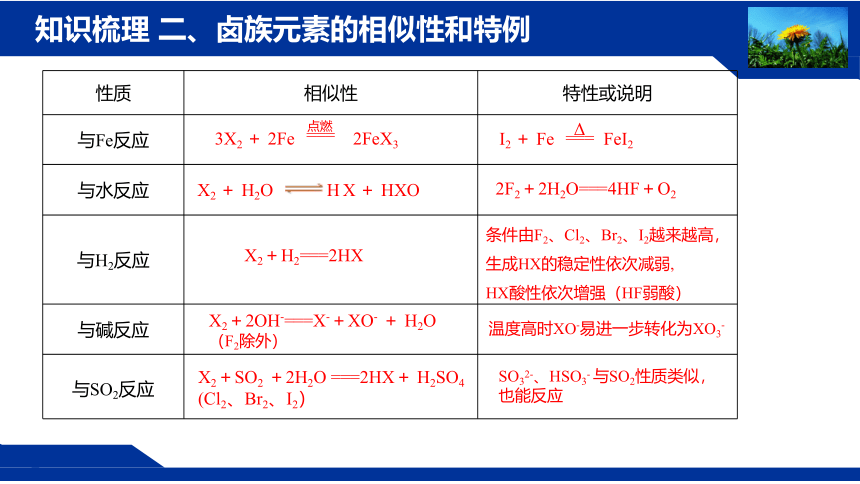
知识梳理 二、卤族元素的相似性和特例
性质 相似性 特性或说明
与Fe反应
与水反应
与H2反应
与碱反应
3X2 + 2Fe 2FeX3
===
点燃
Δ
I2 + Fe FeI2
===
X2 + H2O H X + HXO
2F2+2H2O===4HF+O2
X2+H2===2HX
条件由F2、Cl2、Br2、I2越来越高,生成HX的稳定性依次减弱,
HX酸性依次增强(HF弱酸)
X2+2OH-===X-+XO- + H2O
(F2除外)
温度高时XO-易进一步转化为XO3-
X2+SO2 +2H2O ===2HX+ H2SO4
(Cl2、Br2、I2)
与SO2反应
SO32-、HSO3- 与SO2性质类似,也能反应
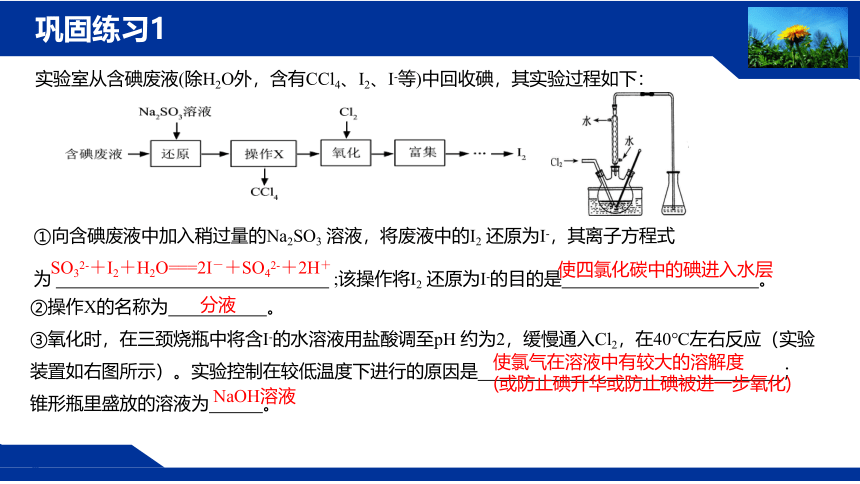
实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
①向含碘废液中加入稍过量的Na2SO3 溶液,将废液中的I2 还原为I-,其离子方程式为 ;该操作将I2 还原为I-的目的是 。
②操作X的名称为 。
③氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH 约为2,缓慢通入Cl2,在40℃左右反应(实验装置如右图所示)。实验控制在较低温度下进行的原因是 ;锥形瓶里盛放的溶液为 。
SO32-+I2+H2O===2I-+SO42-+2H+
使四氯化碳中的碘进入水层
分液
使氯气在溶液中有较大的溶解度
(或防止碘升华或防止碘被进一步氧化)
NaOH溶液
巩固练习1
1.沉淀法:
2.萃取法:
3.淀粉法:
知识梳理 三、卤素离子的检验
AgCl、AgBr、AgI难溶于水和稀硝酸
AgBr用于感光材料
AgI用于人工降雨
室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
A 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 X溶液中一定含有Fe2+
B 向浓度均为0.05 mol·L 1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 Ksp(AgI)> Ksp(AgCl)
C 向3 mL KI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 Br2的氧化性比I2的强
D 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 HNO2电离出H+的能力比CH3COOH的强
C
巩固练习2
知识梳理 四、溴碘的提取工艺
从海水中提取溴:
(1) 氧化: 。
(2) 吹出:利用溴的 性,通入 ,吹出溴蒸气。
(3) 吸收: (或: )
(4) 制粗溴: (或: )
(5) 精制:粗溴精制后得到高纯度溴。
易挥发
热空气或水蒸气
SO2+Br2+2H2O===2HBr+ H2SO4
3Br2+3Na2CO3===5NaBr+NaBrO3+3CO2↑
Cl2+2Br-===Br2+2Cl-
5Br-+BrO3- +6H+===3Br2+3H2O
Cl2+2Br-===Br2+2Cl-
知识梳理 四、溴碘的提取工艺
从海带中提取碘:
问:涉及的离子方程式:
①:
②:
③:
2I-+2H++H2O2===I2+2H2O
3I2+6OH-===5I-+IO3-+3H2O
5I-+IO3-+6H+===3I2+3H2O
知识梳理 四、溴碘的提取工艺
从海带中提取碘:
问:①浸泡时如何提高碘的浸出率?
②加NaOH溶液碱化的目的?
将干海带粉碎、适当提高浸取液的温度、延长浸泡时间、搅拌等。
干海带浸泡时除碘离子外部分有机质(褐藻糖胶,具有抗氧化性)也会进入溶液,这部分有机质会降低碘提取的效率,可以通过加入NaOH形成有机物沉淀而除去。
实战演练
1. 下列叙述中正确的是
A. 液溴应保存于带磨口玻璃塞的棕色细口瓶中,并加水“水封”以减少其挥发
B. 碘易升华,可用加热升华法除去NH4Cl中混有的I2
C. 食盐中的加碘物质为KIO3,加淀粉变蓝
D. 溴化银具有感光性,可用于人工降雨
A
实战演练
C
3. 下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
实战演练
B
4. 通过下列实验可从I2的CCl4溶液中回收I2。
下列说法正确的是
NaOH溶液与I2反应的离子方程式:
B. 通过过滤可将水溶液与CCl4分离
C. 向加酸后的上层清液中滴加AgNO3溶液生成AgI沉淀,
1个AgI晶胞(如图)中含14个I-
D. 回收的粗碘可通过升华进行纯化
实战演练
D
5. 常用的杀菌消毒剂二氯异氰尿酸钠(C3N3O3Cl2Na)优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为:
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol L-1Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①通过计算判断该样品是否为优质品 。(已知, )
②若在检测中加入稀硫酸的量过少,将导致样品有效氯测定值 (填“偏高”或“偏低”)。
实战演练
知识体系
谢 谢
高二化学复习
高二化学复习
卤族元素
1. 掌握氯、溴、碘单质及其化合物的递变规律和重要用途;
2. 了解卤素离子的检验方法;
3. 了解溴、碘的提取工艺。
复习目标
卤素 F2 Cl2 Br2 I2
颜色
状态
熔沸点逐渐 ,密度逐渐 。 溶解 水中 剧烈反应
有机溶剂
氧化性 还原性(X-) 浅黄绿色
黄绿色
深红棕色
紫黑色
气体
气体
液体
固体
升高
增大
浅黄绿色
紫红色
橙红色
黄绿色
橙色
棕黄色
卤素单质在水中溶解度较小,但易溶于有机溶剂。
F2>Cl2>Br2>I2
F-
特性:易升华;淀粉遇碘变蓝。
知识梳理 一、卤族元素的递变规律
知识梳理 二、卤族元素的相似性和特例
性质 相似性 特性或说明
与Fe反应
与水反应
与H2反应
与碱反应
3X2 + 2Fe 2FeX3
===
点燃
Δ
I2 + Fe FeI2
===
X2 + H2O H X + HXO
2F2+2H2O===4HF+O2
X2+H2===2HX
条件由F2、Cl2、Br2、I2越来越高,生成HX的稳定性依次减弱,
HX酸性依次增强(HF弱酸)
X2+2OH-===X-+XO- + H2O
(F2除外)
温度高时XO-易进一步转化为XO3-
X2+SO2 +2H2O ===2HX+ H2SO4
(Cl2、Br2、I2)
与SO2反应
SO32-、HSO3- 与SO2性质类似,也能反应
实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
①向含碘废液中加入稍过量的Na2SO3 溶液,将废液中的I2 还原为I-,其离子方程式为 ;该操作将I2 还原为I-的目的是 。
②操作X的名称为 。
③氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH 约为2,缓慢通入Cl2,在40℃左右反应(实验装置如右图所示)。实验控制在较低温度下进行的原因是 ;锥形瓶里盛放的溶液为 。
SO32-+I2+H2O===2I-+SO42-+2H+
使四氯化碳中的碘进入水层
分液
使氯气在溶液中有较大的溶解度
(或防止碘升华或防止碘被进一步氧化)
NaOH溶液
巩固练习1
1.沉淀法:
2.萃取法:
3.淀粉法:
知识梳理 三、卤素离子的检验
AgCl、AgBr、AgI难溶于水和稀硝酸
AgBr用于感光材料
AgI用于人工降雨
室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
A 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 X溶液中一定含有Fe2+
B 向浓度均为0.05 mol·L 1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 Ksp(AgI)> Ksp(AgCl)
C 向3 mL KI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 Br2的氧化性比I2的强
D 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 HNO2电离出H+的能力比CH3COOH的强
C
巩固练习2
知识梳理 四、溴碘的提取工艺
从海水中提取溴:
(1) 氧化: 。
(2) 吹出:利用溴的 性,通入 ,吹出溴蒸气。
(3) 吸收: (或: )
(4) 制粗溴: (或: )
(5) 精制:粗溴精制后得到高纯度溴。
易挥发
热空气或水蒸气
SO2+Br2+2H2O===2HBr+ H2SO4
3Br2+3Na2CO3===5NaBr+NaBrO3+3CO2↑
Cl2+2Br-===Br2+2Cl-
5Br-+BrO3- +6H+===3Br2+3H2O
Cl2+2Br-===Br2+2Cl-
知识梳理 四、溴碘的提取工艺
从海带中提取碘:
问:涉及的离子方程式:
①:
②:
③:
2I-+2H++H2O2===I2+2H2O
3I2+6OH-===5I-+IO3-+3H2O
5I-+IO3-+6H+===3I2+3H2O
知识梳理 四、溴碘的提取工艺
从海带中提取碘:
问:①浸泡时如何提高碘的浸出率?
②加NaOH溶液碱化的目的?
将干海带粉碎、适当提高浸取液的温度、延长浸泡时间、搅拌等。
干海带浸泡时除碘离子外部分有机质(褐藻糖胶,具有抗氧化性)也会进入溶液,这部分有机质会降低碘提取的效率,可以通过加入NaOH形成有机物沉淀而除去。
实战演练
1. 下列叙述中正确的是
A. 液溴应保存于带磨口玻璃塞的棕色细口瓶中,并加水“水封”以减少其挥发
B. 碘易升华,可用加热升华法除去NH4Cl中混有的I2
C. 食盐中的加碘物质为KIO3,加淀粉变蓝
D. 溴化银具有感光性,可用于人工降雨
A
实战演练
C
3. 下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
实战演练
B
4. 通过下列实验可从I2的CCl4溶液中回收I2。
下列说法正确的是
NaOH溶液与I2反应的离子方程式:
B. 通过过滤可将水溶液与CCl4分离
C. 向加酸后的上层清液中滴加AgNO3溶液生成AgI沉淀,
1个AgI晶胞(如图)中含14个I-
D. 回收的粗碘可通过升华进行纯化
实战演练
D
5. 常用的杀菌消毒剂二氯异氰尿酸钠(C3N3O3Cl2Na)优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为:
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用0.1000mol L-1Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液20.00mL。
①通过计算判断该样品是否为优质品 。(已知, )
②若在检测中加入稀硫酸的量过少,将导致样品有效氯测定值 (填“偏高”或“偏低”)。
实战演练
知识体系
谢 谢
高二化学复习
同课章节目录
