3.1卤代烃课件2021-2022学年高二化学人教版(2019)选择性必修3(25张ppt)
文档属性
| 名称 | 3.1卤代烃课件2021-2022学年高二化学人教版(2019)选择性必修3(25张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-16 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
第一节 卤代烃
高二—人教版—化学—选择性必修3—第三章
1.能辨识卤代烃的官能团,并根据官能团对卤代烃进行分类;能列举典型卤代烃
的主要物理性质及应用。
2.能从溴乙烷的官能团和化学键特点预测可能的断键部位和化学性质,结合实验
了解溴乙烷与NaOH水溶液的反应,能写出相应的化学方程式。
3.通过1-溴丁烷取代反应和消去反应的探究实验进行对比和归纳,形成“化学
反应可以调控”的观念,通过类比迁移形成对卤代烃反应基本规律的认识。
4.通过了解卤代烃在生活中的应用,认识化学对满足人类生活需要的积极贡献,
树立保护环境和可持续发展的意识。
学习目标
复方氯乙烷气雾剂
我们经常看到足球场上球员受伤后,队医会往伤处喷一种液体,喷完以后没什么大碍的球员就可以上场比赛了,这种喷雾的主要成分——氯乙烷,就属于卤代烃。
氯乙烷为什么可以用于紧急治疗呢?
卤代烃能发生哪些反应呢?
生活中还有哪些物质属于卤代烃呢?
阅读课本P52第一段及资料卡片,思考以下问题:
1. 什么是卤代烃?有哪些分类?
2. 结合第二章学习的烃,想想通过哪些反应可以将烃转化为卤代烃?
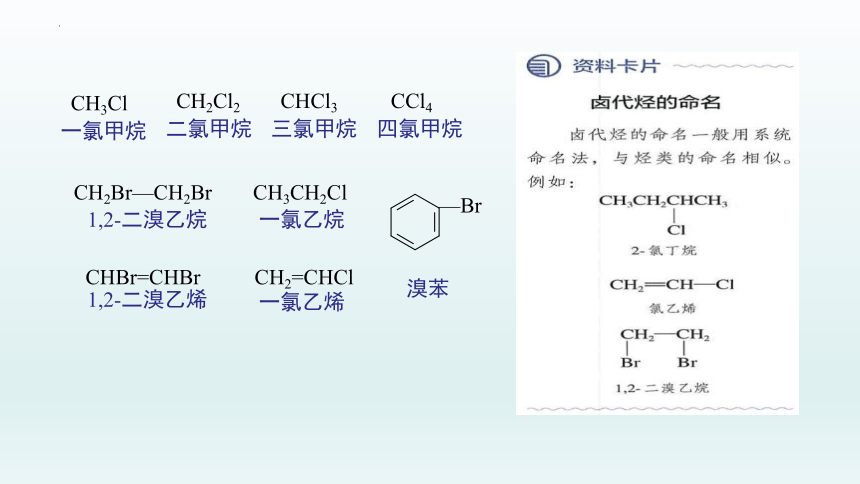
3. 卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出
卤代烃的命名原则。
一. 卤代烃
烃分子中的氢原子被卤素原子(X)取代后生成的化合物
1. 分类
饱和一元卤代烃的通式:CnH2n+1X
CH2=CH2 + HCl CH3CH2Cl
一定条件
CH3CH3 + Cl2 CH3CH2Cl + HCl
光
加成反应
取代反应
用R—X表示
CH3Cl
CH2Cl2
CHCl3
CCl4
CH2Br—CH2Br
CH3CH2Cl
CHBr=CHBr
CH2=CHCl
一氯甲烷
二氯甲烷
三氯甲烷
四氯甲烷
溴苯
1,2-二溴乙烷
一氯乙烷
1,2-二溴乙烯
一氯乙烯
—Br
一. 卤代烃
2. 命名
选主链
定编号
写名称
从距简单取代基近的一端编号,
有碳碳双键从距离碳碳双键近的一端编号
3-甲基-4-氯-1-丁烯
以烃为母体,卤原子为取代基,类似烃的命名
2-甲基-2-溴丙烷
3. 物理性质
一. 卤代烃
常温下,个别是气体,大多数为液体或固体
不溶于水,可溶于有机溶剂
名称 结构简式 液态时密度/(g·cm—3) 沸点/℃
氯甲烷 CH3Cl 0.916 -24
氯乙烷 CH3CH2Cl 0.898 12
1-氯丙烷 CH3CH2CH2Cl 0.890 46
1-氯丁烷 CH3CH2CH2CH2Cl 0.886 78
1-氯戊烷 CH3CH2CH2CH2CH2Cl 0.882 108
气体
气体
液体
液体
液体
③状态:
④溶解性:
随碳原子数的增加而升高
②沸点:
一氟代烃和一氯代烃的密度比水小,其余卤代烃密度都比水大
①密度:
随碳原子数的增加而减小
课本P52表3-1 卤代烃的密度和沸点
二. 溴乙烷
1. 分子结构
分子式
结构式
C2H5Br
结构简式
CH3CH2Br 或 C2H5Br
官能团
2. 物理性质
无色液体,沸点38.4℃,密度比水大,难溶于水,易溶于有机溶剂
碳溴键C-Br
球棍模型
核磁共振氢谱
电子式
空间填充模型
颜色 状态 密度 沸点
溴乙烷C2H5Br 无色 液体 比水大 38.4℃
乙烷C2H6 无色 气体 比水小 - 88.6 ℃
结合选择性必修2的知识,思考:为什么溴乙烷的密度、沸点比乙烷大呢?
乙烷和溴乙烷都属于分子晶体,结构相似,
由于溴原子取代了氢原子,
导致溴乙烷的相对分子质量比乙烷大,范德华力增大,沸点升高
官能团C—Br的引入影响了物理性质
结 构 分 析
物 理 性 质
解 释
结 构 分 析
化 学 性 质
推 断
化学键 C—C C—H C—Br
键长/pm 154 110 194
键能/(kJ/mol) 347.3 414.2 284.5
溴原子电负性比碳原子大,C—Br键为极性键
C—Br键键长较长,键能较小
电负性:C:2.5 Br:2.8 H:2.1
δ+
δ—
C—Br键较易断裂生成Br-
结合选择性必修2的知识,思考:溴乙烷的可能断键位置?
乙基是推电子基团,使C—Br键极性更强
二. 溴乙烷
3. 化学性质
CH3CH2—Br + H—OH
CH3CH2—OH + HBr
如何通过实验证明此反应断裂了C—Br键,产生了Br-?
溴乙烷
滴加AgNO3溶液
滴加AgNO3溶液
溴乙烷不能电离出Br-
溴乙烷、水
断裂C—Br键,生成了Br-
实验设想:
(1) 水解反应
(1) 水解反应、取代反应
请认真观看课本P53【实验3—1】溴乙烷水解反应的视频,记录实验现象。
结论:溴乙烷确实发生了水解反应,断裂了C—Br键,生成了Br-
现象:有淡黄色AgBr沉淀生成
取一支试管,滴入10~15滴溴乙烷,再加入1mL 5%NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察实验现象。
阅读课本P53【实验3—1】,思考以下问题:
1. 加热的作用是什么?
加快反应速率
4. 为什么要加入稀硝酸?
2. 为什么会分层?溴乙烷在哪一层?
溴乙烷不溶于水,比水重,溴乙烷在下层
3. 从平衡移动的角度分析,加入NaOH的作用是什么?
加入NaOH,使HBr的浓度减小,平衡向正反应方向移动
中和未反应完的NaOH,防止其与AgNO3反应生成黑褐色沉淀Ag2O
Ag+ + OH- == AgOH(白色)↓ 2AgOH == Ag2O(褐色) + H2O
分层消失:
溴乙烷彻底反应
需要过量!
(1)水解反应、取代反应
NaOH + HBr == NaBr + H2O
二. 溴乙烷
3. 化学性质
CH3CH2—Br + H—OH
CH3CH2—OH + HBr
CH3CH2Br + NaOH CH3CH2OH + NaBr
水
△
(2)消去反应
二. 溴乙烷
3. 化学性质
有机物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O,HX等 ),而生成含不饱和键的化合物的反应
CH3CH2Br
CH2=CH2↑ + NaBr
乙醇
△
+NaOH
+H2O
NaOH + HBr == NaBr + H2O
比较溴乙烷的取代反应和消去反应:
取代反应 消去反应
反应物 CH3CH2Br CH3CH2Br
反应条件
生成物
化学键变化
结论
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2OH、NaBr
CH2=CH2、NaBr、H2O
溴乙烷在不同的条件下发生不同类型的反应
同一物质,在不同条件下,断裂不同键,发生不同反应,生成不同物质
课本P54【探究】1-溴丁烷的化学性质
(1)1-溴丁烷的取代反应
CH3CH2CH2CH2Br + NaOH
水
△
用哪种分析手段可以检验出产物1-丁醇
测物质的波谱图,如红外光谱,核磁共振氢谱
如何检验卤代烃中的卤素原子?
R-X
NaOH水溶液
△
过量稀HNO3
AgNO3溶液
淡黄色沉淀(AgBr)
取上层清液
黄色沉淀(AgI)
白色沉淀(AgCl)
CH3CH2CH2CH2OH + NaBr
课本P54【探究】1-溴丁烷的化学性质
(2)1-溴丁烷的消去反应
CH3CH2CH2CH2Br
乙醇
△
+NaOH
如何检验产物1-丁烯?
课本P54实验方案:
向圆底烧瓶中加入2 gNaOH和15mL无水乙醇,搅拌。
再向其中加入5 mL1-溴丁烷和几片碎瓷片,微热。
将产生的气体先通入盛水的试管后,
再通入酸性KMnO4溶液进行检验。
现象:酸性KMnO4溶液褪色
CH3CH2CH=CH2 ↑+ NaBr + H2O
课本P54【探究】1-溴丁烷的化学性质
为什么要先通入盛有水的试管,再通入酸性KMnO4溶液?
吸收挥发出来的乙醇,排除干扰
(乙醇也会使酸性KMnO4溶液褪色)
还可以用什么方法检验1-丁烯?
此时还有必要将气体先通入水中吗
不需要先通入水中
(乙醇不能使溴的四氯化碳溶液或者溴水褪色)
通入溴的四氯化碳溶液或者溴水中,观察褪色
(2)1-溴丁烷的消去反应
CH3CH2CH2CH2Br
CH3CH2CH=CH2 ↑+ NaBr
乙醇
△
+NaOH
+H2O
2-丁烯
CH2
CH
Br
H
CHCH3
H
1
2
3
4
(3)预测2-溴丁烷发生消去反应的可能产物
CH2
CH
Br
H
CHCH3
H
1
2
3
4
CH2=CHCH2CH3
1-丁烯
CH3CH=CHCH3
能发生消去反应的卤代烃结构:
—C—C—
X H
连着卤素的碳原子相邻的碳原子上有氢原子
CH3Br
C
CH3
CH3
CH3-
-
-
-CH2Br
能发生消去反应吗?
×
×
溶剂
卤代烃
致冷剂
医用
灭火剂
麻醉剂
农药
三. 生活中的卤代烃
七氟丙烷
灭火器
三氯乙烷
修正液
四氯乙烯
干洗剂
DDT
农药
碳氟化合物
人造血液
氟氯代烷
致冷剂
聚四氟乙烯
聚氯乙烯
卤代烃是有机合成的重要原料,可以造福我们的生活
臭氧层空洞
合理使用卤代烃,保护臭氧层
【课堂小结】
第一节 卤代烃
高二—人教版—化学—选择性必修3—第三章
1.能辨识卤代烃的官能团,并根据官能团对卤代烃进行分类;能列举典型卤代烃
的主要物理性质及应用。
2.能从溴乙烷的官能团和化学键特点预测可能的断键部位和化学性质,结合实验
了解溴乙烷与NaOH水溶液的反应,能写出相应的化学方程式。
3.通过1-溴丁烷取代反应和消去反应的探究实验进行对比和归纳,形成“化学
反应可以调控”的观念,通过类比迁移形成对卤代烃反应基本规律的认识。
4.通过了解卤代烃在生活中的应用,认识化学对满足人类生活需要的积极贡献,
树立保护环境和可持续发展的意识。
学习目标
复方氯乙烷气雾剂
我们经常看到足球场上球员受伤后,队医会往伤处喷一种液体,喷完以后没什么大碍的球员就可以上场比赛了,这种喷雾的主要成分——氯乙烷,就属于卤代烃。
氯乙烷为什么可以用于紧急治疗呢?
卤代烃能发生哪些反应呢?
生活中还有哪些物质属于卤代烃呢?
阅读课本P52第一段及资料卡片,思考以下问题:
1. 什么是卤代烃?有哪些分类?
2. 结合第二章学习的烃,想想通过哪些反应可以将烃转化为卤代烃?
3. 卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出
卤代烃的命名原则。
一. 卤代烃
烃分子中的氢原子被卤素原子(X)取代后生成的化合物
1. 分类
饱和一元卤代烃的通式:CnH2n+1X
CH2=CH2 + HCl CH3CH2Cl
一定条件
CH3CH3 + Cl2 CH3CH2Cl + HCl
光
加成反应
取代反应
用R—X表示
CH3Cl
CH2Cl2
CHCl3
CCl4
CH2Br—CH2Br
CH3CH2Cl
CHBr=CHBr
CH2=CHCl
一氯甲烷
二氯甲烷
三氯甲烷
四氯甲烷
溴苯
1,2-二溴乙烷
一氯乙烷
1,2-二溴乙烯
一氯乙烯
—Br
一. 卤代烃
2. 命名
选主链
定编号
写名称
从距简单取代基近的一端编号,
有碳碳双键从距离碳碳双键近的一端编号
3-甲基-4-氯-1-丁烯
以烃为母体,卤原子为取代基,类似烃的命名
2-甲基-2-溴丙烷
3. 物理性质
一. 卤代烃
常温下,个别是气体,大多数为液体或固体
不溶于水,可溶于有机溶剂
名称 结构简式 液态时密度/(g·cm—3) 沸点/℃
氯甲烷 CH3Cl 0.916 -24
氯乙烷 CH3CH2Cl 0.898 12
1-氯丙烷 CH3CH2CH2Cl 0.890 46
1-氯丁烷 CH3CH2CH2CH2Cl 0.886 78
1-氯戊烷 CH3CH2CH2CH2CH2Cl 0.882 108
气体
气体
液体
液体
液体
③状态:
④溶解性:
随碳原子数的增加而升高
②沸点:
一氟代烃和一氯代烃的密度比水小,其余卤代烃密度都比水大
①密度:
随碳原子数的增加而减小
课本P52表3-1 卤代烃的密度和沸点
二. 溴乙烷
1. 分子结构
分子式
结构式
C2H5Br
结构简式
CH3CH2Br 或 C2H5Br
官能团
2. 物理性质
无色液体,沸点38.4℃,密度比水大,难溶于水,易溶于有机溶剂
碳溴键C-Br
球棍模型
核磁共振氢谱
电子式
空间填充模型
颜色 状态 密度 沸点
溴乙烷C2H5Br 无色 液体 比水大 38.4℃
乙烷C2H6 无色 气体 比水小 - 88.6 ℃
结合选择性必修2的知识,思考:为什么溴乙烷的密度、沸点比乙烷大呢?
乙烷和溴乙烷都属于分子晶体,结构相似,
由于溴原子取代了氢原子,
导致溴乙烷的相对分子质量比乙烷大,范德华力增大,沸点升高
官能团C—Br的引入影响了物理性质
结 构 分 析
物 理 性 质
解 释
结 构 分 析
化 学 性 质
推 断
化学键 C—C C—H C—Br
键长/pm 154 110 194
键能/(kJ/mol) 347.3 414.2 284.5
溴原子电负性比碳原子大,C—Br键为极性键
C—Br键键长较长,键能较小
电负性:C:2.5 Br:2.8 H:2.1
δ+
δ—
C—Br键较易断裂生成Br-
结合选择性必修2的知识,思考:溴乙烷的可能断键位置?
乙基是推电子基团,使C—Br键极性更强
二. 溴乙烷
3. 化学性质
CH3CH2—Br + H—OH
CH3CH2—OH + HBr
如何通过实验证明此反应断裂了C—Br键,产生了Br-?
溴乙烷
滴加AgNO3溶液
滴加AgNO3溶液
溴乙烷不能电离出Br-
溴乙烷、水
断裂C—Br键,生成了Br-
实验设想:
(1) 水解反应
(1) 水解反应、取代反应
请认真观看课本P53【实验3—1】溴乙烷水解反应的视频,记录实验现象。
结论:溴乙烷确实发生了水解反应,断裂了C—Br键,生成了Br-
现象:有淡黄色AgBr沉淀生成
取一支试管,滴入10~15滴溴乙烷,再加入1mL 5%NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察实验现象。
阅读课本P53【实验3—1】,思考以下问题:
1. 加热的作用是什么?
加快反应速率
4. 为什么要加入稀硝酸?
2. 为什么会分层?溴乙烷在哪一层?
溴乙烷不溶于水,比水重,溴乙烷在下层
3. 从平衡移动的角度分析,加入NaOH的作用是什么?
加入NaOH,使HBr的浓度减小,平衡向正反应方向移动
中和未反应完的NaOH,防止其与AgNO3反应生成黑褐色沉淀Ag2O
Ag+ + OH- == AgOH(白色)↓ 2AgOH == Ag2O(褐色) + H2O
分层消失:
溴乙烷彻底反应
需要过量!
(1)水解反应、取代反应
NaOH + HBr == NaBr + H2O
二. 溴乙烷
3. 化学性质
CH3CH2—Br + H—OH
CH3CH2—OH + HBr
CH3CH2Br + NaOH CH3CH2OH + NaBr
水
△
(2)消去反应
二. 溴乙烷
3. 化学性质
有机物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O,HX等 ),而生成含不饱和键的化合物的反应
CH3CH2Br
CH2=CH2↑ + NaBr
乙醇
△
+NaOH
+H2O
NaOH + HBr == NaBr + H2O
比较溴乙烷的取代反应和消去反应:
取代反应 消去反应
反应物 CH3CH2Br CH3CH2Br
反应条件
生成物
化学键变化
结论
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2OH、NaBr
CH2=CH2、NaBr、H2O
溴乙烷在不同的条件下发生不同类型的反应
同一物质,在不同条件下,断裂不同键,发生不同反应,生成不同物质
课本P54【探究】1-溴丁烷的化学性质
(1)1-溴丁烷的取代反应
CH3CH2CH2CH2Br + NaOH
水
△
用哪种分析手段可以检验出产物1-丁醇
测物质的波谱图,如红外光谱,核磁共振氢谱
如何检验卤代烃中的卤素原子?
R-X
NaOH水溶液
△
过量稀HNO3
AgNO3溶液
淡黄色沉淀(AgBr)
取上层清液
黄色沉淀(AgI)
白色沉淀(AgCl)
CH3CH2CH2CH2OH + NaBr
课本P54【探究】1-溴丁烷的化学性质
(2)1-溴丁烷的消去反应
CH3CH2CH2CH2Br
乙醇
△
+NaOH
如何检验产物1-丁烯?
课本P54实验方案:
向圆底烧瓶中加入2 gNaOH和15mL无水乙醇,搅拌。
再向其中加入5 mL1-溴丁烷和几片碎瓷片,微热。
将产生的气体先通入盛水的试管后,
再通入酸性KMnO4溶液进行检验。
现象:酸性KMnO4溶液褪色
CH3CH2CH=CH2 ↑+ NaBr + H2O
课本P54【探究】1-溴丁烷的化学性质
为什么要先通入盛有水的试管,再通入酸性KMnO4溶液?
吸收挥发出来的乙醇,排除干扰
(乙醇也会使酸性KMnO4溶液褪色)
还可以用什么方法检验1-丁烯?
此时还有必要将气体先通入水中吗
不需要先通入水中
(乙醇不能使溴的四氯化碳溶液或者溴水褪色)
通入溴的四氯化碳溶液或者溴水中,观察褪色
(2)1-溴丁烷的消去反应
CH3CH2CH2CH2Br
CH3CH2CH=CH2 ↑+ NaBr
乙醇
△
+NaOH
+H2O
2-丁烯
CH2
CH
Br
H
CHCH3
H
1
2
3
4
(3)预测2-溴丁烷发生消去反应的可能产物
CH2
CH
Br
H
CHCH3
H
1
2
3
4
CH2=CHCH2CH3
1-丁烯
CH3CH=CHCH3
能发生消去反应的卤代烃结构:
—C—C—
X H
连着卤素的碳原子相邻的碳原子上有氢原子
CH3Br
C
CH3
CH3
CH3-
-
-
-CH2Br
能发生消去反应吗?
×
×
溶剂
卤代烃
致冷剂
医用
灭火剂
麻醉剂
农药
三. 生活中的卤代烃
七氟丙烷
灭火器
三氯乙烷
修正液
四氯乙烯
干洗剂
DDT
农药
碳氟化合物
人造血液
氟氯代烷
致冷剂
聚四氟乙烯
聚氯乙烯
卤代烃是有机合成的重要原料,可以造福我们的生活
臭氧层空洞
合理使用卤代烃,保护臭氧层
【课堂小结】
