第四单元课题4化学式与化合价 课件-2022-2023学年九年级化学人教版上册(共34张PPT)
文档属性
| 名称 | 第四单元课题4化学式与化合价 课件-2022-2023学年九年级化学人教版上册(共34张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-16 00:00:00 | ||
图片预览










文档简介
(共34张PPT)
课题4 化学式与化合价
人教版初中九年级化学上册第四单元
《自然界的水》
新课教学课件
第四单元《自然界的水》
§课题4
化学式与化合价
《赋得古原草送别》
唐-白居易
离离原上草,一岁一枯荣。
野火烧不尽,春风吹又生。
远芳侵古道,晴翠接荒城。
又送王孙去,萋萋满别情。
古代诗词中蕴含有化学知识“野火烧不尽,春风吹又生”.草木灰烬中含有化学物质碳酸钾,
1.【概念】用元素符号和数字的组合表示物质组成的式子叫化学式。
一、化学式
2、【注意】
①.只有纯净物才有化学式
②.每种纯净物的组成是固定不变的,所以,一种物质的化学式只有一个。
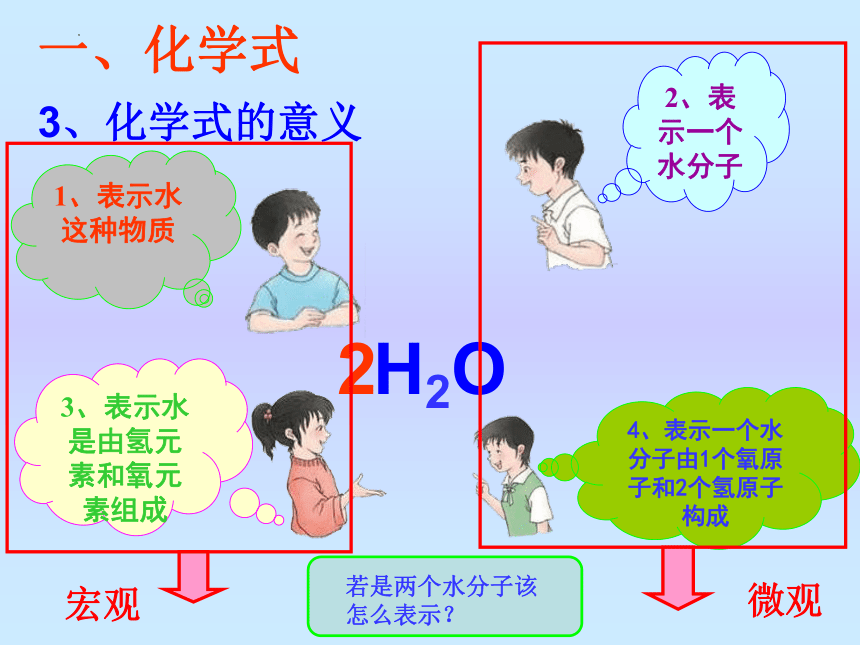
3、化学式的意义
H2O
2
宏观
微观
2、表示一个水分子
3、表示水是由氢元素和氧元素组成
4、表示一个水分子由1个氧原子和2个氢原子构成
若是两个水分子该怎么表示?
一、化学式
1、表示水这种物质
①表示一种物质
②表示该物质的元素组成
① 物质的一个分子
②物质的分子构成
宏观:
微观:
注意:要考虑到构成物质的粒子是分子还是原子。
3、化学式的意义
一、化学式
①表示氢元素;②一个氢原子。
H:
2H:
2H2:
H2:
【讨论】
说出下列符号所表示的含义:
①表示两个氢气分子。
②一个氢气分子由两个氢原子构成。
③一个氢气分子
②氢气由氢元素组成
①表示氢气这种物质
④一个氢气分子由两个氢原子构成。
表示两个氢原子。
4、化学式的书写和读法
一、化学式
单质
(1)金属和某些固态非金属单质
(结构较复杂,直接用元素符号表示)
如:Fe、Cu、Al,C、S、P等
(3)气态非金属单质
(在元素符号后面加上相应的数字)
如:O2、N2、H2、O3等
(2)稀有气体
由原子构成,用元素符号表示
如:He、Ne、Ar等
4、化学式的书写和读法
一、化学式
化合物
(2)氧化物中氧元素写后面
如 CO2、Fe3O4、P2O5、 MnO2、H2O
读作:“几氧化几某”
(2)金属元素写前面,非金属元素写后面 如:ZnS、KCl、MgCl2等;
读法:从右往左读作“某化某”
(1)当某组成元素原子个数比为1时,1可省略。
思考:观察下列表格,你发现了什么?
二、化合价
一些物质组成元素的原子个数比
物质 HCl H2O NaCl Fe2O3
原子个数比
1:1
2:1
1:1
2:3
规律:
1、形成化合物的元素有固定的原子个数比。
2、不同元素相互结合时,其原子个数比并不都是1:1。
构成物质的元素的原子的个数比表示原子之间相互化合的数目,原子在化合时表现出来的这种性质在化学中用化合价来表示。
1、定义:
二、化合价
是元素在形成化合物时表现出的一种性质。化合价是用来表示原子之间形成化合物时的数目的。
2、特点:
②在化合物里正负化合价的代数和为零
①化合价有正价和负价
3.原子团:做为一个整体参加反应的原子集团,也叫根。如OH-,CO32-。根也有化合价。
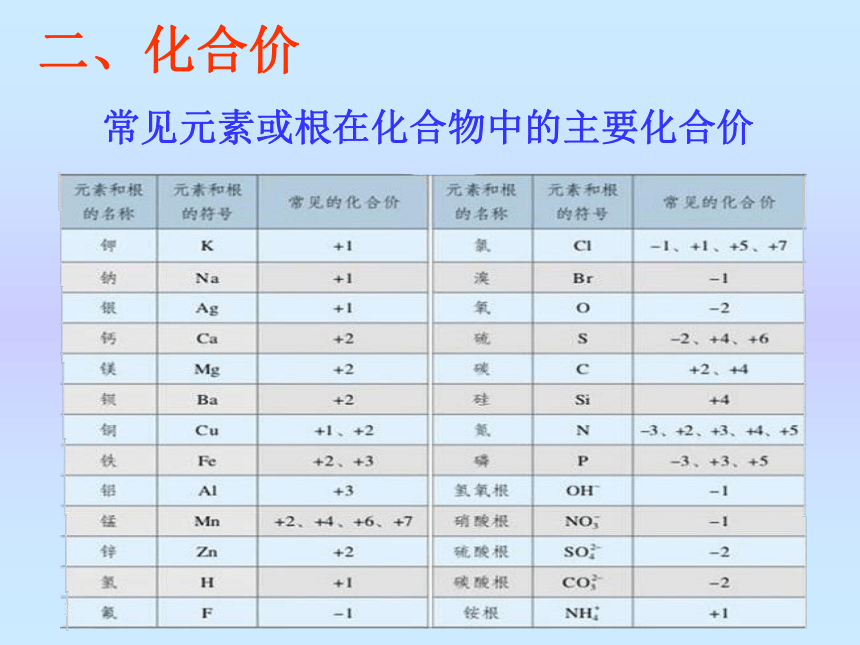
二、化合价
常见元素或根在化合物中的主要化合价
二、化合价
4、确定化合价时的注意事项:
①金属元素与非金属元素化合时,金属元素显正价,非金属元素显负价;
②一些元素在不同物质中可显不同的化合价;
③元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此,在单质里,元素的化合价为0.
二、化合价
5、化合价规律口诀:
一价氢氯钾钠银 二价氧钙钡镁锌
三铝四硅五价磷 二三铁,二四碳
二四六硫都齐全 铜汞二价最常见
条件不同价不同 单质为零永不变
①一些常见元素化合价口诀
②一些常见原子团的化合价
负一硝酸氢氧根 负二硫酸碳酸根
负三记住磷酸根 正一价的是铵根
二、化合价
6、化合价的应用:
①已知化合价,书写化学式:
例题:已知磷为+5价,氧为-2价,写出磷的这种化合物的化学式。
解: 1.写出组成的元素:正价在前,负价在后,
2.求正负化合价绝对值的最小公倍数→
3.求各元素的原子数:
4.原子个数写在元素符号右下方
5.检查正误:正负化合价代数和=0
P O
5×2=10
P: O:
P2O5
+5×2+(-2)×5=0
原则:化合物里正负化合价的代数和为零
例:试确定氯酸钾(KClO3)中氯元素的化合价
解:设氯元素的化合价为x,则
(+1)+ x +(-2)x 3=0
x = +5
所以,在氯酸钾中,氯元素的化合价为+5价
二、化合价
6、化合价的应用:
②已知化学式,求化合价:
三、有关相对分子质量的计算
1、计算相对分子质量:
②如何理解相对分子质量
1、是化学式中各原子的相对原子质量的总和
2、是分子的相对质量
3、它的单位也是 1
①概念:化学式中各原子的相对原子质量的总和,就是相对分子质量。(符号为Mr)
三、有关相对分子质量的计算
1、计算相对分子质量:
书写格式:
O2的相对分子质量= 16×2=32
(NH4)2CO3的相对分子质量
=96
H2O的相对分子质量=1×2 + 16=18
例题1:计算02、H2O、(NH4)2CO3的相对分子质量
=(14+1×4)×2 + 12 + 16 ×3
三、有关相对分子质量的计算
2、计算物质组成元素的质量比:
例题2:计算硝酸铵中各元素的质量比
m(N) : m(H) : m( O ) = 14×2 : 1×4 : 16×3
在NH4NO3中
= 28 : 4 : 48
= 7 : 1 : 12
元素质量比=(相对原子质量×原子个数)之比
例如:
二氧化碳(CO2) 中
碳元素质量︰氧元素质量 = 12 ︰(16×2)
= 3 ︰8
解:
三、有关相对分子质量的计算
3、计算物质中某元素的质量分数:
物质的相对分子质量
该元素的相对原子质量
×
该元素的原子个数
元素的质量分数
=
×
100%
注意事项:
①质量分数——用百分数来表示
②意义:
每100克物质中含有某元素的质量
③药品、食品等商品的标签或说明书上常常用质量分数来表示物质的成分或纯度。
例题3:计算硝酸铵中氮元素的质量分数。
解 : 在NH4NO3中
N的质量分数=
氮的相对原子质量×氮原子个数
硝酸铵的相对分子质量
×100%
14×2
14×2 + 1×4 + 16×3
×100%
=
=
28
80
×100%
=35%
三、有关相对分子质量的计算
3、计算物质中某元素的质量分数:
1.下列符号中能正确表示+3价铝元素的是 ( )
(A) (B) (C)3Al (D)
2.下列化学式中,书写错误的是 ( )
(A)氧化钙(OCa) (B)氧化镁(MgO)
(C)三氯化铁(FeCl3)(D)三氧化硫(SO3)
3.化学式Fe2O3的读法是 ( )
(A)铁二氧三 (B)二铁化三氧 (C)三氧化二铁 (D)二氧化二铁 (E)氧化铁
B
A
C、E
4.Mg(OH)2相对分子质量的计算式为 ( )
(A)24+16+1×2 (B)24×(16+1)×2
(C)24×16+1×2 (D)24+(16+1)×2
5.2H2O相对分子质量的计算式为 ( )
(A)2+1×2+16 (B)2×1×2×16
(C)2 ×(1×2+16) (D)2×1×2+16
6.H2SO4的相对分子质量为 ,在H2SO4
中氢、硫、氧三种元素的质量比是 。
氢、硫、氧三种元素的原子个数比是 。
D
C
98
1:16:32
2:1:4
7.用数字和化学式表示出:
(1)五个氧分子
(2)2个水分子
(3)四个硫酸分子
(4)10个氢氧化钠分子
8.下列化学符号表示两个氢分子的是 ( )
(A)2H (B)H2 (C)2H2 (D)H2O
5O2
2H2O
4H2SO4
10NaOH
C
9.下列化学式中,书写错误的是 ( )
(A)氧化钙(OCa)(B)氧化镁(MgO)
(C)三氯化铁 (FeCl3)
(D)三氧化硫(SO3)
10.化学式Fe3O4的读法是 ( )
(A)铁三氧四 (B)三铁化四氧
(C)四氧化三铁 (D)三氧化二铁
A
C
11、150千克的硝酸铵中有多少氮元素?
解 : 在NH4NO3中
=
14×2
14×2 + 1×4 + 16×3
×100%
=
28
80
×100%
= 35%
∴150千克的硝酸铵中含有的N元素的质量为
150千克×35% = 52.5 千克
答:150千克的硝酸铵中有52.5千克氮元素。
N的质量分数=
Ar(N) ×2
Mr(NH4NO3)
×100%
在NH4NO3中
=
14×2
14×2 + 1×4 + 16×3
×100%
=
28
80
×100%
= 35%
∴ X × 35% = 100 吨
X=285.7 吨
答:285.7 吨的硝酸铵中有100吨氮元素。
12、多少吨的硝酸铵中含有100吨的氮元素?
解 :设质量为X的硝酸铵中含有100吨的氮元素.
N的质量分数=
Ar(N) ×2
Mr(NH4NO3)
×100%
13、最近,科学家研究发现,某些食品中使用的苏丹红I 号可能致癌。苏丹红I 号的化学式为C10H12N2O,它的一个分子中共含有_____个原子,它是由____种元素组成的,其中氮、氧元素的质量比为________。
25
四
7︰4
14、油炸食品,烧烤食品等被营养专家称作“垃圾食品”,这是因为在制作过程中不仅产生大量有害气体污染环境,而且食物中还会产生一些强致癌物质,故此类食品不易多吃、常吃。如在食物煎炸过程中会产生一种有害物质-----丙烯醛,化学式为C2H3CHO。试回答:
(1)丙烯醛的相对分子质量是____。
(2)丙烯醛中氧元素的质量分数为________(结果保留一位小数)。
56
28.6%
15、已知某氮氧元素组成的氧化物中,氮与氧的
质量比是 7 :16,该化合物的化学式为 。
解: 设化学式为 NX OY,
14X
16Y
=
7
16
X
Y
=
1
2
∴该化合物的化学式是 NO2
NO2
16、相同质量的SO2和SO3中氧元素的质量比是( )
A、2:3 B、3:2
C、5:6 D、6:5
解析:设SO2和SO3的质量均为m,则:
C
16×2
64
×100%
SO2中O的质量= m×
80
×100%
16×3
SO3中O的质量=m×
所以, SO2和SO3中的O的质量比是5:6
17、欲使SO2和SO3两种物质中,所含氧元素的质量相等,则SO2和SO3的质量比为( )
A、1:1 B、2:3
C、3:2 D、6:5
方法1 解析:设SO2的质量为m,SO3的质量均为n,则:
D
16×2
64
×100%
SO2中O的质量= m×
80
×100%
16×3
SO3中O的质量=n×
∵SO2和SO3中的O的质量相等
16×2
64
×100%
m×
80
×100%
16×3
n×
=
m :n
=
6:5
3×(32 + 16×2)
2×(32 + 16×3)
方法2 解析:设在二氧化硫中SO2的分子数目为m,
在三氧化硫中SO3的分子数目为n,
18、欲使SO2和SO3两种物质中,所含氧元素的质量相等,则SO2和SO3的质量比为( )
A、1:1 B、2:3
C、3:2 D、6:5
D
m :n
=
3:2
∵ mSO2中和nSO3中氧元素质量相等
∴ m×2 ×16 = n×3×16
mSO2的质量
nSO3的质量
∴
=
=
6
5
19、由A、B两元素组成的化合物甲和乙,已知甲中A的质量分数为50%,乙中B的质量分数为60%。若甲的化学式为AB2,试确定乙 的化学式_________.
解析:设乙的化学式为AxBy, A的相对原子质量为a,B的相对原子质量为b,:
=
a ×1
b ×2
50%
1-50%
a ×x
b ×y
=
1-60%
60%
x:y = 1:3
所以,乙的化学式为AB3
由题意得
课题4 化学式与化合价
人教版初中九年级化学上册第四单元
《自然界的水》
新课教学课件
第四单元《自然界的水》
§课题4
化学式与化合价
《赋得古原草送别》
唐-白居易
离离原上草,一岁一枯荣。
野火烧不尽,春风吹又生。
远芳侵古道,晴翠接荒城。
又送王孙去,萋萋满别情。
古代诗词中蕴含有化学知识“野火烧不尽,春风吹又生”.草木灰烬中含有化学物质碳酸钾,
1.【概念】用元素符号和数字的组合表示物质组成的式子叫化学式。
一、化学式
2、【注意】
①.只有纯净物才有化学式
②.每种纯净物的组成是固定不变的,所以,一种物质的化学式只有一个。
3、化学式的意义
H2O
2
宏观
微观
2、表示一个水分子
3、表示水是由氢元素和氧元素组成
4、表示一个水分子由1个氧原子和2个氢原子构成
若是两个水分子该怎么表示?
一、化学式
1、表示水这种物质
①表示一种物质
②表示该物质的元素组成
① 物质的一个分子
②物质的分子构成
宏观:
微观:
注意:要考虑到构成物质的粒子是分子还是原子。
3、化学式的意义
一、化学式
①表示氢元素;②一个氢原子。
H:
2H:
2H2:
H2:
【讨论】
说出下列符号所表示的含义:
①表示两个氢气分子。
②一个氢气分子由两个氢原子构成。
③一个氢气分子
②氢气由氢元素组成
①表示氢气这种物质
④一个氢气分子由两个氢原子构成。
表示两个氢原子。
4、化学式的书写和读法
一、化学式
单质
(1)金属和某些固态非金属单质
(结构较复杂,直接用元素符号表示)
如:Fe、Cu、Al,C、S、P等
(3)气态非金属单质
(在元素符号后面加上相应的数字)
如:O2、N2、H2、O3等
(2)稀有气体
由原子构成,用元素符号表示
如:He、Ne、Ar等
4、化学式的书写和读法
一、化学式
化合物
(2)氧化物中氧元素写后面
如 CO2、Fe3O4、P2O5、 MnO2、H2O
读作:“几氧化几某”
(2)金属元素写前面,非金属元素写后面 如:ZnS、KCl、MgCl2等;
读法:从右往左读作“某化某”
(1)当某组成元素原子个数比为1时,1可省略。
思考:观察下列表格,你发现了什么?
二、化合价
一些物质组成元素的原子个数比
物质 HCl H2O NaCl Fe2O3
原子个数比
1:1
2:1
1:1
2:3
规律:
1、形成化合物的元素有固定的原子个数比。
2、不同元素相互结合时,其原子个数比并不都是1:1。
构成物质的元素的原子的个数比表示原子之间相互化合的数目,原子在化合时表现出来的这种性质在化学中用化合价来表示。
1、定义:
二、化合价
是元素在形成化合物时表现出的一种性质。化合价是用来表示原子之间形成化合物时的数目的。
2、特点:
②在化合物里正负化合价的代数和为零
①化合价有正价和负价
3.原子团:做为一个整体参加反应的原子集团,也叫根。如OH-,CO32-。根也有化合价。
二、化合价
常见元素或根在化合物中的主要化合价
二、化合价
4、确定化合价时的注意事项:
①金属元素与非金属元素化合时,金属元素显正价,非金属元素显负价;
②一些元素在不同物质中可显不同的化合价;
③元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此,在单质里,元素的化合价为0.
二、化合价
5、化合价规律口诀:
一价氢氯钾钠银 二价氧钙钡镁锌
三铝四硅五价磷 二三铁,二四碳
二四六硫都齐全 铜汞二价最常见
条件不同价不同 单质为零永不变
①一些常见元素化合价口诀
②一些常见原子团的化合价
负一硝酸氢氧根 负二硫酸碳酸根
负三记住磷酸根 正一价的是铵根
二、化合价
6、化合价的应用:
①已知化合价,书写化学式:
例题:已知磷为+5价,氧为-2价,写出磷的这种化合物的化学式。
解: 1.写出组成的元素:正价在前,负价在后,
2.求正负化合价绝对值的最小公倍数→
3.求各元素的原子数:
4.原子个数写在元素符号右下方
5.检查正误:正负化合价代数和=0
P O
5×2=10
P: O:
P2O5
+5×2+(-2)×5=0
原则:化合物里正负化合价的代数和为零
例:试确定氯酸钾(KClO3)中氯元素的化合价
解:设氯元素的化合价为x,则
(+1)+ x +(-2)x 3=0
x = +5
所以,在氯酸钾中,氯元素的化合价为+5价
二、化合价
6、化合价的应用:
②已知化学式,求化合价:
三、有关相对分子质量的计算
1、计算相对分子质量:
②如何理解相对分子质量
1、是化学式中各原子的相对原子质量的总和
2、是分子的相对质量
3、它的单位也是 1
①概念:化学式中各原子的相对原子质量的总和,就是相对分子质量。(符号为Mr)
三、有关相对分子质量的计算
1、计算相对分子质量:
书写格式:
O2的相对分子质量= 16×2=32
(NH4)2CO3的相对分子质量
=96
H2O的相对分子质量=1×2 + 16=18
例题1:计算02、H2O、(NH4)2CO3的相对分子质量
=(14+1×4)×2 + 12 + 16 ×3
三、有关相对分子质量的计算
2、计算物质组成元素的质量比:
例题2:计算硝酸铵中各元素的质量比
m(N) : m(H) : m( O ) = 14×2 : 1×4 : 16×3
在NH4NO3中
= 28 : 4 : 48
= 7 : 1 : 12
元素质量比=(相对原子质量×原子个数)之比
例如:
二氧化碳(CO2) 中
碳元素质量︰氧元素质量 = 12 ︰(16×2)
= 3 ︰8
解:
三、有关相对分子质量的计算
3、计算物质中某元素的质量分数:
物质的相对分子质量
该元素的相对原子质量
×
该元素的原子个数
元素的质量分数
=
×
100%
注意事项:
①质量分数——用百分数来表示
②意义:
每100克物质中含有某元素的质量
③药品、食品等商品的标签或说明书上常常用质量分数来表示物质的成分或纯度。
例题3:计算硝酸铵中氮元素的质量分数。
解 : 在NH4NO3中
N的质量分数=
氮的相对原子质量×氮原子个数
硝酸铵的相对分子质量
×100%
14×2
14×2 + 1×4 + 16×3
×100%
=
=
28
80
×100%
=35%
三、有关相对分子质量的计算
3、计算物质中某元素的质量分数:
1.下列符号中能正确表示+3价铝元素的是 ( )
(A) (B) (C)3Al (D)
2.下列化学式中,书写错误的是 ( )
(A)氧化钙(OCa) (B)氧化镁(MgO)
(C)三氯化铁(FeCl3)(D)三氧化硫(SO3)
3.化学式Fe2O3的读法是 ( )
(A)铁二氧三 (B)二铁化三氧 (C)三氧化二铁 (D)二氧化二铁 (E)氧化铁
B
A
C、E
4.Mg(OH)2相对分子质量的计算式为 ( )
(A)24+16+1×2 (B)24×(16+1)×2
(C)24×16+1×2 (D)24+(16+1)×2
5.2H2O相对分子质量的计算式为 ( )
(A)2+1×2+16 (B)2×1×2×16
(C)2 ×(1×2+16) (D)2×1×2+16
6.H2SO4的相对分子质量为 ,在H2SO4
中氢、硫、氧三种元素的质量比是 。
氢、硫、氧三种元素的原子个数比是 。
D
C
98
1:16:32
2:1:4
7.用数字和化学式表示出:
(1)五个氧分子
(2)2个水分子
(3)四个硫酸分子
(4)10个氢氧化钠分子
8.下列化学符号表示两个氢分子的是 ( )
(A)2H (B)H2 (C)2H2 (D)H2O
5O2
2H2O
4H2SO4
10NaOH
C
9.下列化学式中,书写错误的是 ( )
(A)氧化钙(OCa)(B)氧化镁(MgO)
(C)三氯化铁 (FeCl3)
(D)三氧化硫(SO3)
10.化学式Fe3O4的读法是 ( )
(A)铁三氧四 (B)三铁化四氧
(C)四氧化三铁 (D)三氧化二铁
A
C
11、150千克的硝酸铵中有多少氮元素?
解 : 在NH4NO3中
=
14×2
14×2 + 1×4 + 16×3
×100%
=
28
80
×100%
= 35%
∴150千克的硝酸铵中含有的N元素的质量为
150千克×35% = 52.5 千克
答:150千克的硝酸铵中有52.5千克氮元素。
N的质量分数=
Ar(N) ×2
Mr(NH4NO3)
×100%
在NH4NO3中
=
14×2
14×2 + 1×4 + 16×3
×100%
=
28
80
×100%
= 35%
∴ X × 35% = 100 吨
X=285.7 吨
答:285.7 吨的硝酸铵中有100吨氮元素。
12、多少吨的硝酸铵中含有100吨的氮元素?
解 :设质量为X的硝酸铵中含有100吨的氮元素.
N的质量分数=
Ar(N) ×2
Mr(NH4NO3)
×100%
13、最近,科学家研究发现,某些食品中使用的苏丹红I 号可能致癌。苏丹红I 号的化学式为C10H12N2O,它的一个分子中共含有_____个原子,它是由____种元素组成的,其中氮、氧元素的质量比为________。
25
四
7︰4
14、油炸食品,烧烤食品等被营养专家称作“垃圾食品”,这是因为在制作过程中不仅产生大量有害气体污染环境,而且食物中还会产生一些强致癌物质,故此类食品不易多吃、常吃。如在食物煎炸过程中会产生一种有害物质-----丙烯醛,化学式为C2H3CHO。试回答:
(1)丙烯醛的相对分子质量是____。
(2)丙烯醛中氧元素的质量分数为________(结果保留一位小数)。
56
28.6%
15、已知某氮氧元素组成的氧化物中,氮与氧的
质量比是 7 :16,该化合物的化学式为 。
解: 设化学式为 NX OY,
14X
16Y
=
7
16
X
Y
=
1
2
∴该化合物的化学式是 NO2
NO2
16、相同质量的SO2和SO3中氧元素的质量比是( )
A、2:3 B、3:2
C、5:6 D、6:5
解析:设SO2和SO3的质量均为m,则:
C
16×2
64
×100%
SO2中O的质量= m×
80
×100%
16×3
SO3中O的质量=m×
所以, SO2和SO3中的O的质量比是5:6
17、欲使SO2和SO3两种物质中,所含氧元素的质量相等,则SO2和SO3的质量比为( )
A、1:1 B、2:3
C、3:2 D、6:5
方法1 解析:设SO2的质量为m,SO3的质量均为n,则:
D
16×2
64
×100%
SO2中O的质量= m×
80
×100%
16×3
SO3中O的质量=n×
∵SO2和SO3中的O的质量相等
16×2
64
×100%
m×
80
×100%
16×3
n×
=
m :n
=
6:5
3×(32 + 16×2)
2×(32 + 16×3)
方法2 解析:设在二氧化硫中SO2的分子数目为m,
在三氧化硫中SO3的分子数目为n,
18、欲使SO2和SO3两种物质中,所含氧元素的质量相等,则SO2和SO3的质量比为( )
A、1:1 B、2:3
C、3:2 D、6:5
D
m :n
=
3:2
∵ mSO2中和nSO3中氧元素质量相等
∴ m×2 ×16 = n×3×16
mSO2的质量
nSO3的质量
∴
=
=
6
5
19、由A、B两元素组成的化合物甲和乙,已知甲中A的质量分数为50%,乙中B的质量分数为60%。若甲的化学式为AB2,试确定乙 的化学式_________.
解析:设乙的化学式为AxBy, A的相对原子质量为a,B的相对原子质量为b,:
=
a ×1
b ×2
50%
1-50%
a ×x
b ×y
=
1-60%
60%
x:y = 1:3
所以,乙的化学式为AB3
由题意得
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
