氮及其重要化合物(一)(22张ppt)
文档属性
| 名称 | 氮及其重要化合物(一)(22张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 974.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-17 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
氮 及 其 重 要 化 合 物(一)
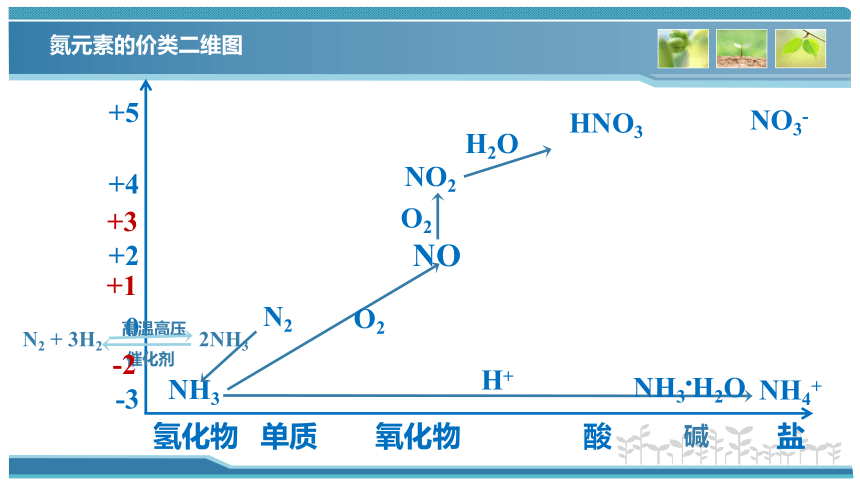
氮元素的价类二维图
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
NO3-
NH3 H2O
碱
N2 + 3H2 2NH3
高温高压
催化剂
+3
+1
-2
含氮物质间的转换
【例1】阅读下列资料,完成1~3题:N2是合成氨工业的重要原料,N2不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。
2NO(g)+O2(g)=2NO2(g) ΔH=-116.4 kJ·mol 1
大气中过量的NOx和水体中过量的NH4+、NO3 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3 转化为N2。
1.下列有关NH3、 NH4+和NO3 的说法正确的是
A.NH3能形成分子间氢键
B. NO3 的空间构型为三角锥形
C.NH3与NH4+中的键角相等
D.NH3与Ag+生成的[Ag(NH3)2]+中含有6个配位键
A
【例1】阅读下列资料,完成1~3题:N2是合成氨工业的重要原料,N2不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。
2NO(g)+O2(g)=2NO2(g) ΔH=-116.4 kJ·mol 1
大气中过量的NOx和水体中过量的NH4+、NO3 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3 转化为N2。
C
含氮物质间的转换
【例1】阅读下列资料,完成1~3题:N2是合成氨工业的重要原料,N2不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。
2NO(g)+O2(g)=2NO2(g) ΔH=-116.4 kJ·mol 1
大气中过量的NOx和水体中过量的NH4+、NO3 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3 转化为N2。
A
含氮物质间的转换
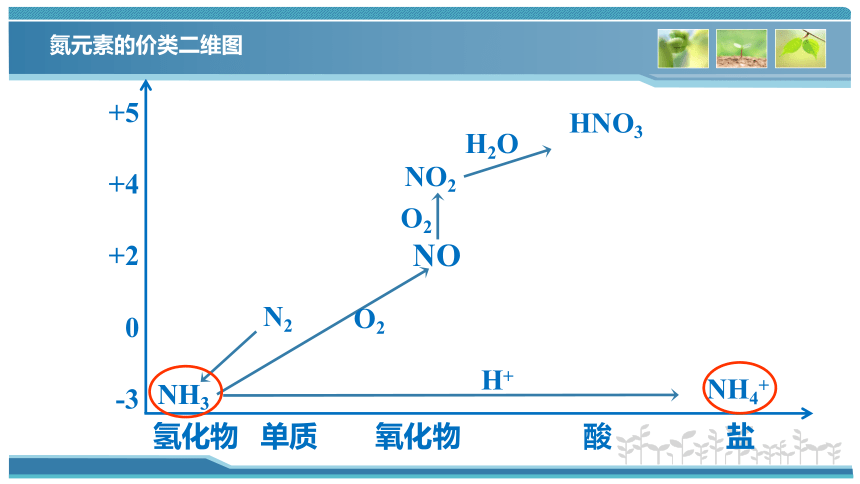
氮元素的价类二维图
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
氨
加热氯化铵
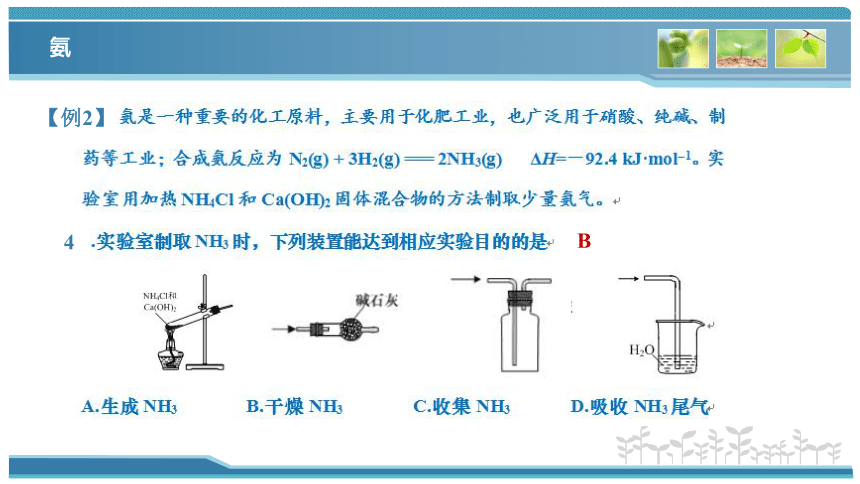
【例2】
B
【例2】
氨
4
B
【例2】
氨
5
C
【例2】
氨
6
投入MgCl2和Na2HPO4可将溶液中的NH4+或NH3·H2O转化为MgNH4PO4·6H2O沉淀除去,除去NH3·H2O的离子方程式为
Mg2++NH3·H2O+HPO42-+5H2O===MgNH4PO4·6H2O↓
废水中氨氮的去除-----沉淀法
溶液pH过大或过小都不利于MgNH4PO4·6H2O的生成,原因_______。
pH过大,NH4+、Mg2+易与OH-结合生成NH3·H2O、Mg(OH)2,使NH4+和Mg2+浓度降低;pH过小,不利于HPO42-电离,PO43-浓度偏低
【例3】
废水中氨氮的去除-----沉淀法
皮革厂的废水中含有一定量的氨氮(以NH3、NH4+形式存在),通过沉淀和氧化两步处理后可使水中氨氮达到国家规定的排放标准。
(1)沉淀:向酸性废水中加入适量Fe2(SO4)3溶液,废水中的氨氮转化为NH4Fe3(SO4)2(OH)6沉淀。
①该反应的离子方程式为_________。
②废水中氨氮去除率随pH的变化如题14图-1所示,当1.3<pH<1.8时,氨氮去除率随pH升高而
降低的原因是________________。
【例4】
部分Fe3+生成Fe(OH)3沉淀,溶液中Fe3+浓度降低
废水中氨氮的去除-----氧化法
(2)氧化:调节经沉淀处理后的废水pH约为6,加入NaClO溶液进一步氧化处理。
①NaClO将废水中的氨氮转化为N2,该反应的离子方程式为_
______________。
②研究发现,废水中氨氮去除率随温度升高呈先升后降趋势。当温度大于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是____________。
③n(ClO-)/n(氨氮)对废水中氨氮去除率和总氮去除率的影响如题14图-2所示。当n(ClO-)/n(氨氮)>1.54后,总氮去除率下降的原因是_____________。
【例4】
氨氮的去除
NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业废气中的NH3可通过催化氧化为N2除去。将一定比例NH3、O2和N2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、N2的选择性[ ×100%]与温度的关系如题图所示。
【例5】
(1)在175~300℃范围内,随着温度的升高,出口处氮气和氮氧化物的量如何变化?为什么?
氮氧化物的处理
NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业废气中的NH3可通过催化氧化为N2除去。将一定比例NH3、O2和N2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、N2的选择性[ ×100%]与温度的关系如题图所示。
【例5】
(2)催化氧化除去尾气中的NH3应选择怎样的反应温度?
(3)高效除去尾气中的氨气,你有什么建议?
需研发低温下NH3转化率高和N2选择性高的催化剂
应选择反应温度225℃左右
含氮污染的处理
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
8NH3+6NO2 7N2+12H2O
催化剂
4NH3+6NO 5N2+6H2O
催化剂
脱除烟气中的氮氧化物(主要是指NO和NO2)可净化空气、改善环境,是环境保护的主要课题。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如题14图-2所示。当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为 。
氮氧化物的处理
【例6】
(2)一种通过氧化钡和硝酸钡的相互转化脱除二氧化氮的原理如图所示,脱除二氧化氮的总反应为
氮氧化物的处理
氮氧化物的处理
(3)NO2的消除。可以用碳酸钠溶液来进行吸收,在产生CO2的同时,会生成NaNO2等物质,NaNO2是工业盐的主要成分,在漂白、电镀等方面应用广泛。
写出碳酸钠溶液消除NO2的化学方程式: 。
氮元素的价类二维图
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
+3
NO3-
NO2-
HNO2
氮氧化物的处理
(4)用酸性(NH2)2CO水溶液吸收氮氧化物,吸收过程中存在HNO2与(NH2)2CO
生成N2和CO2的反应。写出该反应的化学方程式: 。
(5)利用电化学装置可消除氮氧化物污染,变废为宝。 下图为电解NO制备
NH4NO3的装置,该装置中阳极的电极反应式为 。
谢 谢!
氮 及 其 重 要 化 合 物(一)
氮元素的价类二维图
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
NO3-
NH3 H2O
碱
N2 + 3H2 2NH3
高温高压
催化剂
+3
+1
-2
含氮物质间的转换
【例1】阅读下列资料,完成1~3题:N2是合成氨工业的重要原料,N2不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。
2NO(g)+O2(g)=2NO2(g) ΔH=-116.4 kJ·mol 1
大气中过量的NOx和水体中过量的NH4+、NO3 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3 转化为N2。
1.下列有关NH3、 NH4+和NO3 的说法正确的是
A.NH3能形成分子间氢键
B. NO3 的空间构型为三角锥形
C.NH3与NH4+中的键角相等
D.NH3与Ag+生成的[Ag(NH3)2]+中含有6个配位键
A
【例1】阅读下列资料,完成1~3题:N2是合成氨工业的重要原料,N2不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。
2NO(g)+O2(g)=2NO2(g) ΔH=-116.4 kJ·mol 1
大气中过量的NOx和水体中过量的NH4+、NO3 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3 转化为N2。
C
含氮物质间的转换
【例1】阅读下列资料,完成1~3题:N2是合成氨工业的重要原料,N2不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。
2NO(g)+O2(g)=2NO2(g) ΔH=-116.4 kJ·mol 1
大气中过量的NOx和水体中过量的NH4+、NO3 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO3 转化为N2。
A
含氮物质间的转换
氮元素的价类二维图
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
氨
加热氯化铵
【例2】
B
【例2】
氨
4
B
【例2】
氨
5
C
【例2】
氨
6
投入MgCl2和Na2HPO4可将溶液中的NH4+或NH3·H2O转化为MgNH4PO4·6H2O沉淀除去,除去NH3·H2O的离子方程式为
Mg2++NH3·H2O+HPO42-+5H2O===MgNH4PO4·6H2O↓
废水中氨氮的去除-----沉淀法
溶液pH过大或过小都不利于MgNH4PO4·6H2O的生成,原因_______。
pH过大,NH4+、Mg2+易与OH-结合生成NH3·H2O、Mg(OH)2,使NH4+和Mg2+浓度降低;pH过小,不利于HPO42-电离,PO43-浓度偏低
【例3】
废水中氨氮的去除-----沉淀法
皮革厂的废水中含有一定量的氨氮(以NH3、NH4+形式存在),通过沉淀和氧化两步处理后可使水中氨氮达到国家规定的排放标准。
(1)沉淀:向酸性废水中加入适量Fe2(SO4)3溶液,废水中的氨氮转化为NH4Fe3(SO4)2(OH)6沉淀。
①该反应的离子方程式为_________。
②废水中氨氮去除率随pH的变化如题14图-1所示,当1.3<pH<1.8时,氨氮去除率随pH升高而
降低的原因是________________。
【例4】
部分Fe3+生成Fe(OH)3沉淀,溶液中Fe3+浓度降低
废水中氨氮的去除-----氧化法
(2)氧化:调节经沉淀处理后的废水pH约为6,加入NaClO溶液进一步氧化处理。
①NaClO将废水中的氨氮转化为N2,该反应的离子方程式为_
______________。
②研究发现,废水中氨氮去除率随温度升高呈先升后降趋势。当温度大于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是____________。
③n(ClO-)/n(氨氮)对废水中氨氮去除率和总氮去除率的影响如题14图-2所示。当n(ClO-)/n(氨氮)>1.54后,总氮去除率下降的原因是_____________。
【例4】
氨氮的去除
NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业废气中的NH3可通过催化氧化为N2除去。将一定比例NH3、O2和N2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、N2的选择性[ ×100%]与温度的关系如题图所示。
【例5】
(1)在175~300℃范围内,随着温度的升高,出口处氮气和氮氧化物的量如何变化?为什么?
氮氧化物的处理
NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业废气中的NH3可通过催化氧化为N2除去。将一定比例NH3、O2和N2的混合气体以一定流速通过装有催化剂的反应管,NH3的转化率、N2的选择性[ ×100%]与温度的关系如题图所示。
【例5】
(2)催化氧化除去尾气中的NH3应选择怎样的反应温度?
(3)高效除去尾气中的氨气,你有什么建议?
需研发低温下NH3转化率高和N2选择性高的催化剂
应选择反应温度225℃左右
含氮污染的处理
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
8NH3+6NO2 7N2+12H2O
催化剂
4NH3+6NO 5N2+6H2O
催化剂
脱除烟气中的氮氧化物(主要是指NO和NO2)可净化空气、改善环境,是环境保护的主要课题。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如题14图-2所示。当NO2与NO的物质的量之比为1∶1时,与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为 。
氮氧化物的处理
【例6】
(2)一种通过氧化钡和硝酸钡的相互转化脱除二氧化氮的原理如图所示,脱除二氧化氮的总反应为
氮氧化物的处理
氮氧化物的处理
(3)NO2的消除。可以用碳酸钠溶液来进行吸收,在产生CO2的同时,会生成NaNO2等物质,NaNO2是工业盐的主要成分,在漂白、电镀等方面应用广泛。
写出碳酸钠溶液消除NO2的化学方程式: 。
氮元素的价类二维图
+5
+4
+2
0
-3
氢化物 单质 氧化物 酸 盐
NH3
NH3
NO
O2
NO2
O2
H2O
HNO3
NH4+
H+
N2
+3
NO3-
NO2-
HNO2
氮氧化物的处理
(4)用酸性(NH2)2CO水溶液吸收氮氧化物,吸收过程中存在HNO2与(NH2)2CO
生成N2和CO2的反应。写出该反应的化学方程式: 。
(5)利用电化学装置可消除氮氧化物污染,变废为宝。 下图为电解NO制备
NH4NO3的装置,该装置中阳极的电极反应式为 。
谢 谢!
同课章节目录
