用元素化合物知识解释客观事实(二)(15张ppt)
文档属性
| 名称 | 用元素化合物知识解释客观事实(二)(15张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-17 00:00:00 | ||
图片预览





文档简介
(共15张PPT)
用金属元素化合物知识
解释客观事实(二)
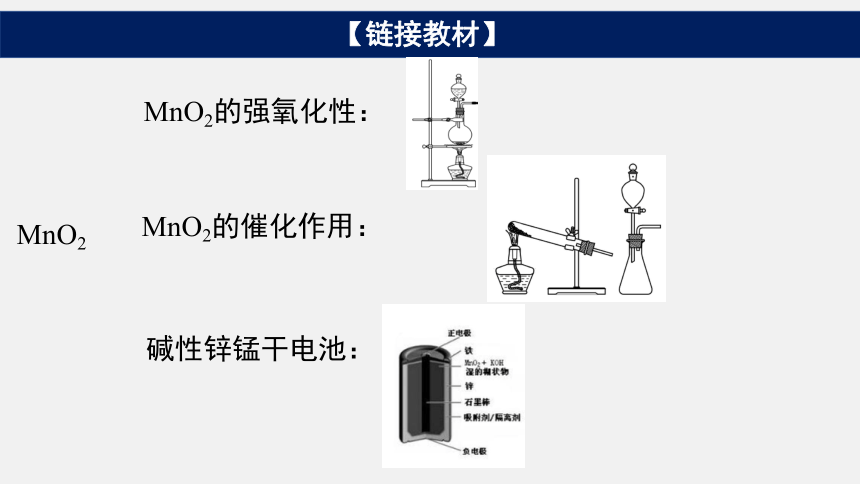
【链接教材】
MnO2
MnO2的强氧化性:
MnO2的催化作用:
碱性锌锰干电池:
KMnO4
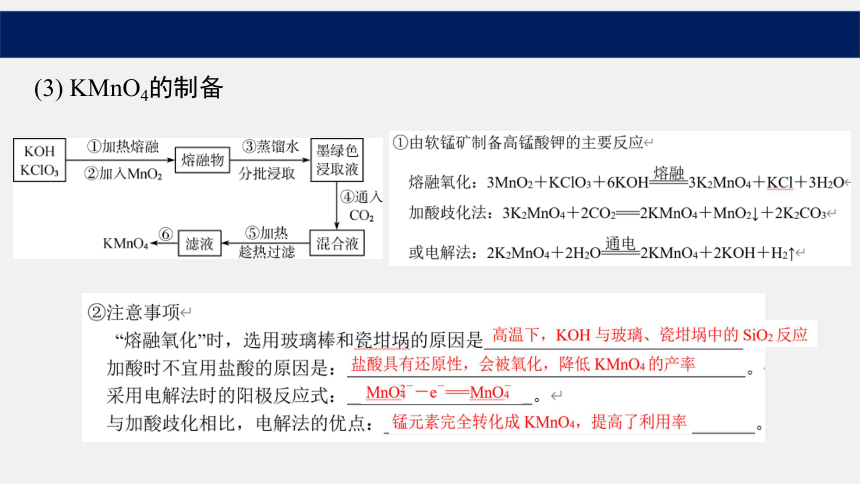
(3) KMnO4的制备
【典型例题】
一、软锰矿的浸取
[拓展]
[拓展]
二、碳酸锰的制备
[拓展]
三、锰的氧化物的制备
[拓展]
四、锰的氧化物的含量测定
同学们再见!
备
·o
员
万
正电极
铁
Mn02+KOH
湿的湖状物
锌
石里养
吸附剂/隔离剂
负电极
(1)KMnO4强氧化性
①酸性介质:还原产物为Mn2+
2MnO4+5SO3+6H+=2Mn2++5SO4+3H20
MnQ4+5Fe2++8H+一Mn2++5Fe3++4H2O(用于定量测定铁含量)
2MnO4+5H2C2O4+6H+=2Mn2++10C02↑+8H2O(用于KMnO4浓度标定)
②中性、弱碱性介质还原产物为MnO2:MnQ4+I+H2O一2MnO2↓+IO3+2OH
③碱性介质中,还原产物为MnQ好:MnQ4+SO3+2OH一=2MnQ4+SO4+H2O
(2)KMnO4溶液的自催化
4KMO4+2H20光照
4KOH+4MnO2↓+302↑
反应生成的MnO2是该反应的催化剂,当KMnO4一旦分解,就会加速分解的进行,称
作“自动催化”。因此KMnO4溶液应置于阴凉避光处保存,常用棕色瓶存放。
KOH
①加热熔融
③蒸馏水
墨绿色
熔融物
KC1O
②加入MnO2
分批浸取
浸取液
④通入
C02
⑤加热
KMnO4
滤液
趁执过滤
混合液
①由软锰矿制备高锰酸钾的主要反应<
熔融氧化:3MnO2十KC103十6KOH熔融
3K2Mn04+KCI+3H2O
加酸歧化法:3K2MnO4+2CO2=2KMnO4十MnO2↓十2K2CO3
或电解法:2K2MnO4十2H2O
通电
2KMnO4+2KOH+H2↑
②注意事项<
熔融氧化时,选用玻璃棒和瓷坩埚的原因是
加酸时不宜用盐酸的原因是:
采用电解法时的阳极反应式:
与加酸歧化相比,电解法的优点:
0.5
0一
0.4
c(MnSO4)
c(H2SO4)
0.3
0.2
0.1
0
0.5
1.0
1.52.0
2.53.0
t/h
向一定量软锰矿浆软锰矿浆(主要成分MnO2,杂质为Fe、
A1等元素的氧化物)中匀速通入烟气(含有SO2、O2等),
溶液中c(H2SO4)、c(MnSO.4)随吸收时间的变化如图所示。随
着吸收时间增加,溶液中c(H2SO4)的增加呈现由慢到快的趋
势,其主要原因
用金属元素化合物知识
解释客观事实(二)
【链接教材】
MnO2
MnO2的强氧化性:
MnO2的催化作用:
碱性锌锰干电池:
KMnO4
(3) KMnO4的制备
【典型例题】
一、软锰矿的浸取
[拓展]
[拓展]
二、碳酸锰的制备
[拓展]
三、锰的氧化物的制备
[拓展]
四、锰的氧化物的含量测定
同学们再见!
备
·o
员
万
正电极
铁
Mn02+KOH
湿的湖状物
锌
石里养
吸附剂/隔离剂
负电极
(1)KMnO4强氧化性
①酸性介质:还原产物为Mn2+
2MnO4+5SO3+6H+=2Mn2++5SO4+3H20
MnQ4+5Fe2++8H+一Mn2++5Fe3++4H2O(用于定量测定铁含量)
2MnO4+5H2C2O4+6H+=2Mn2++10C02↑+8H2O(用于KMnO4浓度标定)
②中性、弱碱性介质还原产物为MnO2:MnQ4+I+H2O一2MnO2↓+IO3+2OH
③碱性介质中,还原产物为MnQ好:MnQ4+SO3+2OH一=2MnQ4+SO4+H2O
(2)KMnO4溶液的自催化
4KMO4+2H20光照
4KOH+4MnO2↓+302↑
反应生成的MnO2是该反应的催化剂,当KMnO4一旦分解,就会加速分解的进行,称
作“自动催化”。因此KMnO4溶液应置于阴凉避光处保存,常用棕色瓶存放。
KOH
①加热熔融
③蒸馏水
墨绿色
熔融物
KC1O
②加入MnO2
分批浸取
浸取液
④通入
C02
⑤加热
KMnO4
滤液
趁执过滤
混合液
①由软锰矿制备高锰酸钾的主要反应<
熔融氧化:3MnO2十KC103十6KOH熔融
3K2Mn04+KCI+3H2O
加酸歧化法:3K2MnO4+2CO2=2KMnO4十MnO2↓十2K2CO3
或电解法:2K2MnO4十2H2O
通电
2KMnO4+2KOH+H2↑
②注意事项<
熔融氧化时,选用玻璃棒和瓷坩埚的原因是
加酸时不宜用盐酸的原因是:
采用电解法时的阳极反应式:
与加酸歧化相比,电解法的优点:
0.5
0一
0.4
c(MnSO4)
c(H2SO4)
0.3
0.2
0.1
0
0.5
1.0
1.52.0
2.53.0
t/h
向一定量软锰矿浆软锰矿浆(主要成分MnO2,杂质为Fe、
A1等元素的氧化物)中匀速通入烟气(含有SO2、O2等),
溶液中c(H2SO4)、c(MnSO.4)随吸收时间的变化如图所示。随
着吸收时间增加,溶液中c(H2SO4)的增加呈现由慢到快的趋
势,其主要原因
同课章节目录
