人教版(五四学制)化学八年级全册 第六单元 课题1 金刚石、石墨和C60 教案(表格式)
文档属性
| 名称 | 人教版(五四学制)化学八年级全册 第六单元 课题1 金刚石、石墨和C60 教案(表格式) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-18 00:00:00 | ||
图片预览




文档简介
金刚石,石墨和C
1. 教学目标
1. 知识与技能
(1) 了解金刚石和石墨的物理性质和用途;
(2) 知道碳的化学性质;
(3) 知道不同种元素可以组成不同的物质,同种元素也可以组成不同的物质。
2. 过程与方法
(1) 能认真观察实验现象,通过对现象进行分析归纳,总结出重要的知识点;
(2) 通过对金刚石,石墨和C中碳原子排列方式的分析,懂得物质结构,性质和用途之间的关系。
3. 情感态度与价值观
以发展的观点看待碳的单质,树立物质的性质决定用途的观点。
2. 教学重点和难点
重点:碳单质的化学性质;
难点:碳跟某些氧化物的反应。
3. 教学设计思路
本课题包括两部分:碳的单质和碳的化学性质。碳的单质主要介绍了金刚石的“硬”,石墨的“软”和优良的导电性及C分子的结构特点。碳的化学性质主要介绍了碳与氧气及某些氧化物的反应。
在介绍碳的单质时,通过展示相关图片,让学生了解3种碳单质的物理性质及用途,再联系最新科技成就,帮助学生树立物质的性质决定用途的观点,使学生认识到随着科技的发展,碳单质的用途将不断扩大。
碳的化学性质是本课题的教学重点,其中碳与氧化物的反应是本课题的教学难点,因此在介绍碳的化学性质时,将学生的实际生活和已有的知识进行联系。首先展示北宋黄庭坚的书法和一幅古代山水画的图片,提出问题:为什么古代的书法和山水画能保存至今而不变色?由此引出常温下,碳的化学性质不活泼。再通过创设情境:小强和2位同学去烧烤,引发学生思考:当温度升高时,碳的化学性质发生什么变化?从而引出碳能与氧气及某些氧化物反应的性质。
本课题安排为一课时,利用多媒体的教学方式,课件内容包括文本,图片和视频,整个教学过程采用PowerPoint方式放映,直观,生动地把本节课的学习内容结合在一起,能够激发学生的学习兴趣,帮助学生理解所学的知识,突破重点和难点,将教师的主导作用和学生的主体作用相结合,达到较好的教学效果。
4. 教学设计
教学环节 活动设计 设计意图
导入新课 【提出问题】在前面的学习中,我们知道不同的元素可以组成不同的物质,那么同种元素能不能组成不同的物质呢?(学生思考并回答,教师归纳总结,进入新课的学习)【教师小结】同种元素可以组成不同的物质,如金刚石,石墨和C,它们都是由碳元素组成的,但却是3种不同的物质。今天我们就来学习碳的单质及碳的化学性质。 提出问题,引发学生思考,引出学习主题
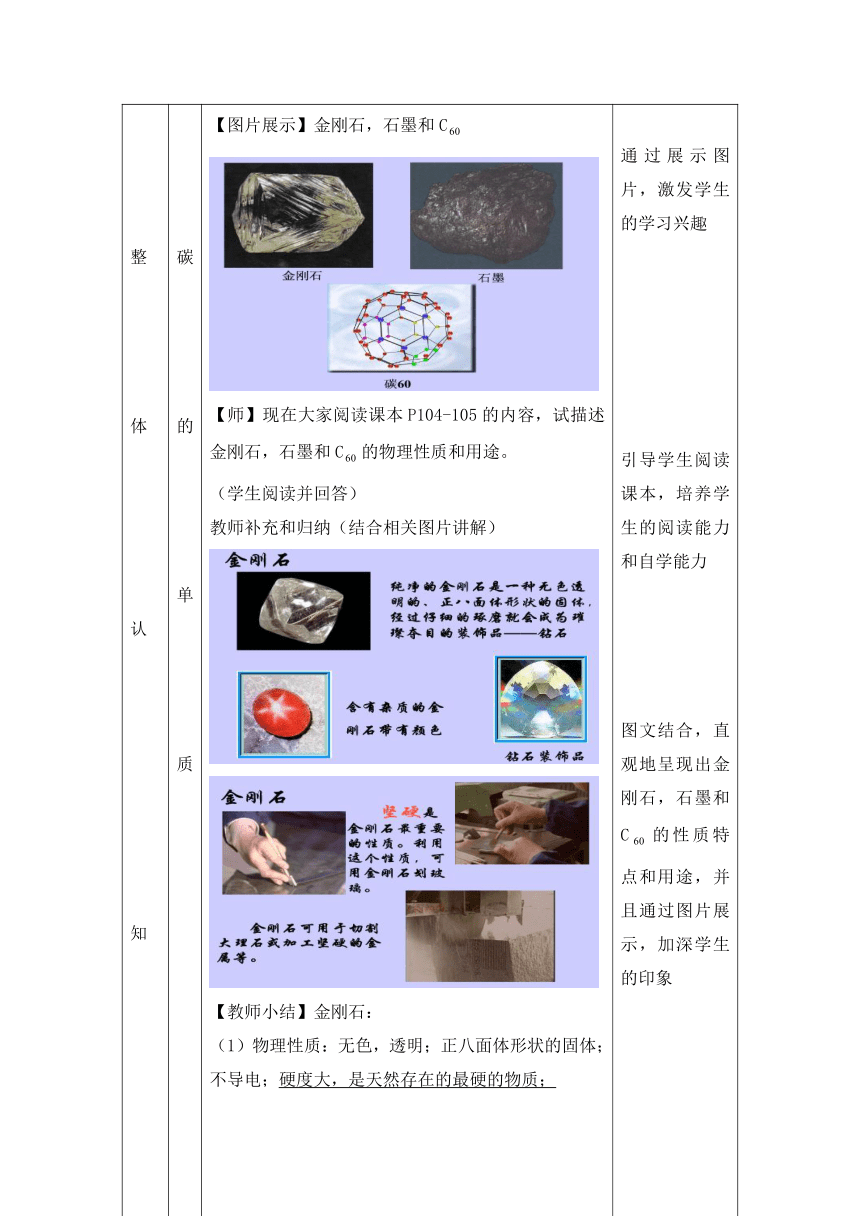
整体认知 碳的单质 【图片展示】金刚石,石墨和C【师】现在大家阅读课本P104-105的内容,试描述金刚石,石墨和C的物理性质和用途。(学生阅读并回答)教师补充和归纳(结合相关图片讲解) 【教师小结】金刚石:(1)物理性质:无色,透明;正八面体形状的固体;不导电;硬度大,是天然存在的最硬的物质; 通过展示图片,激发学生的学习兴趣引导学生阅读课本,培养学生的阅读能力和自学能力图文结合,直观地呈现出金刚石,石墨和C的性质特点和用途,并且通过图片展示,加深学生的印象
(2)用途:①雕琢作装饰品;②玻璃刀刀头。【教师小结】石墨物理性质:深灰色;有金属光泽;不透明;细磷片状固体;质软,有滑腻感;具有优良的导电性;用途:①制铅笔芯;②作石墨电极;③作润滑剂。 【教师小结】C:形似足球,很稳定。【师生活动】通过比较金刚石和石墨的物理性质和用 通过生生互动,师生互动
途,得出物质的性质和用途之间的关系: 【实验分析】P105 实验6-1现象:红色液体变为无色【讨论】为什么加入木炭或活性炭后,红色液体会变为无色?(学生积极讨论并回答)【教师小结】木炭,活性炭都是由石墨的微小晶体和少量杂质构成的,具有疏松多孔的结构,具有吸附性,所以红色液体变为无色。 的方式调动学生参与教学的积极性通过学生的交流讨论,充分调动学生的积极性,不但能活跃课堂气氛,还能培养学生的思维能力和语言表达能力
过渡 【师】刚才我们介绍的是由碳元素组成的单质的物理性质和用途,接下来我们来了解碳的化学性质。 自然过渡
碳的化学性质 【图片展示】①北宋黄庭坚用墨写的字②古代画家用墨水画成的一幅山水画 展示图片,激发学生的学习兴趣
整体认知
【提问】为什么古代的书法和山水画能保存至今而不变色?(学生思考并回答)【教师总结】古代书写和绘画都是用墨水,墨是由炭黑等制成的,炭黑的主要成分是碳,而常温下,碳的化学性质不活泼。【创设情境】周末到了,小强和两位同学一起去烧烤【思考】小强他们烧烤时所用的燃料是什么?(学生讨论并回答)教师对学生的回答进行整理,归纳:烧烤所用的燃料是木炭,木炭的主要成分是碳。说明当温度升高时,碳的化学性质会变得活泼,并且碳能跟氧气反应,具有可燃性。【提问】同学们还记得第二单元中碳与氧气的反应吗?能不能写出这个反应的化学方程式? 学生通过思考,领会碳在常温下化学性质稳定的性质
整体认知 碳的化学 (学生回答并读出化学方程式)【教师总结,补充】碳中氧气中燃烧,只有当氧气充足时,才生成二氧化碳,,如果氧气不足的话,则生成另外一种物质---一氧化碳, 【讨论】在前面的学习中,我们知道CO是一种污染空气的气体,它是一种有毒的气体,因此在冬天用煤炉生火取暧时,应注意什么问题 【学生】要注意保持空气流通,防止屋内产生过多的CO,导致中毒事件的发生。【师】碳能够跟单质氧结合,那么能不能跟氧化物中的氧结合呢?例如氧化铜(CuO),如果能,反应后会生成什么物质呢?【播放视频】碳化原氧化铜实验引导学生观察思考:试管中澄清石灰水发生什么变化?大试管中的粉末发生了什么变化?在反应中生成什么物质?(学生在教师的指导下,认真观看实验,并分析产生该现象的原因)【教师总结】现象:澄清石灰水变浑浊,大试管粉末中有红色物质; 复习旧知识,引入新知识联系实际,对学生进行安全教育提出问题,激发学生的学习兴趣播放视频,让学生更直观地观察到实验现象,作为探究实验的切入点,培养学生通过实验探究科学知识的意识
性质 原因:碳能与氧化物反应,具有还原性,【师】在这个反应中,CuO中的氧被C夺走,变成Cu,像这样含氧化合物中的氧被夺走的反应叫做还原反应,能夺走含氧化合物中的氧的物质具有还原性。单质碳的还原性可用于冶练金属,例如,焦炭可以把铁从它的氧化物矿石里还原出来 拓展知识
课堂小结 【师】通过今天的学习,我们知道同种元素也可以组成不同的物质,了解了几种碳单质的性质和用途,并且知道了碳在常温下很稳定,在加热或高温条件下则具有可燃性和还原性。(结合板书进行详细的总结) 自然过渡,明确本节课的学习重点
知识巩固 1.根据下列物质的性质,写出其对应的一种用途:(1)金刚石的硬度很大: (金刚石可用来裁玻璃)(2)石墨导电性能好: (石墨可做电极)(3)单质碳具有还原性: (焦炭可以把铁从它的氧化物矿物中还原出来)2.“钻石恒永久,一颗永流传”(钻石的主要成份是碳)这句广告说明碳在常温下化学性质(稳定)3.木制的电线杆在埋入地下前,将其表面烧焦的目的是什么?(木头烤焦后变成木炭,木炭与空气,水分接触不容易发生反应,可以保存较长的时间) 巩固知识,联系实际生活,达到学以致用
5. 教学反思
本课题教学设计可操作性强,授课时脉络清晰,实现了教学设计的意图。首先认识了几种不同的碳单质,并了解了它们的物理性质和用途,然后重点分析总结碳的化学性质。
本课题能突出以学生为主体,教师为主导,在教学中注意对学生的指导,关注学生对知识的掌握情况,并强化了化学联系实际生活的功能,培养了学生观察,分析和解决问题的探究能力,课堂教学效果良好。
6. 板书设计
第六单元 碳和碳的氧化物
课题1 金刚石、石墨和C
1. 碳的单质
1.金刚石:硬度大,是天然存在的最硬的物质
2.石墨:质软,有滑腻感;具有优良的导电性
3. C:形似足球,很稳定
4.木炭,活性炭具有吸附性
5.物质的性质和用途之间的关系:
2. 碳的化学性质——常温下不活泼
1.能与氧气反应——具有可燃性
(氧气充足)
(氧气不足)
2.能与某些氧化物反应——具有还原性
还原反应:含氧化合物中的氧被夺走的反应
还原性;能夺走含氧化合物中的氧的物质具有还原性
1. 教学目标
1. 知识与技能
(1) 了解金刚石和石墨的物理性质和用途;
(2) 知道碳的化学性质;
(3) 知道不同种元素可以组成不同的物质,同种元素也可以组成不同的物质。
2. 过程与方法
(1) 能认真观察实验现象,通过对现象进行分析归纳,总结出重要的知识点;
(2) 通过对金刚石,石墨和C中碳原子排列方式的分析,懂得物质结构,性质和用途之间的关系。
3. 情感态度与价值观
以发展的观点看待碳的单质,树立物质的性质决定用途的观点。
2. 教学重点和难点
重点:碳单质的化学性质;
难点:碳跟某些氧化物的反应。
3. 教学设计思路
本课题包括两部分:碳的单质和碳的化学性质。碳的单质主要介绍了金刚石的“硬”,石墨的“软”和优良的导电性及C分子的结构特点。碳的化学性质主要介绍了碳与氧气及某些氧化物的反应。
在介绍碳的单质时,通过展示相关图片,让学生了解3种碳单质的物理性质及用途,再联系最新科技成就,帮助学生树立物质的性质决定用途的观点,使学生认识到随着科技的发展,碳单质的用途将不断扩大。
碳的化学性质是本课题的教学重点,其中碳与氧化物的反应是本课题的教学难点,因此在介绍碳的化学性质时,将学生的实际生活和已有的知识进行联系。首先展示北宋黄庭坚的书法和一幅古代山水画的图片,提出问题:为什么古代的书法和山水画能保存至今而不变色?由此引出常温下,碳的化学性质不活泼。再通过创设情境:小强和2位同学去烧烤,引发学生思考:当温度升高时,碳的化学性质发生什么变化?从而引出碳能与氧气及某些氧化物反应的性质。
本课题安排为一课时,利用多媒体的教学方式,课件内容包括文本,图片和视频,整个教学过程采用PowerPoint方式放映,直观,生动地把本节课的学习内容结合在一起,能够激发学生的学习兴趣,帮助学生理解所学的知识,突破重点和难点,将教师的主导作用和学生的主体作用相结合,达到较好的教学效果。
4. 教学设计
教学环节 活动设计 设计意图
导入新课 【提出问题】在前面的学习中,我们知道不同的元素可以组成不同的物质,那么同种元素能不能组成不同的物质呢?(学生思考并回答,教师归纳总结,进入新课的学习)【教师小结】同种元素可以组成不同的物质,如金刚石,石墨和C,它们都是由碳元素组成的,但却是3种不同的物质。今天我们就来学习碳的单质及碳的化学性质。 提出问题,引发学生思考,引出学习主题
整体认知 碳的单质 【图片展示】金刚石,石墨和C【师】现在大家阅读课本P104-105的内容,试描述金刚石,石墨和C的物理性质和用途。(学生阅读并回答)教师补充和归纳(结合相关图片讲解) 【教师小结】金刚石:(1)物理性质:无色,透明;正八面体形状的固体;不导电;硬度大,是天然存在的最硬的物质; 通过展示图片,激发学生的学习兴趣引导学生阅读课本,培养学生的阅读能力和自学能力图文结合,直观地呈现出金刚石,石墨和C的性质特点和用途,并且通过图片展示,加深学生的印象
(2)用途:①雕琢作装饰品;②玻璃刀刀头。【教师小结】石墨物理性质:深灰色;有金属光泽;不透明;细磷片状固体;质软,有滑腻感;具有优良的导电性;用途:①制铅笔芯;②作石墨电极;③作润滑剂。 【教师小结】C:形似足球,很稳定。【师生活动】通过比较金刚石和石墨的物理性质和用 通过生生互动,师生互动
途,得出物质的性质和用途之间的关系: 【实验分析】P105 实验6-1现象:红色液体变为无色【讨论】为什么加入木炭或活性炭后,红色液体会变为无色?(学生积极讨论并回答)【教师小结】木炭,活性炭都是由石墨的微小晶体和少量杂质构成的,具有疏松多孔的结构,具有吸附性,所以红色液体变为无色。 的方式调动学生参与教学的积极性通过学生的交流讨论,充分调动学生的积极性,不但能活跃课堂气氛,还能培养学生的思维能力和语言表达能力
过渡 【师】刚才我们介绍的是由碳元素组成的单质的物理性质和用途,接下来我们来了解碳的化学性质。 自然过渡
碳的化学性质 【图片展示】①北宋黄庭坚用墨写的字②古代画家用墨水画成的一幅山水画 展示图片,激发学生的学习兴趣
整体认知
【提问】为什么古代的书法和山水画能保存至今而不变色?(学生思考并回答)【教师总结】古代书写和绘画都是用墨水,墨是由炭黑等制成的,炭黑的主要成分是碳,而常温下,碳的化学性质不活泼。【创设情境】周末到了,小强和两位同学一起去烧烤【思考】小强他们烧烤时所用的燃料是什么?(学生讨论并回答)教师对学生的回答进行整理,归纳:烧烤所用的燃料是木炭,木炭的主要成分是碳。说明当温度升高时,碳的化学性质会变得活泼,并且碳能跟氧气反应,具有可燃性。【提问】同学们还记得第二单元中碳与氧气的反应吗?能不能写出这个反应的化学方程式? 学生通过思考,领会碳在常温下化学性质稳定的性质
整体认知 碳的化学 (学生回答并读出化学方程式)【教师总结,补充】碳中氧气中燃烧,只有当氧气充足时,才生成二氧化碳,,如果氧气不足的话,则生成另外一种物质---一氧化碳, 【讨论】在前面的学习中,我们知道CO是一种污染空气的气体,它是一种有毒的气体,因此在冬天用煤炉生火取暧时,应注意什么问题 【学生】要注意保持空气流通,防止屋内产生过多的CO,导致中毒事件的发生。【师】碳能够跟单质氧结合,那么能不能跟氧化物中的氧结合呢?例如氧化铜(CuO),如果能,反应后会生成什么物质呢?【播放视频】碳化原氧化铜实验引导学生观察思考:试管中澄清石灰水发生什么变化?大试管中的粉末发生了什么变化?在反应中生成什么物质?(学生在教师的指导下,认真观看实验,并分析产生该现象的原因)【教师总结】现象:澄清石灰水变浑浊,大试管粉末中有红色物质; 复习旧知识,引入新知识联系实际,对学生进行安全教育提出问题,激发学生的学习兴趣播放视频,让学生更直观地观察到实验现象,作为探究实验的切入点,培养学生通过实验探究科学知识的意识
性质 原因:碳能与氧化物反应,具有还原性,【师】在这个反应中,CuO中的氧被C夺走,变成Cu,像这样含氧化合物中的氧被夺走的反应叫做还原反应,能夺走含氧化合物中的氧的物质具有还原性。单质碳的还原性可用于冶练金属,例如,焦炭可以把铁从它的氧化物矿石里还原出来 拓展知识
课堂小结 【师】通过今天的学习,我们知道同种元素也可以组成不同的物质,了解了几种碳单质的性质和用途,并且知道了碳在常温下很稳定,在加热或高温条件下则具有可燃性和还原性。(结合板书进行详细的总结) 自然过渡,明确本节课的学习重点
知识巩固 1.根据下列物质的性质,写出其对应的一种用途:(1)金刚石的硬度很大: (金刚石可用来裁玻璃)(2)石墨导电性能好: (石墨可做电极)(3)单质碳具有还原性: (焦炭可以把铁从它的氧化物矿物中还原出来)2.“钻石恒永久,一颗永流传”(钻石的主要成份是碳)这句广告说明碳在常温下化学性质(稳定)3.木制的电线杆在埋入地下前,将其表面烧焦的目的是什么?(木头烤焦后变成木炭,木炭与空气,水分接触不容易发生反应,可以保存较长的时间) 巩固知识,联系实际生活,达到学以致用
5. 教学反思
本课题教学设计可操作性强,授课时脉络清晰,实现了教学设计的意图。首先认识了几种不同的碳单质,并了解了它们的物理性质和用途,然后重点分析总结碳的化学性质。
本课题能突出以学生为主体,教师为主导,在教学中注意对学生的指导,关注学生对知识的掌握情况,并强化了化学联系实际生活的功能,培养了学生观察,分析和解决问题的探究能力,课堂教学效果良好。
6. 板书设计
第六单元 碳和碳的氧化物
课题1 金刚石、石墨和C
1. 碳的单质
1.金刚石:硬度大,是天然存在的最硬的物质
2.石墨:质软,有滑腻感;具有优良的导电性
3. C:形似足球,很稳定
4.木炭,活性炭具有吸附性
5.物质的性质和用途之间的关系:
2. 碳的化学性质——常温下不活泼
1.能与氧气反应——具有可燃性
(氧气充足)
(氧气不足)
2.能与某些氧化物反应——具有还原性
还原反应:含氧化合物中的氧被夺走的反应
还原性;能夺走含氧化合物中的氧的物质具有还原性
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
