第七章《有机化合物》单元综合测试卷一2022年高一化学必修第二册(人教版2019)(Word含答案)
文档属性
| 名称 | 第七章《有机化合物》单元综合测试卷一2022年高一化学必修第二册(人教版2019)(Word含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 391.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-19 00:00:00 | ||
图片预览




文档简介
第七章《有机化合物》单元综合测试卷一
一、单选题(本大题共14题)
1.乙醇分子结构式如图所示,下列反应及断键部位正确的是
A.乙醇与钠的反应是⑤键断裂
B.乙醇的催化氧化反应是①③键断裂
C.乙醇的酯化反应是②键断裂
D.乙醇与酸性高锰酸钾反应是所有键都断裂
2.短周期元素A、B、C、D的原子序数依次增加。甲、乙、丙是由这些元素组成的二元化合物,常温下0.1 mol·L-1丙溶液的pH为1,丁是元素D的单质,为黄绿色气体,戊是难溶于水的混合物,己的水溶液具有漂白性。上述物质的转化关系如图所示。下列说法正确的是
A.甲可能是丁烷,常温常压下呈气态
B.原子半径的大小: A<B<C<D
C.氧化物对应水化物的酸性: D>B
D.己的结构式:A-D-C
3.已知最简单的有机物E和直线型分子G在光照条件下反应,生成四面体型分子L和直线型分子M(组成G分子的元素为第三周期的元素),如图。则下列判断错误的是
A.常温常压下,E是一种无色无味的气体 B.上述反应类型是取代反应
C.G能使干燥的红色布条变成无色 D.在光照条件L能与G继续发生与上述类似的反应
4.碳原子成键的多样性、同分异构现象等是有机物种类繁多的原因。丁烷和2-甲基丙烷的结构式如图,下列关于上述两种物质的说法不正确的是
A.分子式相同
B.互为同分异构体
C.等物质的量的两物质中碳氢键(C- H)数目相同
D.物理性质、化学性质完全相同
5.下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
②除去SiO2中少量的Al2O3:用稀盐酸洗涤,过滤、洗涤、干燥;
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的水:加足量生右灰,蒸馏。
A.①② B.②④ C.③④ D.②③
6.材料是人类文明的重要组成部分,下列有关材料的说法错误的是
A.SiC陶瓷、光导纤维和碳纳米管都是新型无机非金属材料
B.在水泥砂浆中添加适量的水玻璃可以提高水泥砂浆的黏结性和胶凝性
C.塑料、天然橡胶、麻、蚕丝等都是天然高分子材料
D.通过淀粉发酵方法获得味精
7.下列化学用语书写正确的是
A.CH3CHO的球棍模型:
B. 按照系统命名法的名称:2-乙基丙烷
C.过氧化氢的空间填充模型:
D.-NH2的电子式:
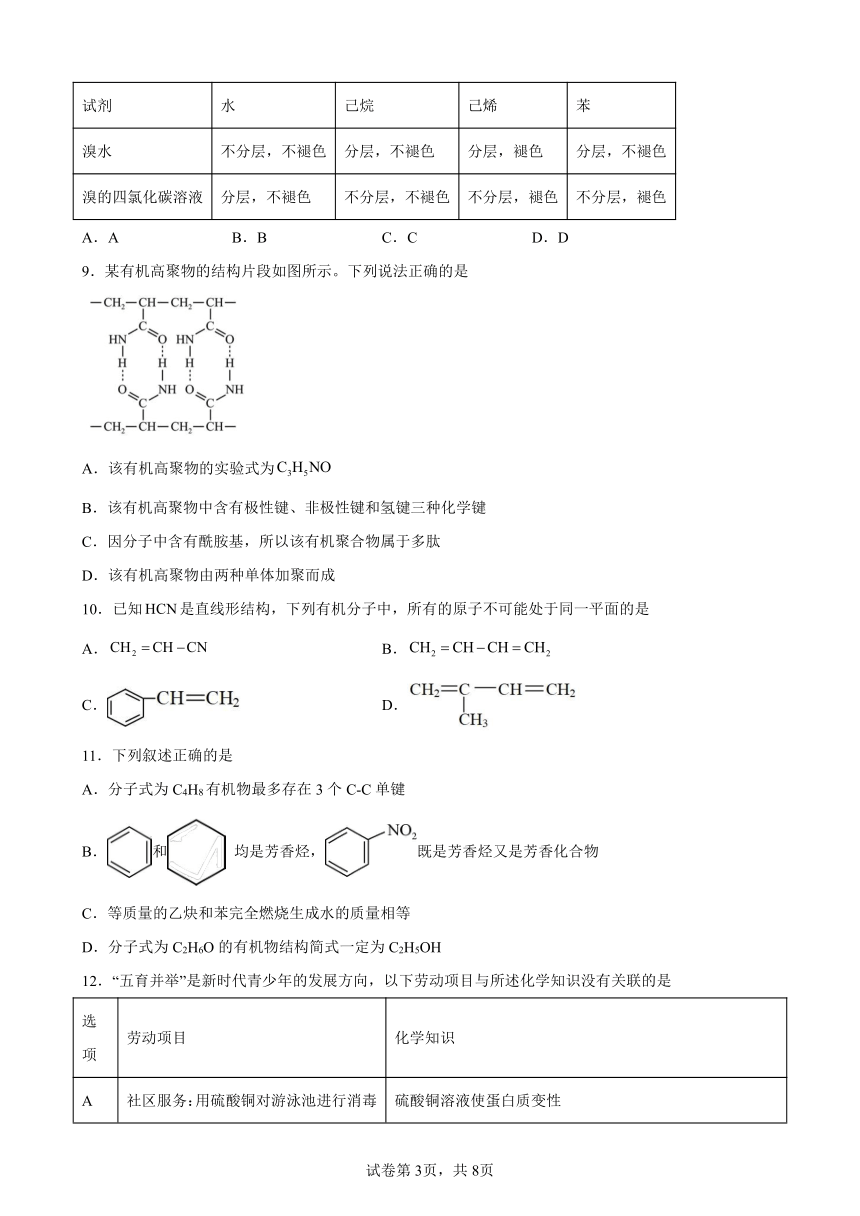
8.下列现象的记录完全有错误的是
选项 A B C D
试剂 水 己烷 己烯 苯
溴水 不分层,不褪色 分层,不褪色 分层,褪色 分层,不褪色
溴的四氯化碳溶液 分层,不褪色 不分层,不褪色 不分层,褪色 不分层,褪色
A.A B.B C.C D.D
9.某有机高聚物的结构片段如图所示。下列说法正确的是
A.该有机高聚物的实验式为
B.该有机高聚物中含有极性键、非极性键和氢键三种化学键
C.因分子中含有酰胺基,所以该有机聚合物属于多肽
D.该有机高聚物由两种单体加聚而成
10.已知是直线形结构,下列有机分子中,所有的原子不可能处于同一平面的是
A. B.
C. D.
11.下列叙述正确的是
A.分子式为C4H8有机物最多存在3个C-C单键
B.和 均是芳香烃,既是芳香烃又是芳香化合物
C.等质量的乙炔和苯完全燃烧生成水的质量相等
D.分子式为C2H6O的有机物结构简式一定为C2H5OH
12.“五育并举”是新时代青少年的发展方向,以下劳动项目与所述化学知识没有关联的是
选项 劳动项目 化学知识
A 社区服务:用硫酸铜对游泳池进行消毒 硫酸铜溶液使蛋白质变性
B 感恩父母:蒸武昌鱼时加少许料酒与食醋提香 乙醇与醋酸酯化产物有香味
C 爱牙日宣传:用碳酸氢钠清洗牙垢 碳酸氢钠有碱性
D 志愿活动:用水玻璃涂刷木材阻燃 Na2SiO3水解生成硅酸粘附在木材表面,阻碍木柴与氧气的接触而阻燃
A.A B.B C.C D.D
13.已知:CH2=CH—CH=CH2+Br2→BrCH2—CH=CH—CH2Br(1,4—加成反应)。下列说法不正确的是(提示以下氯代物或产物均不考虑立体异构)
A.甲苯完全氢化后的环烷烃的一氯代物有5种
B.某烃()与按物质的量之比为1∶1加成时,所得产物有5种
C.螺[2,2]戊烷()的二氯代物有4种
D.环丙叉环丙烷()的二氯代物有4种
14.最近,国外报道了首例猪肾脏成功移植入人体的新闻,吗替麦考酚酯主要用于预防器官排斥反应,其结构简式如图所示。下列说法错误的是
A.该分子中含有三种含氧官能团
B.分子式为
C.可以发生取代反应、加聚反应、氧化反应
D.1 mol该分子与足量的发生加成反应,最多消耗6 mol
二、非选择题(本大题共7题)
15.回答下列问题:
(1)有下列各组物质:A.和 B.和 C.和 D.甲烷和新戊烷 E.和 F.和(填字母)
①_______组两物质间互为同位素。
②_______组两物质间互为同素异形体。
③_______组两物质属于同系物。
④_______组两物质互为同分异构体。
⑤_______组是同一物质。
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④溶于水、⑤溶于水、⑥溶于水、⑦溶于水。仅破坏离子键的是_______(填序号,下同);仅破坏共价键的是_______;既破坏离子键又破坏共价键的是_______。
(3)写出下列物质的电子式:_______,_______。
16.乙烯(CH2=CH2)是非常重要的化工基础原料,由乙烯可以制备很多有机物。
I.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol水,发生CH2=CH2(g)+H2O(g)CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
时间(min) 0 2 4 6 8 10
乙醇的物质的量(mol) 0 0.3 0.5 0.6 0.65 0.65
(1)乙烯和水生成乙醇的反应类型是_______。该反应涉及到的三种物质中属于烃类的是_______(填分子式)。
(2)计算在0-6min内的反应速率v(H2O)=_______mol·L-1·min-1。
(3)8min时反应达到化学平衡状态,其理由是:_______。
II.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)C2H6(g),容器内气体的压强与反应时间的关系如下图:
时间(min) 0 2 4 6 8 10
气体压强(MPa) 100 80 70 65 60 60
(4)有机物C2H6的名称是_______。该有机物属于_______(填序号)。
A.烯烃B.芳香烃C.环状饱和烃D.链状饱和烃(烷烃)
(5)该反应的类型属于_______(填序号)。
A.取代反应 B.加成反应 C.加成聚合反应 D.聚合反应
(6)达到化学平衡状态时,下列数值与开始时相同的是_______(填序号)
A.容器内气体的压强 B.容器内n(H2) C.容器内c(CH2=CH2) D.容器内气体的总质量
(7)反应进行到10min时,乙烯(CH2=CH2)的转化率a%=_______。
17.阅读短文,回答问题。
我国科研团队在人工合成淀粉方面取得重要进展,在实验室实现从二氧化碳到淀粉的全合成。
人工合成淀粉是如何实现的?科研团队利用催化剂将高浓度二氧化碳在氢气作用下还原成碳一化合物,然后将碳一化合物聚合成碳三化合物,又将碳三化合物聚合成碳六化合物,再进一步合成淀粉。
人工合成淀粉有多大意义?检测发现,人工合成淀粉分子与天然淀粉分子的组成结构一致。如果人工合成淀粉产业化成功,全球性的粮食危机有望得到彻底解决。同时合成过程中使用大量的二氧化碳,引起全球变暖的最主要温室气体将被有效利用。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)二氧化碳和淀粉都属于含碳物质。_______
(2)从碳一化合物逐步合成淀粉的过程中,碳链逐渐增长。_______
(3)人工合成淀粉分子与天然淀粉分子的组成结构不同。_______
(4)人工合成淀粉产业化,有利于解决粮食危机和缓解温室效应。_______
18.现有下列物质:①HCl、②CO2、③H2O、④NaOH、⑤Cl2、⑥NaHSO4、⑦MgCl2、⑧CaO、⑨He请回答下列问题。
(1)NaOH是以___________化学键结合的;不含化学键的物质是___________(填序号)。
(2)写出CO2的电子式___________;用电子式表示MgCl2的形成过程___________。
(3)存在分子间作用力的物质有___________(填序号)。
(4)哪些物质属于离子化合物___________(填序号);哪些物质属于共价化合物___________(填序号)。
(5)HCl溶于水时,断开的化学键类型是___________;NaHSO4加热熔化时,断开的化学键类型是___________。
19.烷烃
(1)乙烷和丙烷
名称 乙烷 丙烷
分子式 _______ _______
结构简式 _______ _______
结构式 _______ _______
(2)烷烃的结构特点
每个碳原子形成_______个共价键,碳原子之间都以_______相连成_______状,其他的价键都用于与_______结合,达到“饱和”。
(3)烷烃的组成通式:_______。
(4)烷烃的命名
分子中含1~10个碳原子的烷烃,按照分子中碳原子数目依次用_______命名,如C5H12称为_______。分子中碳原子数超过10个的,直接根据_______称为某烷,如C16H34称为_______。
20.乙酸的化学性质
(1)弱酸性
①乙酸水溶液加入紫色石蕊试液,溶液变_______色,乙酸在水中的电离方程式为_______。
②乙酸的酸性比碳酸_______,乙酸与碳酸钠溶液反应的实验现象是_______,化学方程式为_______。
③与活泼金属反应
乙酸与镁反应的方程式为:_______。
(2)与乙醇的反应
①实验操作:在试管里先加入3 mL_______,边振荡,边慢慢地加入2 mL_______和2 mL_______。用酒精灯小心加热试管3~5 min。产生的蒸气经导管通到_______的液面上。
②实验现象:饱和Na2CO3溶液的液面上有_______,闻到_______味。
③化学方程式:_______。
(3)酯化反应
①概念:_______和_______作用生成_______和_______的反应。
②乙酸和乙醇的反应机理:乙酸乙酯是乙醇分子中的_______取代了乙酸分子中的_______的生成物。即乙酸脱去_______,乙醇脱去羟基上的_______,结合成水,剩余部分结合成酯。
21.葡萄糖[CH2OH(CHOH)4CHO]和核糖(CH2OH—CHOH—CHOH—CHOH—CHO)都是人类生命活动不可缺少的物质,根据两者的结构,回答下列问题。
(1)下列有关葡萄糖和核糖的叙述正确的是___________。
A.两者都属于单糖
B.两者都能溶于水
C.两者互为同系物
D.两者都不能使酸性KMnO4溶液褪色
E.两者都可以和银氨溶液反应形成银镜
F.两者都是还原性糖,都可以被催化氧化
G.等物质的量的葡萄糖和核糖分别和足量的金属钠反应,生成氢气的物质的量之比为5∶4
(2)1mol核糖最多能与___________mol乙酸发生酯化反应。检验某糖尿病人的尿液中是否含有葡萄糖的试剂为___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.C
4.D
5.B
6.C
7.D
8.D
9.A
10.D
11.C
12.C
13.C
14.D
15.(1) B A D E CF
(2) ②③ ④ ⑥⑦
(3)
16.(1) 加成反应 C2H4
(2)0.1
(3)乙醇的浓度不再发生变化(或乙醇的物质的量不再发生变化)
(4) 乙烷 D
(5)B
(6)D
(7)80%
17.(1)对
(2)对
(3)错
(4)对
18.(1) 离子键和共价键 ⑨
(2)
(3)①②③⑤⑨
(4) ④⑥⑦⑧ ①②③
(5) 共价键 离子键
19.(1) C2H6 C3H8 CH3CH3 CH3CH2CH3
(2) 4 单键 链 氢原子
(3)CnH2n+2(n≥1)
(4) 甲、乙、丙、丁、戊、己、庚、辛、壬、癸 戊烷 中文数字 十六烷
20.(1) 红 CH3COOHCH3COO-+H+ 强
有无色气体产生 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O 2CH3COOH+Mg→(CH3COO)2Mg+H2↑
(2) 乙醇 98%浓硫酸 冰醋酸 饱和碳酸钠溶液 油状液体生成 香 CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
(3) 醇 酸 酯 水 乙氧基(CH3CH2O-) 羟基(-OH) 氢原子 氢
21.(1)ABEFG
(2) 4 新制氢氧化铜悬浊液
答案第1页,共2页
答案第1页,共2页
一、单选题(本大题共14题)
1.乙醇分子结构式如图所示,下列反应及断键部位正确的是
A.乙醇与钠的反应是⑤键断裂
B.乙醇的催化氧化反应是①③键断裂
C.乙醇的酯化反应是②键断裂
D.乙醇与酸性高锰酸钾反应是所有键都断裂
2.短周期元素A、B、C、D的原子序数依次增加。甲、乙、丙是由这些元素组成的二元化合物,常温下0.1 mol·L-1丙溶液的pH为1,丁是元素D的单质,为黄绿色气体,戊是难溶于水的混合物,己的水溶液具有漂白性。上述物质的转化关系如图所示。下列说法正确的是
A.甲可能是丁烷,常温常压下呈气态
B.原子半径的大小: A<B<C<D
C.氧化物对应水化物的酸性: D>B
D.己的结构式:A-D-C
3.已知最简单的有机物E和直线型分子G在光照条件下反应,生成四面体型分子L和直线型分子M(组成G分子的元素为第三周期的元素),如图。则下列判断错误的是
A.常温常压下,E是一种无色无味的气体 B.上述反应类型是取代反应
C.G能使干燥的红色布条变成无色 D.在光照条件L能与G继续发生与上述类似的反应
4.碳原子成键的多样性、同分异构现象等是有机物种类繁多的原因。丁烷和2-甲基丙烷的结构式如图,下列关于上述两种物质的说法不正确的是
A.分子式相同
B.互为同分异构体
C.等物质的量的两物质中碳氢键(C- H)数目相同
D.物理性质、化学性质完全相同
5.下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
②除去SiO2中少量的Al2O3:用稀盐酸洗涤,过滤、洗涤、干燥;
③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④除去乙醇中少量的水:加足量生右灰,蒸馏。
A.①② B.②④ C.③④ D.②③
6.材料是人类文明的重要组成部分,下列有关材料的说法错误的是
A.SiC陶瓷、光导纤维和碳纳米管都是新型无机非金属材料
B.在水泥砂浆中添加适量的水玻璃可以提高水泥砂浆的黏结性和胶凝性
C.塑料、天然橡胶、麻、蚕丝等都是天然高分子材料
D.通过淀粉发酵方法获得味精
7.下列化学用语书写正确的是
A.CH3CHO的球棍模型:
B. 按照系统命名法的名称:2-乙基丙烷
C.过氧化氢的空间填充模型:
D.-NH2的电子式:
8.下列现象的记录完全有错误的是
选项 A B C D
试剂 水 己烷 己烯 苯
溴水 不分层,不褪色 分层,不褪色 分层,褪色 分层,不褪色
溴的四氯化碳溶液 分层,不褪色 不分层,不褪色 不分层,褪色 不分层,褪色
A.A B.B C.C D.D
9.某有机高聚物的结构片段如图所示。下列说法正确的是
A.该有机高聚物的实验式为
B.该有机高聚物中含有极性键、非极性键和氢键三种化学键
C.因分子中含有酰胺基,所以该有机聚合物属于多肽
D.该有机高聚物由两种单体加聚而成
10.已知是直线形结构,下列有机分子中,所有的原子不可能处于同一平面的是
A. B.
C. D.
11.下列叙述正确的是
A.分子式为C4H8有机物最多存在3个C-C单键
B.和 均是芳香烃,既是芳香烃又是芳香化合物
C.等质量的乙炔和苯完全燃烧生成水的质量相等
D.分子式为C2H6O的有机物结构简式一定为C2H5OH
12.“五育并举”是新时代青少年的发展方向,以下劳动项目与所述化学知识没有关联的是
选项 劳动项目 化学知识
A 社区服务:用硫酸铜对游泳池进行消毒 硫酸铜溶液使蛋白质变性
B 感恩父母:蒸武昌鱼时加少许料酒与食醋提香 乙醇与醋酸酯化产物有香味
C 爱牙日宣传:用碳酸氢钠清洗牙垢 碳酸氢钠有碱性
D 志愿活动:用水玻璃涂刷木材阻燃 Na2SiO3水解生成硅酸粘附在木材表面,阻碍木柴与氧气的接触而阻燃
A.A B.B C.C D.D
13.已知:CH2=CH—CH=CH2+Br2→BrCH2—CH=CH—CH2Br(1,4—加成反应)。下列说法不正确的是(提示以下氯代物或产物均不考虑立体异构)
A.甲苯完全氢化后的环烷烃的一氯代物有5种
B.某烃()与按物质的量之比为1∶1加成时,所得产物有5种
C.螺[2,2]戊烷()的二氯代物有4种
D.环丙叉环丙烷()的二氯代物有4种
14.最近,国外报道了首例猪肾脏成功移植入人体的新闻,吗替麦考酚酯主要用于预防器官排斥反应,其结构简式如图所示。下列说法错误的是
A.该分子中含有三种含氧官能团
B.分子式为
C.可以发生取代反应、加聚反应、氧化反应
D.1 mol该分子与足量的发生加成反应,最多消耗6 mol
二、非选择题(本大题共7题)
15.回答下列问题:
(1)有下列各组物质:A.和 B.和 C.和 D.甲烷和新戊烷 E.和 F.和(填字母)
①_______组两物质间互为同位素。
②_______组两物质间互为同素异形体。
③_______组两物质属于同系物。
④_______组两物质互为同分异构体。
⑤_______组是同一物质。
(2)在下列变化中:①水的汽化、②NaCl熔化、③NaOH溶于水、④溶于水、⑤溶于水、⑥溶于水、⑦溶于水。仅破坏离子键的是_______(填序号,下同);仅破坏共价键的是_______;既破坏离子键又破坏共价键的是_______。
(3)写出下列物质的电子式:_______,_______。
16.乙烯(CH2=CH2)是非常重要的化工基础原料,由乙烯可以制备很多有机物。
I.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol水,发生CH2=CH2(g)+H2O(g)CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
时间(min) 0 2 4 6 8 10
乙醇的物质的量(mol) 0 0.3 0.5 0.6 0.65 0.65
(1)乙烯和水生成乙醇的反应类型是_______。该反应涉及到的三种物质中属于烃类的是_______(填分子式)。
(2)计算在0-6min内的反应速率v(H2O)=_______mol·L-1·min-1。
(3)8min时反应达到化学平衡状态,其理由是:_______。
II.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)C2H6(g),容器内气体的压强与反应时间的关系如下图:
时间(min) 0 2 4 6 8 10
气体压强(MPa) 100 80 70 65 60 60
(4)有机物C2H6的名称是_______。该有机物属于_______(填序号)。
A.烯烃B.芳香烃C.环状饱和烃D.链状饱和烃(烷烃)
(5)该反应的类型属于_______(填序号)。
A.取代反应 B.加成反应 C.加成聚合反应 D.聚合反应
(6)达到化学平衡状态时,下列数值与开始时相同的是_______(填序号)
A.容器内气体的压强 B.容器内n(H2) C.容器内c(CH2=CH2) D.容器内气体的总质量
(7)反应进行到10min时,乙烯(CH2=CH2)的转化率a%=_______。
17.阅读短文,回答问题。
我国科研团队在人工合成淀粉方面取得重要进展,在实验室实现从二氧化碳到淀粉的全合成。
人工合成淀粉是如何实现的?科研团队利用催化剂将高浓度二氧化碳在氢气作用下还原成碳一化合物,然后将碳一化合物聚合成碳三化合物,又将碳三化合物聚合成碳六化合物,再进一步合成淀粉。
人工合成淀粉有多大意义?检测发现,人工合成淀粉分子与天然淀粉分子的组成结构一致。如果人工合成淀粉产业化成功,全球性的粮食危机有望得到彻底解决。同时合成过程中使用大量的二氧化碳,引起全球变暖的最主要温室气体将被有效利用。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)二氧化碳和淀粉都属于含碳物质。_______
(2)从碳一化合物逐步合成淀粉的过程中,碳链逐渐增长。_______
(3)人工合成淀粉分子与天然淀粉分子的组成结构不同。_______
(4)人工合成淀粉产业化,有利于解决粮食危机和缓解温室效应。_______
18.现有下列物质:①HCl、②CO2、③H2O、④NaOH、⑤Cl2、⑥NaHSO4、⑦MgCl2、⑧CaO、⑨He请回答下列问题。
(1)NaOH是以___________化学键结合的;不含化学键的物质是___________(填序号)。
(2)写出CO2的电子式___________;用电子式表示MgCl2的形成过程___________。
(3)存在分子间作用力的物质有___________(填序号)。
(4)哪些物质属于离子化合物___________(填序号);哪些物质属于共价化合物___________(填序号)。
(5)HCl溶于水时,断开的化学键类型是___________;NaHSO4加热熔化时,断开的化学键类型是___________。
19.烷烃
(1)乙烷和丙烷
名称 乙烷 丙烷
分子式 _______ _______
结构简式 _______ _______
结构式 _______ _______
(2)烷烃的结构特点
每个碳原子形成_______个共价键,碳原子之间都以_______相连成_______状,其他的价键都用于与_______结合,达到“饱和”。
(3)烷烃的组成通式:_______。
(4)烷烃的命名
分子中含1~10个碳原子的烷烃,按照分子中碳原子数目依次用_______命名,如C5H12称为_______。分子中碳原子数超过10个的,直接根据_______称为某烷,如C16H34称为_______。
20.乙酸的化学性质
(1)弱酸性
①乙酸水溶液加入紫色石蕊试液,溶液变_______色,乙酸在水中的电离方程式为_______。
②乙酸的酸性比碳酸_______,乙酸与碳酸钠溶液反应的实验现象是_______,化学方程式为_______。
③与活泼金属反应
乙酸与镁反应的方程式为:_______。
(2)与乙醇的反应
①实验操作:在试管里先加入3 mL_______,边振荡,边慢慢地加入2 mL_______和2 mL_______。用酒精灯小心加热试管3~5 min。产生的蒸气经导管通到_______的液面上。
②实验现象:饱和Na2CO3溶液的液面上有_______,闻到_______味。
③化学方程式:_______。
(3)酯化反应
①概念:_______和_______作用生成_______和_______的反应。
②乙酸和乙醇的反应机理:乙酸乙酯是乙醇分子中的_______取代了乙酸分子中的_______的生成物。即乙酸脱去_______,乙醇脱去羟基上的_______,结合成水,剩余部分结合成酯。
21.葡萄糖[CH2OH(CHOH)4CHO]和核糖(CH2OH—CHOH—CHOH—CHOH—CHO)都是人类生命活动不可缺少的物质,根据两者的结构,回答下列问题。
(1)下列有关葡萄糖和核糖的叙述正确的是___________。
A.两者都属于单糖
B.两者都能溶于水
C.两者互为同系物
D.两者都不能使酸性KMnO4溶液褪色
E.两者都可以和银氨溶液反应形成银镜
F.两者都是还原性糖,都可以被催化氧化
G.等物质的量的葡萄糖和核糖分别和足量的金属钠反应,生成氢气的物质的量之比为5∶4
(2)1mol核糖最多能与___________mol乙酸发生酯化反应。检验某糖尿病人的尿液中是否含有葡萄糖的试剂为___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.C
4.D
5.B
6.C
7.D
8.D
9.A
10.D
11.C
12.C
13.C
14.D
15.(1) B A D E CF
(2) ②③ ④ ⑥⑦
(3)
16.(1) 加成反应 C2H4
(2)0.1
(3)乙醇的浓度不再发生变化(或乙醇的物质的量不再发生变化)
(4) 乙烷 D
(5)B
(6)D
(7)80%
17.(1)对
(2)对
(3)错
(4)对
18.(1) 离子键和共价键 ⑨
(2)
(3)①②③⑤⑨
(4) ④⑥⑦⑧ ①②③
(5) 共价键 离子键
19.(1) C2H6 C3H8 CH3CH3 CH3CH2CH3
(2) 4 单键 链 氢原子
(3)CnH2n+2(n≥1)
(4) 甲、乙、丙、丁、戊、己、庚、辛、壬、癸 戊烷 中文数字 十六烷
20.(1) 红 CH3COOHCH3COO-+H+ 强
有无色气体产生 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O 2CH3COOH+Mg→(CH3COO)2Mg+H2↑
(2) 乙醇 98%浓硫酸 冰醋酸 饱和碳酸钠溶液 油状液体生成 香 CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
(3) 醇 酸 酯 水 乙氧基(CH3CH2O-) 羟基(-OH) 氢原子 氢
21.(1)ABEFG
(2) 4 新制氢氧化铜悬浊液
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
