第三章第一节《金属的化学性质》第二课时
文档属性
| 名称 | 第三章第一节《金属的化学性质》第二课时 |

|
|
| 格式 | zip | ||
| 文件大小 | 644.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-05-25 00:00:00 | ||
图片预览




文档简介
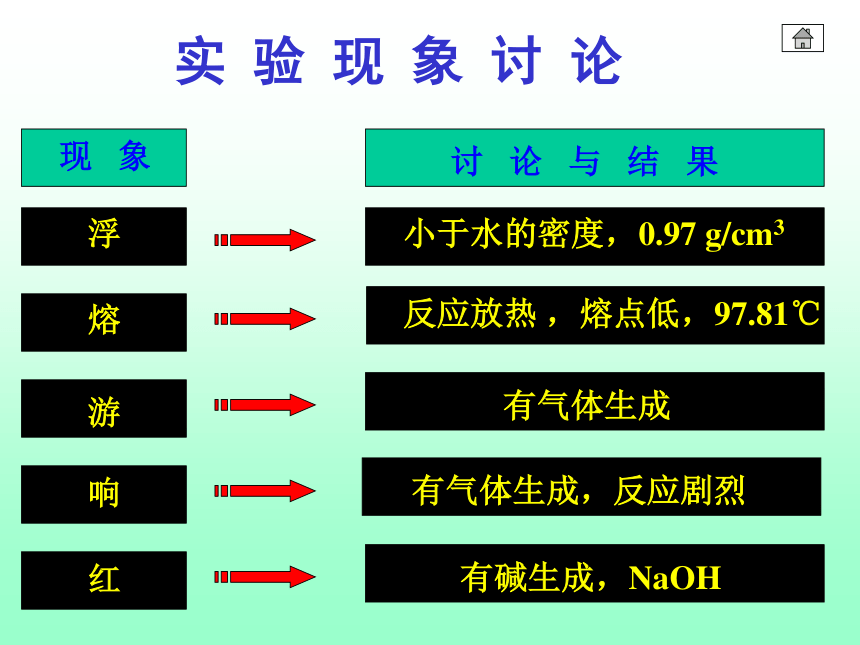
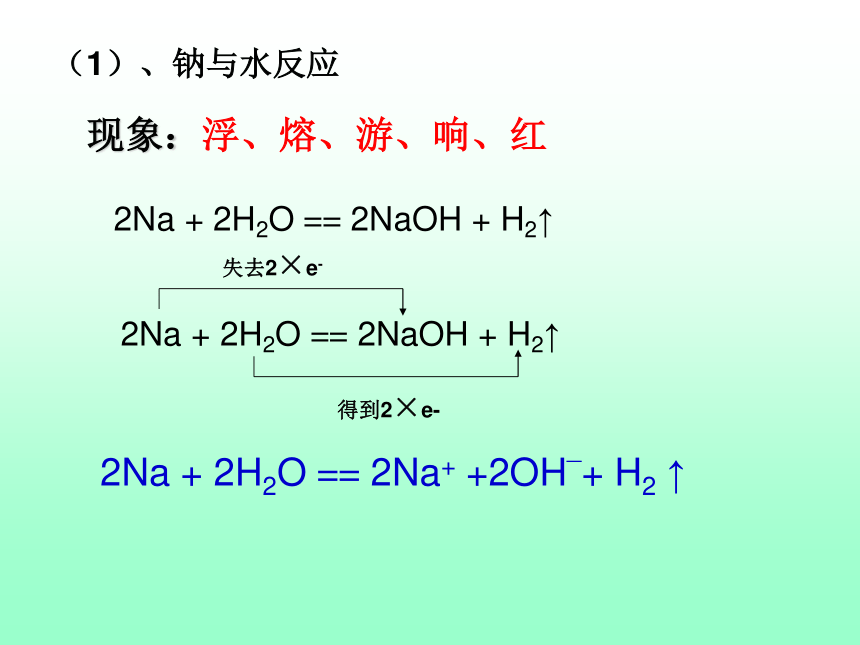
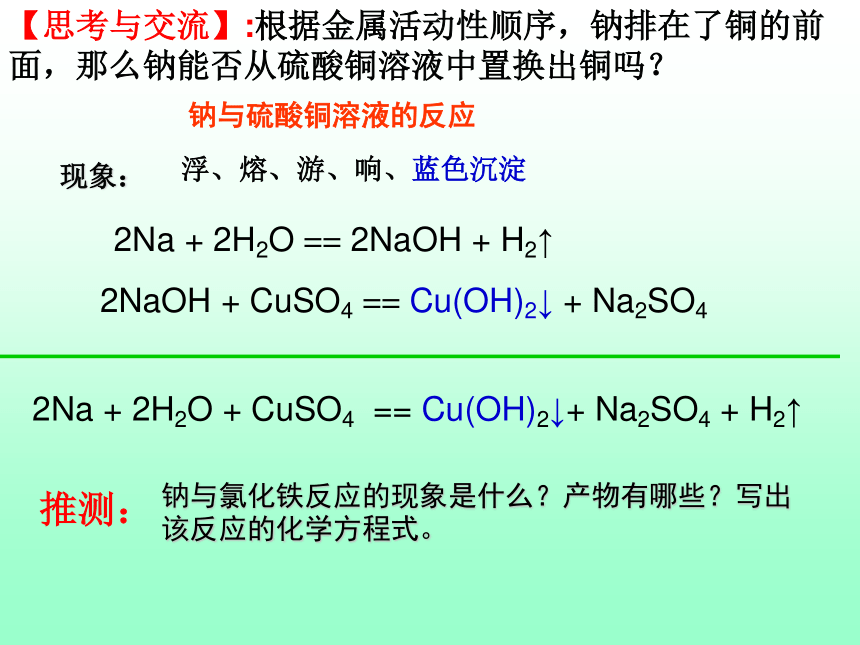
课件18张PPT。第一节 金属的化学性质第二课时二、金属与酸和水的反应实质:金属与酸电离出的H+反应(1)、钠与水反应实验3-3: 将一小块金属钠投入滴有酚酞的水中【思考】:有什么实验现象?2、金属与水反应浮在水面上熔成一个闪亮的小球小球在水面上四处游动发出“嘶嘶”的响声反应后滴有酚酞的水溶液变红浮:熔:游:响:红:(1)、钠与水反应【实验现象归纳】实 验 现 象 讨 论(1)、钠与水反应现象:浮、熔、游、响、红2Na + 2H2O == 2NaOH + H2↑2Na + 2H2O == 2Na+ +2OH_+ H2 ↑2Na + 2H2O == 2NaOH + H2↑失去2×e-得到2×e-浮、熔、游、响、蓝色沉淀2Na + 2H2O == 2NaOH + H2↑2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO42Na + 2H2O + CuSO4 == Cu(OH)2↓+ Na2SO4 + H2↑【思考与交流】:根据金属活动性顺序,钠排在了铜的前面,那么钠能否从硫酸铜溶液中置换出铜吗?规律:钠与盐溶液反应时,钠首先与溶液中的水反应,然后再考虑生成的NaOH盐溶液反应(如果能反应),而不是钠去置换盐溶液里的金属。(2)铁与水蒸气的反应 铁不能与冷、热水反应,但能否与水蒸气反应?方案1:水蒸气的发生装置水蒸气与铁粉反应装置产物收集装置方案2:方案3:现象:加热时试管内铁粉保持红热,在导管口产生肥皂泡,点燃肥皂泡可听到轻微的爆鸣声结论:铁可以和水蒸气反应小结:金属活动顺序表,从左到右,金属与水反应的难易程度是:归纳总结:钠的物理性质颜色:硬度:密度:熔点:导电、导热性:银白色金属小小低热和电的良导体银白色金属钠
(Na) 表面变暗
(生成Na2O) 出现白色固体
(生成NaOH)表面变成溶液 (NaOH潮解)白色粉末状物质
(生成Na2CO3) 白色块状物
(生成Na2CO3·10H2O)O2风化CO2H2OH2O思考:Na长时间暴露空气,最后生成什么物质?①⑤④③②例1、把一块钠投入盛有煤油和水的烧杯中,可以观察的是( )
A.钠浮在烧杯中的液面上
B.钠沉在烧杯的底部
C.煤油会燃烧起来,产生很浓的黑烟
D.钠会在水和煤油的交界面上下浮动,直到反应结束D课堂练习:例题2:把Na投入CuSO4溶液中可能出现的现象是( )
①生成红色的物质 ②有气体生成
③熔成小球 ④生成蓝色沉淀
A.①③④ B. ②③④
C.①④ D. ①③④B课堂练习:
(Na) 表面变暗
(生成Na2O) 出现白色固体
(生成NaOH)表面变成溶液 (NaOH潮解)白色粉末状物质
(生成Na2CO3) 白色块状物
(生成Na2CO3·10H2O)O2风化CO2H2OH2O思考:Na长时间暴露空气,最后生成什么物质?①⑤④③②例1、把一块钠投入盛有煤油和水的烧杯中,可以观察的是( )
A.钠浮在烧杯中的液面上
B.钠沉在烧杯的底部
C.煤油会燃烧起来,产生很浓的黑烟
D.钠会在水和煤油的交界面上下浮动,直到反应结束D课堂练习:例题2:把Na投入CuSO4溶液中可能出现的现象是( )
①生成红色的物质 ②有气体生成
③熔成小球 ④生成蓝色沉淀
A.①③④ B. ②③④
C.①④ D. ①③④B课堂练习:
