人教版化学九年级下册同步课时练习:第8单元 课题3 金属资源的利用和保护 第1课时 铁的冶炼(word版 含答案)
文档属性
| 名称 | 人教版化学九年级下册同步课时练习:第8单元 课题3 金属资源的利用和保护 第1课时 铁的冶炼(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 312.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-21 00:00:00 | ||
图片预览


文档简介
课题3 金属资源的利用和保护
第1课时 铁的冶炼
知识点 1 常见的金属矿物
1.下列金属在自然界中有单质形式存在的是 ( )
A.钾 B.钠
C.镁 D.金
2.写出下列金属矿石的主要成分的化学式。
知识点 2 铁的冶炼
3.下列关于工业炼铁的叙述中错误的是 ( )
A.使用的设备是高炉
B.主要原料为铁矿石、石灰石、焦炭和热空气等
C.主要原理是2Fe2O3+3C4Fe+3CO2↑
D.主要产物为生铁
4.小明的笔记中有一处错误,你认为是下列中的哪一处 ( )
A.a处 B.b处
C.c处 D.d处
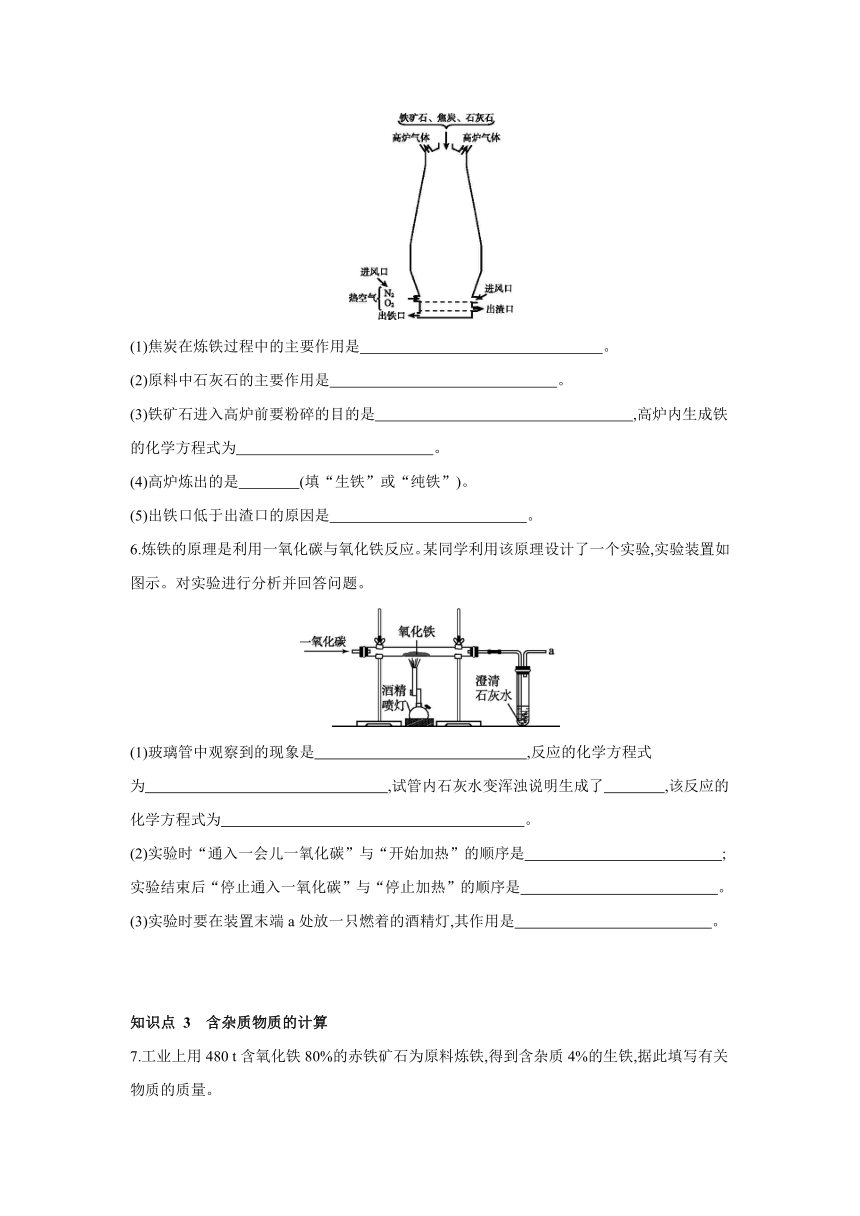
5.煤加工得到的焦炭广泛用于炼铁,如图高炉炼铁的示意图,回答下列问题。
(1)焦炭在炼铁过程中的主要作用是 。
(2)原料中石灰石的主要作用是 。
(3)铁矿石进入高炉前要粉碎的目的是 ,高炉内生成铁的化学方程式为 。
(4)高炉炼出的是 (填“生铁”或“纯铁”)。
(5)出铁口低于出渣口的原因是 。
6.炼铁的原理是利用一氧化碳与氧化铁反应。某同学利用该原理设计了一个实验,实验装置如图示。对实验进行分析并回答问题。
(1)玻璃管中观察到的现象是 ,反应的化学方程式为 ,试管内石灰水变浑浊说明生成了 ,该反应的化学方程式为 。
(2)实验时“通入一会儿一氧化碳”与“开始加热”的顺序是 ;
实验结束后“停止通入一氧化碳”与“停止加热”的顺序是 。
(3)实验时要在装置末端a处放一只燃着的酒精灯,其作用是 。
知识点 3 含杂质物质的计算
7.工业上用480 t含氧化铁80%的赤铁矿石为原料炼铁,得到含杂质4%的生铁,据此填写有关物质的质量。
8.某钢铁厂若日产含铁1.4×104 t的生铁,至少需要含Fe2O3 80%的赤铁矿的质量是多少 (写出计算过程)
9.某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如图所示,请回答问题。
(1)A的化学式: 。
(2)写出反应②的化学方程式: 。
(3)写出反应③的化学方程式: 。
10.《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO3)和煤炭饼装入炼锌罐(如图示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。(已知:锌的熔点为419 ℃,沸点为907 ℃)
(1)反应区中,ZnCO3分解生成ZnO和另一种氧化物,反应的化学方程式为 。C与ZnO发生置换反应得到Zn,该反应的化学方程式为 。
(2)冷凝区中,锌由气态转化为液态,理论上该区应控制的温度范围是 。
(3)“冷定”后方能“毁罐”取锌,从化学变化角度解释其原因: 。
11.[2020·宁波] 如图示是某化学老师设计的一氧化碳还原氧化铁的实验装置。
(1)在B装置中液面下降到安全线之前,不能加热氧化铁,这是因为
。
(2)反应结束后停止加热,继续通一氧化碳,此时B装置的作用是 。
12.太钢自主研发的手撕钢、笔尖钢为山西国民经济重点行业和关键领域转型升级作出了重要贡献。若钢厂用1160 t含四氧化三铁80%的磁铁矿(其余为不含铁的杂质)炼铁,可炼出含杂质4%的生铁多少吨
13.[2021·连云港节选] 在钢铁工业推进碳减排、碳捕集的过程中,化学发挥了重要作用。一种以“氢能炼钢”替代“焦炭炼钢”的工艺流程如图示。
(1)高温下,用H2炼铁时反应的化学方程式为 。
(2)跟“焦炭炼钢”工艺相比,“氢能炼钢”的主要优点有 。
(3)从物质组成的角度,说明向炼钢炉中加入废钢的目的: 。
答案
课题3 金属资源的利用和保护
第1课时 铁的冶炼
1.D 地球上的金属资源除少数很不活泼的如图金、银等有单质形式存在外,其余都以化合物的形式存在。
2.Fe2O3 Fe3O4 Al2O3
3.C 炼铁的主要原理是利用CO与氧化铁的反应。
4.B
5.(1)提供热量,同时产生CO
(2)将矿石中的二氧化硅转变为炉渣
(3)增大接触面积,加快反应速率
3CO+Fe2O32Fe+3CO2
(4)生铁
(5)生铁的密度比炉渣的密度大
6.(1)红棕色固体逐渐变为黑色
Fe2O3+3CO2Fe+3CO2 CO2
CO2+Ca(OH)2CaCO3↓+H2O
(2)先通入一会儿一氧化碳再开始加热
先停止加热再停止通入一氧化碳
(3)除去未反应的一氧化碳,防止其污染空气
7.480 t 384 t 268.8 t 280 t
8.解:设至少需要含Fe2O3 80%的赤铁矿的质量为x。
3CO+Fe2O32Fe+3CO2
160 112
80%×x 1.4×104 t
= x=2.5×104 t
答:至少需要含Fe2O3 80%的赤铁矿的质量为2.5×104 t。
9.(1)CO2 (2)C+CO22CO
(3)3CO+Fe2O32Fe+3CO2
10.(1)ZnCO3ZnO+CO2↑
C+2ZnO2Zn+CO2↑
(2)419~907 ℃
(3)防止生成的锌在较高的温度下又被氧化成氧化锌
11.(1)CO和空气的混合气体受热时,可能会发生爆炸
(2)收集CO,防止污染空气
(1)由于一氧化碳是可燃性气体,所以反应开始时,先通入一氧化碳一段时间后再加热的目的是排尽玻璃管内的空气,以免加热一氧化碳和空气的混合气体引起爆炸。(2)反应结束时先停止加热,继续通一氧化碳至玻璃管冷却,B装置的作用是收集一氧化碳,防止污染空气。
12.解:设可炼出含杂质4%的生铁的质量为x。
Fe3O4+4CO3Fe+4CO2
232 168
1160 t×80% x×(1-4%)
= x=700 t
答:可炼出含杂质4%的生铁的质量为700 t。
13.(1)3H2+Fe2O32Fe+3H2O
(2)不排放二氧化碳、无污染(合理即可)
(3)调节钢中的含碳量
第1课时 铁的冶炼
知识点 1 常见的金属矿物
1.下列金属在自然界中有单质形式存在的是 ( )
A.钾 B.钠
C.镁 D.金
2.写出下列金属矿石的主要成分的化学式。
知识点 2 铁的冶炼
3.下列关于工业炼铁的叙述中错误的是 ( )
A.使用的设备是高炉
B.主要原料为铁矿石、石灰石、焦炭和热空气等
C.主要原理是2Fe2O3+3C4Fe+3CO2↑
D.主要产物为生铁
4.小明的笔记中有一处错误,你认为是下列中的哪一处 ( )
A.a处 B.b处
C.c处 D.d处
5.煤加工得到的焦炭广泛用于炼铁,如图高炉炼铁的示意图,回答下列问题。
(1)焦炭在炼铁过程中的主要作用是 。
(2)原料中石灰石的主要作用是 。
(3)铁矿石进入高炉前要粉碎的目的是 ,高炉内生成铁的化学方程式为 。
(4)高炉炼出的是 (填“生铁”或“纯铁”)。
(5)出铁口低于出渣口的原因是 。
6.炼铁的原理是利用一氧化碳与氧化铁反应。某同学利用该原理设计了一个实验,实验装置如图示。对实验进行分析并回答问题。
(1)玻璃管中观察到的现象是 ,反应的化学方程式为 ,试管内石灰水变浑浊说明生成了 ,该反应的化学方程式为 。
(2)实验时“通入一会儿一氧化碳”与“开始加热”的顺序是 ;
实验结束后“停止通入一氧化碳”与“停止加热”的顺序是 。
(3)实验时要在装置末端a处放一只燃着的酒精灯,其作用是 。
知识点 3 含杂质物质的计算
7.工业上用480 t含氧化铁80%的赤铁矿石为原料炼铁,得到含杂质4%的生铁,据此填写有关物质的质量。
8.某钢铁厂若日产含铁1.4×104 t的生铁,至少需要含Fe2O3 80%的赤铁矿的质量是多少 (写出计算过程)
9.某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如图所示,请回答问题。
(1)A的化学式: 。
(2)写出反应②的化学方程式: 。
(3)写出反应③的化学方程式: 。
10.《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO3)和煤炭饼装入炼锌罐(如图示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。(已知:锌的熔点为419 ℃,沸点为907 ℃)
(1)反应区中,ZnCO3分解生成ZnO和另一种氧化物,反应的化学方程式为 。C与ZnO发生置换反应得到Zn,该反应的化学方程式为 。
(2)冷凝区中,锌由气态转化为液态,理论上该区应控制的温度范围是 。
(3)“冷定”后方能“毁罐”取锌,从化学变化角度解释其原因: 。
11.[2020·宁波] 如图示是某化学老师设计的一氧化碳还原氧化铁的实验装置。
(1)在B装置中液面下降到安全线之前,不能加热氧化铁,这是因为
。
(2)反应结束后停止加热,继续通一氧化碳,此时B装置的作用是 。
12.太钢自主研发的手撕钢、笔尖钢为山西国民经济重点行业和关键领域转型升级作出了重要贡献。若钢厂用1160 t含四氧化三铁80%的磁铁矿(其余为不含铁的杂质)炼铁,可炼出含杂质4%的生铁多少吨
13.[2021·连云港节选] 在钢铁工业推进碳减排、碳捕集的过程中,化学发挥了重要作用。一种以“氢能炼钢”替代“焦炭炼钢”的工艺流程如图示。
(1)高温下,用H2炼铁时反应的化学方程式为 。
(2)跟“焦炭炼钢”工艺相比,“氢能炼钢”的主要优点有 。
(3)从物质组成的角度,说明向炼钢炉中加入废钢的目的: 。
答案
课题3 金属资源的利用和保护
第1课时 铁的冶炼
1.D 地球上的金属资源除少数很不活泼的如图金、银等有单质形式存在外,其余都以化合物的形式存在。
2.Fe2O3 Fe3O4 Al2O3
3.C 炼铁的主要原理是利用CO与氧化铁的反应。
4.B
5.(1)提供热量,同时产生CO
(2)将矿石中的二氧化硅转变为炉渣
(3)增大接触面积,加快反应速率
3CO+Fe2O32Fe+3CO2
(4)生铁
(5)生铁的密度比炉渣的密度大
6.(1)红棕色固体逐渐变为黑色
Fe2O3+3CO2Fe+3CO2 CO2
CO2+Ca(OH)2CaCO3↓+H2O
(2)先通入一会儿一氧化碳再开始加热
先停止加热再停止通入一氧化碳
(3)除去未反应的一氧化碳,防止其污染空气
7.480 t 384 t 268.8 t 280 t
8.解:设至少需要含Fe2O3 80%的赤铁矿的质量为x。
3CO+Fe2O32Fe+3CO2
160 112
80%×x 1.4×104 t
= x=2.5×104 t
答:至少需要含Fe2O3 80%的赤铁矿的质量为2.5×104 t。
9.(1)CO2 (2)C+CO22CO
(3)3CO+Fe2O32Fe+3CO2
10.(1)ZnCO3ZnO+CO2↑
C+2ZnO2Zn+CO2↑
(2)419~907 ℃
(3)防止生成的锌在较高的温度下又被氧化成氧化锌
11.(1)CO和空气的混合气体受热时,可能会发生爆炸
(2)收集CO,防止污染空气
(1)由于一氧化碳是可燃性气体,所以反应开始时,先通入一氧化碳一段时间后再加热的目的是排尽玻璃管内的空气,以免加热一氧化碳和空气的混合气体引起爆炸。(2)反应结束时先停止加热,继续通一氧化碳至玻璃管冷却,B装置的作用是收集一氧化碳,防止污染空气。
12.解:设可炼出含杂质4%的生铁的质量为x。
Fe3O4+4CO3Fe+4CO2
232 168
1160 t×80% x×(1-4%)
= x=700 t
答:可炼出含杂质4%的生铁的质量为700 t。
13.(1)3H2+Fe2O32Fe+3H2O
(2)不排放二氧化碳、无污染(合理即可)
(3)调节钢中的含碳量
同课章节目录
