人教版化学九年级下册同步课时练习:第9单元 课题3 溶液的浓度 第1课时 溶质的质量分数(word版 含答案)
文档属性
| 名称 | 人教版化学九年级下册同步课时练习:第9单元 课题3 溶液的浓度 第1课时 溶质的质量分数(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 172.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-21 00:00:00 | ||
图片预览



文档简介
课题3 溶液的浓度
第1课时 溶质的质量分数
知识点 1 溶质的质量分数
1.农业生产上常用溶质质量分数为16%的氯化钠溶液来选种,对该溶液的认识正确的是 ( )
A.溶液中含16 g氯化钠
B.溶液质量为100 g
C.每100 g溶液中含16 g氯化钠
D.每100 g水中含16 g氯化钠
2.常温下,将15 g氯化钠完全溶解在60 g水中,所得溶液的溶质质量分数是 ( )
A.15% B.20%
C.25% D.33.3%
3.在实验室中,配制溶质质量分数为10%的氯化钠溶液45 g,需要氯化钠固体的质量是 g。将45 g 10%的氯化钠溶液配制成溶质质量分数为0.9%的氯化钠溶液,得到氯化钠溶液的质量是 g。
4.[2020·德州] 用4 g酚酞与酒精配制溶质质量分数为4%的酚酞溶液,需要酒精的质量是
g,这些酒精的体积为 mL。(酒精的密度为0.8 g/mL)
5.如图氯化钠的溶解度曲线。20 ℃时,在100 g水中加入40 g氯化钠,充分搅拌后,有
g固体未溶解,所得溶液的溶质质量分数的计算式为 ,所得溶液的溶质质量分数 (填“大于”或“小于”)36%。
知识点 2 溶液稀释的计算
6.溶液在稀释前后保持不变的是 ( )
A.溶质的质量分数
B.溶质的质量
C.溶液的质量
D.溶剂的质量
7.将50 g溶质质量分数为20%的氯化钾溶液稀释到200 g,稀释后所得溶液中溶质的质量分数是( )
A.1% B.5%
C.10% D.20%
8.将100 g溶质质量分数为98%的浓硫酸注入900 g水中,所得稀硫酸中溶质的质量分数为 ( )
A.9.8% B.10.0%
C.10.9% D.11.1%
9.若配制500 g溶质质量分数为3%的过氧化氢溶液,需溶质质量分数为30%的过氧化氢溶液的质量是 。
10.化学实验室现有质量分数为98%的浓硫酸,但在实验室中常需要用较稀的硫酸。请回答下列问题。
(1)上述浓硫酸中溶剂的质量分数是 。
(2)要把50 g上述浓硫酸稀释成质量分数为10%的硫酸,需要水的质量是多少 (写出计算过程)
11.某温度时,向一定量的硝酸钾不饱和溶液中加入硝酸钾晶体,同时不断搅拌。下列表示所得溶液中硝酸钾的质量分数a%与加入硝酸钾的质量m关系的图像中,正确的是 ( )
12.如图示一杯刚配制的饱和KNO3溶液,要使该溶液中溶质的质量分数增大,下列操作正确的是 ( )
A.降温 B.升温
C.加KNO3 D.搅拌
13.下表是氯化铵在不同温度时的溶解度,下列说法正确的是 ( )
温度/℃ 0 20 40 60 80
溶解度/g 29.4 37.2 45.8 55.2 65.6
A.20 ℃时,氯化铵的饱和溶液中溶质的质量分数为37.2%
B.将60 ℃时氯化铵的饱和溶液降温到20 ℃时,溶质的质量分数不变
C.40 ℃时,将50 g氯化铵加入100 g水中充分搅拌后,所得溶液中溶质的质量分数为×100%
D.60 ℃时,将50 g氯化铵加入100 g水中充分搅拌后,所得溶液中溶质的质量分数为×100%
14.预防“新冠肺炎”有效的方法之一是用消毒液对空气消毒。某校决定放学后用二氧化氯(ClO2)消毒液对全校教室进行全面消毒。所用二氧化氯消毒液的标签如图下表所示。
二氧化氯消毒液1000 mL
溶质的质量分数 80%
密度 1.2 g/cm3
相对分子质量 67.5
强腐蚀性,阴冷、密封贮藏
(1)该1000 mL二氧化氯消毒液含溶质二氧化氯 g。
(2)欲配制30 kg溶质质量分数为20%的二氧化氯消毒液用来消毒,需要 kg水。
15.[2020·自贡] 甲、乙两种物质的溶解度曲线如图示。
(1)A点的含义是 。
(2)t2 ℃时,将甲、乙两种固体各8 g分别投入25 g水中,充分搅拌。
① (填“甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入 g溶质可使其达到饱和。
②乙所得溶液中溶质的质量分数为 %。
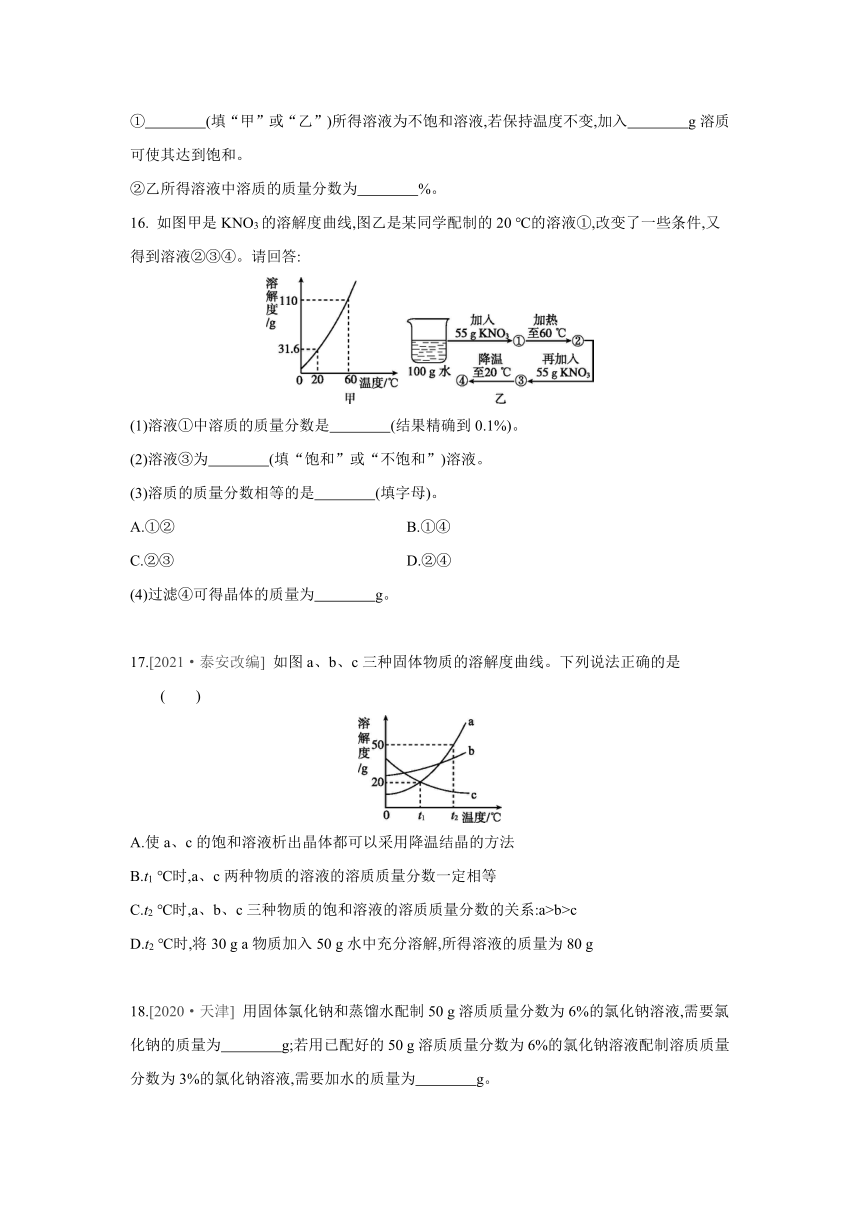
16. 如图甲是KNO3的溶解度曲线,图乙是某同学配制的20 ℃的溶液①,改变了一些条件,又得到溶液②③④。请回答:
(1)溶液①中溶质的质量分数是 (结果精确到0.1%)。
(2)溶液③为 (填“饱和”或“不饱和”)溶液。
(3)溶质的质量分数相等的是 (填字母)。
A.①② B.①④
C.②③ D.②④
(4)过滤④可得晶体的质量为 g。
17.[2021·泰安改编] 如图a、b、c三种固体物质的溶解度曲线。下列说法正确的是 ( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液的溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液的溶质质量分数的关系:a>b>c
D.t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液的质量为80 g
18.[2020·天津] 用固体氯化钠和蒸馏水配制50 g溶质质量分数为6%的氯化钠溶液,需要氯化钠的质量为 g;若用已配好的50 g溶质质量分数为6%的氯化钠溶液配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为 g。
答案
课题3 溶液的浓度
第1课时 溶质的质量分数
1.C 2.B
3.4.5 500
4.96 120
溶液的质量为4 g÷4%=100 g,溶剂酒精的质量为100 g-4 g=96 g,酒精的体积V===120 mL。
5.4 ×100% 小于
6.B
7.B 溶液稀释前后溶质质量不变,则稀释后所得溶液中溶质的质量分数为×100%=5%。
8.A 设所得稀硫酸中溶质的质量分数为x,根据溶液稀释前后,溶质的质量不变,则100 g×98%=(100 g+900 g)×x,x=9.8%。
9.50 g
设需溶质质量分数为30%的过氧化氢溶液的质量为x,则500 g×3%=x×30%,x=50 g。
10.(1)2%
(2)解:设稀释后溶液的质量为 x。
50 g×98%=x×10%
x=490 g
需要水的质量为490 g-50 g=440 g。
答:需要水的质量是440 g。
11.D 不饱和硝酸钾溶液的溶质质量分数不为零;向其中加入硝酸钾晶体后,溶质质量分数会增大,当达到该温度的饱和状态时,溶质质量分数会保持不变。
12.B 搅拌只能加快KNO3的溶解速率,不能增大KNO3的溶解度。升高温度,KNO3的溶解度增大,未溶解的KNO3继续溶解,该溶液中溶质的质量分数增大。
13.D 20 ℃时,氯化铵的溶解度为37.2 g,其饱和溶液中溶质的质量分数为×100%<37.2%;氯化铵的溶解度随温度的升高而增大,其饱和溶液降低温度,有晶体析出,溶质的质量分数减小;40 ℃时,氯化铵的溶解度为45.8 g,将50 g氯化铵加入100 g水中充分搅拌后,有4.2 g未溶解,所得溶液中溶质的质量分数为×100%。
14.(1)960 (2)22.5
(1)1000 mL(1 mL=1 cm3)消毒液中含溶质的质量为1000 cm3×1.2 g/cm3×80%=960 g。(2)设配制30 kg溶质质量分数为20%的二氧化氯消毒液需要80%的消毒液的质量为x,则30 kg×20%=x×80%,x=7.5 kg,则需要水的质量为30 kg-7.5 kg=22.5 kg。
15.(1)t1 ℃时,甲、乙两种物质的溶解度相等
(2)①甲 4.5 ②20
(2)①t2 ℃时,乙物质的溶解度是25 g,即t2 ℃时,100 g水中最多能溶解25 g乙,则25 g 水中最多能溶解6.25 g乙,所以t2 ℃时,将8 g乙投入25 g水中,所得溶液为饱和溶液;t2 ℃时,甲物质的溶解度是50 g,即t2 ℃时,100 g 水中最多能溶解50 g甲,则25 g水中最多能溶解 12.5 g甲,所以t2 ℃时,将8 g甲投入25 g 水中,所得溶液为不饱和溶液,为使其达到饱和,要加入溶质的质量为12.5 g-8 g=4.5 g。②t2 ℃时,将8 g乙投入25 g水中,所得溶液为饱和溶液,所以溶液中溶质的质量分数为×100%=20%。
16.(1)24.0% (2)饱和
(3)B (4)78.4
20 ℃时KNO3的溶解度是31.6 g,故在100 g水中加入55 g KNO3,固体不能完全溶解,所得溶液①中溶质的质量分数为×100%=24.0%;加热至60 ℃时,KNO3的溶解度是110 g,故②是硝酸钾的不饱和溶液;再加入55 g KNO3后得到的溶液③恰好是60 ℃时KNO3的饱和溶液;再降温至20 ℃时会析出晶体110 g-31.6 g=78.4 g,此时得到的溶液④依然是 20 ℃时KNO3的饱和溶液,与溶液①中溶质的质量分数相等。
17.C a的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,采用降温结晶的方法,a的饱和溶液能够析出晶体,c的饱和溶液不能析出晶体;t1 ℃时,a、c两种物质的溶解度相等,该温度下,a、c两种物质的饱和溶液的溶质质量分数相等,而溶液(没有指明是否饱和)的溶质质量分数不一定相等;t2 ℃时,a、b、c三种物质的溶解度大小关系是a>b>c,所以饱和溶液中溶质质量分数的大小关系是a>b>c;t2 ℃时,a的溶解度是50 g,将30 g a物质加入50 g水中,充分溶解,只能溶解25 g,所得溶液质量=25 g+50 g=75 g。
18.3 50
配制50 g溶质质量分数为6%的氯化钠溶液,需要氯化钠固体的质量为50 g×6%=3 g;将50 g 溶质质量分数为6%的氯化钠溶液稀释成3%的溶液时,依据溶质质量不变,所得稀溶液的质量为(50 g×6%)÷3%=100 g,需要水的质量为100 g-50 g=50 g。
第1课时 溶质的质量分数
知识点 1 溶质的质量分数
1.农业生产上常用溶质质量分数为16%的氯化钠溶液来选种,对该溶液的认识正确的是 ( )
A.溶液中含16 g氯化钠
B.溶液质量为100 g
C.每100 g溶液中含16 g氯化钠
D.每100 g水中含16 g氯化钠
2.常温下,将15 g氯化钠完全溶解在60 g水中,所得溶液的溶质质量分数是 ( )
A.15% B.20%
C.25% D.33.3%
3.在实验室中,配制溶质质量分数为10%的氯化钠溶液45 g,需要氯化钠固体的质量是 g。将45 g 10%的氯化钠溶液配制成溶质质量分数为0.9%的氯化钠溶液,得到氯化钠溶液的质量是 g。
4.[2020·德州] 用4 g酚酞与酒精配制溶质质量分数为4%的酚酞溶液,需要酒精的质量是
g,这些酒精的体积为 mL。(酒精的密度为0.8 g/mL)
5.如图氯化钠的溶解度曲线。20 ℃时,在100 g水中加入40 g氯化钠,充分搅拌后,有
g固体未溶解,所得溶液的溶质质量分数的计算式为 ,所得溶液的溶质质量分数 (填“大于”或“小于”)36%。
知识点 2 溶液稀释的计算
6.溶液在稀释前后保持不变的是 ( )
A.溶质的质量分数
B.溶质的质量
C.溶液的质量
D.溶剂的质量
7.将50 g溶质质量分数为20%的氯化钾溶液稀释到200 g,稀释后所得溶液中溶质的质量分数是( )
A.1% B.5%
C.10% D.20%
8.将100 g溶质质量分数为98%的浓硫酸注入900 g水中,所得稀硫酸中溶质的质量分数为 ( )
A.9.8% B.10.0%
C.10.9% D.11.1%
9.若配制500 g溶质质量分数为3%的过氧化氢溶液,需溶质质量分数为30%的过氧化氢溶液的质量是 。
10.化学实验室现有质量分数为98%的浓硫酸,但在实验室中常需要用较稀的硫酸。请回答下列问题。
(1)上述浓硫酸中溶剂的质量分数是 。
(2)要把50 g上述浓硫酸稀释成质量分数为10%的硫酸,需要水的质量是多少 (写出计算过程)
11.某温度时,向一定量的硝酸钾不饱和溶液中加入硝酸钾晶体,同时不断搅拌。下列表示所得溶液中硝酸钾的质量分数a%与加入硝酸钾的质量m关系的图像中,正确的是 ( )
12.如图示一杯刚配制的饱和KNO3溶液,要使该溶液中溶质的质量分数增大,下列操作正确的是 ( )
A.降温 B.升温
C.加KNO3 D.搅拌
13.下表是氯化铵在不同温度时的溶解度,下列说法正确的是 ( )
温度/℃ 0 20 40 60 80
溶解度/g 29.4 37.2 45.8 55.2 65.6
A.20 ℃时,氯化铵的饱和溶液中溶质的质量分数为37.2%
B.将60 ℃时氯化铵的饱和溶液降温到20 ℃时,溶质的质量分数不变
C.40 ℃时,将50 g氯化铵加入100 g水中充分搅拌后,所得溶液中溶质的质量分数为×100%
D.60 ℃时,将50 g氯化铵加入100 g水中充分搅拌后,所得溶液中溶质的质量分数为×100%
14.预防“新冠肺炎”有效的方法之一是用消毒液对空气消毒。某校决定放学后用二氧化氯(ClO2)消毒液对全校教室进行全面消毒。所用二氧化氯消毒液的标签如图下表所示。
二氧化氯消毒液1000 mL
溶质的质量分数 80%
密度 1.2 g/cm3
相对分子质量 67.5
强腐蚀性,阴冷、密封贮藏
(1)该1000 mL二氧化氯消毒液含溶质二氧化氯 g。
(2)欲配制30 kg溶质质量分数为20%的二氧化氯消毒液用来消毒,需要 kg水。
15.[2020·自贡] 甲、乙两种物质的溶解度曲线如图示。
(1)A点的含义是 。
(2)t2 ℃时,将甲、乙两种固体各8 g分别投入25 g水中,充分搅拌。
① (填“甲”或“乙”)所得溶液为不饱和溶液,若保持温度不变,加入 g溶质可使其达到饱和。
②乙所得溶液中溶质的质量分数为 %。
16. 如图甲是KNO3的溶解度曲线,图乙是某同学配制的20 ℃的溶液①,改变了一些条件,又得到溶液②③④。请回答:
(1)溶液①中溶质的质量分数是 (结果精确到0.1%)。
(2)溶液③为 (填“饱和”或“不饱和”)溶液。
(3)溶质的质量分数相等的是 (填字母)。
A.①② B.①④
C.②③ D.②④
(4)过滤④可得晶体的质量为 g。
17.[2021·泰安改编] 如图a、b、c三种固体物质的溶解度曲线。下列说法正确的是 ( )
A.使a、c的饱和溶液析出晶体都可以采用降温结晶的方法
B.t1 ℃时,a、c两种物质的溶液的溶质质量分数一定相等
C.t2 ℃时,a、b、c三种物质的饱和溶液的溶质质量分数的关系:a>b>c
D.t2 ℃时,将30 g a物质加入50 g水中充分溶解,所得溶液的质量为80 g
18.[2020·天津] 用固体氯化钠和蒸馏水配制50 g溶质质量分数为6%的氯化钠溶液,需要氯化钠的质量为 g;若用已配好的50 g溶质质量分数为6%的氯化钠溶液配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为 g。
答案
课题3 溶液的浓度
第1课时 溶质的质量分数
1.C 2.B
3.4.5 500
4.96 120
溶液的质量为4 g÷4%=100 g,溶剂酒精的质量为100 g-4 g=96 g,酒精的体积V===120 mL。
5.4 ×100% 小于
6.B
7.B 溶液稀释前后溶质质量不变,则稀释后所得溶液中溶质的质量分数为×100%=5%。
8.A 设所得稀硫酸中溶质的质量分数为x,根据溶液稀释前后,溶质的质量不变,则100 g×98%=(100 g+900 g)×x,x=9.8%。
9.50 g
设需溶质质量分数为30%的过氧化氢溶液的质量为x,则500 g×3%=x×30%,x=50 g。
10.(1)2%
(2)解:设稀释后溶液的质量为 x。
50 g×98%=x×10%
x=490 g
需要水的质量为490 g-50 g=440 g。
答:需要水的质量是440 g。
11.D 不饱和硝酸钾溶液的溶质质量分数不为零;向其中加入硝酸钾晶体后,溶质质量分数会增大,当达到该温度的饱和状态时,溶质质量分数会保持不变。
12.B 搅拌只能加快KNO3的溶解速率,不能增大KNO3的溶解度。升高温度,KNO3的溶解度增大,未溶解的KNO3继续溶解,该溶液中溶质的质量分数增大。
13.D 20 ℃时,氯化铵的溶解度为37.2 g,其饱和溶液中溶质的质量分数为×100%<37.2%;氯化铵的溶解度随温度的升高而增大,其饱和溶液降低温度,有晶体析出,溶质的质量分数减小;40 ℃时,氯化铵的溶解度为45.8 g,将50 g氯化铵加入100 g水中充分搅拌后,有4.2 g未溶解,所得溶液中溶质的质量分数为×100%。
14.(1)960 (2)22.5
(1)1000 mL(1 mL=1 cm3)消毒液中含溶质的质量为1000 cm3×1.2 g/cm3×80%=960 g。(2)设配制30 kg溶质质量分数为20%的二氧化氯消毒液需要80%的消毒液的质量为x,则30 kg×20%=x×80%,x=7.5 kg,则需要水的质量为30 kg-7.5 kg=22.5 kg。
15.(1)t1 ℃时,甲、乙两种物质的溶解度相等
(2)①甲 4.5 ②20
(2)①t2 ℃时,乙物质的溶解度是25 g,即t2 ℃时,100 g水中最多能溶解25 g乙,则25 g 水中最多能溶解6.25 g乙,所以t2 ℃时,将8 g乙投入25 g水中,所得溶液为饱和溶液;t2 ℃时,甲物质的溶解度是50 g,即t2 ℃时,100 g 水中最多能溶解50 g甲,则25 g水中最多能溶解 12.5 g甲,所以t2 ℃时,将8 g甲投入25 g 水中,所得溶液为不饱和溶液,为使其达到饱和,要加入溶质的质量为12.5 g-8 g=4.5 g。②t2 ℃时,将8 g乙投入25 g水中,所得溶液为饱和溶液,所以溶液中溶质的质量分数为×100%=20%。
16.(1)24.0% (2)饱和
(3)B (4)78.4
20 ℃时KNO3的溶解度是31.6 g,故在100 g水中加入55 g KNO3,固体不能完全溶解,所得溶液①中溶质的质量分数为×100%=24.0%;加热至60 ℃时,KNO3的溶解度是110 g,故②是硝酸钾的不饱和溶液;再加入55 g KNO3后得到的溶液③恰好是60 ℃时KNO3的饱和溶液;再降温至20 ℃时会析出晶体110 g-31.6 g=78.4 g,此时得到的溶液④依然是 20 ℃时KNO3的饱和溶液,与溶液①中溶质的质量分数相等。
17.C a的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,采用降温结晶的方法,a的饱和溶液能够析出晶体,c的饱和溶液不能析出晶体;t1 ℃时,a、c两种物质的溶解度相等,该温度下,a、c两种物质的饱和溶液的溶质质量分数相等,而溶液(没有指明是否饱和)的溶质质量分数不一定相等;t2 ℃时,a、b、c三种物质的溶解度大小关系是a>b>c,所以饱和溶液中溶质质量分数的大小关系是a>b>c;t2 ℃时,a的溶解度是50 g,将30 g a物质加入50 g水中,充分溶解,只能溶解25 g,所得溶液质量=25 g+50 g=75 g。
18.3 50
配制50 g溶质质量分数为6%的氯化钠溶液,需要氯化钠固体的质量为50 g×6%=3 g;将50 g 溶质质量分数为6%的氯化钠溶液稀释成3%的溶液时,依据溶质质量不变,所得稀溶液的质量为(50 g×6%)÷3%=100 g,需要水的质量为100 g-50 g=50 g。
同课章节目录
