人教版化学九年级下册同步课时练习:第9单元 实验活动5 一定溶质质量分数的氯化钠溶液的配制(word版 含答案)
文档属性
| 名称 | 人教版化学九年级下册同步课时练习:第9单元 实验活动5 一定溶质质量分数的氯化钠溶液的配制(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 273.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-21 00:00:00 | ||
图片预览


文档简介
实验活动5 一定溶质质量分数的氯化钠溶液的配制
类型1 教材实验原型练
1.小孟在实验室欲配制一定溶质质量分数的氯化钠溶液,可供选择的仪器如图图SY5-1所示。
图SY5-1
(1)B仪器的名称是 。
(2)根据实验操作选择相应的仪器(填字母)。
①称量氯化钠 ;②量取水 、 ;③溶解氯化钠 、
。
2.某同学用固体氯化钾配制质量分数为8%的氯化钾溶液。请按操作步骤回答下列问题。
(1) :配制100 g质量分数为8%的氯化钾溶液,所需氯化钾的质量为 g,需要水的质量为 g。
(2) :用托盘天平称量所需的氯化钾,托盘天平调节平衡后,接下来的操作应该是 (填字母)。
A.先在左盘纸片上加氯化钾,后在右盘纸片上加砝码
B.先在右盘纸片上加砝码,后在左盘纸片上加氯化钾
(3)量取:量取水读数时,视线要与量筒内液体的 保持水平,量好后倒入盛有氯化钾的烧杯中。
(4)溶解:溶解时需用 搅拌,以 。
(5)装瓶:将配制好的溶液装入 (填“广口瓶”或“细口瓶”)中,盖上瓶塞,贴好标签,请填写标签。
图SY5-2
3. 溶液具有广泛的用途。在实际生产、生活中,我们常常要把较浓的溶液加水稀释成所需的较稀的溶液,现用溶质质量分数为12%的氯化钠溶液(密度约为1.09 g/cm3)配制20 g溶质质量分数为6%的氯化钠溶液,其操作步骤如图下:
(1)计算:依据溶液稀释前后, 的质量不变,计算出需要质量分数为12%的氯化钠溶液 (计算结果精确到0.1)mL,需要水 mL(水的密度为1 g/cm3)。
(2)量取:应选用规格为 (填“10 mL”“20 mL”或“50 mL”)的量筒。
(3) : 配制该溶液的过程中用到的仪器除了上述步骤涉及的量筒、胶头滴管外,还需要 。
(4)把配制好的上述溶液装入 (填“广口瓶”或“细口瓶”)中,盖好瓶塞并贴上标签。
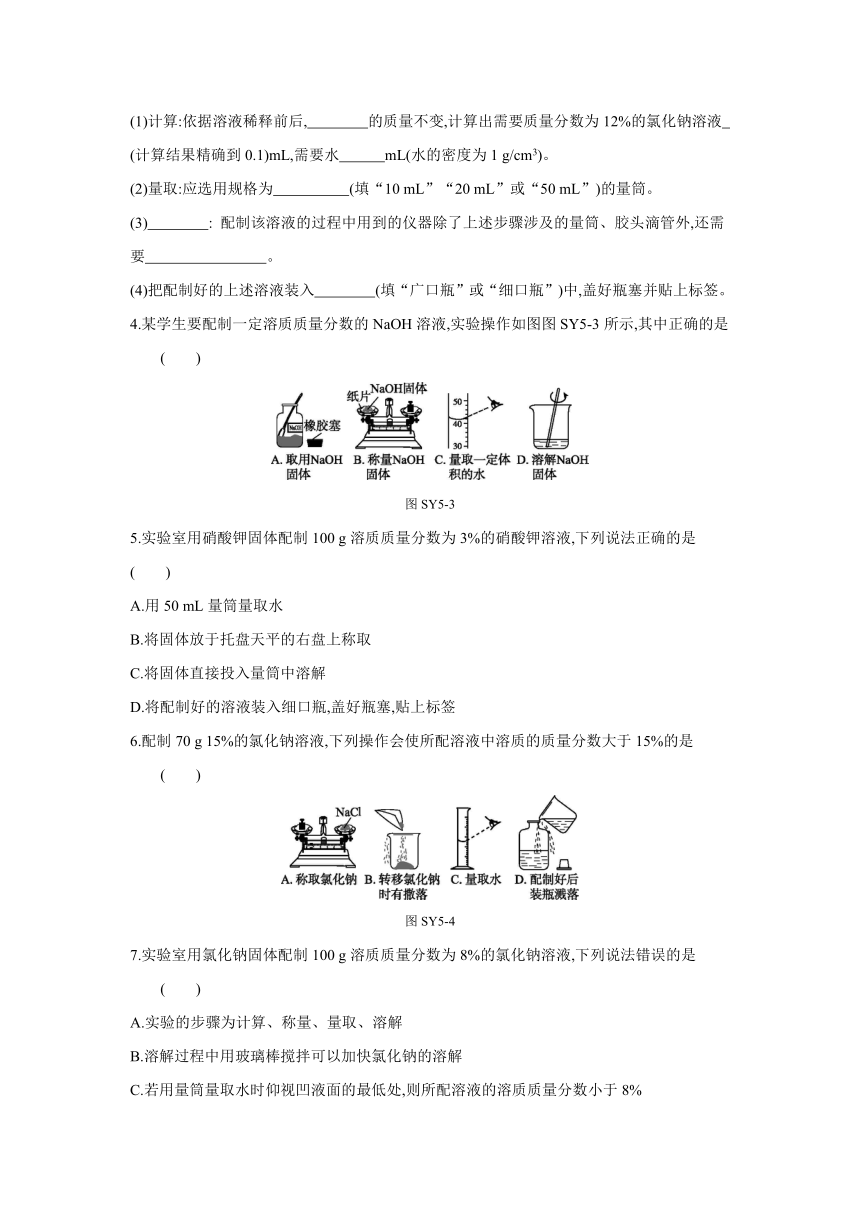
4.某学生要配制一定溶质质量分数的NaOH溶液,实验操作如图图SY5-3所示,其中正确的是 ( )
图SY5-3
5.实验室用硝酸钾固体配制100 g溶质质量分数为3%的硝酸钾溶液,下列说法正确的是( )
A.用50 mL量筒量取水
B.将固体放于托盘天平的右盘上称取
C.将固体直接投入量筒中溶解
D.将配制好的溶液装入细口瓶,盖好瓶塞,贴上标签
6.配制70 g 15%的氯化钠溶液,下列操作会使所配溶液中溶质的质量分数大于15%的是 ( )
图SY5-4
7.实验室用氯化钠固体配制100 g溶质质量分数为8%的氯化钠溶液,下列说法错误的是 ( )
A.实验的步骤为计算、称量、量取、溶解
B.溶解过程中用玻璃棒搅拌可以加快氯化钠的溶解
C.若用量筒量取水时仰视凹液面的最低处,则所配溶液的溶质质量分数小于8%
D.将配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶,并贴上标签
类型2 教材实验拓展练
8.配制一定溶质质量分数的氯化钠溶液是初中化学的基础实验。下列操作与分析均正确的是 ( )
选项 实验操作 分析
A 称量氯化钠时,将取出的过量的氯化钠放回原瓶 目的是节约药品
B 溶解时用玻璃棒搅拌 目的是增大氯化钠的溶解度
C 用量筒量取液体,倾倒至接近刻度时,改用胶头滴管滴加 防止倾倒时过量
D 称量时氯化钠放在右盘 一定会导致配制的溶液的溶质质量分数偏小
9.用溶质质量分数为98%的浓硫酸配制490 g溶质质量分数为20%的稀硫酸。下列说法不正确的是 ( )
A.实验中用到的玻璃仪器:量筒、胶头滴管、烧杯、玻璃棒
B.配制该稀硫酸需要加水390 mL
C.配制时需要溶质质量分数为98%的浓硫酸100 g
D.配制的步骤是计算、称量、量取、溶解、装瓶贴标签
10.[2020·岳阳改编] 某同学需要配制50 g质量分数为15%的氯化钠溶液,步骤如图图SY5-5所示。下列分析正确的是 ( )
图SY5-5
A.配制过程中出现了两处操作错误
B.实验操作步骤为:计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后装瓶时有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体的质量为7.0 g
11.配制一定溶质质量分数的氯化钠溶液的过程如图图SY5-6所示。
图SY5-6
(1)写出图中标号a仪器的名称: 。
(2)配制50 g质量分数为15%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠 g,水 g。
(3)用托盘天平称量所需氯化钠时,氯化钠应放在 (填“左”或“右”)盘,加入氯化钠后,发现托盘天平的指针向右偏转,接下来的操作是 。
(4)溶解过程中玻璃棒的作用是 。
(5)对配制的溶液进行检测,发现溶质质量分数偏小,其原因可能有 (填字母)。
A.称量时,药品与砝码放反了,且使用了游码
B.量取水时,仰视读数
C.装瓶时,有少量溶液洒出
(6)把50 g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需加水的质量是 g。
12.在对抗席卷全球的“新冠肺炎”疫情中,常用过氧化氢溶液作消毒剂。小欣同学准备用以下仪器,完成“用溶质质量分数为30%的过氧化氢溶液配制150 g溶质质量分数为3%的过氧化氢溶液”这一实验。
图SY5-7
(1)仪器A的名称为 。
(2)完成此实验不会用到上述仪器中的 (填字母),实验过程中需要加入 g水。
(3)用量筒量取溶质质量分数为30%的过氧化氢溶液时,若俯视读数,则所配制溶液的溶质质量分数 (填“大于”“小于”或“等于”)3%。
(4)过氧化氢溶液用于伤口消毒时,在生物酶的催化作用下会产生大量气泡,发生反应的化学方程式为 。
答案
实验活动5 一定溶质质量分数的氯化钠溶液的配制
1.(1)烧杯 (2)①G ②D F ③B E
2.(1)计算 8 92 (2)称量 B
(3)凹液面的最低处
(4)玻璃棒 加速溶解
(5)细口瓶
3.(1)溶质 9.2 10
(2)10 mL
(3)混匀 烧杯、玻璃棒
(4)细口瓶
4.D 取用药品时,瓶塞要倒放;氢氧化钠固体易吸水潮解且有腐蚀性,应放在玻璃器皿中称量,不能放在纸片上称量;用量筒量取水,读数时视线要与量筒内液体凹液面的最低处保持水平;溶解氢氧化钠时,用玻璃棒搅拌,可以加速溶解。
5.D
6.C 配制70 g 15%的氯化钠溶液,需氯化钠的质量为70 g×15%=10.5 g,称量氯化钠固体时“左码右物”且使用了游码,则实际称取氯化钠的质量为10 g-0.5 g=9.5 g,所配溶液中溶质的质量分数小于15%;转移氯化钠时,若氯化钠固体有撒落,则所配溶液中溶质的质量分数小于15%;量取水时,若俯视读数,则实际量取水的体积小于理论所需值,所配溶液中溶质的质量分数大于15%;配制好溶液后,装瓶时溶液溅落,不影响所配溶液中溶质的质量分数大小。
7.D 用氯化钠固体配制100 g溶质质量分数为8%的氯化钠溶液的步骤为:①计算所需溶质的质量、溶剂的质量;②用天平称量所需的溶质(氯化钠固体);③用量筒量取所需的溶剂(水);④溶解,配制溶液。在溶解过程中用玻璃棒搅拌可加快氯化钠固体的溶解。用量筒量取水时,仰视凹液面的最低处,读数偏小,实际量取的水的体积偏大,则所配溶液的溶质质量分数小于8%。
8.C 实验中多余的药品不能放回原瓶;在溶解过程中用玻璃棒搅拌的目的是加快氯化钠固体的溶解,而不是增大氯化钠的溶解度;用托盘天平称量固体时,若不用游码,即使“左码右物”,也不影响所称固体的质量,配制的溶液的溶质质量分数不会偏小,若称量时用了游码,会使所称固体的质量偏小,使配制的溶液的溶质质量分数偏小。
9.D
10.A 托盘天平的使用要遵循“左物右码”的原则,图中药品与砝码放反了,量取液体时,视线应与液体凹液面的最低处保持水平,图中仰视刻度,操作错误;配制溶液的操作步骤为:计算、称量、量取、溶解;若所有操作都正确,完全溶解后装瓶时有液滴溅出,不会导致溶质的质量分数偏小;配制时应称量氯化钠固体的质量为50 g×15%=7.5 g。
11.(1)量筒
(2)7.5 42.5
(3)左 继续向左盘中加入氯化钠固体至天平平衡
(4)搅拌,加速氯化钠的溶解
(5)AB (6)100
12.(1)烧杯 (2)B 135
(3)小于
(4)2H2O22H2O+O2↑
计算方法如图下:
设需要30%的过氧化氢溶液的质量为x,
则30%×x=150 g×3%,x=15 g。
需要水的质量为150 g-15 g=135 g。
用量筒量取30%的过氧化氢溶液时,若俯视读数,读数比实际液体体积大,会造成实际量取的30%的过氧化氢溶液的体积偏小,则使所配溶液溶质质量分数偏小。
类型1 教材实验原型练
1.小孟在实验室欲配制一定溶质质量分数的氯化钠溶液,可供选择的仪器如图图SY5-1所示。
图SY5-1
(1)B仪器的名称是 。
(2)根据实验操作选择相应的仪器(填字母)。
①称量氯化钠 ;②量取水 、 ;③溶解氯化钠 、
。
2.某同学用固体氯化钾配制质量分数为8%的氯化钾溶液。请按操作步骤回答下列问题。
(1) :配制100 g质量分数为8%的氯化钾溶液,所需氯化钾的质量为 g,需要水的质量为 g。
(2) :用托盘天平称量所需的氯化钾,托盘天平调节平衡后,接下来的操作应该是 (填字母)。
A.先在左盘纸片上加氯化钾,后在右盘纸片上加砝码
B.先在右盘纸片上加砝码,后在左盘纸片上加氯化钾
(3)量取:量取水读数时,视线要与量筒内液体的 保持水平,量好后倒入盛有氯化钾的烧杯中。
(4)溶解:溶解时需用 搅拌,以 。
(5)装瓶:将配制好的溶液装入 (填“广口瓶”或“细口瓶”)中,盖上瓶塞,贴好标签,请填写标签。
图SY5-2
3. 溶液具有广泛的用途。在实际生产、生活中,我们常常要把较浓的溶液加水稀释成所需的较稀的溶液,现用溶质质量分数为12%的氯化钠溶液(密度约为1.09 g/cm3)配制20 g溶质质量分数为6%的氯化钠溶液,其操作步骤如图下:
(1)计算:依据溶液稀释前后, 的质量不变,计算出需要质量分数为12%的氯化钠溶液 (计算结果精确到0.1)mL,需要水 mL(水的密度为1 g/cm3)。
(2)量取:应选用规格为 (填“10 mL”“20 mL”或“50 mL”)的量筒。
(3) : 配制该溶液的过程中用到的仪器除了上述步骤涉及的量筒、胶头滴管外,还需要 。
(4)把配制好的上述溶液装入 (填“广口瓶”或“细口瓶”)中,盖好瓶塞并贴上标签。
4.某学生要配制一定溶质质量分数的NaOH溶液,实验操作如图图SY5-3所示,其中正确的是 ( )
图SY5-3
5.实验室用硝酸钾固体配制100 g溶质质量分数为3%的硝酸钾溶液,下列说法正确的是( )
A.用50 mL量筒量取水
B.将固体放于托盘天平的右盘上称取
C.将固体直接投入量筒中溶解
D.将配制好的溶液装入细口瓶,盖好瓶塞,贴上标签
6.配制70 g 15%的氯化钠溶液,下列操作会使所配溶液中溶质的质量分数大于15%的是 ( )
图SY5-4
7.实验室用氯化钠固体配制100 g溶质质量分数为8%的氯化钠溶液,下列说法错误的是 ( )
A.实验的步骤为计算、称量、量取、溶解
B.溶解过程中用玻璃棒搅拌可以加快氯化钠的溶解
C.若用量筒量取水时仰视凹液面的最低处,则所配溶液的溶质质量分数小于8%
D.将配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶,并贴上标签
类型2 教材实验拓展练
8.配制一定溶质质量分数的氯化钠溶液是初中化学的基础实验。下列操作与分析均正确的是 ( )
选项 实验操作 分析
A 称量氯化钠时,将取出的过量的氯化钠放回原瓶 目的是节约药品
B 溶解时用玻璃棒搅拌 目的是增大氯化钠的溶解度
C 用量筒量取液体,倾倒至接近刻度时,改用胶头滴管滴加 防止倾倒时过量
D 称量时氯化钠放在右盘 一定会导致配制的溶液的溶质质量分数偏小
9.用溶质质量分数为98%的浓硫酸配制490 g溶质质量分数为20%的稀硫酸。下列说法不正确的是 ( )
A.实验中用到的玻璃仪器:量筒、胶头滴管、烧杯、玻璃棒
B.配制该稀硫酸需要加水390 mL
C.配制时需要溶质质量分数为98%的浓硫酸100 g
D.配制的步骤是计算、称量、量取、溶解、装瓶贴标签
10.[2020·岳阳改编] 某同学需要配制50 g质量分数为15%的氯化钠溶液,步骤如图图SY5-5所示。下列分析正确的是 ( )
图SY5-5
A.配制过程中出现了两处操作错误
B.实验操作步骤为:计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后装瓶时有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体的质量为7.0 g
11.配制一定溶质质量分数的氯化钠溶液的过程如图图SY5-6所示。
图SY5-6
(1)写出图中标号a仪器的名称: 。
(2)配制50 g质量分数为15%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠 g,水 g。
(3)用托盘天平称量所需氯化钠时,氯化钠应放在 (填“左”或“右”)盘,加入氯化钠后,发现托盘天平的指针向右偏转,接下来的操作是 。
(4)溶解过程中玻璃棒的作用是 。
(5)对配制的溶液进行检测,发现溶质质量分数偏小,其原因可能有 (填字母)。
A.称量时,药品与砝码放反了,且使用了游码
B.量取水时,仰视读数
C.装瓶时,有少量溶液洒出
(6)把50 g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需加水的质量是 g。
12.在对抗席卷全球的“新冠肺炎”疫情中,常用过氧化氢溶液作消毒剂。小欣同学准备用以下仪器,完成“用溶质质量分数为30%的过氧化氢溶液配制150 g溶质质量分数为3%的过氧化氢溶液”这一实验。
图SY5-7
(1)仪器A的名称为 。
(2)完成此实验不会用到上述仪器中的 (填字母),实验过程中需要加入 g水。
(3)用量筒量取溶质质量分数为30%的过氧化氢溶液时,若俯视读数,则所配制溶液的溶质质量分数 (填“大于”“小于”或“等于”)3%。
(4)过氧化氢溶液用于伤口消毒时,在生物酶的催化作用下会产生大量气泡,发生反应的化学方程式为 。
答案
实验活动5 一定溶质质量分数的氯化钠溶液的配制
1.(1)烧杯 (2)①G ②D F ③B E
2.(1)计算 8 92 (2)称量 B
(3)凹液面的最低处
(4)玻璃棒 加速溶解
(5)细口瓶
3.(1)溶质 9.2 10
(2)10 mL
(3)混匀 烧杯、玻璃棒
(4)细口瓶
4.D 取用药品时,瓶塞要倒放;氢氧化钠固体易吸水潮解且有腐蚀性,应放在玻璃器皿中称量,不能放在纸片上称量;用量筒量取水,读数时视线要与量筒内液体凹液面的最低处保持水平;溶解氢氧化钠时,用玻璃棒搅拌,可以加速溶解。
5.D
6.C 配制70 g 15%的氯化钠溶液,需氯化钠的质量为70 g×15%=10.5 g,称量氯化钠固体时“左码右物”且使用了游码,则实际称取氯化钠的质量为10 g-0.5 g=9.5 g,所配溶液中溶质的质量分数小于15%;转移氯化钠时,若氯化钠固体有撒落,则所配溶液中溶质的质量分数小于15%;量取水时,若俯视读数,则实际量取水的体积小于理论所需值,所配溶液中溶质的质量分数大于15%;配制好溶液后,装瓶时溶液溅落,不影响所配溶液中溶质的质量分数大小。
7.D 用氯化钠固体配制100 g溶质质量分数为8%的氯化钠溶液的步骤为:①计算所需溶质的质量、溶剂的质量;②用天平称量所需的溶质(氯化钠固体);③用量筒量取所需的溶剂(水);④溶解,配制溶液。在溶解过程中用玻璃棒搅拌可加快氯化钠固体的溶解。用量筒量取水时,仰视凹液面的最低处,读数偏小,实际量取的水的体积偏大,则所配溶液的溶质质量分数小于8%。
8.C 实验中多余的药品不能放回原瓶;在溶解过程中用玻璃棒搅拌的目的是加快氯化钠固体的溶解,而不是增大氯化钠的溶解度;用托盘天平称量固体时,若不用游码,即使“左码右物”,也不影响所称固体的质量,配制的溶液的溶质质量分数不会偏小,若称量时用了游码,会使所称固体的质量偏小,使配制的溶液的溶质质量分数偏小。
9.D
10.A 托盘天平的使用要遵循“左物右码”的原则,图中药品与砝码放反了,量取液体时,视线应与液体凹液面的最低处保持水平,图中仰视刻度,操作错误;配制溶液的操作步骤为:计算、称量、量取、溶解;若所有操作都正确,完全溶解后装瓶时有液滴溅出,不会导致溶质的质量分数偏小;配制时应称量氯化钠固体的质量为50 g×15%=7.5 g。
11.(1)量筒
(2)7.5 42.5
(3)左 继续向左盘中加入氯化钠固体至天平平衡
(4)搅拌,加速氯化钠的溶解
(5)AB (6)100
12.(1)烧杯 (2)B 135
(3)小于
(4)2H2O22H2O+O2↑
计算方法如图下:
设需要30%的过氧化氢溶液的质量为x,
则30%×x=150 g×3%,x=15 g。
需要水的质量为150 g-15 g=135 g。
用量筒量取30%的过氧化氢溶液时,若俯视读数,读数比实际液体体积大,会造成实际量取的30%的过氧化氢溶液的体积偏小,则使所配溶液溶质质量分数偏小。
同课章节目录
