人教版化学九年级下册同步课时练习:第10单元 课题1 常见的酸和碱 第3课时 几种常见的碱(word版 含答案)
文档属性
| 名称 | 人教版化学九年级下册同步课时练习:第10单元 课题1 常见的酸和碱 第3课时 几种常见的碱(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 156.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-06-21 00:00:00 | ||
图片预览


文档简介
课题1 常见的酸和碱
第3课时 几种常见的碱
知识点 1 氢氧化钠的性质和用途
1.下列不是氢氧化钠俗称的是 ( )
A.火碱 B.烧碱
C.纯碱 D.苛性钠
2.下列有关氢氧化钠的性质和用途的说法中,错误的是 ( )
A.氢氧化钠是白色固体,溶于水放出热量
B.有强烈的腐蚀性,沾到皮肤上要用大量的水冲洗,再涂上硫酸
C.能除去油污,可作炉具清洁剂
D.固体氢氧化钠易吸收水蒸气而潮解,可作某些气体的干燥剂
3.氢氧化钠固体曝露在空气中,容易 而使表面潮湿并逐渐溶解,这种现象叫作 ,这一变化过程属于 变化。此外,氢氧化钠可直接吸收空气中的CO2而变质,这一变化属于 变化。根据以上两点性质,氢氧化钠固体可用作某些气体的干燥剂,且应 保存。
知识点 2 氢氧化钙的性质和用途
4.下列有关熟石灰的说法错误的是 ( )
A.熟石灰又称消石灰
B.熟石灰是白色粉末状固体,微溶于水
C.熟石灰的溶解度随温度的升高而增大
D.熟石灰对皮肤、衣服等有腐蚀作用
5.氢氧化钙俗称熟石灰,在生产和生活中有重要应用。下列说法错误的是 ( )
A.建筑上可用熟石灰与沙子混合来砌砖
B.农业上可用熟石灰改良酸性土壤
C.实验室中用熟石灰作干燥剂
D.在树木上涂抹石灰浆可保护树木
6.市售“自热米饭”的自加热原理:饭盒夹层中的水与生石灰接触发生反应,放出大量热。该反应的化学方程式为 。
知识点 3 碱的化学性质
7.下列溶液中能使紫色石蕊溶液变蓝,酚酞溶液变红的是 ( )
A.石灰水
B.白醋
C.氯化钠溶液
D.稀盐酸
8.氢氧化钙和氢氧化钠溶液都能与二氧化碳反应。
(1)向澄清石灰水中通入二氧化碳,会观察到石灰水 ,据此,可用澄清石灰水检验二氧化碳;用石灰浆粉刷墙壁,干燥后墙面变硬。请写出以上两个变化中涉及的化学方程式:
。
(2)曝露在空气中的氢氧化钠易与二氧化碳反应,写出该反应的化学方程式:
。
(3)三氧化硫与碱的反应与上面两个反应类似,写出三氧化硫与氢氧化钠溶液反应的化学方程式: 。
9.下列关于酸和碱的说法正确的是 ( )
A.氢氧化钠可用于干燥二氧化碳气体
B.人体胃液中含有硫酸,可以帮助消化
C.氢氧化钙可用于配制波尔多液、改良酸性土壤
D.氢氧化钠和氢氧化钙溶于水都会放出大量的热
10.1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2OCa(OH)2。下列说法不正确的是 ( )
A.该反应属于化合反应
B.该反应会放出热量
C.由此反应推测氧化钙可干燥CO2气体
D.此反应可制备氢氧化钙
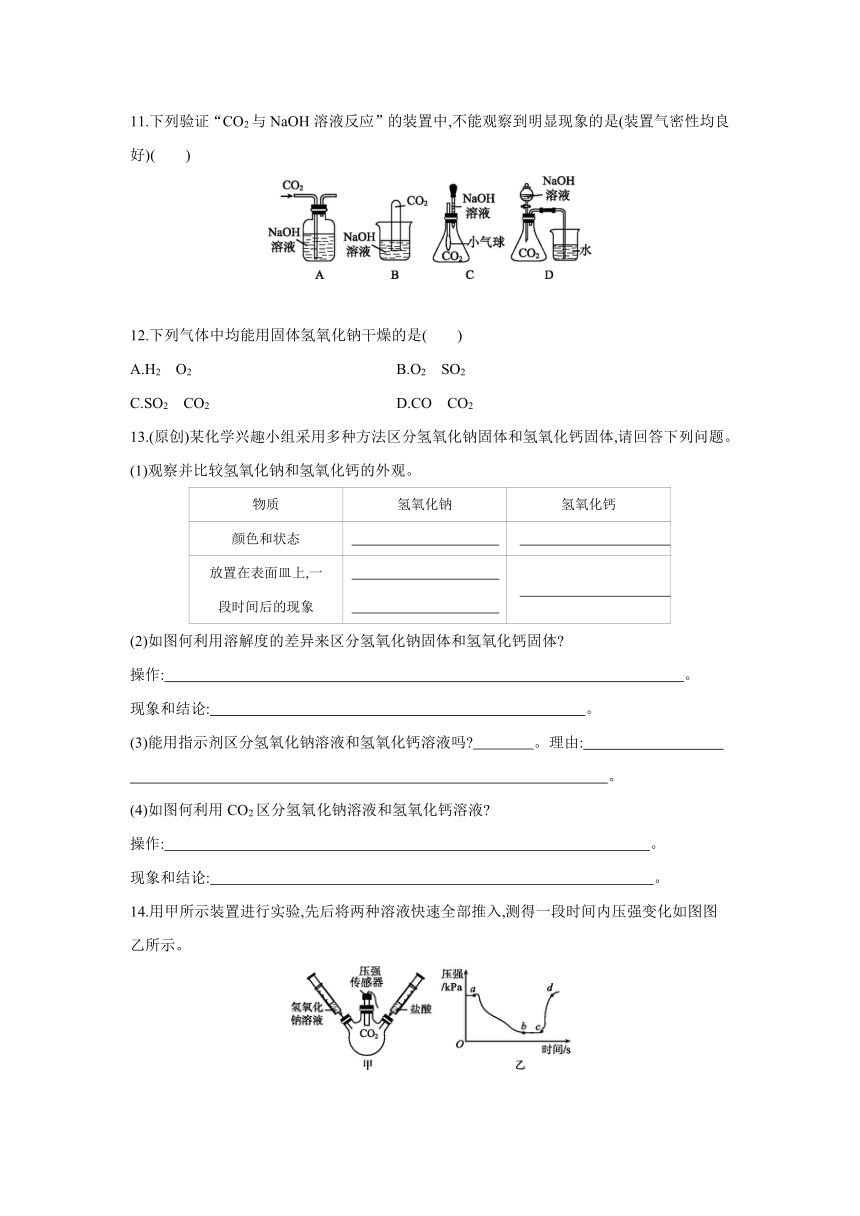
11.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
12.下列气体中均能用固体氢氧化钠干燥的是( )
A.H2 O2 B.O2 SO2
C.SO2 CO2 D.CO CO2
13.(原创)某化学兴趣小组采用多种方法区分氢氧化钠固体和氢氧化钙固体,请回答下列问题。
(1)观察并比较氢氧化钠和氢氧化钙的外观。
物质 氢氧化钠 氢氧化钙
颜色和状态
放置在表面皿上,一 段时间后的现象
(2)如图何利用溶解度的差异来区分氢氧化钠固体和氢氧化钙固体
操作: 。
现象和结论: 。
(3)能用指示剂区分氢氧化钠溶液和氢氧化钙溶液吗 。理由:
。
(4)如图何利用CO2区分氢氧化钠溶液和氢氧化钙溶液
操作: 。
现象和结论: 。
14.用甲所示装置进行实验,先后将两种溶液快速全部推入,测得一段时间内压强变化如图图乙所示。
(1)先推入的溶液是 ;a点压强升高的原因是
。
(2)用化学方程式解释ab段压强降低的原因: 。
(3)bc段压强不变,原因是 。
(4)cd段压强升高,用化学方程式解释: 。
15.将二氧化碳通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象。二氧化碳和氢氧化钠是否发生了化学反应 小明和其他同学一起设计了甲、乙两个实验进行验证,如图所示。
(1)甲、乙中的现象分别是 。
(2)小王同学认为上述实验是可行的,其共同原理是 。
(3)小余同学提出了疑问,他认为上述实验还不足以证明二氧化碳和氢氧化钠确实发生了反应,其原因是 ,请另设计实验证明:
。
16.[2021·邵阳] 下列关于氢氧化钠的描述中错误的是 ( )
A.对皮肤有强烈的腐蚀作用
B.其水溶液能使石蕊溶液变红
C.能去除油污,可作炉具清洁剂
D.易溶于水,溶解时放出热量
答案
课题1 常见的酸和碱
第3课时 几种常见的碱
1.C 2.B
3.吸收空气中的水分 潮解 物理 化学 密封
4.C 熟石灰即氢氧化钙,它的溶解度随温度的升高而减小。
5.C 熟石灰微溶于水,也不能与水反应,不能用作干燥剂。
6.CaO+H2OCa(OH)2
7.A
8.(1)变浑浊
CO2+Ca(OH)2CaCO3↓+H2O
(2)2NaOH+CO2Na2CO3+H2O
(3)SO3+2NaOHNa2SO4+H2O
9.C 氢氧化钠能与二氧化碳反应,不能用来干燥二氧化碳;人体胃液中含有的是盐酸,而不是硫酸;氢氧化钙溶于水不会放出大量的热。
10.C
11.A B中试管内液面会上升,最终高于烧杯中液面,C中小气球会变大,D中水会倒流到锥形瓶中。
12.A CO2、SO2均能和氢氧化钠发生化学反应,故不能用氢氧化钠干燥。
13.(1)白色固体 白色粉末状固体 表面潮湿并逐渐溶解 无明显现象
(2)操作:分别取2 g待区分样品于两只烧杯中,然后向其中逐滴加入水,并不断搅拌
现象和结论:先完全溶解的是氢氧化钠,另一种是氢氧化钙(现象和结论与操作对应合理即可)
(3)不能 因为氢氧化钠溶液和氢氧化钙溶液都显碱性,使指示剂的变色情况相同
(4)操作:分别向待区分溶液中通入二氧化碳气体
现象和结论:变浑浊的是氢氧化钙溶液,无明显现象的是氢氧化钠溶液
14.(1)氢氧化钠溶液 加入的氢氧化钠溶液挤压气体,使瓶内压强增大
(2)CO2+2NaOHNa2CO3+H2O
(3)氢氧化钠溶液与二氧化碳充分反应,反应停止
(4)Na2CO3+2HCl2NaCl+H2O+CO2↑
15.(1)甲中软塑料瓶变瘪,乙中熟鸡蛋进入玻璃容器内
(2)氢氧化钠和二氧化碳反应后装置内压强减小
(3)二氧化碳能溶于水且能与水反应,也会导致装置内压强减小
取两个装有相同体积二氧化碳的软塑料瓶,分别加入相同体积的氢氧化钠溶液和蒸馏水,振荡,对比软塑料瓶变瘪的程度(合理即可)
16.B 氢氧化钠的水溶液显碱性,其水溶液能使石蕊溶液变蓝。
第3课时 几种常见的碱
知识点 1 氢氧化钠的性质和用途
1.下列不是氢氧化钠俗称的是 ( )
A.火碱 B.烧碱
C.纯碱 D.苛性钠
2.下列有关氢氧化钠的性质和用途的说法中,错误的是 ( )
A.氢氧化钠是白色固体,溶于水放出热量
B.有强烈的腐蚀性,沾到皮肤上要用大量的水冲洗,再涂上硫酸
C.能除去油污,可作炉具清洁剂
D.固体氢氧化钠易吸收水蒸气而潮解,可作某些气体的干燥剂
3.氢氧化钠固体曝露在空气中,容易 而使表面潮湿并逐渐溶解,这种现象叫作 ,这一变化过程属于 变化。此外,氢氧化钠可直接吸收空气中的CO2而变质,这一变化属于 变化。根据以上两点性质,氢氧化钠固体可用作某些气体的干燥剂,且应 保存。
知识点 2 氢氧化钙的性质和用途
4.下列有关熟石灰的说法错误的是 ( )
A.熟石灰又称消石灰
B.熟石灰是白色粉末状固体,微溶于水
C.熟石灰的溶解度随温度的升高而增大
D.熟石灰对皮肤、衣服等有腐蚀作用
5.氢氧化钙俗称熟石灰,在生产和生活中有重要应用。下列说法错误的是 ( )
A.建筑上可用熟石灰与沙子混合来砌砖
B.农业上可用熟石灰改良酸性土壤
C.实验室中用熟石灰作干燥剂
D.在树木上涂抹石灰浆可保护树木
6.市售“自热米饭”的自加热原理:饭盒夹层中的水与生石灰接触发生反应,放出大量热。该反应的化学方程式为 。
知识点 3 碱的化学性质
7.下列溶液中能使紫色石蕊溶液变蓝,酚酞溶液变红的是 ( )
A.石灰水
B.白醋
C.氯化钠溶液
D.稀盐酸
8.氢氧化钙和氢氧化钠溶液都能与二氧化碳反应。
(1)向澄清石灰水中通入二氧化碳,会观察到石灰水 ,据此,可用澄清石灰水检验二氧化碳;用石灰浆粉刷墙壁,干燥后墙面变硬。请写出以上两个变化中涉及的化学方程式:
。
(2)曝露在空气中的氢氧化钠易与二氧化碳反应,写出该反应的化学方程式:
。
(3)三氧化硫与碱的反应与上面两个反应类似,写出三氧化硫与氢氧化钠溶液反应的化学方程式: 。
9.下列关于酸和碱的说法正确的是 ( )
A.氢氧化钠可用于干燥二氧化碳气体
B.人体胃液中含有硫酸,可以帮助消化
C.氢氧化钙可用于配制波尔多液、改良酸性土壤
D.氢氧化钠和氢氧化钙溶于水都会放出大量的热
10.1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2OCa(OH)2。下列说法不正确的是 ( )
A.该反应属于化合反应
B.该反应会放出热量
C.由此反应推测氧化钙可干燥CO2气体
D.此反应可制备氢氧化钙
11.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
12.下列气体中均能用固体氢氧化钠干燥的是( )
A.H2 O2 B.O2 SO2
C.SO2 CO2 D.CO CO2
13.(原创)某化学兴趣小组采用多种方法区分氢氧化钠固体和氢氧化钙固体,请回答下列问题。
(1)观察并比较氢氧化钠和氢氧化钙的外观。
物质 氢氧化钠 氢氧化钙
颜色和状态
放置在表面皿上,一 段时间后的现象
(2)如图何利用溶解度的差异来区分氢氧化钠固体和氢氧化钙固体
操作: 。
现象和结论: 。
(3)能用指示剂区分氢氧化钠溶液和氢氧化钙溶液吗 。理由:
。
(4)如图何利用CO2区分氢氧化钠溶液和氢氧化钙溶液
操作: 。
现象和结论: 。
14.用甲所示装置进行实验,先后将两种溶液快速全部推入,测得一段时间内压强变化如图图乙所示。
(1)先推入的溶液是 ;a点压强升高的原因是
。
(2)用化学方程式解释ab段压强降低的原因: 。
(3)bc段压强不变,原因是 。
(4)cd段压强升高,用化学方程式解释: 。
15.将二氧化碳通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象。二氧化碳和氢氧化钠是否发生了化学反应 小明和其他同学一起设计了甲、乙两个实验进行验证,如图所示。
(1)甲、乙中的现象分别是 。
(2)小王同学认为上述实验是可行的,其共同原理是 。
(3)小余同学提出了疑问,他认为上述实验还不足以证明二氧化碳和氢氧化钠确实发生了反应,其原因是 ,请另设计实验证明:
。
16.[2021·邵阳] 下列关于氢氧化钠的描述中错误的是 ( )
A.对皮肤有强烈的腐蚀作用
B.其水溶液能使石蕊溶液变红
C.能去除油污,可作炉具清洁剂
D.易溶于水,溶解时放出热量
答案
课题1 常见的酸和碱
第3课时 几种常见的碱
1.C 2.B
3.吸收空气中的水分 潮解 物理 化学 密封
4.C 熟石灰即氢氧化钙,它的溶解度随温度的升高而减小。
5.C 熟石灰微溶于水,也不能与水反应,不能用作干燥剂。
6.CaO+H2OCa(OH)2
7.A
8.(1)变浑浊
CO2+Ca(OH)2CaCO3↓+H2O
(2)2NaOH+CO2Na2CO3+H2O
(3)SO3+2NaOHNa2SO4+H2O
9.C 氢氧化钠能与二氧化碳反应,不能用来干燥二氧化碳;人体胃液中含有的是盐酸,而不是硫酸;氢氧化钙溶于水不会放出大量的热。
10.C
11.A B中试管内液面会上升,最终高于烧杯中液面,C中小气球会变大,D中水会倒流到锥形瓶中。
12.A CO2、SO2均能和氢氧化钠发生化学反应,故不能用氢氧化钠干燥。
13.(1)白色固体 白色粉末状固体 表面潮湿并逐渐溶解 无明显现象
(2)操作:分别取2 g待区分样品于两只烧杯中,然后向其中逐滴加入水,并不断搅拌
现象和结论:先完全溶解的是氢氧化钠,另一种是氢氧化钙(现象和结论与操作对应合理即可)
(3)不能 因为氢氧化钠溶液和氢氧化钙溶液都显碱性,使指示剂的变色情况相同
(4)操作:分别向待区分溶液中通入二氧化碳气体
现象和结论:变浑浊的是氢氧化钙溶液,无明显现象的是氢氧化钠溶液
14.(1)氢氧化钠溶液 加入的氢氧化钠溶液挤压气体,使瓶内压强增大
(2)CO2+2NaOHNa2CO3+H2O
(3)氢氧化钠溶液与二氧化碳充分反应,反应停止
(4)Na2CO3+2HCl2NaCl+H2O+CO2↑
15.(1)甲中软塑料瓶变瘪,乙中熟鸡蛋进入玻璃容器内
(2)氢氧化钠和二氧化碳反应后装置内压强减小
(3)二氧化碳能溶于水且能与水反应,也会导致装置内压强减小
取两个装有相同体积二氧化碳的软塑料瓶,分别加入相同体积的氢氧化钠溶液和蒸馏水,振荡,对比软塑料瓶变瘪的程度(合理即可)
16.B 氢氧化钠的水溶液显碱性,其水溶液能使石蕊溶液变蓝。
同课章节目录
